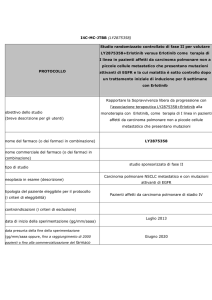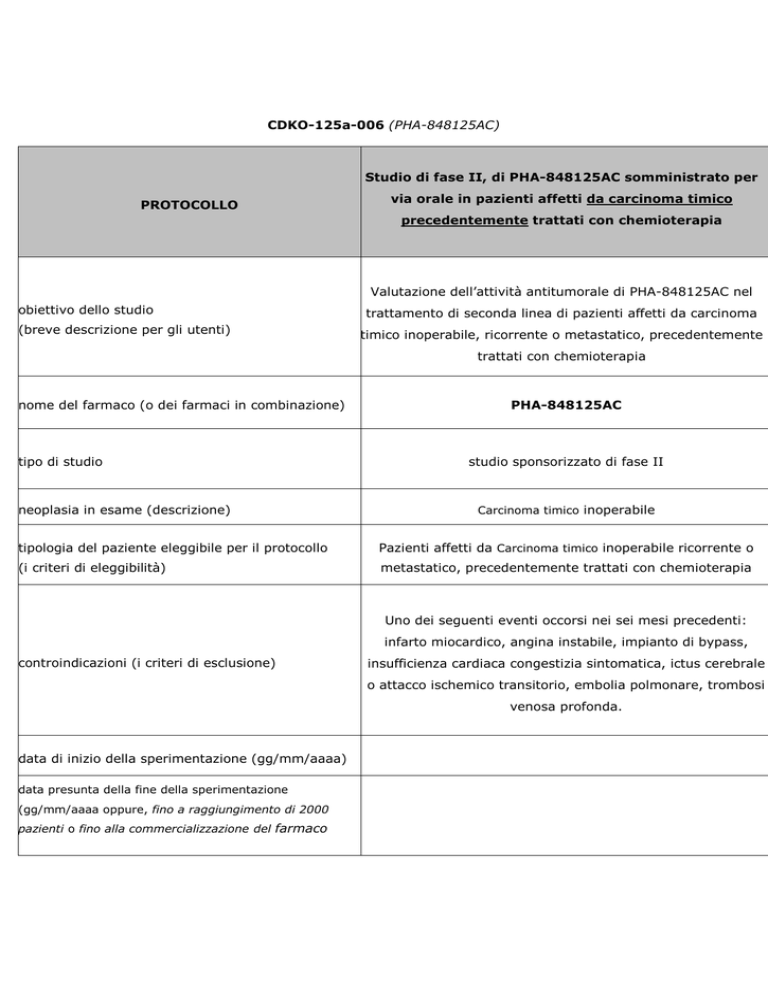
CDKO-125a-006 (PHA-848125AC)
Studio di fase II, di PHA-848125AC somministrato per
PROTOCOLLO
via orale in pazienti affetti da carcinoma timico
precedentemente trattati con chemioterapia
Valutazione dell’attività antitumorale di PHA-848125AC nel
obiettivo dello studio
(breve descrizione per gli utenti)
trattamento di seconda linea di pazienti affetti da carcinoma
timico inoperabile, ricorrente o metastatico, precedentemente
trattati con chemioterapia
nome del farmaco (o dei farmaci in combinazione)
tipo di studio
neoplasia in esame (descrizione)
PHA-848125AC
studio sponsorizzato di fase II
Carcinoma timico inoperabile
tipologia del paziente eleggibile per il protocollo
Pazienti affetti da Carcinoma timico inoperabile ricorrente o
(i criteri di eleggibilità)
metastatico, precedentemente trattati con chemioterapia
Uno dei seguenti eventi occorsi nei sei mesi precedenti:
infarto miocardico, angina instabile, impianto di bypass,
controindicazioni (i criteri di esclusione)
insufficienza cardiaca congestizia sintomatica, ictus cerebrale
o attacco ischemico transitorio, embolia polmonare, trombosi
venosa profonda.
data di inizio della sperimentazione (gg/mm/aaaa)
data presunta della fine della sperimentazione
(gg/mm/aaaa oppure, fino a raggiungimento di 2000
pazienti o fino alla commercializzazione del farmaco