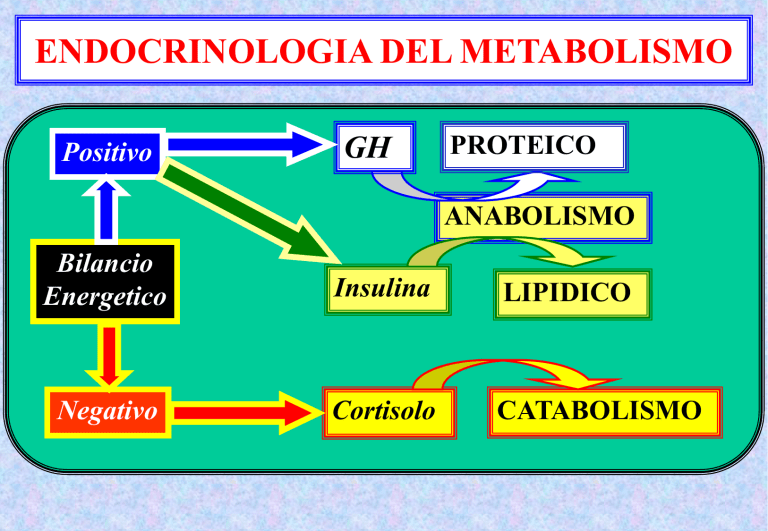
ENDOCRINOLOGIA DEL METABOLISMO
Positivo
GH
PROTEICO
ANABOLISMO
Bilancio
Energetico
Insulina
LIPIDICO
Negativo
Cortisolo
CATABOLISMO
M
e
t
a
b
o
l
i
s
m
o
CICLO DI
KREBS
O DELL’ACIDO
CITRICO
Schema dei Prodotti del Ciclo di Krebs
Acetato
C2
NADH
FADH
CO2
GTP
NADH
NADH
CO2
Reazione sintetica di utilizzo dell’acetato
CO2
Acetato
C2
CO2
FADH
GTP
NADH
NADH
NADH
Schema delle fonti del Ciclo di Krebs
Tre,
Leu,
Val,
Ile,
Met
CO2
Ala, Gli,
Ser, Cis,
Trp
Glicerolo,
Glicole
propilenico
CO2
Sintesi delle fonti glucidiche del Ciclo di Krebs
Sono fonti per il ciclo di Krebs:
Il GLUCOSIO tramite l’ ACIDO LATTICO (C3)
Gli AMINOACIDI, direttamente (sull’alfa cheto glutarato) od
indirettamente tramite PIRUVATO E PROPIONATO (C3),
il GLICOLE PROPILENICO ed il GLICEROLO (C3),.
SIGNIFICATI BIOLOGICI DEL
CICLO DI KREBS
Il Ciclo di Krebs può avere sia un
significato:
CATABOLICO allorquando “brucia” l’acetato
(legato al coenzima A) derivato:
dalla demolizione dei lipidi di riserva (acidi grassi e colesterolo) o
dall’ossidazione dei lipidi alimentari.
ANABOLICO allorquando “LAVORA” per la
gluconeogenesi
GLUCONEOGENESI
2 P-Trioso
2ATP
2ADP
2 x C3
→
→
2 P-Trioso-P
→
P-Fruttosio-P
C6
Isome
rasi
GLUCOSIO-P
CATABOLISMO
il Ciclo di Krebs è il processo centrale del catabolismo in quanto l’acetato che
proviene dalla demolizione di acidi grassi a lunga catena e colesterolo deve essere
utilizzato per formare ATP con liberazione di 2 molecole di CO2 per ogni molecola
di acetato.
NEFA
Colesterolo
Alcool
Acetato
Ossala
cetato
Glucosio
ATP
2CO2
MORALE DEL CATABOLISMO
CHETOSI
SE MANCA OSSALACETATO (O SUOI PRECURSORI) L’ACETATO
NON PUÒ ESSERE “BRUCIATO” E SI ACCUMULA NEL FEGATO
COSÌ SI FORMANO I PRODOTTI DI CONDENSAZIONE:
Acetato + Acetato
Acetoacetato
H2
b-OH butirrato
CO2
Acetone
CHETOSI
In caso di eccesso di grassi rispetto agli zuccheri la degrazione dei primi
si arresta all’acetato. 2 molecole di quest’ultimo nel fegato vengono
condensate a corpi chetonici:
- Acido aceto-acetico, che può essere ridotto a
- Acido b-OH butirrico, che può essere decarbossilato ottenendo
- Acetone.
La situazione di accumulo di questi ultimi nell’organismo è patologica e
prende il nome di
chetosi
.
EPATOSTEATOSI
Per il verificarsi della chetosi è necessario un bilancio energetico
negativo (entrate minori delle spese) come si verifica ad esempio nel
digiuno (entrate = 0). Altrimenti la chetosi si può verificare in
carenza di glucidi digeribili (la fibra in gran parte non lo è) o di loro
precursori (le proteine sono ottime fonti gluconeogenetiche).
Se la chetosi perdura si associa sovente l’accumulo di acidi grassi
(NEFA) non ancora demoliti ad acetato nel fegato:
Epatosteatosi
RUMINE E METABOLISMO ANIMALE
Cavità prestomacali:
organi deputati alla digestione degli alimenti
assorbono una grande quantità dei prodotti delle fermentazioni
ASSORBIMENTO NEI DISTRETTI
CEFALICI DELLO STOMACO
CAPRA
PECORA
VACCA
60%
70%
65%
METABOLISMO DEL RUMINANTE
stato funzionale di perenne neoglucogenesi
MODELLO DELL’ASSORBIMENTO DEGLI A.G.V.
ATTRAVERSO L’EPITELIO RUMINALE.
UTILIZZAZIONE DEGLI ACIDI GRASSI VOLATILI
ACETATO
30% utilizzato direttamente dalle cellule dell’epitelio ruminale
attivato ad acetilCoA
produzione di energia nel ciclo di Krebs
sintesi di alcuni composti biologici (corpi chetonici e acidi grassi)
non può essere utilizzato per la sintesi ex-novo di zuccheri
sfugge al metabolismo epatico
Metabolizzato a corpi chetonici nell’epitelio del rumine (50% vacca,
80-85% capra)
BUTIRRATO
utilizzato a scopi energetici (cervello, cuore e tessuto muscolare)
PROPIONATO
•
Convertito nell’epitelio ruminale e nel fegato a succinilCoA
(intermedio del ciclo di Krebs) comune a tutti
Nell’epitelio ruminale (tipico dei RUMINANTI):
50% convertito in lattato
Destino metabolico della
immesso in circolo
catena carboniosa
riutilizzato nel ciclo di Cori
del propionato
altri tessuti
effetto anaplerotico del succinilCoA sul ciclo di Krebs
CICLO DI CORI
GLUCOSIO
GLUCOSIO
GLICOGENO
ACIDO LATTICO
ACIDO LATTICO
ACIDO LATTICO
FEGATO
SANGUE
MUSCOLO
UTILIZZAZIONE DI PROTEINE E AMINOACIDI
PROTEINE A DISPOSIZIONE DELL’ANIMALE:
• proteine digeribili di origine microbica
• proteine alimentari by-pass
LA COMPOSIZIONE MEDIA DELLE PROTEINE ESPRESSE
DAI BATTERI O DAI PROTOZOI NEL RUMINE E’ RELATIVAMENTE
COSTANTE INDIPENDENTEMENTE DAL TIPO DI ALIMENTO.
PROTEINE DEI BATTERI
• 53% della materia secca
• digeribilità del 75-83%
• ricche in valina, arginina e triptofano
PROTEINE DEI PROTOZOI
• > digeribilità
• > valore biologico
• ricche in lisina, leucina e isoleucina
MISCELA BATTERI-PROTOZOI
contenuto proteico del 50%
digeribilità di circa l’80%
AMINOACIDI
AMINOACIDI GLUCONEOGENETICI:
• quelli che possiedono una catena carboniosa che può essere
• trasformata in intermedi del ciclo di Krebs o in piruvato
• fegato e corteccia renale
• cervello e muscolo scheletrico
• aspartato, tirosina, fenilalanina, isoleucina, metionina, valina, glutammato, istidina, prolina,
arginina
SOLO FEGATO E RENE CEDONO GLUCOSIO
AL CIRCOLO EMATICO (glucosio-6-fosfatasi)
ALANINA, GLICINA, SERINA, CISTEINA, TRIPTOFANO:
• metabolizzati ad acido piruvico
• carbossilato ad ossalacetato (gluconeogenesi)
• decarbossilato ossidativamente ad acetilCoA (chetogenesi)
Leucina e lisina: strettamente chetogenetici
SINTESI DELL’UREA
NEL FEGATO
SINTESI
DELL’UREA
NEL
FEGATO
SIGNIFICATO BIOLOGICO DELLA
SINTESI EPATICA DELL’UREA
Detossificazione dell’ammoniaca
presente nel sangue
L’ESCREZIONE AZOTATA
Condensazione dell’ammoniaca e dell’anidride
carbonica nel mitocondrio
O
OH
Carbamil fosfato
NH3 + CO2
H2N—C—O—P=O
OH
2 ATP
2 ADP + Pi
SINTESI DELL’UREA
Reazione sintetica
NH3+
NH3 + CO2 + -OOCCH2CHCOOAspartato
3 ATP
O
2 ADP + 2 Pi + AMP + PPi
-OOCCHCHCOOHNCNH
+
2
2
Urea
Fumarato
40
6,7
30
5,0
20
3,3
10
1,7
UREA NEL LATTE
50
8,3
RELAZIONE TRA I LIVELLI DI UREA
NEL SANGUE E NEL LATTE
10
1,7
20
3,3
30
40
5,0
6,7
UREA EMATICA
50
8,3
mg/100 ml
mmol/l
INTERPRETAZIONE DEI LIVELLI DI UREA NEL LATTE
(PEYRAUD, 1989)
mmol/l
mg/100 ml
ZONA
OTTIMALE
razione equilibrata
carenza di azoto
degradabile o
eccesso di energia
fermentescibile
nella razione
Eccesso di azoto
degradabile o
carenza di energia
fermentescibile
nella razione
CALO DI INGESTIONE
CALO DI DIGERIBILITA’
RISCHIO DI ACIDOSI
CALO DI PRODUZIONE
PROBLEMI DI FERTILITA’
MORTALITA’ EMBRIONALE
METRITI, ZOPPIE
CHETOSI
PIU’ LATTE
INDICAZIONE DEI “LIMITI DI RIFERIMENTO”
PER L’UREA NEL SANGUE E NEL LATTE
ASCIUTTA
LATTAZIONE
20 - 25 kg/d
> 25 kg/d
PLASMA (mg/100 ml) 16,8 - 25,8
27,0 - 34,2
30,0 - 39,0
LATTE (mg/100 ml)
25,0 - 33,0
28,5 - 37,0
---
RELAZIONI FRA LA PROTEINA ALIMENTARE
E UREA NEL LATTE
(Roeseler e coll., 1993)
Urea ematica = 10.7+0.016 X DIP + 0.0256 X UIP – 1.26 X NEL
(mg/100ml)
(g/d)
(g/d)
(Mcal)
R2 = 0.67
METABOLISMO LIPIDICO NEL RUMINE
DIGESTIONE DEI LIPIDI
Animali non-ruminanti
duodeno
Animali ruminanti
prestomaci (non completa)
LIPASI DI ORIGINE MICROBICA
idrolisi dei lipidi esterificati
(trigliceridi, mono- e di-galattogliceridi e fosfolipidi)
IDROGENAZIONE DEI LIPIDI POLIINSATURI
Formazione di isomeri dienoici e monoenoici 18C
FORMAZIONE DI MOLECOLE PARTICOLARI
acidi grassi a numero dispari di atomi di C
acidi grassi a catena ramificata (isoacidi = isobutirrico, isovalerico)
Nel rumine gli esteri di acidi grassi polinsaturi vengono
bioidrogenati (ridotti ed isomerizzati) così dal C18:3 e dal
C18:2 si può arrivare al C18:0.
Gli intermedi del processo sono de “dieni coniugati”:
i CLA appunto.
SCHEMA DELLA BIOIDROGENAZIONE
RUMINALE DELL’ACIDO LINOLEICO
C18:2 cis-9, cis-12
acido linoleico
isomerizzazione
C18:2 cis-9, trans-11
acido rumenico
idrogenazione
C18:1 trans-11
acido trans-vaccenico
idrogenazione
C18:0
acido stearico
ACIDO LINOLEICO E SUOI PRINCIPALI
ISOMERI CONIUGATI: CLA










