Chemioterapia
• Insieme dottrinale e metodologico volto
alla ricerca di sostanze chimiche artificiali
e naturali dotate di tossicità selettiva nei
confronti di cellule procariote o eucariote
responsabili di infezioni, infestazioni,
neoplasie o disordini immunologici.
(P. Ehrlich, 1910)
IN FUNZIONE DEI DIVERSI BERSAGLI SI
DISTINGUONO TRE SETTORI DELLA CHEMIOTERAPIA:
• 1)
ANTIMICROBICA
(antibatterica,
antimicotica)
antivirale,
• 2) ANTIBLASTICA
• 3) IMMUNOMODULANTE
• Dall'introduzione dei primi agenti chemioterapici
(1935) la mortalità per malattie infettive e
parassitarie si è ridotta drasticamente.
Mortalità per malattie infettive e
parassitarie nel mondo industrializzato
mortalità/100.000 abitanti
160
140
120
100
80
60
40
20
Malattie infettive e parassitarie
del mondo industrializzato
sulfanilamide
clorochina
benzilpenicillina
streptomicina
eritromicina
ampicillina
cefalotina
aztreonam
imipenem
aciclovir
ceftriaxone
cefpiroma
?
0
1920 1930 1940 1950 1960 1970 1980 1990 2000 2010
anno
Le 10 più importanti cause di morte negli Stati Uniti nel
1900 e 1997
Chemioterapia antimicrobica
• Chemioterapici: farmaci ottenuti per sintesi
chimica (es. sulfamidici)
• Antibiotici: farmaci di origine naturale o
semisintetica prodotti
come metaboliti
secondari da varie specie di microrganismi,
funghi ed attinomiceti capaci di inibire la
crescita di (batteriostatici) o di uccidere
(battericidi) altri microrganismi (anche
farmaci la cui struttura è simile a quelli
naturali, ma di origine totalmente sintetica)
Chemioterapia
antimicrobica
• Poiché il bersaglio della
terapia
chemioterapica
antimicrobica è l'agente
eziologico della malattia
infettiva (batterio, virus,
protozoo, micete o elminta)
i farmaci usati a questo
scopo sono "selettivi" e ben
si applica a queste molecole
il concetto di "tossicità
selettiva"
(Paul Erlich)
Principali bersagli della
chemioterapia nella cellula
procariotica ed eucariotica
FATTORI DI TOSSICITA’ SELETTIVA
• Azione batteriostatica: il farmaco impedisce
la moltiplicazione dell’agente patogeno (es.
sostanze cha alterano la sintesi proteica).
Agiscono su microorganismi in fase di attiva
moltiplicazione.
Le
difese
immunitarie
dell’organismo sono quelle che poi vincono
l’infezione.
• Azione battericida: il farmaco uccide l’agente
patogeno (e. sostanze che alterano la struttura
della parete batterica).
• Spettro d’azione: alcuni antibiotici
(es.
penicillina)
agiscono
prevalentemente sui batteri Gram+, altri
(es. l’isoniazide) agiscono solo sui
batteri della tubercolosi, altri (es. le
tetracicline) agiscono su un maggior
numero di agenti patogeni. Questi sono
chiamati antibiotici a largo spettro.
• Questi possono provocare pericolo di
“superinfezione” (es. da Candida) in
quanto la distruzione della normale flora
batterica può portare alla invasione delle
mucose da parte di batteri patogeni
Differenze molecolari tra cellule pro- ed eucariote
e possibili bersagli della terapia antimicrobica
Struttura
cellulare
Procarioti
Eucarioti
Farmaci
Membrana
cellulare
Pochi steroli
Molti steroli
Polimixina
Ribosomi
70S
80S
Parete cellulare
Peptidoglicano assenza
Macrolidi,
Lincomicina,
cloramfenicolo
β-lattamine,
vancomicina
Penicilline,
cefalosporine
Polimixine
Sulfamidici
Diaminopiridina
Inibitori della girasi
Nitroimidazoli
Rifampicina
Tetracicline
Aminoglicosidi
Cloramfenicolo
Macrolidi
Mupirocina
NH2
Antagonisti del folato
PABA
Sulfamidici (1935) e
Trimetoprim (1962)
SO2NH2
Spettro antimicrobico dei sulfamidici
(batteriostatici)
• Streptococco pyrogenes,
streptococco pneumoniae,
chlamydiae,
• shigelle*
*molti ceppi di Shigelle sono
resistenti
Effetti collaterali
• cristalluria, nausea, vomito,
reazioni di ipersensibilità (cute),
anemia emolitica (0.05%),
agranulocitosi.
Indicazioni terapeutiche tipiche dei Sulfamidici
Sono poco utilizzati
Sulfametoxazolo + Trimetoprim
Cotrimossazolo (Bactrim)
Il cotrimossazolo ha uno spetto più
ampio. Ha effetti battericidi
Resistenza minore
Effetti collaterali
nausea, vomito,
Stomatite, glossite
reazioni di ipersensibilità (cute),
anemia megaloblastica,
neutropenia, citopenia
Interazioni col Warfarin.
Indicazioni terapeutiche del Cotrimossazolo
Inibenti la sintesi della parete cellulare
Parete cellulare nelle specie Gram+ e Gram-
Inibenti la sintesi della parete cellulare
E’ il principale gruppo di antibiotici; all’interno di questa categoria i più
importanti sono la penicillina, le cefalosporine, la bacitracina, la
vancomicina ed altri più recenti. Inibiscono il processo di costruzione
del peptidoglicano un indispensabile componente della parete cellulare
dei batteri (in particolare di quelli Gram+).
La penicillina è il più rappresentativo degli antibiotici e se ne
considerano due categorie: naturale e semisintetica. Quella naturale è
ricavata direttamente da muffe.
Le seconde sono prodotte artificialmente o derivate dalla penicillina
naturale per modifica o aggiunta di radicali in grado di conferire nuove
proprietà
all’antibiotico
aumentandone
lo
spettro
d’azione
comprendendo anche i batteri Gram-.
Le cefalosporine sono una classe di antibatterici prodotti da un fungo
marino che presentano uno spettro d’azione battericida simile alla
penicillina semisintetica. Questi antibiotici, le penicilline e le
cefalosporine, vengono chiamati b-lattamici.
Formula di struttura della Penicillina G
Anello beta lattamico
Punto di idrolisi dalle beta-lattamasi
(resistenza batterica)
Gli antibiotici beta-lattamici inibiscono la sintesi
peptidoglicano, e bloccano la sintesi della parete batterica.
del
Sono antibiotici battericidi. Hanno pochi effetti sui batteri a
riposo, sono letali per i batteri in fase di moltiplicazione, poichè le
pareti batteriche non ben sintetizzate non permettono la vita dei
batteri in condizioni ipotoniche.
Indicazioni della penicillina G
Betalattamine e reazioni allergiche
INCIDENZA REAZIONI ALLERGICHE
PENICILLINA
1-10% dei trattati
CEFALOSPORINE
0,9-3,2% dei trattati
INCIDENZA REAZIONI ANAFILATTICHE
PENICILLINA
1/10.000 trattati
morte
1/50.000 - 1/100.000
CEFALOSPORINE
non determinata, ma definita molto rara
REATTIVITA’ CROCIATA
Reazioni allergiche alle CEFALOSPORINE in pazienti allergici alla PENICILLINA: 415%
•Ipersensibilità e manifestazioni allergiche con rash cutanei, dermatiti,
fino a shock anafilattico.
•Le penicilline e i loro prodotti catabolici possono legarsi alle proteine e
funzionare da apteni, stimolando la formazione di anticorpi.
•Allergia crociata tra penicilline e cefalosporine.
Effetti indesiderati delle penicilline
TIPO DI EFFETTO
INCIDENZA %
Reazioni locali (uso parenterale)
5-30
Disturbi gastroenterici (uso orale)
5-20
Tossicità immunoimmediata (esantemi,
dermatite esfoliativa, anemia emolitica,
eosinofilia, febbre)
Shock anafilattico
0,7-10
0,004-0,04
Disordini dell’emostasi (alterazioni fattori
coagulazione, trombocitopenia)
Rara
Nefrotossicità (insuff. renale oligurica e
non)
Rara
Epatotossicità (aumento transaminasi
sieriche)
0,002-5
Neurotossicità (eccitazione, tremori,
mioclonie, allucinazioni, convulsioni)
Dose dipendente
L’ampicillina (Amplital) è attiva nei confronti di
alcuni batteri Gram+ e Gram-, ma è inattivata dalle
penicillinasi.
Quasi tutti gli stafilococchi, il 50% dei ceppi di E.
coli e il 15% dei ceppi di Haemophilus influenzae
sono resistenti. L’eventualità di resistenza
dovrebbe quindi essere considerata prima di
scegliere l’ampicillina per il trattamento delle
infezioni; in particolare, non dovrebbe essere
impiegata per i pazienti ricoverati senza prima
aver fatto un antibiogramma che ne dimostri
l’efficacia in vitro.
L’ampicillina può essere somministrata per bocca,
ma ha bassa biodisponibilità, e l’assorbimento è
ridotto dalla presenza di cibo.
L’amoxicillina (Velamox, Zymox) è un derivato dell’ampicillina e ha uno
spettro antibatterico simile. Per bocca è assorbita meglio
dell’ampicillina e mostra concentrazioni plasmatiche e tessutali più alte;
inoltre l’assorbimento non è influenzato dalla presenza di cibo nello
stomaco.
Associazione amoxicillina e acido clavulanico
L’associazione
amoxicillina
e
acido
clavulanico
(Augmentin)
consiste
nell’unione di una penicillina con un
inibitore delle betalattamasi.
L’acido clavulanico da solo non ha
un’attività antibatterica significativa ma,
inattivando
le
betalattamasi,
non
permette la degradazione degli antibiotici
che normalmente sono un substrato di
questo enzima.
L’associazione dovrebbe essere riservata
al trattamento di infezioni probabilmente
o certamente causate da ceppi resistenti
all’amoxicillina
produttori
di
betalattamasi.
Cefalosporine
• Le cefalosporine (Cefacloro, Cefalexina) sono antibiotici ad
ampio spettro usati per il trattamento di setticemia, polmonite,
meningite, infezioni delle vie biliari, peritonite e infezioni delle
vie urinarie.
• Hanno tutte uno spettro antibatterico simile, nonostante i singoli
farmaci abbiano un’attività differente nei confronti di alcuni
microrganismi.
• La farmacologia delle cefalosporine è simile a quella delle
penicilline, con un’escrezione in prevalenza renale.
• Le cefalosporine penetrano in modo scarso nel liquido
cerebrospinale a meno che le meningi non siano infiammate; la
cefotaxima è comunque utilizzabile per le infezioni del sistema
nervoso centrale (per esempio la meningite).
• L’effetto indesiderato principale delle cefalosporine è
l’ipersensibilità; circa il 10% dei pazienti allergici alle penicilline
lo è anche alle cefalosporine.
• Ad alcune cefalosporine sono state associate emorragie causate
da un’interferenza con i fattori della coagulazione.
Attivi sulla membrana batterica
Ne fanno parte le polimixine, nistatina e
amfotericina B. Sono antibiotici battericidi che
agiscono sulla membrana batterica rendendola più
debole e facendo quindi fuoriuscire il contenuto
cellulare con la conseguente morte del batterio.
Alcuni di questi antibiotici sono sostanze abbastanza
tossiche e perciò se ne consiglia un uso locale.
La polimixina può essere utilizzata per via sistemica in
caso di gravi infezioni quali la sepsi.
Inibitori la sintesi proteica
Vi appartengono antibiotici antisettici, fanno parte a questo gruppo il
cloramfenicolo, le tetracicline, i macrolidi (eritromicina,
claritromicina, azitromicina) e gli aminoglicosidi (gentamicina,
amikacina, neomicina, tobramicina).
Sono gli antibiotici più largamente utilizzati per le infezioni
batteriche; essi vanno a colpire i batteri inibendo la sintesi delle
proteine. Più precisamente vanno ad impedire che le informazioni
genetiche contenute nell’RNAm vengano tradotte nei ribosomi e
vadano a formare la catena di aminoacidi. L’antibiotico più
rappresentativo di questa categoria è la streptomicina che ha la
caratteristica di essere attiva sui batteri resistenti alla penicillina e
ai sulfamidici. Il cloramfenicolo, l’eritromicina e le tetracicline sono
antibiotici con un largo spettro di azione che colpiscono batteri sia
Gram+ che Gram-, in particolare l’eritromicina è attiva su gran parte
dei batteri resistenti alla penicillina e alla streptomicina, e le
tetracicline non hanno effetto sui batteri dei generi Proteus,
Pseudomonas e Salmonella.
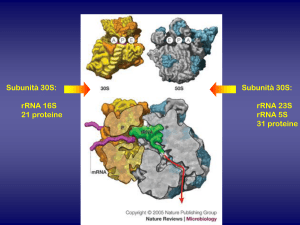
Bersagli ribosomiali di antibiotici
RIBOSOMA 70S
(procariotico)
30 S
RIBOSOMA 80S
(eucariotico)
TETRACICLINE
AMINOGLUCOSIDI
40 S
CLORAMFENICOLO
50 S
ERITROMICINA
CICLOEXIMIDE
PUROMICINA
60 S
Aminoglicosidi
Prodotti dagli actinomicetei (batteri del terreno) o
derivati semi-sintetici.
Attivi sui GramStreptomicina
Kanamicina
Neomicina
Gentamicina
Il ribosoma batterico a 70S differisce da quello
eucariotico a 80S.
Gli aminoglicosidi si legano alla subunità 30S del ribosoma
batterico e interferiscono col complesso di iniziazione
causando lettura sbagliata del mRNA.
Tetracicline
Sono prodotti naturali derivati da attinomiceti del
suolo, o derivati semisintetici
Clortetracicline (Aureomicina)
Oxytetracicline (Terramicina)
Doxicicline
Le tetracicline si legano alla subunità 30S del
ribosoma batterico. Prevengono il trasferimento
degli aminoacidi attivati al ribosoma, terminando la
sintesi proteica.
Sono assorbite in modo incompleto dopo
somministrazione orale. Tuttavia l’assunzione di
questi farmaci con il lette e derivati fa diminuire
l’assorbimento a causa della formazione di chelati
non assorbibili. Chelati si formano anche con altri
cationi.
Applicazioni terapeutiche delle tetracicline
La tossicità selettiva delle tetracicline come risultante
di una elettiva concentrazione nella cellula batterica
BATTERIO
Trasporto attivo
(proteine di trasporto)
Diffusione passiva
TETRACICLINE
Diffusione passiva
CELLULA
ANIMALE
Principali effetti tossici delle tetracicline
BERSAGLIO
TIPO
Apparato
gastrointestinale
Neusea, vomito, diarrea, stomatite, glossite, proctite
Fegato
Tossicità letale
Rene
> azotemia, sindrome di Fanconi, diabete insipido
nefrogenico
Cute
Fototossicità, onicolisi, rash
Denti
Colorazione, disgenesie
Ossa
Diminuzione temporanea accrescimento
Sangue
Anemia, neutropenia, eosinofilia, ritardata coagulazione
Metabolismo
Effetti catabolici
Superinfezioni
Candida, stafilococchi resistenti e batteri Gram-negativi
Allergia
Rash, orticaria, reazioni anafilattiche, edema
angioneurotico
Vari
> pressione endocranica, vertigini (minociclina)
Macrolidi
Anche i Macrolidi sono prodotti naturali degli
attinomiceti o sono derivati semi-sintetici. Si legano alla
subunità 50S del ribosoma batterico e bloccano l’uscita
della catena peptidica in formazione.
Eritromicina
azitromicina (Zithromax®),
claritromicina (Biaxin®) sono macrolidi prescritti
comunemente.
Classificazione dei macrolidi
in uso clinico
Naturali
Eritromicina
Oleandomicina
Spiramicina
Josamicina
Midecamicina
Semisintetici
Roxitromicina
Claritromicina
Fluritromicina
Diritromicina
Azitromicina
Miocamicina
Rokitamicina
Applicazioni terapeutiche dei macrolidi
Interazioni
farmacocinetiche
dell’eritromicina
Effetti indesiderati dei macrolidi
DISTURBI
GASTROENTERICI
dolori addominali, diarrea,
flatulenza, nausea, vomito,
(E 28%; R 3,1%; A 9,6%; C 8,7%)
REAZIONI ALLERGICHE
eruzioni cutanee
(0,5%)
EPATOTOSSICITA'
epatite colostatica
OTOTOSSICITA'
tinnito, sordità temporanea
REAZIONI LOCALI
somministrazione
parenterale
Fluorochinoloni
I fluorochinoloni bloccano l’azione dell’enzima
batterico DNA girasi che apre l’elica di DNA
batterico quiando l’elica viene aperta in preparazione
di replicazione, trascrizione o riparazione.
Gli Eucarioti non hanno la DNA girasi.
Entrano nelle cellule batteriche mediante l’azione di
porine.
Ciprofloxacin (Cipro®),
levofloxacin
moxifloxacin
Cipro è l’antibiotico di scelta per chi è stato esposto
all’antrace, anche se altri antibiotici sembrano
ugualmente efficaci.
Applicazioni terapeutiche dei fluorochinoloni
Inibenti il metabolismo degli acidi nucleici (DNA & RNA): sono
particolari antibiotici che interferiscono con il metabolismo degli acidi
nucleici sia delle cellule batteriche, sia delle cellule dell’organismo
ospite. Per questo motivo sono tossici anche per l’uomo e quindi
vengono raramente utilizzati. Di questo gruppo fanno parte due tipi di
antibiotici:
•inibenti la sintesi del DNA: gli antibiotici che fanno parte di
questo gruppo, come la mitomicina, agiscono impedendo che nella cellula
avvenga il processo di duplicazione del DNA;
•inibenti la sintesi dell’RNA: gli antibiotici di questo gruppo,
come l’actinomicina e la rifampicina, agiscono impedendo che nella
cellula abbia luogo la trascrizione del DNA, il processo durante il
quale le informazioni genetiche del DNA vengono trascritte sotto
forma di RNA.
In quest’ultima categoria l’unico antibiotico a non risultare tossico per
l’uomo è la rifampicina (utilizzata nella tubercolosi), in quanto inibisce
la sola RNA-polimerasi batterica, l’enzima che nei batteri dà luogo alla
trascrizione del DNA.
Meccanismo d’azione dei principali antimicrobici
Classe di antimicrobici
β-lattamici
(penicilline, cefalosporine,
ecc.);
Peptidici (vancomicina,
teicoplanina, bacitracina)
Meccanismo d’azione
Polipeptidi ciclici
(polimixina)
Chinolonici
(Ciprofloxacina, ac.
Nalidissico)
Alterazione della membrana
cellulare
-Inibizione transpeptidasi, e
legame PBP
alterazione
struttura parete cellulare e lisi;
- inibizione sintesi parete
cellulare (vari mecc.)
Inibizione replicazione DNA
per interazione con DNA girasi
e topoisomerasi IV (continua)
Meccanismo d’azione dei principali antimicrobici
Classe di antimicrobici
Tetracicline
Meccanismo d’azione
Macrolidi (Eritromicina,
Claritromicina)
Blocco sintesi proteica per
legame subunità ribosomiale
50S
Blocco subunità ribosomiale
30S ed errori nella traduzione
mRNA proteica
Amminoglicosidi
(Streptomicina,
neomicina, gentamicina)
Blocco sintesi proteica per
legame subunità ribosomiale
30S
(continua)
Meccanismo d’azione dei principali antimicrobici
Classe di antimicrobici
In.sintesi ac. nucleici
(Sulfamidici)
(Trimetoprim)
Meccanismo d’azione
Rifamicine
(rifampicina)
Nitroimidazoli
(Metronidazolo)
Inibizione sintesi RNA per
DNA-RNA polimerasi
In. sintesi tetraidrofolico
In.diidropteroato sintetasi;
In.deidrofolato reduttasi
Danni sul DNA
β-lattamine, aminoglicosidi,
Tetracicline
β-lattamine,sulfamidici,
macrolidi
MECCANISMI DI CHEMIORESISTENZA BATTERICA
• MODIFICA DEL BERSAGLIO
•
•
•
•
•
Betalattamine
Macrolidi
Cotrimoxazolo
Glicopeptidi
Fluorochinoloni
• RIDOTTA PERMEABILITA’ (porine, efflusso)
•
•
•
•
•
•
Fluorochinoloni
Betalattamine
Macrolidi
Tetracicline
Aminoglucosidi
Cotrimoxazolo
• INATTIVAZIONE ENZIMATICA
• Betalattamine
• Aminoglucosidi
• Macrolidi
Meccanismi di sviluppo della
“resistenza” ai farmaci antimicrobici
• Uso improprio dei farmaci in medicina
umana e veterinaria;
• Uso improprio di farmaci per scopi
non terapeutici.
Uso improprio di farmaci
antimicrobici per scopi non
terapeutici
Uso improprio di farmaci antimicrobici in
medicina umana e veterinaria
• Antibiotico inadeguato;
• Dose inefficace o scarsamente efficace;
• Durata della terapia non congrua con
l’abbattimento della popolazione patogena;
• Uso inadeguato di antimicrobico in assenza
di elementi clinici e/o epidemiologici di
infezione;
• Uso di antimicrobici in profilassi in quelle
condizioni in cui non ne è documentata
l’efficacia.
Antibiotic resistance spread in food
• Nutritive and therapeutic treatment of farm animals with antibiotics,
amounting to half of the world's antibiotic output, has selected for
resistant bacteria that may contaminate the food produced.
Antibiotic-resistant enterococci and staphylococci from animals are
found in food when they survive the production processes, as in raw
cured sausages and raw milk cheeses.
• When analysed in 1991 and 1995, this cheese brand had also
contained different enterococci resistant to tetracycline,
chloramphenicol, gentamycin, penicillin, erythromycin, lincomycin
and vancomycin
• This cheese was the source of a Listeria monocytogenes epidemic
in 20 patients in 19955………..
• To preserve the life-saving potential of antibiotics, the spread of
resistance genes at all levels must be stopped. Distribution routes
like those between animals, food and consumers have to be
interrupted. In this example, it could be achieved by using
pasteurized milk for cheese making. The situation might also be
helped by stopping the inappropriate use of the selective antibiotics
in animal husbandry……
•
VINCENT PERRETEN, FRANZISKA SCHWARZ, LUANA CRESTA, MARIANNE BOEGLIN, GOTTFRIED DASEN & MICHAEL TEUBER
Laboratory of Food Microbiology, Department of Food Science, Swiss Federal Institute of Technology, ETH-Zentrum, CH8092 Zurich, Switzerland
e-mail:
[email protected]
Nature 389, 801 - 802 (1997)
Efficacia clinica di un farmaco
CHEMIOTERAPICO
• a) Tipo di meccanismo d'azione
• b) Distribuzione agente antimicrobico nella
sede di infezione
• c) Raggiungimento di concentrazioni
efficaci (>MIC) per tempi adeguati
• d) Acquisita resistenza delle specie
microbiche farmaco-sensibili
Chemioprofilassi antimicrobica
preoperatoria in chirurgia
•
a.
b.
c.
d.
Fattori di prevenzione delle infezioni secondarie da
intervento chirurgico:
Tecnica operatoria;
Selezione del paziente;
Immunocompetenza dell’ospite;
Entità contaminazione batterica nel campo operatorio;
e. Adeguati livelli tissutali di antimicrobici (>MIC)
attivi nei confronti di agenti batterici più
frequentemente responsabili di infezione delle
ferite operatorie per ciascun tipo di intervento
chirurgico.
Rischio di complicanze infettive in
funzione del tipo di chirurgia
Tipo di chirurgia
•
•
•
•
•
•
Otorinolaringoiatra
Gastrica
Colorettale
Urologica
Ginecologica
Ortopedica
Infezione %
Ferita
a distanza
• 10
10
• 17
30
• 23
47
• 12
37
• 8
25
• 10
10
Chemioprofilassi antimicrobica in
chirurgia
Perchè…..
• Rischio di infezione >5%
• Estrema gravità delle complicanze
• Pazienti immunodepressi
Chemioprofilassi antimicrobica in
chirurgia
……….con quale farmaco ideale.
• Largo spettro;
• Bassa tossicità ed alta tollerabilità;
• Parametri farmacocinetici favorevoli (alta
penetrabilità nei tessuti, lunga emivita);
• Battericida dose-dipendente;
Chemioprofilassi antimicrobica in
chirurgia
…………e quando…..
• Somministrazione subito prima
dell’intervento (1 h).
Chemioprofilassi antimicrobica in
chirurgia
Sintesi della parete
Duplicazione del DNA (DNA girasi)
RNA polimerasi DNA-dipendente
Sintesi proteica
Metabolismo
dell’acido folico
(inibitori del ribosoma 50S)
Sintesi proteica
(inibitori del ribosoma 30S)
Membrana cellulare