Metilazione del DNA
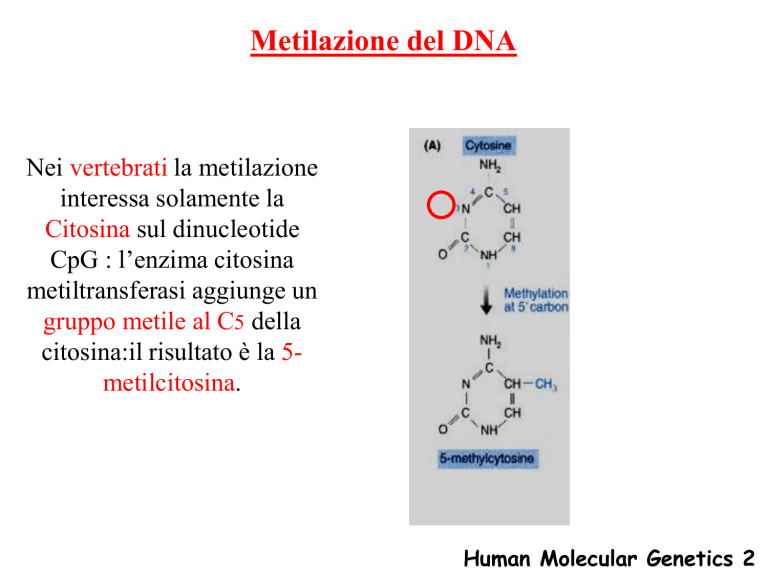
Nei vertebrati la metilazione
interessa solamente la
Citosina sul dinucleotide
CpG : l’enzima citosina
metiltransferasi aggiunge un
gruppo metile al C5 della
citosina:il risultato è la 5metilcitosina.
Human Molecular Genetics 2
Metilazione del DNA
Le sequenze CpG sono sotto-rappresentate nel genoma (probabilmente
per la tendenza della 5-metilcitosina a venire deaminata e mutata in T)
ma abbondanti nelle regioni promotrici dei geni
In cellule non embrionali, 80% dei CpG sono metilati, ad eccezione
delle isole CpG dei promotori
Dnmt1 ha particolare affinità per le sequenze emi-metilate: tende
quindi a metilare il nuovo filamento che si è formato su uno stampo
metilato-> mantenimento del pattern di metilazione
Corepressori
HDAC 1
HDAC 2
MeCP2
Repres.
CH3 CH3 CH3 CH3
Deacetilazione delle lisine di H3 e H4
Metilazione e regolazione genica:
Dnmt metilano il DNA
Il DNA metilato è legato da proteine che legano il metile
(MeCP2, MBD1-4)
Queste a loro volta sono in grado di reclutare diversi HDAC ->
repressione della trascrizione
Inibitori delle HDAC: una nuova terapia anti-cancro
Diverse sostanze che causano differenziamento, arresto della crescita
e/o apoptosi di cellule trasformate -> inibitori di HDAC
(es. DMSO, Tricostatina A (TSA), butirrato)
Questi inibitori causano arresto del ciclo cellulare in G1 o G2,
differenziamento e/o apoptosi in vitro, documentati in tutti i tipi
cellulari trasformati incluse linee cellulari derivate sia da tumori
ematologici (leucemie, linfomi, mielomi) che epiteliali (tumore dei
polmoni, delle ovaie, del seno, della prostata)
Le concentrazioni biologicamente attive correlano con quelle richieste
per causare accumulazione di istoni acetilati
SI IGNORA quali siano gli HDAC la cui attività deve essere bloccata
Gli inibitori causano aumento dell’ acetilazione sugli istoni (H2A,
H2B, H3 e H4) anche in cellule normali, ma l’attività di soppressione
della crescita sembra essere limitata alle cellule trasformate.
Geni bersaglio:
CDKN1A (codificante per l’inibitore dell’attività cinasica ciclinadipendente p21/WAF1) (tramite un sito di SP1 sul promotore)
CDKN2A (p16)
Ciclina E
Ingestione di fibre vegetali non digeribili
Nella parte terminale dell’intestino vengono
usate come fonte di energia da batteri simbionti
Formazione di acido butirrico come prodotto
CH3CH2CH2COOH
Costituisce la fonte energetica primaria delle cellule del colon
La metilazione del promotore e' uno dei meccanismi
principali coinvolti nell'inattivazione di geni oncosoppressori
Nel 10% dei tumori colorettali sporadici e’ inattivato il gene
responsabile della sintesi di una proteina addetta al
“mismatch repair” (MLH1)
Mismatch repair : riparo di una coppia di basi male appaiata
Es. T/G probabilmente a causa di una mutazione
Cellule tumorali del colon mostrano una ipermetilazione del
Promotore di MLH1 che e’ cosi inattivo
Trattamento combinato con 5-azadeossicitidina e
butirrato
Ipometilazione di MLH1
Espressione del gene che codifica per MLH1
Apoptosi
DAF
Normale
DAF
Tumorale
DAF
DAF
DAF
La presenza di DAF nelle cellule tumorali del
Colon rende inefficace il sistema del Complemento
EFFETTO DEL BUTIRRATO SUL mRNA di DAF
EFFETTO DEL BUTIRRATO
SULLA PROTEINA DAF
EFFETTO DEL BUTIRRATO SULL’ATTACCO DEL COMPLEMENTO
EFFETTO DEL BUTIRRATO SUL PROMOTORE di DAF
EFFETTO DEL
BUTIRRATO
SULLA STABILITA’
DEL mRNA di DAF
Cellule tumorali del colon sembrano avere
una ipometilazione
Di RB1 (una proteina regolatrice del
ciclo cellulare)
Il butirrato aumenta la metilazione di
RB1
Quali sono i mediatori?
Kruppel-like factor-4 (KLF4/GKLF) e’ un fattore di
trascrizione che mostra proprieta’ simili a quelle del
butirrato in cellule del colon
QuickTime™ and a
YUV420 codec decompressor
are needed to see this picture.
-Il butirrato aumenta l’mRNA di KLF4
-Questo aumento e’ dovuto ad una maggiore attivita’ del promotore
-HDAC (Istone Deacetilasi) inibisce questo aumento
Fibre alimentari
Butirrato
KLF4
Apoptosi
Acetilazione del promotore KLF4