ADF Semeiotica
Potassio
E.Fiaccadori
[email protected]
Dipartimento di Clinica Medica Nefrologia
& Scienze della Prevenzione
Potassio
•
•
•
•
Principale catione intracellulare (K+)
Peso molecolare 39
Range valori normali 3.5 – 5.0 mEq/L (o mmol/L)
Partecipa alla regolazione dell’attività elettrica
cellulare
Il potassio nell’alimentazione umana
Il potassio è il principale catione intracellulare
(per il 99% è contenuto nelle cellule)
Nelle cellule, il
potassio è legato a
differenti anioni
(proteine, fosfati,
bicarbonato etc),
oltre che al
glicogeno
Distribuzione del potassio nell’organismo
La maggior parte del pool potassico dell’organismo
è contenuta nelle cellule dei muscoli scheletrici
Pool potassico
45-50 mEq/Kg
Valori di potassiemia
determinati da:
• Apporto di K
• Distribuzione intraextracellulare
• Escrezione urinaria
Rapporti tra potassiemia e pool potassico
Per ogni
riduzione della
potassiemia di
0.3 mEq/L, il
deficit
prevedibile è
circa di 100 mEq
(quantità
indicativa)
La distribuzione cellulare del potassio è mantenuta dalla Na-K-ATPasi
Omeostasi del potassio:
due componenti fondamentali
• Distribuzione extra-intracellulare
(Bilancio interno)
• Scambio con l’esterno (Bilancio
esterno)
Entrambe le componenti sono
essenziali per il mantenimento
dei valori normali di potassiemia
Regolazione della potassiemia
Due strategie di controllo della potassiemia:
- In acuto: meccanismi cellulari
(redistribuzione tra intra ed extracellulare)
- In cronico: meccanismi renali di
escrezione (aldosterone)
Redistribuzione cellulare del potassio
e adattamento ad un carico acuto
Nel soggetto normale un carico di
potassio provoca modeste variazioni
della potassiemia, che sono comunque
sufficienti ad attivare i meccanismi di
compenso acuti e cronici
Na-K-ATPasi e distribuzione del potassio
La maggior parte dei
fattori
che
influenzano
la
distribuzione
del
potassio
agisce
direttamente
o
indiretamente sulla
Na-K-ATPasi (ad es.
ormoni e farmaci
adrenergici)
La somministrazione di glucosio determina ingresso
di K nelle cellule (se l’insulina è presente e funziona)
Agenti adrenergici e potassiemia
L’acidosi (metabolica) aumenta la
fuoriuscita di K dalle cellule
La somministrazione di bicarbonato riduce la
potassiemia nel soggetto con acidosi metabolica
Il danno e/o la lisi cellulare determinano
fuoriuscita di K dalle cellule
•
•
•
•
•
•
Ischemia
Trauma
Catabolismo
Chemioterapia
ipotermia
Esercizio massimale in
condizioni climatiche
estreme
K out
L’anabolismo determina ingresso di K nelle cellule
L’anabolismo promuove
l’ingresso di potassio
nelle cellule, ma una
volta ricaricati i depositi
cellulari
di
K,
il
sovrappiù
viene
eliminato nelle urine
inutile
introdurre
quantità eccessive di K
Bilancio esterno del potassio
Il controllo a medio e lungo termine del bilancio del
potassio dipende dal rene (bilancio esterno del K)
Il principale sito renale di regolazione del bilancio
del potassio è il nefrone distale (tubulo collettore
corticale)
Il
tubulo
collettore
corticale,
per
effetto
dell’aldosterone, è in grado di eliminare o
conservare il potassio a seconda delle necessità,
mantenendo valori di potassiemia normali
Controllo della secrezione di aldosterone
potassiemia
Rene e aldosterone: un meccanismo a grande
capacità per l’adattamento al carico di K
Conservazione del potassio
• In caso di necessità, il rene può eliminare
completamente il potassio dalle urine, oppure
ne può eliminare quantità elevate
• nel paziente ipopotassiemico la potassiuria
dovrebbe essere praticamente assente, e cioè
< 5 mEq/L (se i meccanismi renali di
conservazione del K sono integri)
• non è possibile avere iperpotassiemia se i
meccanismi renali di eliminazione del K sono
integri (compresa la risposta all’aldosterone),
Rene e potassio
Il
potassio
è
liberamente
filtrato
nel glomerulo
Viene completamente
riassorbito nel tubulo
prossimale e distale
In
base
alle
necessità,
di
eliminazione,
viene
secreto a livello del
tubulo
collettore
corticale
Modelli cellulari del
trasporto di potassio
lungo il nefrone: a livello
basolaterale i
trasportatori sono simili,
mentre a livello apicale
differiscono a seconda
delle cellule prese in
considerazione
Meccanismo di secrezione del K nel collettore
Tre tappe:
1
1.
Nelle
cellule
principali
del
collettore corticale, la pompa
Na-K-ATPasi
mantiene
una
concentrazione elevata di K e
bassa di Na l’ingresso di Na
dal lume è favorito
2.
Il sodio entra nella cellula
attraverso i canali del sodio
luminali, seguendo il gradiente
di concentrazione. Il movimento
di Na+, non accompagnato da Clche resta nel lume, crea un
gradiente
elettrico
lumenegativo (trasporto eletrogenico
di Na+)
3.
Il K+ esce dalle cellule verso il
lume
utilizzando
dei
canali
specifici (canali del potassio),
seguendo
sia
il
gradiente
elettrico che il gradiente di
concentrazione secrezione K+
2
Cl-
3
Controllo dell’escrezione renale di K (I°)
•
•
•
•
Aldosterone e attività mineralcorticoide
Flusso distale
Potassiemia
Anioni nonriassorbibili
L’aldosterone viene prodotto nella corticale
surrenalica; il precursore è il colesterolo
Effetti cellulari dell’aldosterone
(cellule principali del t. collettore corticale)
• Aumento del numero di pompe Na-K-ATPasi a
livello del lato basolaterale della cellula tubulare
• Aumento del numero dei canali del sodio a livello
del lato luminale della cellula tubulare
• Aumento del gradiente elettrico per il
riassorbimento del K
I mineralcorticoidi hanno un effetto sull’escrezione
di potassio sovrapponibile a quello dell’aldosterone
( un eccesso di aldosterone o mineralcorticoidi
provoca aumento dell’eliminazione di K)
L’aldosterone è in grado di regolare in maniera
separata l’escrezione di sodio e di potassio
• Ciò che conta ai fini della regolazione differenziata
è il flusso al nefrone distale, a sua volta
influenzato dallo stato dei volumi. Due possibilità:
1)
Se l’aldosterone è elevato perché c’è
deplezione di volume risparmio di Na,
secrezione di K invariata o ridotta (essendo il
flusso basso, anche se l’aldosterone è elevato,
il gradiente è sfavorevole all’uscita di K dalle
cellule)
2) Se l’aldosterone è elevato perché c’è
iperpotassiemia, e i volumi sono normali
flusso nel nefrone distale normale
aumentata escrezione di K
Controllo dell’escrezione renale di K (II°)
•
•
•
•
Aldosterone e attività mineralcorticoide
Potassiemia
Flusso nel tubulo distale (sodio e acqua)
Anioni nonriassorbibili
Potassiemia e secrezione renale di potassio:
l’aumento della potassiemia aumenta l’escrezione
di K indipendentemente dall’effetto dell’aldosterone
• Aumento del numero di pompe Na-K-ATPasi a livello del
lato basolaterale
• Aumento del numero dei canali del sodio a livello del
lato luminale
• Aumento del numero dei canali del potassio, con
facilitazione dell’escrezione di potassio
• Aumento del gradiente elettrico che favorisce la
diffusione del K nel lume tubulare
Controllo dell’escrezione renale di K (III°)
•
•
•
•
Aldosterone e attività mineralcorticoide
Potassiemia
Flusso nel tubulo distale
Anioni nonriassorbibili
L’escrezione urinaria di K aumenta all’aumentare del
flusso urinario a livello del tubulo distale
Controllo dell’escrezione renale di K (IV°)
•
•
•
•
Aldosterone e attività mineralcorticoide
Potassiemia
Flusso nel tubulo distale
Anioni nonriassorbibili
La presenza di anioni
non riassorbibili nel
lume tubulare
aumenta la negatività
luminale e quindi il
gradiente elettrico tra
cellule tubulare e
lume è favorita la
diffusione del K dalla
cellula al lume
Acid/base balance and K+ secretion
ACUTE ACIDOSIS: impairs K+ secretion
• inhibition of Na+/K+-ATPase
• decreased apical permeability to K+
CHRONIC ACIDOSIS: increases K+ secretion
• Na+/K+ ATPase inhibition decreases proximal water
and NaCl absorption
• increased tubular flow, increased distal K+ secretion
• reduced ECF stimulates aldosterone secretion
• high plasma [K+] stimulates aldosterone secretion
Ipopotassiemia
• K < 3.5 mEq/L (o mmol/L)
• Può essere dovuta a
redistribuzione cellulare, ridotto
apporto alimentare, aumentate
perdite (renali o extrarenali)
Ipopotassiemia: diagnosi differenziale (I°)
1
2
3
Perdite extrarenali di K
• Cause legate a patologie del tratto
gastroenterico (più spesso diarrea)
• Il rene è in grado di ridurre l’escrezione
potassica a < 5 mEq/die
• Soggetti a rischio: etilisti, anziani,
anoressia nervosa
Ipopotassiemia: diagnosi differenziale (II°)
Composizione elettrolitica dei
fluidi gastroenterici
HCO3
mEq/L
Na
mEq/L
K
mEq/L
Cl
mEq/L
plasma
22-26
135-145
3.5-5
98-106
bile
30-40
130-140
4-6
95-105
pancreas
80-100
130-140
4-6
40-60
Int tenue
80-100
130-140
4-6
40-60
Colon
30-50
80-140
25-45
80-100
Ipopotassiemia da perdite renali di K: ruolo centrale della
potassiuria (valori inappropriatamente elevati) e della
valutazione dell’equilibrio acido-base nella diagnosi differenziale
Fattori che influenzano l’escrezione renale di K
• Flusso di preurina nel nefrone distale
• Aldosterone e attività mineralcorticoide
• Anioni nonriassorbibili
Meccanismi di aumentata escrezione
urinaria di K nelle condizioni di aumentata
perdita renale di potassio
Aumento flusso di preurina nel nefrone distale
-
Diuretici
Sindrome di Bartter
Sindrome di Gitelman
Aumento anioni nonriassorbibili nel lume tubulare
-
chetoacidosi diabetica
vomito
Acidosi tubulare renale
toluene
Aumentata attività mineralcorticoide
-
iperaldosteronismo primitivo
Sindrome di Cushing
Iperplasia surrenalica congenita
Iperreninismo
pseudoiperldosteronismo
Perdite renali di K secondarie a diuretici
e alle sindromi di Bartter e Gitelman
Aumentata Perdita di Na
Diuretici tiazidici
Diuretici dell’ansa
B
A
Aumentata
secrezione di K
Meccanismi di aumentata escrezione
urinaria di K nelle condizioni di aumentata
perdita renale di potassio
Aumento flusso di preurina nel nefrone distale
-
Diuretici
Sindrome di Bartter
Sindrome di Gitelman
Aumento anioni nonriassorbibili nel lume tubulare
-
Chetoacidosi diabetica
Vomito
Acidosi tubulare renale prossimale
Farmaci e tossici (toluene)
Aumentata attività mineralcorticoide
-
iperaldosteronismo primitivo (sindrome di Conn, iperplasia
surrenalica, carcinoma del surrene)
Sindrome di Cushing
Iperplasia surrenalica congenita (deficit di 17α-idrossilasi o 11βidrossilasi)
Iperreninismo (stenosi dell’arteria renale)
Pseudoiperldosteronismo (liquerizia, carbenoxolone etc.)
Anioni non riassorbibili
• La presenza nel lume di anioni non riassorbibili (a
differenza del Cl che è in parte riassorbibile) che
accompagnano il Na, rende ancor più negativo il lume in
caso di riassorbimento di quest’ultimo
• Nel lume tubulare di conseguenza passeranno quantità
maggiori di K
• Gli anioni non riassorbibili in causa sono i corpi chetonici
(chetoacidosi diabetica), il bicarbonato (vomito, acidosi
tubulare
prossimale),
farmaci
(antibiotici
come
piperacillina
e
ticarcillina),
tossici
(ippurato
nell’intossicazione da toluene)
Meccanismi di aumentata escrezione
urinaria di K nelle condizioni di aumentata
perdita renale di potassio
Aumento flusso di preurina nel nefrone distale
-
Diuretici
Sindrome di Bartter
Sindrome di Gitelman
Aumento anioni nonriassorbibili nel lume tubulare
-
chetoacidosi diabetica
vomito
Acidosi tubulare renale
toluene
Aumentata attività mineralcorticoide
-
iperaldosteronismo primitivo (sindrome di Conn, iperplasia
surrenalica, carcinoma del surrene)
Sindrome di Cushing
Iperplasia surrenalica congenita (deficit di 17α-idrossilasi o 11βidrossilasi)
Iperreninismo (stenosi dell’arteria renale)
Pseudoiperldosteronismo (liquerizia, carbenoxolone etc.)
Eccesso di mineracorticoidi
• Ipopotassiemia
• Alcalosi metabolica
• Ipertensione art.
Meccanismo dell’aumento dell’attività mineracorticoide nel
deficit congenito di 11ß-HSD o nell’eccesso di liquerizia
•
•
•
Il cortisolo in vivo esercita
scarso effetto mineralcorticoide
nonostante l’elevata affinità per
il recettore dell’aldosterone, per
la presenza nelle cellule tubulari
della
11ß-idrossisteroidedeidrogenasi (11ß-HSD), che
converte il cortisolo in cortisone
(che
non
esercita
azione
mineralcorticoide)
L’enzima
è
inibito
competitivamente
dall’acido
glicirretinico contenuto nella
liquerizia
Esistono anche sindromi da
apparente
eccesso
di
mineralcorticoidi,
dovute
a
deficit congenito dell’enzima
Ipopotassiemia da aumentata attività mineralcorticoide: il paziente è
un soggetto con ipertensione arteriosa nel quale la diagnosi
differenziale è basata sui valori di aldosterone, PRA e cortisolemia
I deficits di 11β-idrossilasi e di 17α-idrossilasi
determinano eccesso di mineralcorticoidi
vomitus
Il gradiente transtubulare di potassio per
distinguere perdite renali da perdite extrarenali
• Un gradiente > 2
è compatibile con
perdite renali di K
Ipopotassiemia: sintomi e segni
• Il potassio è critico per la generazione dei
potenziali di membrana nelle cellule eccitabili
(cellule nervose e muscolari)
• la clinica dell’ipopotassiemia, al di là dei
segni e sintomi specifici delle patologie che si
associano allo squilibrio (per es. sindrome di
Cushing), sarà caratterizzata soprattutto da
astenia muscolare e aritmie cardiache
• Un fattore importante, oltre alla gravità della
deplezione potassica, è rappresentato dal
ritmo di instaurazione dello squilibrio
Sindrome di Cushing
Sintomi e segni
• Obesità centrale
• Accumulo di grasso
dorsocervicale e
sopraclavicolare
• Cute sottile
• Strie
• Rallentata cicatrizzazione
ferite
• Ipertensione art.
• Acne, irsutismo, amenorrea
• Osteopenia
• Debolezza muscolare
• Depressione, psicosi
Laboratorio
•
•
•
•
•
•
Ipopotassiemia
Alcalosi metabolica
Iperglicemia
Iperlipemia
Ipofosfatemia
ipercalciuria
Ipopotassiemia e attività
elettrica delle cellule
Potenziale d’azione nelle cellule eccitabili
Effetti dell’ipopotassiemia sul potenziale d’azione:
minore eccitabilità cellulare (singola cellula)
Ipopotassiemia: sintomi e segni muscolari
Muscolo scheletrico
• Debolezza
• Mialgie
• Crampi
• Parestesie
• Paralisi
• Dolore
• Aumento CPK, LDH,
mioglobina
• Rabdomiolisi
• Insuff. ventilatoria
Muscolo liscio
• Ileo paralitico
• Stipsi
• Distensione
addominale
• Anoressia
• Vomito
QRS
Onda P
ST
T
- P = attivaz. atriale
- QRS = attivaz. ventricoli
- T = ripolarizz. ventricoli
ECG nell’ipopotassiemia
• Onde T appiattite
• Depressione ST
• Onda U prominente
Depressione ST
Onda U
Aritmie da ipopotassiemia
•
•
•
•
•
Extrasistoli atriali
Extrasistoli ventricolari
Tachiaritmie sopraventricolari
Tachiaritmie ventricolari
Aumentato rischio di aritmie
da intossicazione digitalica
Iperpotassiemia
• Potassio > 5 mEq/L (o 5 mmol/L)
• Può essere dovuta ad aumentato apporto
(raramente come meccanismo isolato),
redistribuzione cellulare (fuoriuscita di K),
ridotta escrezione renale
Una iperpotassiemia acuta è più spesso
dovuta al concorso di varie cause (ruolo
centrale della funzione renale)
Una iperpotassiemia cronica è sempre
dovuta ad una ridotta escrezione renale
Aumentato apporto di K come
causa di iperpotassiemia
•
•
•
Aumentato apporto per
os: causa rara in assenza
di riduzione della
funzione renale
(necessaria l’ingestione
rapida di almeno 150
mEq di K)
Notevole capacità di
adattamento dei
meccanismi di escrezione
renale
Inappropriato apporto
e.v.: più frequente,
soprattutto nei pazienti
ospedalizzati (soluzioni
per parenterale e farmaci
contenenti potassio)
Il danno e/o la lisi cellulare possono
Determinare iperpotassiemia
•
•
•
•
•
•
Ischemia
Trauma
Catabolismo
Chemioterapia
ipotermia
Esercizio massimale in
condizioni climatiche
estreme
K out
Iperpotassiemia
Fattori in causa per una
adeguata escrezione renale di K
• Aldosterone e attività mineralcorticoide
• Tubulo collettore corticale funzionante
• Flusso di preurina nel tubulo distale (apporto
di Na al tubulo distale)
Meccanismi renali di inadeguata
eliminazione di potassio (I°)
flusso preurina
aldosterone
Cellula principale
normofunzionante
Meccanismi renali di inadeguata
eliminazione di potassio (II°)
flusso preurina
aldosterone
Cellula principale
normofunzionante
Meccanismi renali di inadeguata
eliminazione di potassio (III°)
flusso preurina
aldosterone
Cellula principale
normofunzionante
Meccanismi renali di inadeguata
eliminazione di potassio (IV°)
flusso preurina
aldosterone
Cellula principale
normofunzionante
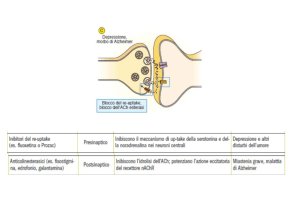
Farmaci che provocano iperpotassiemia interferendo
con l’asse renina-angiotensina-aldosterone
•
•
•
FANS: bloccano la sintesi di
prostaglandine.
Poiché
le
prostaglandine stimolano il
rilascio di renina, i FANS
possono
provocare
iperpotassiemia inibendo il
rilascio di renina
ACE inibitori: bloccano il
passaggio da Ang I a Ang II.
Ang
II
è
uno
stimolo
importante per il rilascio di
aldosterone.
Antagonisti Ang II: l’inibizione
dell’azione dell’Ang II a livello
del
surrene
riduce
la
produzione di aldosterone
Il gradiente transtubulare di potassio nell’iperpotassiemia
• Un gradiente >
10 è compatibile
con cause renali
di iperpotassiemia
Segni e sintomi dell’iperpotassiemia
Effetti dell’iperpotassiemia sul potenziale d’azione: maggiore
eccitabilità cellulare e successivamente ineccitabilità
(depolarizzazione al di sotto del potenziale soglia)
Iperpotassiemia: alterazioni ECG
K > 6 mEq/L: iniziale incremento della velocita’ di
ripolarizzazione l’iperpotassiemia aumenta la permeabilita’ di
membrana al K onde T alte ed appuntite (T a tenda),
accorciamento QT
K > 7 mEq/l: depolarizzazione della membrana al di sotto del
potenziale soglia riduzione del potenziale di membrana
inattivazione parziale dei canali del Na rallentamento della
depolarizzazione disturbi di conduzione intra-atriali ed
intraventricolari
# scomparsa dell’onda P
# allargamento QRS
K > 8 mEq: arresto cardiaco (BAV III°) o fibrillazione
ventricolare
La tossicita’ cardiaca da iperpotassiemia e’ aggravata da:
- intossicazione digitalica
- ipocalcemia
- ipomagnesiemia
- iposodiemia
- acidosi
ECG nell’iperpotassiemia