Lezione: aldeidi e chetoni
Il gruppo funzionale carbonilico
Nomenclatura
Proprietà fisiche
Principali reazioni
Reazioni con HCN
Reazioni con alcoli
Reazioni con tioli
Reazioni con ammine
Tautomeria cheto-enolica
Condensazione aldolica
Reazioni di ossidazione e riduzione
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
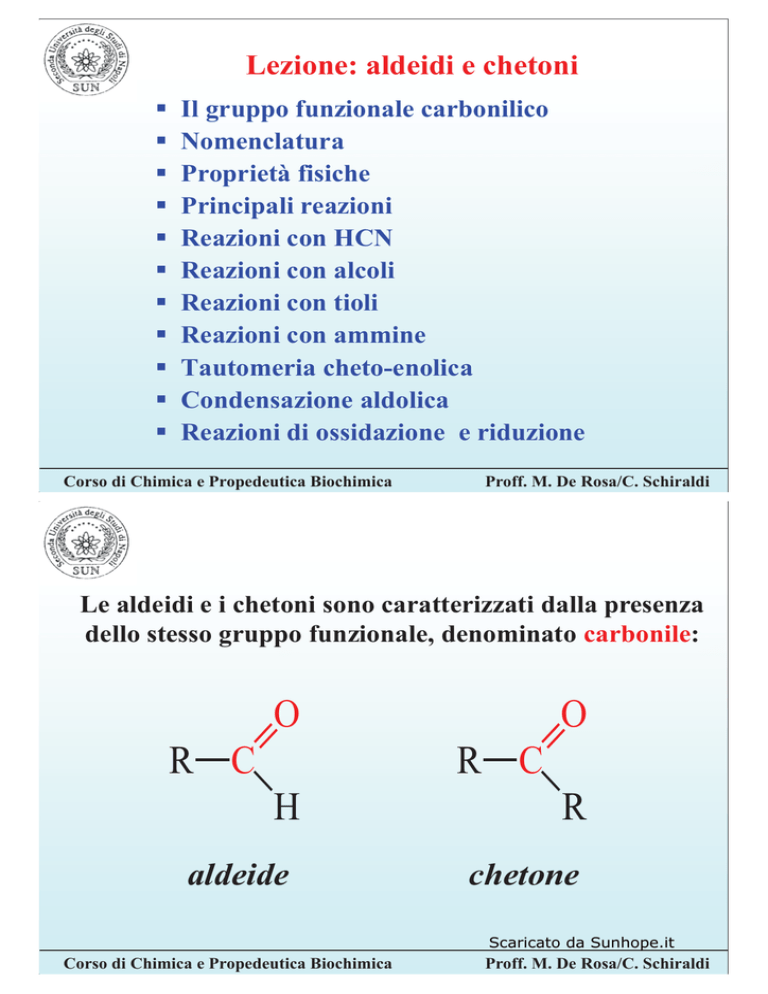
Le aldeidi e i chetoni sono caratterizzati dalla presenza
dello stesso gruppo funzionale, denominato carbonile:
O
R C
O
R C
H
aldeide
R
chetone
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
S
V
R2
R1
xy
¾L’atomo di carbonio è ibridato sp2
¾Il doppio legame carbonio-ossigeno è polarizzato
a causa dell’elettronegatività dell’ossigeno
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Gruppo funzionale carbonilico
O
R C
O
R C
R
R
Risonanza fra due forme limite
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
NOMENCLATURA delle ALDEIDI
Il nome IUPAC si costruisce facendo seguire la desinenza
-ale al nome dell’idrocarburo saturo ad ugual numero di
atomi di carbonio.
H
O
O
O
H C
H3C C
H3C C C
H
H
H
metanale
H
etanale
(aldeide formica o
formaldeide)
H H
H3C C
C
propanale
(aldeide acetica o acetaldeide)
O
C
H H
butanale
(aldeide butirrica)
H
H CH3
H C
C
H H
(aldeide propionica)
O
C
H
2-metilpropanale
(aldeide metilpropionica)
La vecchia nomenclatura (ancora in uso) è riportata in corsivo
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Se il gruppo –CHO è legato a strutture cicliche…
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
NOMENCLATURA dei CHETONI
Il nome IUPAC si costruisce facendo seguire la desinenza
-one al nome dell’idrocarburo saturo ad ugual numero di
atomi di carbonio.
O
H3C C
O
H3C C
CH3
Propanone
(acetone)
O
H3C C
CH2CH3
Butanone
(metiletilchetone)
Corso di Chimica e Propedeutica Biochimica
CH2CH2CH3
2-pentanone
(metilpropilchetone)
Proff. M. De Rosa/C. Schiraldi
Proprietà fisiche di aldeidi e chetoni
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Reattività di aldeidi e chetoni
Corso di Chimica e Propedeutica Biochimica
H
R
H
OHR
C
O
C OH
O
Proff. M. De Rosa/C. Schiraldi
H
H2O
R C OH
OH-
OH
aldeide idrata
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
H
H
H H+
R C
R C
O
O H
H+
H H
R C O H
OH
Attacco elettrofilo di un protone
dell’acido sull’ossigeno del carbonile.
OH
H
R C OH
OH
aldeide idrata
La forma idrata delle aldeidi viene anche chiamata gem-diolo.
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
¾ L’addizione nucleofila avviene sia sulle aldeidi
che sui chetoni.
¾ La reattività delle aldeidi è, in linea di massima,
superiore a quella dei chetoni.
¾ Sulle aldeidi esiste un minore impedimento
sterico all’attacco del nucleofilo.
¾ La diversa reattività delle aldeidi e dei chetoni
nei riguardi del nucleofili dipende anche dalla
natura dei radicali legati al carbonile. I radicali
alchilici, essendo elettron-donatori,
neutralizzano in parte l’eccesso di carica positiva
sul carbonio, rendendolo meno disponibile
all’attacco.
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Reattività dei gruppi carbonilici
L’ordine di reattività dei gruppi carbonilici è influenzato
dagli effetti di sottrazione e di cessione elettronica dei
sostituenti.
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Meccanismo 1
Meccanismo 2
C
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
H
H C
H
H
H
CN-
H C
C
O
H
H H
H
C C N
H+
H C C C N
H O H
O
cianidrina
Reazione di addizione nucleofila in ambiente acido
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Per reazione di un’aldeide con HCN si ottengono due
cianidrine stereoisomere, essendo possibile l’attacco
dello ione CN- su ambedue le facce del piano di
ibridazione sp2 del carbonio carbonilico.
C N
H3C
C
H
O
H3C C
C N
H+
H 3C
H
O
C
H3C H OH
H+
C N
Corso di Chimica e Propedeutica Biochimica
H OH
C
C N
Scaricato da Sunhope.it
Proff. M. De Rosa/C. Schiraldi
Reazione con alcoli
H
R
H
H+
H
O R
OH
O
H
R C OR
R C O R
R C
C
H+
H H
OH
OH
emiacetale
L’addizione nucleofila di una molecola di alcole ad
un’aldeide o ad un chetone (in ambiente acido) porta alla
formazione di un emiacetale o emichetale.
Corso di Chimica e Propedeutica Biochimica
H
R
C OR
H+
Proff. M. De Rosa/C. Schiraldi
H
H
R
OH
OH
emiacetale
R
C OR
C OR
H2O
ROH
H
H
R
C OR
OR
H+
H
R
R
C OR
O
H
acetale
Dalla reazione dell’emiacetale con una seconda molecola di alcole
si ottiene un acetale, con meccanismo di sostituzione nucleofila.
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
H
H
R
2 R'OH
C
H+
R
O
C
OR'
OR'
ACETALE
R
R
R
2 R'OH
C
O
H+
R
C
OR'
OR' CHETALE
La reazione dei composti carbonilici con gli alcoli, nel rapporto
stechiometrico di 1:2, porta alla formazione degli acetali o chetali.
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Emiacetali ciclici: zuccheri
La forma ciclica emiacetalica degli zuccheri, molto stabile,
prevale sulla forma aperta
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Quando si fa reagire un’aldeide o un chetone
con tioli si ottiene la formazione di un
emitioacetale.
L’emitioacetale reagisce successivamente con una
seconda molecola di tiolo per formare un tioacetale.
OH
O
R'SH
R C
R C
H
SR'
R'SH
R C
SR'
H2O
H
H
tioacetale
emitioacetale
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
H
H
R' NH2
R C
R
H2O
C
N R'
O
Aldeide
SR'
+ ammina
immina
+
acqua
Basi di Schiff
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
H
H H
CH3
H3C C N CH3
H N H
H3C C
O
Etanale
O H
metilammina
Per
L’ammina
trasposizione
conduce
di due
un attacco
protoni ed
eliminazione
nucleofilo suldicarbonio
una molecola
carbonilico
di
acqua si forma l’immina.
C N CH3
H3C
H
H
H
H3C C N CH3
H3C C N CH3
immina
H2O
Corso di Chimica e Propedeutica Biochimica
O
H
H
Proff. M. De Rosa/C. Schiraldi
Addizione di composti azotati
2,4-Dinitrofenilidrazina
Questi derivati sono importanti per l’identificazione dei
composti carbonilici
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Addizione di composti azotati (II)
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Tautomeria cheto-enolica
Acetone
O
H
H
C
H
C
H
C
H
H
99.9999%
OH
H
H
C
H
C
C
H
H
0,0001%
¾La forma enolica e quella chetonica sono dette tautomere
¾Sono isomeri di struttura che differiscono per la posizione di
un atomo di idrogeno e di un doppio legame.
¾All’equilibrio, in generale, la cheto-forma prevale sull’enolo
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
¾La condensazione aldolica è la “somma” di due molecole di
aldeide.
¾La reazione globale è una combinazione di due passaggi:
a) addizione nucleofila
b) sostituzione in posizione D
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
CONDENSAZIONE ALDOLICA
a)
H
H C
H
OH-
H
C
C
O
H
H2O
H
H
H
H
C
C
O
C
O
H
Nella prima tappa si produce un anione enolato ...
H
b)
H C
H
H
H
C
C
O
H
H H H
H
H C
C
O
C
C
H O H
H
C
O
… che nella seconda tappa compie un attacco nucleofilo su
una seconda molecola di aldeide
H H H
c)
H C
C
C
H O H
H
C
O
H H H
H2O
OH-
H C
C
C
HH
H OH
H
C
O
E-idrossibutanale
da Sunhope.it
Nell’ultima tappa della reazione si forma unaScaricato
E-idrossialdeide.
H H
OH-
H
H2O H3C
O
OH H
O
H
H
C C
H3C C C C
C
2 H3C
H
C H
O
3-ossibutenale
(aldolo)
etanale
trans-2-butenale
(aldeide crotonica)
Nello stesso ambiente che ha portato alla loro sintesi,
dalle E-idrossialdeidi e dai E-idrossichetoni, per eliminazione
interna di acqua, si ottengono aldeidi e chetoni D,E-insaturi
CH3
2 H3C
CH3 H
OH-
CH3
H2O H C
3
C C
H3C C C C
C
O
OH H
O
H
C CH3
H3C
O
4-metil-4-ossi-2-pentanone
(aldolo)
Corso di Chimica e Propedeutica Biochimica
4-metil-3-pentene-2-one
Proff. M. De Rosa/C. Schiraldi
Le aldeidi si ossidano ad acidi carbossilici, mentre l’ossidazione
dei chetoni si produce soltanto in condizioni di reazione molto
energiche (con rottura di legami C-C).
H
CH3CH2
C
O
Cu2+
O
H
H3C C
O
NaOH, tartrato di sodio
H2O
CH3CH2
OH
O
Ag+
NH3
H2O
Cu2O
C
H3C C
Ag
OH
Scaricato da Sunhope.it
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
REAZIONI DI RIDUZIONE
Corso di Chimica e Propedeutica Biochimica
Proff. M. De Rosa/C. Schiraldi
Scaricato da Sunhope.it