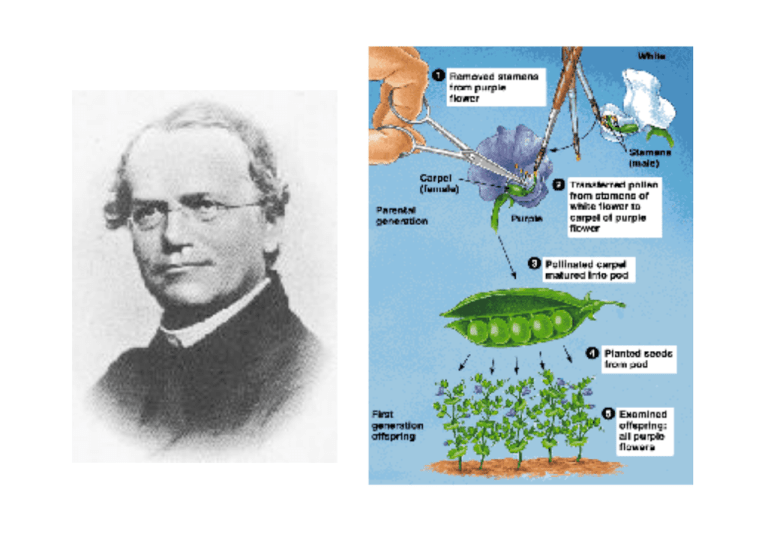
Fenotipo Dominante o Recessivo
Fenotipo Dominante
Fenotipo Recessivo
Albero genealogico
• Mostra la
trasmissione di
un carattere da
una generazione
alle successive
• Permette di
stabilire se il
carattere/malattia
è dominante o
recessivo
Arrotola la lingua
Non piega il pollice
Non arrotola la lingua
Riesce a piegare il pollice
Polidattilia
I
II
III
IV
Test for Red-Green Colorblindness
• Colorblindness is caused
by a malfunction of
light-sensitive cells in the
retina of the eyes
• What number do your
see?
• Like all X-linked
recessive traits,
colorblindness is very
rare in women. Why??
Ereditarietà Y-linked (Olandrica)
• “Hairy ears”
• Sinostosi Radio-ulnare? (fusione di radio & ulna)
ABO System:
A, B & O alleles: Chromosome 9
A & B: 4 nucleotide differences
O: One base deletion and frame-shift
Phenotypes: O, A, B & AB
Rh System:
Rh-D: Chromosome 1
Phenotypes: Rh-positive and Rh-negative
Antigene O
antigene A
Antigene B
N-acetil-galattosamina
N-acetil-glucosamina
galattosio
fucosio
Inheritance of ABO Groups
Allele from
the mother
Allele from
the father
Genotype of
offspring
Blood types of
offspring
A
A
AA
A
A
B
AB
AB
A
O
AO
A
B
A
AB
AB
B
B
BB
B
B
O
BO
B
O
O
OO
O
Rh System
Proteins
RHD gene
RHCE gene
Chromosome 1
Rh System
Gruppi sanguigni ABO e RH
RH D+
A
O
RH d-
Variations in Eye Color
Determinanti dell’espressione del fenotipo
• Natura della mutazione
mutazioni differenti nello stesso gene possono condurre a
fenotipi di gravità differente a seconda dell’effetto della mutazione
stessa sull’espressione del gene o sulla funzionalità del prodotto
proteico
• background genetico
due soggetti di una famiglia possono avere la stessa mutazione
ma differiranno per molti geni, a meno che non siano gemelli
monozigoti, l’espressione di questo background genetico può
modulare l’espressione clinica
•Effetto dell’ambiente
Lo stile di vita e l’esposizione a effetti ambientali tossici può
influenzare il fenotipo
Malattie autosomiche dominanti
• Espresse quando un solo cromosoma della
coppia porta l’allele mutato.
• Allele normale sul cromosoma omologo.
Caratteristiche dell’ereditarietà AD
• Fenotipo di solito presente in tutte le generazioni.
• Rischio pari al 50% di avere un figlio affetto.
• Persone sane non trasmettono la malattia ai propri
figli.
• Nessuna differenza di sesso nella trasmissione.
Può verificarsi la trasmissione da maschio a
maschio.
• Possono verificarsi nuove mutazioni.
Complicazione
non penetranza (NP)
Penetranza
• Penetranza = probabilità che un individuo che
abbia un genotipo (allele dominante) mostri il
fenotipo associato
– Completa
– Incompleta
• Polidattilia
– Indicata come percentuale
Però…
• Nuove mutazioni
- Talvolta un paziente non ha familiari affetti.
- I fenotipi lievi sono per lo più trasmessi alle successive generazioni.
- I fenotipi gravi sono molto spesso dovuti a nuove mutazioni
(acondroplasia, osteogenesi imperfetta,..)
• Età tardiva d’insorgenza
- Penetranza che varia con l’età.
- Nella Chorea di Huntington, a 45 anni soltanto il 50% degli individui
con genotipo mutato mostrano il fenotipo malato.
• Espressività variabile
- Variabilità del fenotipo clinico.
- Neurofibromatosi, Sclerosi tuberosa,…
• Omozigosi (o eterozigosi composita)
- Fenotipo clinico particolarmente accentuato.
- Ipercolesterolemia familiare
Ipercolesterolemia familiare
•
Colesterolemia (mg/dl):
•
Xantomi Tendinei:
•
Coronaropatia precoce (< 55 anni):
190
210 230
400
210
210
430
420
170
420
810
490
420
Deceduto per IMA a 17a
180
Complicazione
variable expression
Espressività
• Espressività = il grado con il quale un allele
esprime un fenotipo
– Variabile tra gli individui
• Influenzata da diversi fattori
– Background Genetico
– Ambiente (p. es. dieta)
• PKU
• Intoleranza al Lattosio
• Ipercolesterolemia familiare
• La comparsa può differire tra i pazienti
• TaySachs, Chorea di Huntington
Sindrome di von Hippel-Lindau (VHL)
Emangioblastoma
Cerebellare
?
Emangioblasto
ma
Cerebellare,
renale & cisti
pancreatiche
?
Emangioblastoma
Cerebellare
?
?
?
?
Malattie autosomiche recessive
• Espresse soltanto quando entrambi i
cromosomi hanno una copia mutata del
gene.
Caratteristiche dell’ereditarietà AR
• Fenotipo presente nei fratelli ma non nei genitori,
figli o altri parenti.
• Maschi e femmine affetti nella stessa proporzione.
• Entrambi i genitori sono carrier asintomatici.
• I genitori possono essere consanguinei.
• Il rischio di recidiva in un fratello è pari al 25%.
Esempi di malattie AR
•
•
•
•
•
Fibrosi cistica
Deficit di Alpha 1-antitripsina
Talassemia
Fenilchetonuria
Malattia di Tay-Sachs
Però…
• Pseudo-dominanza
- Figli di un unione tra un genitore affetto e uno portatore sano. Essi hanno il 50%
di probabilità di mostrare il fenotipo clinico (come nei caratteri/patologie
autosomiche dominanti.
• Espressività variabile
- Variabilità del fenotipo clinico ascrivibile all’eterogeneità allelica e non allelica.
• Eterogeneità non allelica
- La stessa patologia può essere dovuta a mutazioni in geni differenti. Perciò il
figlio di due pazienti con lo stesso fenotipo clinico può non mostrare il fenotipo.
- Sordità congenita non sindromica, Albinismo
Malattie genetiche dell’emoglobina
• varianti strutturali della proteina (emoglobinopatie)
• anemia a cellule falciformi
• codone 6 della β-globina
• GAG (acido glutamico) a GTG (valina)
• falcizzazione dei globuli rossi
• anemia da emoglobina C
• codone 6 della β-globina
• GAG (acido glutamico) a AAG (lisina)
• moderata anemia emolitica
• talassemie (diminuita sintesi delle α- o β-globine)
•persistenza ereditaria dell’emoglobina fetale (HPFH)
SMA I
(Malattia di Werdnig-Hoffmann; MIM#253300)
Età di esordio: entro il sesto
mese di vita
Quadro clinico:
Debolezza muscolare
simmetrica prossimale
Atrofia muscolare
No posizione seduta
autonoma
Attesa di vita: morte entro i 2
anni di vita
SMA II
(Forma intermedia; MIM#253400)
Età di esordio: tra i 6 e i 18
mesi
Quadro clinico:
Debolezza muscolare
simmetrica soprattutto agli
arti inferiori
Atrofia muscolare
Possibile posizione seduta,
no deambulazione autonoma
Attesa di vita: morte tra i 2
anni ed età giovane-adulta
SMA III
(Malattia di Kugelberg-Welander; MIM#253400)
Età di esordio: dopo i 18 mesi
Quadro clinico:
Debolezza muscolare
simmetrica
prossimale>distale; distretto
inferiore>distretto superiore
Atrofia muscolare
Possibile posizione seduta e
deambulazione autonoma.
Attesa di vita: normale
REGIONE SMA
sul braccio lungo del cromosoma 5
posizione 5q13
GENE SMN
• Gene di sopravvivenza del motoneurone (Survival
Motor Neuron Gene);
• Presente in due copie: una telomerica (SMN1) e
una centromerica (SMN2);
• SMN1 ed SMN2 sono geni altamente omologhi
SMN1
Esoni 1-6
SMN2
g
C
a
a
G
Introne 6 Esone 7 Introne 7 Esone 8
a
T
g
g
A
La T nel gene SMN2 determina che gran parte della proteina è
più corta e non funzionale dovuta alla eliminazione dell’esone 7
>90% proteina SMN completa
SMN1
~20% proteina SMN completa
SMN2
~80% proteina SMN
incompleta e non funzionale
7
Individui sani
SMN2
SMN2
SMN1
Pazienti SMA
SMN1
Individui sani
SMN2
SMN2
SMN1
Pazienti SMA
SMN1
SMN1
del/del
Individui sani
SMN2
SMN2
SMN1
Pazienti SMA
SMN1
SMN1
del/del
Individui sani
SMN2
SMN2
SMN1
Pazienti SMA
SMN1
SMN1
del/del
SMN1
del/mut
Il livello della proteina dipende in gran parte dal numero dei
geni SMN2 nei pazienti. Pazienti con forme più lievi hanno
più geni SMN2
SMN2
SMN1
Forma grave
SMN2
SMN1
Forma lieve
Aabb (albino)
aaBB
(albino)
AaBb
(normal)
Complicazione
Sordità congenita non sindromica
Lo stesso fenotipo geni differenti
Albinismo
Kwashiorchor: deficit
proteico da malnutrizione.
Fenocopia dell’albinismo.
Fenocopia
•
•
Fenotipo che mima una malattia genetica.
Causato da cause ambientali
L’esposizione di più soggetti della stessa
famiglia può fare attribuire il fenotipo a
cause genetiche, benchè sia da ascrivere a
casue ambientali.
Malattie legate al cromosoma X
• Dovute a mutazioni in geni presenti sul
cromosoma X.
• Possono essere recessive o dominanti.
Caratteristiche dell’ereditarietà XR
• Incidenza della malattia molto più alta nei maschi.
• Donne eterozigoti di solito sane.
• I geni mutati sono trasmessi dal padre malato alle
figlie che possono trasmetterli ai propri figli nel
50% dei casi.
• Impossibilità di trasmettere la malattia da padre a
figlio maschio.
• In una famiglia, tutti gli affetti sono tra loro
collegati da donne .
• Possibilità di nuove mutazioni.
Mutazioni puntiformi
1
234 56
7 8 9 10 12 13 14
11
15 17 19 21 23 25 26
16 18 20 22
24
Esempi di malattie XR
•
•
•
•
•
•
Distrofia muscolare di Duchenne
Haemophilia A
X Fragile
Amelogenesi imperfecta
Deficit di G6PD
Malattia di Fabry
Un gene più malattie (p.es. distrofina)
Caratteristiche dell’ereditarietà XD
• Maschi affetti con partner sani hanno figli
maschi sani e figlie femmine non normali.
• Tutti i figli di donne affette hanno il 50% di
probabilità di essere affetti.
• Le donne malate possono mostrare un
fenotipo più lieve di quello presete nei
maschi.
Esempi di malattie XD
• X-linked hypophosphataemic rickets
• Incontinentia pigmenti
• Sindrome Orofaciodigitale di tipo 1
Ereditarietà Y-Linked
•
I padri affetti trasmettono il tratto a tutti figli maschi ma a nessuna
delle figlie.