Pagina 1 di 4
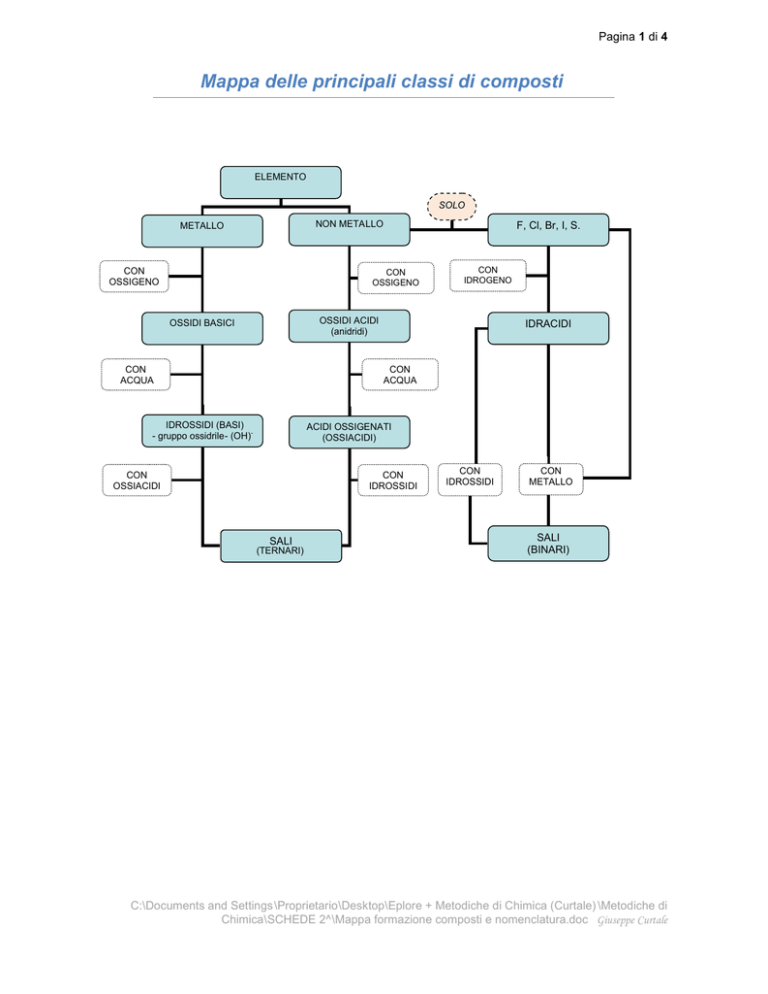
Mappa delle principali classi di composti
ELEMENTO
SOLO
NON METALLO
METALLO
CON
OSSIGENO
F, Cl, Br, I, S.
CON
OSSIGENO
CON
IDROGENO
OSSIDI ACIDI
(anidridi)
OSSIDI BASICI
CON
ACQUA
IDRACIDI
CON
ACQUA
IDROSSIDI (BASI)
- gruppo ossidrile- (OH)-
ACIDI OSSIGENATI
(OSSIACIDI)
CON
OSSIACIDI
CON
IDROSSIDI
SALI
(TERNARI)
CON
IDROSSIDI
CON
METALLO
SALI
(BINARI)
C:\Documents and Settings\Proprietario\Desktop\Eplore + Metodiche di Chimica (Curtale) \Metodiche di
Chimica\SCHEDE 2^\Mappa formazione composti e nomenclatura.doc Giuseppe Curtale
Pagina 2 di 4
NOMENCLATURA
1. Nomenclatura degli ossidi basici
Gli ossidi basici vengono indicati con la denominazione ossido di ……… seguita dal
nome del metallo se l’elemento poss iede un solo numero di ossidazione.
Se l’elemento presenta più di un numero di ossidazione si utilizza : ossido di ………
seguita dal nome del metallo portante la desinenza –oso o –ico per indicare i due
diversi stati di ossidazione.
Esempio:
N° di
Formula
Elemento
Simbolo
Nome
ossidazione
dell’ossido
Ossido di sodio
Sodio
Na
+1
Na2O
Ossido Ferroso
Ferro
Fe
+2
FeO
Ossido Ferrico
+3
Fe2O3
Rame
Cu
+1
+2
Cu2O
CuO
Ossido Rameoso
Ossido Rameico
2. Nomenclatura degli idrossidi
Gli idrossidi sono caratterizzat i dal gruppo ossidrilico (OH) -.
La loro formula è costituita dal simbolo del metallo seguito da un numero di (OH) - pari
al numero di ossidazione del metallo stesso.
Il nome deriva da quello degli ossidi sostituendo la parola ossido con idrossido.
Esempio:
N° di
Formula
Elemento
Simbolo
Nome
ossidazione
dell’ossido
Idrossido di sodio
Sodio
Na
+1
NaOH
Idrossido Ferroso
Ferro
Fe
+2
Fe(OH)2
Idrossido Ferrico
+3
Fe(OH)3
3. Nomenclatura degli ossidi acidi o anidridi
Gli ossidi acidi vengono indicati con la denominazione anidride……. seguita dal nome
del non metallo portante la desinenza –oso o –ico per indicare i numeri di ossidazione
intermedi, mentre per i numeri di ossidazione più piccolo e più grande si
usano,rispettivamente, i prefissi ipo- e per-.
Esempio:
N° di
Formula
Elemento Simbolo
Nome
ossidazione dell’anidride
Anidride ipoclorosa
+1
Cl2O
Anidride
clorosa
+3
Cl2O3
Cloro
Cl
Anidride
clorica
+5
Cl2O5
Anidride perclorica
+7
Cl2O7
C:\Documents and Settings\Proprietario\Desktop\Eplore + Metodiche di Chimica (Curtale) \Metodiche di
Chimica\SCHEDE 2^\Mappa formazione composti e nomenclatura.doc Giuseppe Curtale
Pagina 3 di 4
4. Nomenclatura degli acidi ossigenati o ossiacidi
Gli ossiacidi sono composti ternari.
La loro formula è costituita dall’idrogeno, non metallo e ossigeno, scritti nel rispettivo
ordine.
Il nome deriva da quello delle rispettive anidridi sostituendo la parola anidride con
acido.
Esempio:
Formula
Formula
Nome
Nome
anidride
dell’acido
Anidride perclorica
Acido perclorico
Cl2O7
HClO4
SO3
Anidride solforica
H2SO4
Acido solforico
5. Nomenclatura dei Sali ternari
I Sali vengono indicati con il nome del radicale dell’acido (sostituendo la desine nza)
seguito dal nome del metallo.
Esempio:
Catione
Radicale
Formula
Nome
metallico
dell’acido
del sale
Acido solforoso - SO32Solfito rameico
Cu2+
Cu SO3
Na+
Acido perclorico - ClO4-
NaClO4
Perclorato di sodio
6. Nomenclatura degli idracidi
Gli idracidi sono composti binari che si formano dalla reazione dell’idrogeno con gli
elementi: F, Cl, Br, I e S.
Il nome è formato dalla parola acido…… seguita dal nome dell’elemento portante la
desinenza –idrico.
Esempio:
N° di
Formula
Elemento Simbolo
Nome
ossidazione Dell’idracido
Acido cloridrico
HCl
Cloro
Cl
-1
7. Nomenclatura dei Sali binari
I Sali vengono indicati con il nome del radicale dell’acido (sostituendo la desinenza)
seguito dal nome del metallo.
Esempio:
Catione
Radicale
Formula
Nome
metallico
dell’acido
del sale
Acido cloridrico - ClCloruro di potassio
K+
KCl
C:\Documents and Settings\Proprietario\Desktop\Eplore + Metodiche di Chimica (Curtale) \Metodiche di
Chimica\SCHEDE 2^\Mappa formazione composti e nomenclatura.doc Giuseppe Curtale
Pagina 4 di 4
TABELLE RIASSUNTIVE
1. Nomenclatura degli ossidi basici
N° di
ossidazione
Minore
Nome del
metallo
Maggiore
2. Nomenclatura degli idrossidi
-OSO
N° di
ossidazione
Minore
-ICO
Maggiore
Desinenza
Nome del
metallo
Desinenza
-OSO
-ICO
3. Nomenclatura degli ossidi acidi (anidridi)
N° di
ossidazione
+1
Nome del
non metallo
Prefisso
IPO-
-OSA
+3
-OSA
+5
-ICA
PER-
+7
-ICA
4. Nomenclatura degli acidi ossigenati
(ossiacidi)
N° di
ossidazione
Desinenza
Prefisso
Nome del
non metallo
Desinenza
5. Nomenclatura dei Sali
ternari
Acido
Sale
-OSO
IPO….OSO
IPO….ITO
+3
-OSO
….OSO
....ITO
+5
-ICO
….ICO
….ATO
-ICO
PER….ICO
PER….ATO
+1
+7
IPO-
PER-
6. Nomenclatura idracidi
Nome non metallo
desinenza
-IDRICO
7. Nomenclatura dei Sali binari
Acido
-IDRICO
Sale
-URO
C:\Documents and Settings\Proprietario\Desktop\Eplore + Metodiche di Chimica (Curtale) \Metodiche di
Chimica\SCHEDE 2^\Mappa formazione composti e nomenclatura.doc Giuseppe Curtale