Chimica Organica
Scienze della Terra, dell’Ambiente e
del Territorio
Capitolo 8
Acidi Carbossilici e Derivati
Organic Chemistry, 5th Edition
L. G. Wade, Jr. Prentice Hall
Organic Chemistry, 3rd Edition
Paula Y. Bruice, Prentice Hall
Introduzione
• Il gruppo funzionale degli acidi carbossilici è costituito da un C=O con
legato un –OH.
O
R C
OH
• Il gruppo carbossilico normalmente si scrive -COOH.
• Gli acidi carbossilici alifatici hanno un gruppo alchilico legato al COOH.
• Gli acidi carbossilici aromatici hanno un gruppo arilico legato al COOH.
• Gli acidi grassi sono acidi alifatici a lunga catena.
2
Importanza
• Acido acetico, presente nell’aceto, usato nell’industria come
solvente, catalizzatore e reagente nelle sintesi.
• Acidi grassi presenti in grassi e oli.
• Acidi benzoici nei farmaci e nei conservanti.
• Acido adipico usato per fare il nylon 66.
• Acido ftalico usato per fare i poliesteri.
COOH
COOH
O
C
O
CH3
Acido acetilsalicilico
aspirina
CH3CHCH2
CH3
Acido stearico
Un acido grasso
CHCOOH
CH3
Ibuprofene
moment, antalgyl, nurofen
3
Nomi comuni
• Molti acidi alifatici hanno nomi comuni.
• Le posizioni dei sostituenti lungo la catena sono indicati con le lettere
greche.
Cl O
CH3CH2CHC OH
Acido -clorobutirrico
Ph
CH3CH2CH2CHCH2COOH
Acido -fenilcaproico
4
Nomi IUPAC
• La –o degli alcani è sostituita con -oico e si premette acido.
• Il carbonio carbossilico è il #1.
• Il gruppo carbossilico ha la priorità rispetto a doppi e tripli legami,
gruppi ossidrilici e carbonilici
Ph
Cl O
CH3CH2CHC OH
H
C C
H
Acido 2-clorobutanoico
COOH
Acido trans-3-fenil-2-propenoico
(acido cinnamico)
OH
8
4
7
6
5
2
3
9
1
COOH
O
Acido 5-etil-6-idrossi-7-metil-3-osso-7-nonenoico
5
Acidi bicarbossilici
• Gli acidi bicarbossilici hanno spesso nomi comuni (vanno
memorizzati).
• Nomi IUPAC: il gruppo 1 è quello più vicino al primo sostituente.
• Due gruppi carbossilici su un benzene: acidi ftalici.
Br
HOOCCH2CHCH2CH2COOH
Acido 3-bromoesandioico
(acido -bromoadipico)
6
Struttura del carbossile
• Carbonio sp2.
• Angoli di legame circa 120.
• O-H eclissato con C=O, per avere la sovrapposizione degli orbitali
con il doppietto libero dell’ossigeno.
7
Proprietà fisiche
• Punti di ebollizione più alti di quelli degli alcoli di pari peso
molecolare a causa della formazione di dimeri.
• La solubilità in acqua diminuisce all’aumentare del numero di
carboni.
• Fino a 4 carboni gli acidi sono miscibili con l’acqua.
• Più solubili degli alcoli.
• Solubili anche in solventi moderatamente polari come il cloroformio,
8
si scioglie in forma di dimero.
Acidità
• Gli acidi carbossilici
(Ka~10-5) sono più
acidi dei fenoli
(Ka~10-10) e degli
alcoli (Ka~10-16)
• La maggiore acidità
è dovuta alla
stabilizzazione per
risonanza della
base coniugata
9
Effetto dei sostituenti sull’acidità
COOH
COOH
COOH
COOH
COOH
NO2
NO2
OCH3
p-methoxy benzoic acid
pKa = 4.46
m-nitro
pKa = 4.19 pKa = 3.47
NO2
p-nitro
o-nitro
pKa = 3.41
pKa = 2.16
10
Sali degli acidi carbossilici
• L’idrossido di sodio rimuove un protone dagli acidi formando sali
• Se si aggiunge un acido più forte, come HCl, si riforma l’acido
(l’acido forte sposta l’acido debole).
Aq. NaOH
RCOO-Na+
RCOOH
Aq. HCl
• Nome dell’anione: sotituire -oico con -oato.
• Nome del catione
Cl
-
CH3CH2CHCH2COO K
3-cloropentanoato di potassio
-clorovalerato di potassio
+
Proprietà dei sali
• Di solito solidi ed inodori.
• I carbossilati di Na+, K+, Li+, e NH4+ sono solubili in acqua.
• I saponi sono i sali degli acidi grassi (acidi a lunga catena, 14-20
C).
• I Sali si possono preparare per reazione di un acido con
NaHCO3, si sviluppa CO2.
12
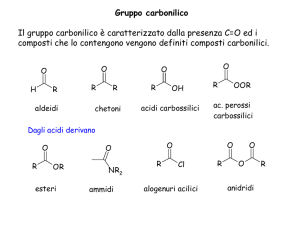
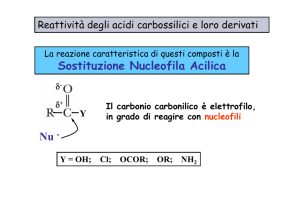
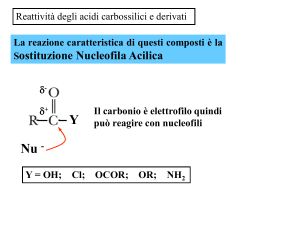
Derivati degli acidi carbossilici
• Il gruppo legato al carbonio acilico determina la classe del
composto:
O
-OH, acidi carbossilici
-Cl, cloruri acilici
-OR’, esteri
-NH2, ammidi
Carbonio acilico
C
R
OH
• Possono essere interconvertiti con una certa facilità
13
Nomenclatura esteri
• Sono identificati come alchil carbossilati.
• Il gruppo alchilico deriva da un alcol, il carbossilato da un acido.
CH3
O
O
HCOCH2
CH3CHCH2OCCH3
benzil metanoato
2-metilpropil etanoato
Esteri ciclici
• Reazione tra un -OH e un -COOH nella stessa molecola, lattone.
• Si premette la parola lattone al nome IUPAC dell’acido.
O
H3C
O
lattone 4-idrossi-2-metilpentanoico
14
CH3
Ammidi
• Formalmente deriva da un acido carbossilico e da ammoniaca o
ammina.
• Non sono basiche perché il doppietto dell’azoto
è delocalizzato.
_
O
C
H
O
N
H
C + H
N
H
H
H
• Ammide primaria: un solo legame C-N (due N-H).
• Ammide secondaria: (N-sostituita) due legami C-N (un N-H).
• Ammide terziaria: (N,N-disostituita) tre legami C-N (nessun N-H)
O
H3C
C
NH2
Ammide 1°
H3C
O
CH3
C
NH
Ammide 2°
H3C
O
CH3
C
N
Ammide 3°
CH2CH3
15
Nomenclatura ammidi
• Per le ammidi 1 sostituire -oico nel nome dell’acido con -ammide.
• Per le 2 e 3, il gruppo alchilico legato all’azoto è preceduto da N-.
O CH3
CH3CHC N CH2CH3
CH3
O
N-etil-N-metil-2-metilpropanammide
Ammidi cicliche (lattami)
• Legame ammidico intramolecolare, lattami.
N H
CH3
-valerolattame
16
Alogenuri acilici
• Si preparano dall’acido per reazione con SOCl2.
O
O
CH3CH2C
OH
SOCl2
CH3CH2C
Cl
• Sono più reattivi degli acidi carbossilici.
• Nome: sostituire -oico dell’acido con -oile e premettere il nome
dell’alogenuro
O
C
Br
Cl
cloruro di benzoile
Benzoil cloruro
O
CH3CHCH2C Br
bromuro di 3-bromobutanoile
3-bromobutanoil bromuro
17
Saponificazione
• Idrolisi degli esteri Base-catalizzata.
• “Saponificatione” perché è il metodo di preparazione tradizionale
dei saponi
• I saponi si preparano facendo bollire NaOH con i grassi
(trigliceridi) si formano i Sali sodici degli acidi grassi.
• Un esempio di sapone è il sodio stearato, Na+ -OOC(CH2)16CH3.
O
O
CH2 O- CR
RCO- CH
+
3 Na OH
saponification
O
CH2 O- CR
A triacylglycerol
(a triglyceride)
CH 2 OH
CHOH
O
+
CH 2 OH
1,2,3-Propanetriol
(Glycerol; Glycerin)
-
+
3 RCO Na
Sodium soaps
18
Come funziona un sapone
NaOH
19
Fine del Capitolo 8
20