Diagnostica delle alterazioni del metabolismo glucidico
Diagnostica biochimico-clinica
Lezione 11
Carboidrati
I carboidrati o saccaridi (dal greco sàkcharon, zucchero) sono le molecole biologiche più
abbondanti. Chimicamente sono costituiti da C, H e O combinati secondo la formula
≥3.
generale (C·H2O)n con n≥
Le unità di base dei carboidrati sono i monosaccaridi che si uniscono poi a dare i
polisaccaridi. I carboidrati svolgono una funzione strutturale ed energetica sia come
sostanze nutrienti che come intermedi metabolici.
Panoramica del catabolismo
Proteine, carboidrati e lipidi sono
sintetizzati a partire da unità più piccole e
degradati nelle stesse unità (amminoacidi,
glucosio e acidi grassi/glicerolo).
L’ossidazione di questi metaboliti
produce energia metabolica sottoforma di
ATP.
Le principali vie metaboliche del
glucosio, acidi grassi e amminoacidi
convergono su piruvato ed acetil-CoA,
composti che occupano posizioni centrali
nel metabolismo energetico.
Alcuni processi metabolici necessitano
della cooperazione tra i vari organi
(cervello, muscolo, tessuto adiposo, fegato
e rene).
Schema generale del metabolismo del glucosio
Il glucosio è una fonte di energia facilmente utilizzabile da tutti i tessuti
Destino del glucosio
Ossidazione a CO2 e H2O
(in tutti i tessuti)
Trasformazione in altri
carboidrati
Immagazzinamento sotto
forma di grassi
(attraverso acetil Co-A)
Glicogenosintesi
e/o
Glicolisi con formazione di acido lattico
(nei muscoli)
GLUCOSIO
Via dei pentosi
(fegato e tessuto adiposo)
Conversione in
amminoacidi
non essenziali
Integrazione del metabolismo
Acidi grassi liberi o non esterificati derivanti dalla lipolisi dei grassi
Cellule adipose con adeguata
riserva di glucosio
In assenza di quantità
adeguate di glucosio
Acidi grassi + glicerolo
Passano in circolo
Trigliceridi
Ossidazione
Amminoacidi
(chetogenici, glucogenici)
Acetil-CoA
(nei tessuti)
Anche nel rene
1. Sintesi di acidi grassi
2. Sintesi di colesterolo
3. Corpi chetonici
(acetoacetato,β
β-idrossibutirrato, acetone)
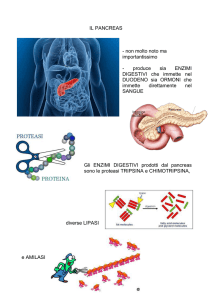
Metabolismo dei carboidrati
Disaccaridi (saccarosio, lattosio) e polisaccaridi, (amido, glicogeno) introdotti con la dieta
Amilasi
Disaccaridasi
(saliva)
(succo pancreatico)
(mucosa intestinale)
Monosacaridi
(glucosio, fruttosio, galattosio)
Glucosio, fruttosio, galattosio, mannosio (deriva dalle glicoproteine), ribosio e deossiribosio
(digestione degli acidi nucleici) vengono assorbiti nella mucosa intestinale
Assorbimento
1. Per diffusione facilitata (gradiente di concentrazione)
2. Per trasporto attivo
Fegato
Destino dei carboidrati
Dopo l’assorbimento nel circolo portale, i carboidrati pervengono al FEGATO, ove si
esplicano attività tese a :
DIMINUIRE la quantità di glucosio immessa nella circolazione sistemica:
trasformazione glucosio in glicogeno e suo deposito nel fegato;
ossidazione del glucosio per produrre energia;
biosintesi di altri composti (ac. grassi, aa, ecc.)
AUMENTARE la quantità di glucosio immessa nella circolazione sistemica:
trasformazione in glucosio del fruttosio o del galattosio;
trasformazione del glicogeno in glucosio (glicogenolisi);
sintesi di glucosio a partire da altri composti (aa, ac. lattico, glicerolo ecc.)
(gluconeogenesi)
La quantità di glucosio in circolazione sistemica è risultante di questi due opposti
meccanismi
Metodi di misura della glicemia
METODO DELLA GLUCOSOSSIDASI-PEROSSIDASI
Glucosio ossidasi
β-D-Glucosio + H2O
Ac. Gluconico + H2O2
Perossidasi
Accettore di O2 (fenolo)+ H2O2
Cromogeno + H2O
METODO DELLA ESOCHINASI-G6PDH
Glucosio + ATP Esochinasi G6P + ADP
G6P + NAD(P)
G6PDH
6-Fosfogluconato + NAD(P)H → Abs a 340 nm
METODI DI MISURA DEGLI ORMONI IMPLICATI NELL’OMEOSTASI GLUCIDICA
RIA
Spettro di assorbimento del NAD+ e del NADH
Glucometro
I glucometri sono utilizzati per l'automonitoraggio della glicemia. Per stimare la glicemia, il
glucometro analizza una piccola goccia di sangue capillare, generalmente prelevata dal
polpastrello, posta su un'apposita striscia reattiva inserita al suo interno.
Il glucosio contenuto nel campione di sangue darà origine ad una reazione enzimatica
ossidandosi grazie alla presenza dell'enzima glucosio-ossidasi nella striscia reattiva.
L’ossidazione darà origine ad una variazione cromatica o ad una corrente elettrica (a
seconda del modello) tradotta poi nel valore glicemico corrispondente.
Omeostasi della glicemia mediante controllo ormonale
La concentrazione del glucosio nel sangue viene mantenuta entro limiti abbastanza ristretti
(70-110 mg/dl) in rapporto a specifiche esigenze funzionali del tessuto nervoso. L’effetto
degli ormoni sulla omeostasi glicemica dipende dai dei rapporti di concentrazione di ormoni
agonisti e antagonisti.
ORMONE IPOGLICEMIZZANTE
INSULINA
abbassa la concentrazione del glucosio ematico
ORMONI IPERGLICEMIZZANTI
GLUCAGONE ED
ORMONE DELLA
CRESCITA (GH)
aumentano la concentrazione in condizioni fisiologiche
GLUCOCORTICOIDI
E ADRENALINA
aumentano la concentrazione in situazioni patologiche (digiuno
protratto e stress).
Controllo ormonale in seguito all’assunzione di alimenti
Subito dopo un pasto, quando glucosio ed acidi grassi sono abbondanti, l’insulina segnala ai
tessuti di accumulare glicogeno e trigliceridi come riserva energetica. L’insulina induce
inoltre nei tessuti diversi dal fegato ad assorbire glucosio tramite il trasportatore GLUT4.
Controllo ormonale in seguito a digiuno/ stress
Quando non sono disponibili carburanti energetici provenienti dalla dieta, il glucagone
induce il fegato a rilasciare glucosio e il tessuto adiposo a rilasciare grassi. In condizioni di
stress, l’adrenalina induce risposte simili.
Effetto degli ormoni
IPOGLICEMIZZANTE
INSULINA
↑ Glicolisi
↑ Glicogenosintesi
↑ Neoglucogenesi
IPERGLICEMIZZANTI
ADRENALINA
GLUCAGONE
↑ Glicogenolisi
↓ Rilascio di insulina
↑ Glicogenolisi
↑ Neoglucogenesi
↓ Glicogenosintesi
GLUCOCORTICOIDI
↑ Neoglucogenesi
↑ Glicogenosintesi
↓ Captazione glucosio
↓ Glicolisi
Insulina
L'insulina è un ormone peptidico di 51 amminoacidi (Mw, 5808 Da) prodotto dalle cellule
beta delle isole di Langerhans del pancreas. L'insulina è formata da due catene unite da due
ponti solfuro: catena A di 21 aminoacidi e catena B di 30 aminoacidi.
Biosintesi e maturazione
L’insulina viene sintetizzata in forma di precursore inattivo (preproinsulina). La
maturazione avviene in due passaggi.
La rimozione del peptide leader porta alla formazione della proinsulina. La rimozione del
segmento intermedio (peptide C) porta alla formazione dell’insulina attiva.
Secrezione dell’insulina
Le cellule endocrine del pancreas fungono da sensori della concentrazione plasmatica di
glucosio.
L'insulina prodotta è presente in vescicole
all’interno delle cellule β. Essa esce dalle cellule
per esocitosi che avviene dal lato cellulare
rivolto verso i capillari sanguigni.
L’ormone passa nel sangue attraverso le
fenestrature dell’endotelio capillare.
Nel sangue l’insulina ha un’emivita di 4/5 min;
essa infatti si fissa rapidamente nei tessuti ove
esplica le sue azioni.
Viene inattivata dopo essere passata per
endocitosi nel citoplasma delle cellule.
Secrezione dell’insulina
Insulina velocità di
secrezione
Insulina velocità di
secrezione (%)
Notevole importanza funzionale assume la “prontezza” con cui le cellule β rispondono alle
variazioni del tasso glicemico.
100
50
0
0
50
150
250
350
Concentrazione plasmatica di
glucosio
Risposta delle cellule β ad un
improvviso innalzamento del livello
glicemico (es. per infusione per via
circolatoria di una soluzione glucosata).
0
10
20
30
40
50
minuti
Andamento bifasico. Le cellule β
posseggono due pool di insulina che
vengono rilasciati con diversa facilità.
Insulina
La sua funzione è quella di regolatore
dei livelli di glucosio ematico
riducendo la glicemia mediante
l'attivazione di diversi processi
metabolici e cellulari.
Regolazione
insulina
della
secrezione
di
Secrezione stimolata dall’ aumento
della glicemia
Secrezione inibita dall’ ipoglicemia
e da alcuni ormoni
Insulina
Meccanismo d’azione
Attivazione del recettore insulinico
situato sulla membrana delle cellule
bersaglio.
Si innesca una cascata di risposte
intracellulari, in particolare ingresso
di glucosio nella cellula attraverso il
trasportatore GLUT-4.
Attivazione di numerose vie
metaboliche
(essenzialmente
a
livello di fegato, muscolo e tessuto
adiposo).
Meccanismi innescati dall’insulina
L’insulina promuove l’utilizzo del glucosio
in tutte le possibili vie metaboliche
Aumento del trasporto del glucosio
Aumento della sintesi di glicogeno
Aumento della sintesi proteica
Inibizione della neoglucogenesi
Inibizione della chetogenesi
Inibizione della glicogenolisi e lipolisi
Inibisce il catabolismo proteico
Accelerata conversione del glucosio in grassi
Principali azioni dell’insulina nelle cellule
Metabolismo
Glucidico
Lipidico
Proteico
Salino
Effetto
Ingresso glucosio
Stimolazione
Glicogenosintesi
Stimolazione
Glicolisi
Stimolazione
Neoglucogenesi
Inibizione (1)
Ingresso NEFA
Stimolazione
Lipogenesi
Stimolazione
Lipolisi
Inibizione (2)
β-ossidazione
Inibizione
Ingresso amminoacidi
Stimolazione
↑ Velocità di trasporto
Sintesi proteica
Stimolazione
↑ Trascrizione e traduzione
Demolizione proteine
Inibizione
↓ Att. Proteasi lisosomiali
Ingresso K+
Stimolazione
↑ Att. Pompa Na+/K+
(1) Soprattutto nel fegato; (2) soprattutto nel tessuto adiposo
↑ Att.glicogeno sintetasi
↑ Att.lipoproteinolipasi
↓ Lipasi
Variazioni dei livelli di glicemia/insulinemia con l’alimentazione
Profilo insulinemico e glicemico nelle 24 h in condizioni fisiologiche
Colazione
Pranzo
Cena
Glucagone
Il glucagone è un polipeptide costituito da 29 aa, prodotto dalle cellule alfa delle isole
pancreatiche. Secreto in risposta ad una condizione ipoglicemica, provocando l’immissione
in circolo di glucosio, attraverso lo stimolo di glicogenolisi e della neoglucogenesi.
Nell’omeostasi glicemica, è importante il rapporto molare tra insulina e glucagone: un
elevato rapporto diminuisce il tasso glicemico e viceversa. L’emivita del glucagone nel
sangue circolante è di circa 6 min e, al contrario dell’insulina, la cui azione ha come
bersaglio vari tessuti, il glucagone ha effetto solo nelle cellule epatiche.
Ormone della crescita
L’ormone della crescita (growth factor, GH) è secreto dall’adenoipofisi ed ha effetto
iperglicemizzante.
Inibisce l’assunzione di glucosio da parte delle cellule
Inibisce la sintesi di acidi grassi a partire da carboidrati
Promuove la lipolisi e la liberazione di FFA dal tessuto adiposo
La somatostatina prodotta dalle cellule δ delle isole
pancreatiche e nell’ipotalamo deve il suo nome alla
capacità di inibire, nell’adenoipofisi, la secrezione
dell’ormone della crescita (GH) o somatotropo. Agisce
anche come potente inibitore della secrezione sia di
insulina che di glucagone.
Fa diminuire le attività gastroenteriche
Diminuisce l’assorbimento di tutte le sostanze
nutritive ed in particolare del glucosio
Induce ipoglicemia ed ipolipemia
Glucocorticoidi e Adrenalina
Nello stress, si ha secrezione di adrenalina (midollare del surrene) e di cortisolo (corticale
del surrene), con aumento della glicemia utile al sistema nervoso.
ADRENALINA
Diminuisce il rilascio di insulina
Inibisce l’assunzione di glucosio da parte delle cellule
Aumenta la glicogenolisi epatica e muscolare
GLICOCORTICOIDI (es. Cortisolo)
Aumentano la neoglucogenesi delle proteine
Inibiscono la sintesi proteica
Aumentano la lipolisi nel tessuto adiposo
Medulla
Cortex
Concentrazione di glucosio nel sangue
Dopo un digiuno di almeno 4 ore, il valore della glicemia è di 70-110 mg/dl. Durante le
prime due ore dopo il pasto, c’è assorbimento intestinale, con aumento della glicemia.
Aumenta 10-15 volte il tasso insulinemico e diminuisce quello di glucagone e GH del
plasma. Tra la seconda e la quarta ora, il tasso glicemico continua a diminuire, pur
mantenendosi leggermente al di sopra di quello basale.
Diabete
Può essere definito come un disordine metabolico caratterizzato da deficit effettivo
d’insulina a livello tissutale, denominato diabete mellito.
Dal greco (diabainein, attraversare, collegato all’eccessiva produzione d’urina). ll suffisso
mellito (dal latino mel, miele, dolce) è stato aggiunto in un secondo momento per il fatto
che il sangue e le urine dei pazienti diabetici avevano un sapore dolce.
CLASSIFICAZIONE
Diabete di tipo I (IDDM: insulin dependent diabetes mellitus)
Diabete di tipo II (NIDDM: non insulin dependent diabetes mellitus)
Ridotta tolleranza al glucosio (IGT)
Forme di diabete dipendenti da altre varie cause (diabete secondario)
Diabete mellito gestazionale (GDM)
DIABETE DI TIPO I (diabete giovanile) o insulino-dipendente
Deficit insulinico dovuto a inefficienza o distruzione delle cellule β (per predisposizione
ereditaria o aggressione autoimmune). Il livello plasmatico di insulina si mantiene
costantemente basso, sia in condizioni basali che in risposta ad aumenti della glicemia.
Presenza di Ab contro le isole di Langherans o antinsulina
Necessità delle terapia insulinica
Insorgenza acuta e giovanile
DIABETE DI TIPO II (diabete dell’adulto) o insulino-indipendente
L’insulina viene prodotta in quantità adeguata ma sono i tessuti che non rispondono
all’ormone. Tra le cause vi è una carenza di recettori per l’insulina, disfunzioni nelle tappe
successive all’interazione insulina-recettore. L’insorgenza è favorita da un’eccessiva
alimentazione per cui si associa a obesità. Ha insorgenza lenta.
Profilo glicemico nel diabete
Principali effetti metabolici della carenza di insulina
Entrata glucosio
nelle cellule
Glicogenolisi
Demolizione
proteine
Mobilizzazazione
lipidi
Sintesi trigliceridi
Neoglucogenesi
IPERGLICEMIA
Glicosuria
Poliuria
DIMAGRIMENTO
IPERLIPEMIA
POLIFAGIA
Entrata di NEFA
nelle cellule
POLIDIPSIA
β-ossidazione
Ipovolemia
Chetonemia
Ipotensione
Chetonuria
(poliuria)
Flusso sanguigno
cerebrale
COMA DIABETICO
ACIDOSI
Impiego terapeutico dell’insulina
Per lungo tempo è stata utilizzata insulina estratta dal pancreas di animali. Oggi si utilizza
quella umana prodotta con procedimenti di ingegneria genetica. L’insulina viene
somministrata per via ipodermica o intramuscolare. Non può essere somministrata per via
orale perché essendo un ormone di natura proteica verrebbe distrutta dai succhi digestivi.
Impiego terapeutico dell’insulina
L’insulina viene rapidamente inattivata nei tessuti ed esplica la sua azione per un tempo
molto breve. Al diabetico viene somministrata quotidianamente una dose “basale” di
insulina ritardata (combinata come sale di zinco o con proteine al fine di prolungarne
l’azione) e si interviene poi con dosi supplementari di insulina rapida nelle ore in cui si
prevede un innalzamento della glicemia.
Diminuita tolleranza al glucosio (Impaired glucose tolerance-IGT)
I pazienti sono caratterizzati da una curva di tolleranza al glucosio con caratteri patologici
che generalmente si normalizza con la dieta. Sindrome iperglicemica asintomatica. Il 20% di
soggetti IGT rischiano però di trasformarsi in pazienti diabetici.
OBESITA’
↑ Introito calorico
↑ Glicemia
↑ Resistenza all’insulina
↑ Insulinemia
↓ recettori
Diabete secondario e diabete in gravidanza
DIABETE SECONDARIO
Si verifica come conseguenza di altre patologie sia pancreatiche che endocrine tra cui
pancreopatie, endocrinopatie, patologie da farmaci e sindromi genetiche.
DIABETE IN GRAVIDANZA
Condizione transitoria che si ristabilizza subito dopo il parto. Si verifica in donne con ridotta
tolleranza al glucosio. Se la glicemia a digiuno rimane superiore a 105 mg/dl per più giorni:
non si effettua la curva da carico per i potenziali rischi per il feto
si determina il profilo glicemico in più prelievi a distanza di 4 ore
Se il secondo valore della glicemia è inferiore a 105 mg/dl si può effettuare la curva da
carico del glucosio in base ai risultati le donne gravide sono classificate in:
1. Normale o ridotta tolleranza al glucosio
2. Diabete mellito in gravidanza
Diabete secondario e diabete in gravidanza
L’importanza del corretto monitoraggio
del diabete nella donna gravida è legata da
una parte alle complicazioni a cui può
andare incontro la donna stessa, dall’altra
al fatto che il feto presenta una condizione
di iper-insulinismo per la continua
stimolazione alla quale sono soggette le sue
cellule pancreatiche in conseguenza
dell’iperglicemia materna.
Alla nascita l’iperinsulinismo, non più
compensato dall’iperglicemia materna, può
portare ad ipoglicemia anche molto grave
con conseguenti disturbi neurologici.
Altre cause di iperglicemia
ENDOCRINOPATIE
• Iperproduzione di cortisolo (Morbo di Cushing) o somministrazione di glucocorticoidi
che inducono gluconeogenesi e inibiscono il metabolismo del glucosio.
• Tireotossicosi: la tiroxina ha azione glicogenolitica.
• Eccesso di aldosterone: l’ipopotassemia associata comporta una ridotta secrezione
insulinica e non permette una normale assunzione del glucosio.
MALATTIE PANCREATICHE
• Provocano distruzione delle cellule insulari
• Pancreatiti acute e croniche, asportazione chirurgica del pancreas
• Calcoli e tumori
FARMACI CHE INIBISCONO LA SECREZIONE O PROVOCANO RESISTENZA INSULINICA
• Steroidi, salicilati, beta bloccanti, barbiturici, contraccettivi orali, estrogeni
INSUFFICIENZA RENALE CRONICA
•Alterata utilizzazione del glucosio
EPATOPATIA CRONICA
•Ridotta glicogenosintesi
Ipoglicemia
Si parla di ipoglicemia quando il valore di concentrazione di glucosio nel sangue è più
bassa rispetto ai valori normali (al di sotto di 40 mg/dl). I sintomi di solito compaiono
quando la glicemia è <50 mg/dl, e riproducono il quadro clinico dell’anossia cerebrale:
ciò mette ancor più in evidenza la stretta correlazione tra metabolismo cerebrale ed
apporto plasmatico di glucosio. Tra le cause di ipoglicemia vi è il rilascio difettoso di
glucosio da parte del fegato o un aumentato assorbimento da parte dei tessuti.
I primi sintomi includono sudorazione, tachicardia ed agitazione (dovute ad aumento di
adrenalina). In seguito si manifestano vertigini, stato letargico e coma che può portare a
lesioni cerebrali permanenti e decesso.
Ipoglicemia
A DIGIUNO
IPOGLICEMIE
REATTIVE (DIPENDONO
DA ALTRI STIMOLI)
A DIGIUNO
Iperplasia delle cellule insulari
Epatopatie
Gravidanza
Neoplasie extrapancreatiche
REATTIVA
Farmaci (insulina o ipoglicemizzanti)
Ingestione di alcool (↓
↓ gluconeogenesi)
Criteri diagnostici di diabete
Il diabete mellito può essere definito da uno dei seguenti criteri (ADA, American diabetes
association):
Negli adulti:
Sintomi classici del diabete e iperglicemia inequivocabile
Glicemia plasmatica a digiuno uguale o >126 mg/dl
Glicemia plasmatica a digiuno <126 mg/dl, ma con test di tolleranza orale al glucosio
nettamente alterato (>200 mg/dl dopo 2h o in tempi intermedi)
Emoglobina glicata (A1c) ≥ 6,5%
Nei bambini:
Sintomatologia classica (poliuria, glicosuria, polidipsia) e valori di glicemia > 200mg/dl
Test di laboratorio per la diagnostica e monitoraggio del diabete
Routine
• Glicemia (65-110mg/dl)
Dubbi diagnostici e soggetti a rischio
• Curva glicemica
• Profilo glicemico
• Glicemia alla seconda ora dopo il pasto
Approfondimenti diagnostici
• Curva insulinemica
• Anticorpi anti-isole pancreatiche (ICA, Islet Cells Antibodies)
• Anticorpi anti-insulina (IAA)
• Monitoraggio dell’emoglobina glicosilata
Test di tolleranza al glucosio (OGTT)
Il test di tolleranza al glucosio (Oral glucose tolerance test, OGTT) o curva da carico orale
di glucosio misura le variazioni nel tempo della glicemia dopo la somministrazione di
glucosio per via endovenosa o orale. La prova si esegue somministrando 75 g di glucosio
in 250 ml di acqua e seguendo nel tempo ad intervalli di 30 min le variazioni della
glicemia, insulinemia, NEFA e glicosuria dopo 2h.
Glucosio
mg/dl
300
diabete
250
200
Ridotta tolleranza
150
normale
100
50
0
0
60
120
minuti
Test di tolleranza al glucosio (OGTT): Insulinemia
Insulina
uU/ml
100
80
60
40
Diabete di II tipo
normale
Diabete I tipo
20
0
0
60
120
minuti
Glicosuria
Presenza di glucosio nelle urine quando la glicemia supera la soglia renale per il glucosio
(160-200 mg/dl). Se abbondante, determina aumento del volume urinario (poliuria
(diuresi > 2500 cc/24h).
METODO DI DOSAGGIO
Impiego di cartine reattive, contenenti glucosio ossidasi-perossidasi e un cromogeno che
subisce cambiamento di colore in relazione a quanta H2O2 si è prodotta. Lettura per
dell’intensità di colore per la quantificazione del risultato.
GLICOSURIA CON IPERGLICEMIA
• E’ presente nel diabete e nelle condizioni patologiche in grado di dare iperglicemia
GLICOSURIA SENZA IPERGLICEMIA
• In gravidanza si può avere aumento della filtrazione glomerulare: il glucosio filtrato
può non venire completamente riassorbito per cui si può avere glicosuria con glicemia
normale
• Nelle tubulopatie renali si verifica un ridotto assorbimento di glucosio
Dosaggio emoglobina glicosilata (HbA1c)
Frazione dell’emoglobina capace di legare il glucosio, utilizzata come marker dei valori
medi di glicemia nei 2-3 mesi precedenti al prelievo, a differenza della glicemia che
esprime il valore di glucosio ematico al momento del prelievo. Il dosaggio dell’HbA1c è
utile nel diabete insulino-dipendente. Aumenta se la terapia del diabete non è efficace
(valori normali < 5%).
Glucosio+emoglobina
Emoglobina glicata
Globuli rossi
La formazione di HbA1c avviene durante tutto il periodo di vita del globulo rosso e
dipende anche dall’età cellulare. Un incremento transitorio della glicemia può produrre
la formazione di una notevole quantità di aldimine, reazione comunque reversibile con la
normalizzazione dei valori glicemici. La persistenza di iperglicemia, tuttavia, rende tale
reazione irreversibile, per cui la molecola di emoglobina resterà “glicata” sino alla morte
del globulo rosso (120 giorni).
Dosaggio emoglobina glicosilata (HbA1c)
L’emoglobina glicosilata rappresenta il
prodotto di una reazione non enzimatica
di condensazione tra il gruppo aldeidico
del glucosio e il gruppo amminico Nterminale delle catene β della Hb.
L’entità
della
glicazione
è
proporzionale alla concentrazione di
glucosio ed al tempo di contatto.
Le emoglobine glicate vengono dosate
mediante
tecniche
cromatografiche
(scambio ionico, affinità, HPLC) oppure
isoelettrofocalizzazione o elettroforesi
capillare.