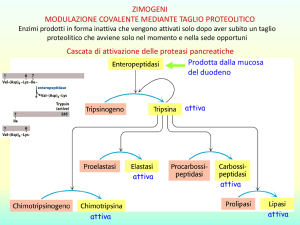
Associazione Nazionale Insegnanti
di Scienze Naturali
Giochi delle Scienze Sperimentali 2014
A - GLI ENZIMI
Gli enzimi sono macromolecole che agiscono da catalizzatori dei sistemi biologici, accelerano cioè la velocità di
una reazione senza essere consumati nel corso della stessa.
L’enzima, specifico per una data molecola di reagente (substrato), lega il substrato formando un complesso
enzima-substrato, accelerandone la trasformazione nel prodotto o nei prodotti della reazione.
Dopo la trasformazione, l’enzima libera il prodotto e può legare un’altra molecola di substrato.
La regione della molecola enzimatica nella quale si lega il substrato è detta sito attivo e, generalmente, si
presenta come una tasca o un solco sulla superficie dell’enzima con forma complementare alla molecola del
substrato.
Le immagini rappresentano le varie fasi dell’attività enzimatica
A
1.
B
C
D
La corretta sequenza delle fasi è:
a.
b.
c.
d.
e.
A-B-C-D
C-A-B-D
C-B-D-A
C-A-D-B
D-B-A-C
La velocità a cui una determinata quantità di enzima catalizza la trasformazione del substrato dipende in parte
dalla concentrazione inziale del substrato: quanto maggiore è il numero di molecole di substrato disponibili
tanto più frequentemente queste si troveranno a interagire con l’enzima e ad essere trasformate.
Esiste tuttavia un limite alla massima velocità della reazione che può essere raggiunta aggiungendo substrato a
una quantità fissa di enzima. Quando, infatti, tutte le molecole di enzima sono legate al substrato, gli enzima sono
saturati e ulteriori incrementi di substrato non determinano l’aumento della velocità di reazione.
2.
Se un enzima è saturato con il substrato, il modo più efficace per ottenere una produzione più rapida dei
prodotti è quello di:
a.
b.
c.
d.
aggiungere altro substrato
aggiungere altro enzima
aumentare la temperatura a 90°C
abbassare la temperatura
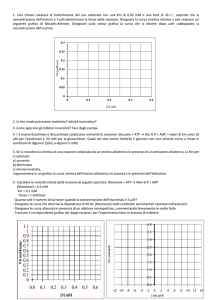
Nel grafico è riportata la velocità con cui un enzima catalizza la trasformazione del substrato.
3.
Quale è il numero di particelle di substrato che saturano l’enzima?
Una ricercatrice, dopo aver aggiunto ad una soluzione enzimatica il substrato specifico, misura la quantità dei
prodotti della reazione.
I risultati vengono riportati in un grafico in cui sull’asse y compare la quantità di prodotto (in mg) e sull’asse x il
tempo (in minuti).
La ricercatrice, osservando il diagramma tracciato, nota che per un certo tempo non compaiono i prodotti della
reazione, quindi la velocità della reazione diviene assai rapida, dopo un certo tempo la reazione rallenta e
successivamente aumenta ancora.
4.
Quale grafico sta analizzando la ricercatrice?
a.
b.
c.
d.
Grafico a
Grafico b
Grafico c
Grafico d
La lattasi è un enzima, localizzato principalmente nella parete intestinale dei mammiferi, che catalizza la
reazione di idrolisi (scissione) del lattosio presente nel latte nelle due molecole componenti, glucosio e
galattosio. Queste, a differenza del lattosio, possono essere assorbite.
In assenza di tale enzima il soggetto manifesta la così detta intolleranza al lattosio, una sindrome caratterizzata
da disturbi gastroenterici, quali crampi addominali, diarrea, meteorismo e flatulenza (produzione e accumulo di
gas nel tratto intestinale).
5.
Nel caso un neonato mancasse dell’enzima lattasi, quale consiglio potresti dare alla madre?
a.
b.
c.
d.
Non somministrare latte e sostituirlo con tè o acqua
Somministrare latte delattosato (detto anche ad alta digeribilità)
Bollire a lungo il latte prima della somministrazione
Aggiungere molto zucchero al latte
B - LA RADIOATTIVITÀ
Il nucleo di ogni atomo è formato da due tipi di particelle: i protoni, con carica positiva, e i neutroni, privi di
carica.
Il numero dei protoni o numero atomico è caratteristico di ogni elemento. In natura non tutti gli atomi di uno
stesso elemento hanno lo stesso numero di neutroni. Ad esempio, la maggior parte degli atomi di idrogeno
contiene nel nucleo un solo protone e nessun neutrone, ma esistono atomi di idrogeno con un protone e un
neutrone e altri con un protone e due neutroni. Si dice allora che l’atomo di idrogeno ha altri due isotopi: il
deuterio (con 1 protone e un neutrone) e il trizio (con un protone e due neutroni).
I neutroni, oltre a conferire massa all’atomo, ne determinano la maggior o minor stabilità: essi rappresentano
una sorta di cuscinetto isolante per i protoni che, essendo tutti dotati della stessa carica positiva, tenderebbero a
respingersi.
Esistono alcuni elementi con elevato numero atomico (cioè con elevato numero di protoni presenti nel nucleo) in
cui il numero di neutroni è più basso rispetto al numero di protoni. I neutroni presenti non sono allora sufficienti
a tenere unite le particelle del nucleo che diviene così instabile e tende a raggiungere la stabilità trasformandosi
nell’atomo di un altro elemento con l'emissione di una o più particelle sotto forma di radiazioni.
Tale trasformazione prende il nome di decadimento radioattivo.
La velocità con cui il nucleo di un elemento, detto radioattivo, decade viene misurata mediante il periodo di
dimezzamento, che è il tempo necessario perché la metà del numero iniziale degli atomi radioattivi di un certo
elemento si trasformi negli atomi di un altro elemento.
Il periodo di dimezzamento varia da elemento a elemento.
Nella tabella sottostante è riportato il tempo di dimezzamento di alcuni elementi radioattivi.
Elemento radioattivo
trizio
radio - 226
radon - 222
potassio - 40
carbonio - 14
torio - 230
uranio - 238
6.
Tempo di dimezzamento
12 anni e 3 mesi
1590 anni
3,8 giorni
1,3 miliardi di anni
5730 anni
80.000 anni
4,51 miliardi di anni
Dopo quanti anni decadono i ¾ degli atomi di uranio?
Grazie alla radioattività di alcuni elementi e al decadimento radioattivo è possibile determinare l’età di una
roccia, stabilire cioè quando si è formata e risalire all’età geologica della zona in cui essa si trova.
È sufficiente determinare in quale proporzione sono presenti gli atomi dell’elemento radioattivo e gli atomi
dell’elemento stabile che dal primo derivano.
La somma del numero degli atomi dell’elemento radioattivo e del numero di atomi dell’elemento stabile indica il
numero di atomi radioattivi inizialmente presenti nella roccia quando questa si è formata. Conoscendo il tempo
di dimezzamento dell’elemento radioattivo, la sua quantità iniziale e quella finale, si può calcolare il tempo
trascorso dalla formazione della roccia, e quindi la sua età.
7.
Supponi che in un frammento di roccia si riscontrino 125 atomi di potassio 40 e 875 atomi di argo
(elemento stabile e non più radioattivo derivante, attraverso una serie di reazioni, dal potassio), qual età ha
la roccia?
8.
Tra le sostanze presenti nella tabella, quale ha minor stabilità?
9.
Calcola quanto trizio rimane dopo 49 anni in un campione che inizialmente era di 24 g.
Massa residua
tempo
Massa residua
Massa residua
10. Quale grafico rappresenta il decadimento radioattivo?
tempo
a
a.
b.
c.
d.
b
c
Grafico a
Grafico b
Grafico c
Nessuno dei tre
C - LE ACQUE MINERALI
Le acque minerali naturali sono acque sotterranee di origine meteorica che durante il tragitto verso la superficie,
si depurano e si mineralizzano acquisendo quei peculiari caratteri chimici, fisici ed organolettici che ne
determinano le proprietà "terapeutiche".
Queste acque differiscono per la qualità e la quantità dei sali minerali presenti, quali calcio, sodio, potassio,
fluoro. Tale quantità viene espressa come residuo fisso a 180°C (R.F.), un valore che indica quanto rimane, in
peso, sotto forma di polvere minerale, dopo l’evaporazione di 1 l di acqua.
In base al residuo fisso, si distinguono:
–
acque minimamente mineralizzate, con R.F. minore di 50 mg/l
–
acque oligominerali o leggermente mineralizzate, con R.F. compreso tra 50 mg/l e 500 mg/l
–
acque medio-minerali o mineralizzate, con R.F. compreso tra 500 mg/l e 1500 mg/l
–
acque ricche di sali minerali, con R.F. superiore a 1500 mg/l
L’etichetta rappresenta la carta d’identità di un prodotto.
Per le acque minerali vi sono delle diciture obbligatorie e delle diciture facoltative da riportare nell’etichette.
Le diciture obbligatorie sono:
–
acqua minerale naturale (tutte, anche le acque addizionate di CO2, riportano questa scritta)
–
denominazione di vendita, località di provenienza, nome del titolare a cui è stata rilasciata
l’autorizzazione
–
risultati delle analisi chimiche e chimico-fisiche (temperatura, pH, conducibilità elettrica, residuo fisso,
gas disciolti e sostanze disciolte)
–
data e laboratorio che ha effettuato le analisi (aggiornate almeno ogni 5 anni)
–
contenuto nominale (la quantità contenuta nella bottiglia, ad es. 50 cl)
–
data di imbottigliamento e numero di lotto
–
addizionata di CO2, se è stata addizionata con anidride carbonica
Si riporta l’etichetta dell’acqua minerale GIOC.
ANALISI CHIMICA E CHIMICO-FISICA
Laboratorio ACAM Acque S.p.A.
Eseguita in data 31 maggio 2013
Temperatura della sorgente (°C) 13,7
pH a 20° C 7,5
Cond. Elettr. Specifica a 20°C 345μS/cm
Residuo fisso a 180°C 170 mg/l
Ammonio e nitrito assenti
ANALISI BIOLOGICA
Laboratorio ACAM Acque S.p.A.
Eseguita in data 31 maggio 2013
ACQUA GIOC
Sostanze presenti in un litro
d’acqua espresse in ioni e mg:
Calcio Ca++
2,6 mg/l
Magnesio Mg++
34,8 mg/l
Sodio Na++
4,2 mg/l
Potassio K+
0,3 mg/l
Solfato SO4=
6,1 mg/l
Idrogeno
Carbonato HCO3169, mg/l
Cloruro Cl7,6 mg/l
Nitrato NO30,5 mg/l
Silice SiO2 34,5 mg/l
I risultati dei controlli e dell’analisi
dimostrano che l’acqua della sorgente
GIOC, prelevata nel Comune di Scorzè (VE)
è risultata batteriologicamente pura.
DA CONSUMARSI PREFERIBILMENTE
ENTRO il 15 /12/2015
1,5 L
AGGIUNTA DI ANIDRIDE CARBONICA
11. In base ai dati riportati nell’etichetta, l’acqua GIOC è un acqua:
a.
b.
c.
d.
Minimamente mineralizzata
Oligominerale
Medio mineralizzata
Ricca di sali minerali
12. Se oggi è il 15 aprile 2014, l’acqua dovrà essere consumata entro:
a.
b.
c.
d.
15 mesi
20 mesi
2 anni
18 mesi
13. In base a quanto riportato nell’etichetta, l’acqua GIOC è:
a. frizzante
b. non frizzante
c. non è possibile stabilirlo
Nella seguente tabella, che riporta il consumo annuale di acqua minerale pro capite in Italia, Germania, Francia,
Spagna, Belgio, Austria, Svizzera, è stata omessa l’indicazione dello stato europeo in corrispondenza delle singole
colonne.
Sappiamo tuttavia che:
in Germania e Spagna il consumo annuale pro capite è lo stesso
il secondo paese per consumo annuale pro capite è la Francia
la Svizzera si colloca immediatamente prima della Germania
in Austria vi è il minor consumo di acqua minerale
in Belgio il consumo pro capite è pari a 128 litri
14. In quale stato europeo vi è il maggior consumo pro capite di acqua minerale?
D – LEBEVANDE ALCOLICHE
Per titolo alcolometrico o gradazione alcolica, espressa con il simbolo “% Vol”, si intende il numero di ml di alcol
etilico (etanolo) contenuti in 100 ml di bevanda alcolica.
Il numero di grammi di alcol etilico presente in 100 ml si ottiene moltiplicando il titolo alcolemico per 0,79
(densità dell’etanolo)
Marco ha acquistato una bottiglia di Bianco Secco, di cui si riporta l’etichetta.
LA FATTORIA
Bianco secco
Podere la Vigna
Castellina in Chianti –Italia
750 ml
12 % Vol
15. Quanti ml di alcol etilico sono contenuti in 150 ml di Bianco Secco?
16. Sapendo che 1 grammo di alcol etilico fornisce 7 kcal, quante calorie si introducono bevendo 150 ml di quel
vino?
La quantità di alcol che un uomo potrebbe assumere giornalmente è pari a 0,6 g per chilogrammo di peso
corporeo.
17. Un uomo che pesa 80 kg quanti ml di Bianco Secco potrebbe assumere in un giorno (arrotonda il valore
all’unità)?
Vi sono dei pregiudizi e dei luoghi comuni sulle bevande alcoliche e sulle modalità di assunzione.
18. Quali delle seguenti proposizioni sono ERRATE.
a.
b.
c.
d.
e.
f.
g.
L’assunzione di elevate quantità di vino stimola la digestione
Negli anziani va ridotta l’assunzione di alcol etilico
È preferibile bere il vino durante i pasti
Il vino e le bevande alcoliche riscaldano
Un bambino può assumere vino se diluito con un uguale quantità d’acqua
L’etanolo è assorbito più rapidamente dall’organismo se assunto a stomaco vuoto
È preferibile assumere in un breve intervallo di tempo la quantità giornaliera di etanolo consentita
E - SALUTE E MALATTIA
Maria è a scuola ma non si sente bene. Ha mal di testa e improvvisamente sente dei brividi di freddo anche se
l’ambiente è ben riscaldato. Dopo poco, qualche violento starnuto fa girare verso di lei i compagni e l’insegnante
che si accorgono del suo malessere.
19. Da cosa è causato il brivido?
a.
b.
c.
d.
Da una reazione dell’organismo che in questo modo scarica la tensione dovuta al malessere
Da una serie di contrazioni muscolari che trasformano in calore l’energia dei muscoli
Da una serie di scosse nel corpo dovute alla conduzione elettrica che si ha nelle cellule nervose
Dall’elaborazione di un segnale da parte dell’organismo che avverte dell’arrivo di un’influenza
20. La madre di Maria, appena a casa, le misura la febbre con un termometro a mercurio. Inizialmente il
termometro segna 36°C. Dopo pochi minuti il mercurio arriva ai 38 °C. Che cosa è avvenuto al mercurio del
termometro?
a.
b.
c.
d.
Il mercurio si scioglie e quindi sale nel tubicino del termometro fino a 38°
Il mercurio si riscalda per conduzione e si dilata, raggiungendo i 38°C
Il mercurio sale per capillarità nel tubicino molto stretto fino ai 38°C
Il mercurio sale nel tubicino fino a 38°C prendendo il posto dell’aria che si rarefà
21. Viene chiamato il dottore che dopo una visita accurata diagnostica l’influenza, probabilmente dovuta ad un
virus. Quale affermazione relativa ai virus è esatta ?
a.
b.
c.
d.
I virus sono microrganismi simili ai batteri in grado di riprodursi autonomamente
I virus sono sensibili agli antibiotici che impediscono la loro riproduzione
Ogni anno ci sono nuovi virus provenienti da mutazioni e quindi nuovi tipi di influenza
Ogni anno ci sono nuovi virus perché le persone viaggiano molto
22. L’organismo reagisce ai virus grazie alle proprie difese immunitarie. Quali sostanze specifiche
costituiscono queste difese?
a.
b.
c.
d.
Quelle prodotte dai globuli bianchi chiamate anticorpi
Quelle prodotte dalle piastrine chiamate fibrina
Quelle prodotte dai globuli rossi insieme all’emoglobina
Quelle che l’organismo trae da alcuni alimenti come le vitamine