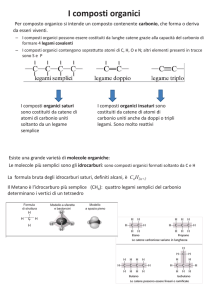
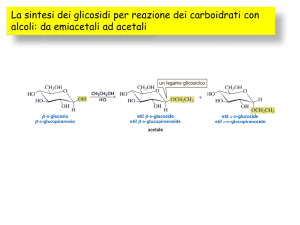
La chimica della vita:
i composti organici.
CARBOIDRATI
LIPIDI
PROTEINE
ACIDI NUCLEICI (DNA, RNA)
POLIMERI
Le cellule sintetizzano un enorme numero di
grosse molecole a partire da una ristretta
serie di molecole più piccole
– Le quattro classi principali di molecole
biologiche sono: carboidrati, lipidi, proteine
e acidi nucleici.
– Molte di queste molecole hanno dimensioni
enormi (dal punto di vista molecolare) e, per
questo, sono definite macromolecole.
POLIMERI (CONDENSAZIONE)
– Le cellule costruiscono la maggior parte delle loro
molecole più grandi unendo molecole organiche più
piccole in catene chiamate polimeri.
– Le cellule legano tra loro i monomeri per formare i
polimeri mediante un processo chimico detto
condensazione.
H
OH
OH
H
Monomero isolato
Breve polimero
Condensazione
H
H2O
OH
Polimero più lungo
POLIMERI (IDROLISI)
– I polimeri sono spezzati in monomeri attraverso la
reazione di idrolisi.
– L’idrolisi è il processo opposto alla condensazione.
H2O
H
OH
Idrolisi
H
OH
OH
H
POLIMERI
CARBOIDRATI
Caratteristiche: Sono composti chimici costituiti da carbonio, idrogeno e ossigeno.
Sono molto abbondanti in natura. Hanno sapore dolce.
Funzioni:
Strutturale: costituiscono strutture essenziali per gli organismi viventi
(funzione di sostegno, soprattutto nei vegetali cellulosa)
Energetica: forniscono energia per svolgere tutte le funzioni dell'organismo
Protezione: costituiscono l’esoscheletro degli invertebrati (chitina)
Organismi autotrofi (Es. piante): sintetizzano
zuccheri (glucosio) a partire da componenti
inorganici quali acqua e CO2 mediante il
processo di fotosintesi clorofilliana.
Organismi eterotrofi (Es. animali): soddisfano il fabbisogno
energetico nutrendosi di alimenti che contengono zuccheri.
Ecco alcuni esempi:
frutta e miele -> fruttosio; glucosio
barbabietola da zucchero, zucchero di canna -> saccarosio
latte e latticini -> lattosio
cereali (pane, pasta, riso), tuberi (patate) e legumi -> amido
carne e pesce -> glicogeno
CARBOIDRATI
Monosaccaridi
(formati da 1
molecola di
zucchero)
Disaccaridi
(formati da
2 molecole
di zucchero)
Polisaccaridi
(formati da
più di 20
molecole di
glucosio)
5C
Ribosio
Desossiribosio
6C
Glucosio principale fonte di energia
Fruttosio si trova nella frutta
Galattosio
Componenti degli acidi nucleici
Glucosio + fruttosio Saccarosio (comune zucchero da cucina)
Glucosio + glucosio Maltosio (deriva da digestione dell’amido)
Glucosio + galattosio Lattosio (in latte e latticini)
Amido riserva energetica nei vegetali (cereali, tuberi, legumi)
si accumula in amiloplasti nella cellula vegetale
si trova nei semi e nelle radici
Glicogeno riserva energetica negli animali
si accumula in muscoli e fegato
Cellulosa funzione di sostegno nei vegetali
si trova nella parete cellulare delle cellule vegetali
può essere digerita solo dagli erbivori
è il composto organico più abbondante sulla Terra
CARBOIDRATI
struttura a sedia
Gruppo Aldeico
C6H12O6
struttura lineare
IL GLUCOSIO
Come si formano i disaccaridi?
Reazione di
condensazione
Glucosio
OH
HO
O
Fruttosio
H2O
Saccarosio
Reazione di
condensazione
Glucosio
OH
HO
O
Glucosio
H2O
Maltosio
Reazione di
condensazione
Glucosio
OH
HO
O
Galattosio
H2O
Lattosio
IDROLISI DI UN DISACCARIDE
I polisaccaridi di interesse biologico
L’amido e il glicogeno immagazzinano zuccheri di riserva
La cellulosa si trova nelle pareti delle cellule vegetali
Granuli di amido in
cellule di tubero di
patata
Ramificazione
Monomeri di
Amido
legame
1-6 glicos.
glucosio
Granuli di glicogeno nel
tessuto muscolare
Glicogeno
Fibre di cellulosa nella parete di
una cellula vegetale
Molecole
di cellulosa
Cellulosa
PROTEINE
Caratteristiche:
sono catene (polimeri) di amminoacidi
sono il più abbondante materiale biologico negli organismi animali
sono essenziali per la struttura e le funzioni degli esseri viventi
Le informazioni per la costruzione delle proteine sono contenute
nei geni, cioè nelle sequenze di DNA
Funzioni:
Strutturale Es. tubulina e actina sono proteine del citoscheletro
cheratina forma i capelli
collagene componente di pelle, tendini, legamenti
proteine della seta ragnatela
Contrazione Es. actina e miosina contrazione muscolare
Riserva ovalbumina, nell’uovo, ha funzione di riserva per l’embrione
Recettoriale recepiscono i segnali inviati dalle cellule
Enzimatica Es. enzimi digestivi facilitano la digestione degli alimenti
Trasporto Es. emoglobina trasporta ossigeno ed anidride carbonica
nei globuli rossi del sangue
Segnale di comunicazione tra le cellule ormoni, fattori di crescita
Difesa immunitaria Es. anticorpi combattono le infezioni
Gli amminoacidi sono le subunità che
costituiscono le proteine
R
Le proteine sono costituite da 20 aminoacidi diversi,
caratterizzate da diversi gruppi R.
IL LEGAME PEPTIDICO
Amminoacido
1
COOH
CH3
H2O
COOH
H
C
CH3
C
H
H–N-H
H–N-
Legame
peptidico
O=C - OH
O=C Amminoacido
2
CH3
C
H
CH3
C
H
NH2
NH2
Dipeptide
Il legame peptidico si forma tra reazione di un gruppo
carbossilico con un gruppo amminico di due amminoacidi diversi,
con la formazione di una molecola di acqua.
La struttura delle proteine
Struttura primaria: sequenza di
amminoacidi che forma una catena
polipeptidica.
Struttura secondaria: catena
polipetidica si ripiega a formare
struttura ad α-elica o struttura a
foglietti β .
Struttura terziaria: catena polipetidica
può essere lineare (proteina fibrosa) o
avvolgersi su se stessa assumendo una
forma quasi sferica (proteina globulare)
Struttura quaternaria: associazione di
più catene polipetidiche. Es. emoglobina
(proteina presente nei globuli rossi, con
funzione di trasporto dell’ossigeno nel
sangue)
La struttura terziaria
dipende dalle interazioni
dei gruppi laterali.
La struttura quaternaria deriva dalle
interazioni tra i polipeptidi.
574 aminoacidi organizzati in 4
catene polipeptidiche, 2 α e 2 β
Le informazioni per la sintesi delle proteine sono
contenute nel DNA
DNA
trascrizione in mRNA
traslocazione del
mRNA nel citoplasma
traduzione nei ribosomi
presenti nel reticolo
endoplasmatico rugoso
Sintesi delle proteine
20
Funzioni delle proteine di membrana
Adesione
Ancoraggio alla matrice
extracellulare
Enzimi che catalizzano
reazioni
Ruolo di riconoscimento
cellulare
Passaggio selettivo di ioni
e molecole
Trasporto di soluti con
apporto di energia
Legame a molecole
segnale
e trasduzione del
segnale
ACIDI NUCLEICI (DNA ed RNA)
Gli acidi nucleici trasmettono il
patrimonio genetico e determinano
la sintesi proteica, quindi la
struttura e le funzioni cellulari.
DNA: acido desossiribonucleico
RNA: acido ribonucleico
ZUCCHERO: Ribosio (RNA)
BASI
AZOTATE:
e Deossiribosio (DNA)
A, G, T, C sono presenti nel DNA
A, G, U, C sono presenti nel RNA
Guanina G
Adenina A
Purine
Uracile U
Pirimidine
U
Timina T
Citosina C
Subunità nucleotidiche del DNA
NUCLEOTIDE= Zucchero +
Base azotata +
Gruppo fosfato.
Pirimidine
Purine
L’ATP
L’adenosintrifosfato (ATP) è formato da una molecola di
adenina, da una di ribosio e da tre gruppi fosfato.
L’idrolisi dell’ATP libera energia: è un meccanismo che
permette alle cellule di spendere piccole quantità di energia,
quando necessario.
Alcuni nucleotidi svolgono un ruolo
importante nei trasferimenti di energia
Il NAD+ funziona da accettori di 2 elettroni e di un
protone che vengono sottratti dal substrato da specifici
enzimi detti deidrogenasi piridiniche.
L’ossidazione del substrato porta alla formazione del
coenzima ridotto (NADH).
La reversibilità della reazione catalizzata dalle
deidrogenasi permette all’enzima di ossidare o ridurre il
substrato a seconda delle richieste metaboliche
NAD+ NADH + H+
non è legato all’enzima, funziona da co-substrato
OSSIDA:
alcol aldeide/chetone
aldeide acido
NAD+ è prevalentemente usato nelle vie cataboliche
ossidative:
- Glicolisi
- Ciclo di Krebs
- β-ossidazione degli acidi grassi
In tali reazioni il NAD+ si riduce a NADH, che si
riossida a NAD+ cedendo elettroni alla catena
respiratoria mitocondriale
DNA: Legami idrogeno tra le basi
Il DNA è costituito da due catene polinucleotidiche
avvolte a formare una doppia elica
Distanza tra le
coppie di basi
Un giro d’elica =
10 coppie di basi
Diametro
dell’elica
Nel 1953 Watson e Crick proposero per il DNA una struttura a
doppia elica con filamenti antiparalleli e con le basi attaccate da
legami idrogeno.
Il loro modello è in accordo con tutte le funzioni attribuite alla
molecola: informazione genica, mutazione e replicazione.
Come detto oltre al DNA, abbiamo un altro acido nucleico che è l’RNA,
questo si presenta in tre forme diverse definite:
mRNA messaggero;
tRNA di trasporto;
rRNA ribosomiale
Organizzazione del DNA in CROMOSOMI


![mutazioni genetiche [al DNA] effetti evolutivi [fetali] effetti tardivi](http://s1.studylibit.com/store/data/004205334_1-d8ada56ee9f5184276979f04a9a248a9-300x300.png)