Master di II Livello
Il trattamento della patologia
degenerativa del ginocchio
La terapia conservativa: ruolo della terapia
medica; ruolo della terapia infiltrativa
Prof. Maurizio Taglialatela
Ordinario di Farmacologia
Dipartimento di Medicina e di Scienze della Salute
Università del Molise
EFFETTO DELLA TERAPIA PROLUNGATA
SULLE FASI EVOLUTIVE DELL’ARTROSI
Gravità dell’artrosi
Terapia
Fasi distruzione
e riparazione
Scompenso
articolare
Tempo
Patologia conclamata
Consensus Conference 2003
EFFETTI CLINICI DI TRATTAMENTI DI
DURATA DIVERSA CON FARMACI
ANTIINFIAMMATORI
Schema tradizionale
Obiettivo terapeutico:
diminuzione del dolore
Soglia
dolore
Remissione
breve
Infiammazione
Tempo
Obiettivo terapeutico:
• diminuzione del dolore
• riduzione dell’infiammazione
Nuovo schema terapeutico
Soglia
dolore
Infiammazione
• riduzione del N°/severità delle
riacutizzazioni
Tempo
• rallentamento
della progressione del danno
Consensus Conference 2003
J Am Osteopath Assoc 2007
OSTEOARTROSI:
OPZIONI FARMACOLOGICHE
TERAPIA TOPICA
Capsaicina
FANS
Lidocaina
TERAPIA ORALE
Paracetamolo
FANS/COXIB
Tramadolo
Oppioidi
TERAPIA INFILTRATIVA
Corticosteroidi
Acido Ialuronico
MECCANISMI DEL DOLORE
Trasmissione
lungo le fibre
sensitive
Genesi del
potenziale d’azione
Attivazione
nocicettori
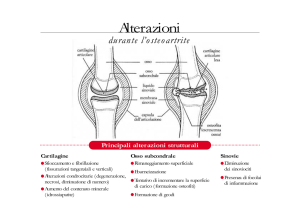
NOCICETTORI
• I nocicettori sono situati a livello della capsula, dei menischi,
del periostio e dell’osso subcondrale, non della cartilagine
articolare.
• In presenza di edema o di mediatori dell’infiammazione, la
soglia di attivazione dei nocicettori è diminuita, per cui anche un
semplice movimento può causare dolore
• Il danneggiamento delle terminazioni nervose può renderle più
sensibili.
• L’attivazione dei nocicettori (e la conseguente genesi del
potenziale d’azione) è possibile grazie a specifici canali ionici.
CANALI, RECETTORI E MECCANISMI
TRASDUZIONALI DELLE VIE NOCICETTIVE
STIMOLO DOLOROSO E CANALI IONICI
TRP: transient receptor potential
TRP
• Canali cationici non selettivi
• Sei domini transmembrana
• Tetramero (omo- o etero-)
• Fra essi, particolare
importanza riveste il
recettore TRPV1
TRPV1 è espresso nei DRG,
nelle vie nervose spinali e in
varie regioni cerebrali.
Oltre ad essere espressi sui
nocicettori (con conseguente
attivazione delle fibre C), i
TRPV1 modulano anche il
rilascio di sostanza P e di
altri peptidi proinfiammatori
(CGRP, CCK ecc) .
TRPV1: ATTIVAZIONE
DIRETTA
CAPSAICINA (VANILLOIDI)
PROTONI
ANANDAMIDE
INDIRETTA
BRADICHININA
PROSTAGLANDINE
TRPV1: ATTIVAZIONE E MODULAZIONE
Scoville Heat Rating
Peppers
Heat Rating
Bell/Pimento
0
Cherry/Pepperoncini
100 - 500
New Mexico
500 - 1000
Poblano/Ancho/Pasilla
1000 - 1500
Rocotillo/Numex Big Jim
1500 - 2500
Jalapeno/Mirasol
2500 - 5000
Chipotle/Yellow Wax/Serrano
5000 - 15000
Manzano/De Arbol
15000 - 30000
Cayenne/Tabasco
30000 - 50000
Thai/Piquin
50000 - 100,000
Habanero/Scotch Bonnet/Birds Eye
100,000 - 350,000
Red Savina Habanero
350,000 - 600,000
Pure Capsaicin
16 Million
CAPSAICINA: meccanismo d’azione
Sebbene sia un agonista dei recettori TRPV1, l’applicazione topica
prolungata della capsaicina provoca una riduzione della sensibilità agli
stimoli dolorosi. Ciò avviene a causa di:
• desensibilizzazione dei TRPV1;
• deplezione di neuropeptidi;
• blocco del trasporto assonale di macromolecole;
• inibizione dei potenziali d’azione da depolarizzazione prolungata;
• inibizione dell’attività mitocondriale;
• riduzione delle fibre nervose sensitive epidermiche
CAPSAICINA: UNA METANALISI
Sebbene più efficace del
placebo, la capsaicina è
meno efficace dei FANS
topici.
Il suo ruolo attuale può
essere definito come
aggiuntivo rispetto a terapie
più tradizionali.
BMJ, 2004
STIMOLO DOLOROSO E CANALI IONICI (II)
• L’intensa stimolazione meccanica porta all’attivazione di una
subpopolazione specifica di recettori (meccanorecettori ad alta soglia).
• Tra I canali ionici implicati nella funzione recettoriale troviamo membri
della famiglia degli ENaC (canali del sodio epiteliali) e degli ASIC (acidsensing ion channel), in particolare il tipo 3; gli ASICs sono responsabili
anche del dolore associato a danno tissutale (con conseguente rilascio di
protoni).
• Il danno tissutale può portare a rilascio di ATP, che può agire sui
recettori P2X2, P2X3 e P2Y2, con successiva attivazione dei nocicettori.
VOLTAGE GATED SODIUM CHANNELS
(VGSC)
• Cruciali nella genesi del
potenziale d’azione e
nella trasmissione del
segnale lungo le fibre
nervose
• Composti da una
subunità α e due subunità
β
• Largamente espressi
nelle terminazioni che
innervano le articolazioni
• La loro attività può
essere modulata
dall’edema o da mediatori
dell’infiammazione
presenti nel liquido
sinoviale
VOLTAGE GATED SODIUM CHANNEL (VGSC)
Subunità α espresse sui neuroni sensitivi primari
Il sottotipo Nav1.7 sembrerebbe un target terapeutico ideale, poiché mutazioni “loss of
function” nel gene codificante per tale subunità causano insensibilità al dolore
(indifferenza congenita al dolore) laddove mutazioni “gain of function” sono responsabili
di sindromi familiari iperalgogene (Dolore rettale familiare, eritermalgia primaria)
CHIUSO
APERTO
INATTIVATO
LIDOCAINA
• La lidocaina è un anestetico locale di tipo amidico
• Si lega al canale del sodio voltaggio dipendente in un sito posto all’interno del
poro
• In virtù di tale caratteristica, l’entità del blocco del canale è frequenza di
stimolo-dipendente, tanto maggiore quanto maggiore è la rapidità di
dissociazione del farmaco dal sito di legame
LIDOCAINA TOPICA
La ridotta stimolazione nervosa
causa la riduzione dei fenomeni di
sensibilizzazione centrale
DOLORE INFIAMMATORIO CRONICO
sensibilizzazione centrale e periferica
Il dolore infiammatorio rappresenta una normale risposta al danno tissutale.
Il danno tissutale può causare cambiamenti nei neuroni sensitivi primari e in quelli
delle corna dorsali
SENSIBILIZZAZIONE PERIFERICA: riduzione della soglia di trasduzione e
aumento della risposta agli stimoli dei nocicettori. Tale effetto è ottenuto
attraverso la liberazione di mediatori come ACTIVINA (TGF beta family), TNF,
CCL3, triptasi e tripsina. Tali molecole attivano pathways (PKC, PKA, PI3 kinase,
MAP) che modulano l’attività di TRP e VGSC.
SENSIBILIZZAZIONE CENTRALE: aumento dell’eccitabilità di membrana e della
risposta sinaptica a livello delle corna dorsali (attivazione di chinasi e
fosforilazione recettore NMDA; aumentata espressione COX-2 e aumento
neurotrasmissione).
ALCUNI MEDIATORI DELLA
RISPOSTA INFIAMMATORIA ACUTA
ATTIVITA’
BIOLOGICHE DI
PRINCIPALI
EICOSANOIDI
GLI ENZIMI CICLOSSIGENASI
Le CICLOSSIGENASI (COX)
catalizzano due diverse
reazioni:
1.
REAZIONE
CICLOSSIGENASICA:
Inserimento di due ossigeni
nell’ a. arachidonico per
sintetizzare PGG2
2.
REAZIONE
PEROSSIDASICA: Riduzione
della PGG2 a PGH2
Esistono almeno due isoforme
di COX:
A. COX 1 o costitutiva
B. COX 2 o inducibile
DIFFERENZE TRA COX1 E 2 NEL SITO
CATALITICO
• L’ aminoacido 523
della COX2 e’ una
valina invece che
una isoleucina
• Ciò crea una tasca
laterale nella COX-2
che manca nella
COX-1
• Qui si legano i
grossi gruppi
laterali dei COXIBs
FANS
Bloccando l’attività della COX-2 i FANS hanno azione analgesica,
antiinfiammmatoria ed antipiretica.
Diverse classi:
SALICILATI (Aspirina)
PARACETAMOLO (ACETAMINOFENE)
DERIVATI DELL’ACIDO ACETICO (Indometacina, Sulindac, Etodolac)
FENAMATI
DICLOFENAC, KETOROLAC
DERIVATI DELL’ACIDO PROPIONICO (Ibuprofene, Naprossene, Ketoprofene)
ACIDI ENOLICI (Enoxicam, Piroxicam)
FARMACI COX-2 SELETTIVI (Coxib)
FANS (II)
• I FANS possono essere somministrati sia per via topica (patch) che per via
sistemica; nel primo caso l’efficacia è limitata alle prime 2 settimane di trattamento.
• Il paracetamolo per os rappresenta spesso il primo approccio terapeutico nei
pazienti con osteoartrosi; il suo effetto è riconduciubile all’inibizione della sintesi della
prostaglandine a livello centrale (scarsa attività a livello periferico): la sua attività è
perciò prevalentemente analgesica.
• La maggiore limitazione all’uso dei FANS è rappresentata dagli effetti colllaterali
gastrointestinali (dispepsia, sanguinamenti).
• Inoltre i FANS possono causare segni di sofferenza renale:
→ Lievi come edema e ritenzione sodica
→ Iperpotassiemia nei pz che assumono integratori di potassio, diuretici
risparmiatori di potassio o ACE-inibitori soprattutto nei pz con
insufficienza cardiaca e diabete mellito.
• Complicanze rare ma molto più gravi come nefropatia interstiziale acuta e la necrosi
papillare renale.
SOLUZIONI SPERIMENTALI:
FANS INTRA-ARTICOLARI IN MICROSFERE
METABOLISMO
DEL
PARACETAMOLO
COXIB
• Introdotti in terapia per la loro azione selettiva sulla COX-2, quindi
potenzialmente privi di tossicità gastrointestinale
• Tuttavia diversi studi hanno dimostrato che essi si associano ad un maggiore
rischio di eventi cardiovascolari acuti (in particolare il rofecoxib, a dosi >25mg è
associato ad un rischio maggiore di IMA rispetto al colecoxib nei primi 90 giorni
di terapia (Circulation. 2004 ).
• I COXIB perciò risultano controindicati nei pazienti con malattia cardiaca o
stroke, o con ipertensione arteriosa non controllata.
• Una recente meta-analisi (Chen et al., Health Technology Assessment 2008;
Vol. 12: No. 11) ha dimostrato che i COXIBs presentano profili di efficacia
sovrapponibili a quelli dei FANS tradizionali (non-selettivi), forse con una
migliore tollerabilità GI.
OPPIOIDI
• Alternativa o supporto nei pazienti in cui FANS e/o COXIB sono
controindicati, scarsamente tollerati o inefficaci
• CODEINA
• TRAMADOLO
• OSSICODONE
1°step
• FENTANIL
• BUPRENORFINA
• MORFINA
2°step
SITI D’AZIONE DEGLI OPPIOIDI
Effetti farmacologici
Gli effetti analgesici sono dovuti
alla capacità di inibire
direttamente la trasmissione
ascendente degli impulsi
nocicettividalle corna dorsali del
midollo spinale e di attivare i
circuiti di controllo del dolore
discendenti dal talamo alle
corna dorsali
Potente effetto analgesico
PAG = sostanza grigia
periacqueduttale
NRPG = nucleo reticolare
paragigantocellulare
TERAPIA DEL DOLORE OSTEOARTROSICO
10 INTOLLERABILE
SCALA
ANALGESIC
A OMS
DOLORE MODERATO
Oppioidi deboli
Fans
Adiuvanti
DOLORE LIEVE
Fans
Adiuvanti
0 ASSENTE
DOLORE FORTE
Oppioidi forti
Fans
Adiuvanti
Il dolore
persiste
o aumenta
GLUCOSAMINA E CONDROITINA
• La glucosamina è un monosaccaride usato come agente capace di
ridurre i sintomi e di ritardare la progressione dell’osteoartrosi.
• Tale farmaco sarebbe capace di stimolare la riparazione della
cartilagine stimolando la sintesi di proteoglicani da parte dei condrociti.
• É un farmaco a lenta insorgenza d’azione (l’effetto è visibile dopo
alcune settimane)
• La condroitina è un glucosamminoglicano capace di aumentare la
viscosità delle articolazioni e in grado di stimolare la riparazione della
cartilagine
GLUCOSAMINA
CONDROITINA
GLUCOSAMINA E CONDROITINA
Possibili meccanismi d’azione
• La biodisponibilità di glucosamina è maggiore di quella di condroitina dopo
somministrazione per os (25% vs 13%).
• Entrambi i farmaci presentano scarsi effetti collaterali (prevalentemente di tipo
gastrointestinale).
• Particolare attenzione nella somministrazione di glucosamina deve essere posta
nei pazienti allergici ai molluschi, in quanto viene estratta dal guscio
chitinoso dei gamberi.
GLUCOSAMINA E CONDROITINA
Studi clinici
Diversi studi clinici sull’efficacia di tali sostanze sono stati condotti, con
risultati non sempre concordanti.
Condroitina e glucosamina, somministrate per via orale, sembrano
comunque ridurre i sintomi associati all’osteoartrosi e rallentare la
progressione della malattia
L’elevatà variabilità dei risultati può dipendere sia dalle diverse
formulazioni utilizzate (per es., la glucosamina solfato sembra essere
più efficace dell’idrocloruro, con un effetto addizionale positivo da parte
della condroitina solfato) che possono alterarne le proprietà
farmacocinetiche e farmacodinamiche, che dalla concomitante terapia
con altri farmaci (es. FANS), o dalla diversa severità della malattia
LINEE GUIDA (I)
LINEE GUIDA (II)
STRUTTURA DELLA CARTILAGINE
LAMINA SPLENDENS
STRATO SUPERFICIALE
STRATO INTERMEDIO
STRATO RADIALE
STRATO MINERALIZZATO
MATRICE EXTRACELLULARE
MATRICE EXTRACELLULARE
• Formata dalla sostanza amorfa e da macromolecole strutturali che
conferiscono al tessuto forma e stabilità.
• La sostanza amorfa è composta da acqua (60-80%), gas, piccole proteine,
metaboliti e cationi.
• Le macromolecole strutturali (20-40%):
proteoglicani, glicoproteine e collagene.
La funzione della sostanza fondamentale è di assorbire le forze di compressione
PROTEOGLICANI:
Assorbono gli shock meccanici
COLLAGENE:
Scarica le forze di trazione
ACIDO IALURONICO (HA)
• L’acido ialuronico è un polimero cosituito da unità
disaccaridiche (acido D-glucuronico e N-Acetil
Glucosamina), isolato ed analizzato per la prima
volta nel 1934.
• É il maggiore componente della matrice
extracellulare
• La sua sintesi è catalizzata da tre enzimi (HA
sintasi)
FUNZIONI DELL’HA
L’HA interagisce con i proteoglicani per generare aggregati con peso
molecolare molto alto capaci di trattenere grandi quantità di acqua
NELLA CARTILAGINE:
• Componente della lamina splendens
• Aggregante dei proteoglicani
• Ammortizzante dei condrociti
• Determina il turgore e la deformabilità
elastica della cartilagine
• Controllo della diffusione dei soluti
• Controllo dei rapporti tra condrociti,
PG, collageni cartilaginei.
NEL LIQUIDO SINOVIALE:
• Controllo della distribuzione dei soluti
• Responsabile della viscosità
• Azione lubrificante e ammortizzante
• Separazione delle superfici articolari in
carico
FUNZIONI DELL’HA (II)
Accanto al ruolo puramente meccanico, negli ultimi anni sono emerse nuove e
più estese funzioni dell’HA; esso sembra essere infatti coinvolto in:
• Ovulazione e fertilizzazione
• Processi neoplastici
• Regolazione del sistema immunitario
Nell’espletamento di quest’ultima funzione, l’HA sembrerebbe legarsi a diverse
molecole recettoriali come CD44, RHAMM, HBP ecc, causando la migrazione
dei linfociti verso il sito di infiammazione.
Inoltre, il legame con CD44 induce il rilascio di numerose citochine da diversi tipi
del cellulari del sistema immunitario (IL-2, IL-1, TNF-alfa, RANTES, MIP1alfa
ecc) e media la proliferazione e la funzione condrocitaria.
L’HA media anche il reclutamento, la migrazione e la maturazione delle cellule
di Langherans, cellule dendritiche a funzione antigene-presentante presenti in
diversi distretti, inclusa la cartilagine.
FUNZIONI DELL’HA (II)
HA E STUDI SPERIMENTALI
Diversi studi hanno evidenziato una molteplicità di effetti dell’HA:
SULLA MATRICE EXTRACELLULARE
• Aumentata sintesi di proteoglicani e di condroitin solfato
• Aumentata produzione di proteoglicani ad alto MW
• Protezione della matrice extracellulare dalla degradazione
SUI MEDIATORI DELL’INFIAMMAZIONE
• Riduzione dei livelli di prostaglandine e leucotrieni
• Soppressione di TNF-alfa
• Aumentata produzione di TIMP-1 (iibitore delle metalloproteinasi)
• Riduzione della produzione di acido arachidonico
• Protezione dal danno da radicali
• Riduzione della produzione di NO
SUL SISTEMA IMMUNITARIO
• Riduzione della motilità e della proliferazione linfocitaria
• Inibizione dell’attività fagocitaria dei macrofagi e della degranulazione dei neutrofili
SULLA CARTILAGINE
• Riduzione della degenerazione cartilaginea
• Protezione della morfologia e della compattezza della cartilagine
• Stimolazione della migrazione dei condrociti
Arthritis Res Ther 2003, 5:54-67
TIPOLOGIE FARMACEUTICHE DI HA
• L’HA iniettato nelle articolazioni è eliminato in meno di 24 ore: per aumentarne
l’emivita sono stati sintetizzati dei composti con maggior peso molecolare
(23x106 dalton), che allungano l’emivita fino a 1,5-9 giorni (Hylans).
• Esistono diverse formulazioni di ialuronani (Hyalgan, Synvisc, Supartz,
Orthovisc, Euflexxa, Hylan GF-20, Durolane, Fermatron, Ostenil) che
differiscono per MW .
Il peso molecolare potrebbe influenzare anche le proprietà farmacodinamiche del
composto: in particolare, composti ad alto MW stimolerebbero maggiormente la sintesi
di HA rispetto a quelli con basso MW. Tuttavia, una recente metanalisi consiglia l’uso
di ialuronani a basso MW (Arthritis Rheum. 2007), a causa della maggiore tossicità
locale di quelli ad alto MW.
1.
2.
3.
HA: EFFICACIA CLINICA
• Gli ialuronani sono somministrati per via intracapsulare con diverse modalità (3
iniezioni di Hylan GF-20, 5 iniezioni di Sodio Ialuronato).
• L’efficacia e la tollerabilità è stata oggetto di diversi studi, nei quali i risultati
sono stati spesso discordanti.
• Una recente metanalisi (Cochrane Database Syst Rev. 2006) ha comunque stabilito
l’efficacia moderata-elevata di tali farmaci, con un effetto massimo che si
raggiunge dopo 5-13 settimane dopo le iniezioni, sebbene vi sia un’elevata
variabilità fra le singole formulazioni e riguardo alcune variabili cliniche. Inoltre
l’effetto degli ialuronani, sebbene con latenza maggiore, sarebbe più
prolungato rispetto a quello dei corticosteroidi per via intraarticolare.
HA: EFFETTI COLLATERALI
• L’HA e i suoi derivati sono farmaci ben tollerati.
• In genere causano disturbi di lieve entità, fra cui:
Dolore temporaneo al sito di iniezione
Gonfiore
Rubor e Calor
Prurito
Ecchimosi
• Tali effetti sono più pronunciati per i derivati ad alto MW.
• Per minimizzare tali reazioni avverse il paziente dovrebbe evitare prolungate e
faticose attività nelle successive 48 ore.
• Gli ialuronani non presentano interazioni farmacologiche significative.
• HA e derivati non sono stati testati su bambini, donne in gravidanza e in allattamento.
TERAPIA INFILTRATIVA: CORTICOSTEROIDI
• I corticosteroidi sono stati ampiamente utilizzati nel corso degli anni come
terapia aggiuntiva, specialmente nei casi di infiammazione locale,
evidenziabili clinicamente con eritema ed effusione sinoviale.
• Il loro effetto nel controllo del dolore è però limitato nel tempo (in genere
non più di una settimana, fino ad un massimo di tre settimane) ed è scarso
nei soggetti senza abbondante liquido sinoviale.
• Inoltre non esistono prove certe a sostegno di una possibile azione
ritardante la progressione della malattia.
• Per tale motivo i glucocorticoidi in genere non sono somministrati in
monoterapia.
• In alcuni studi clinici è stata riportata una maggiore efficacia del
triamcinolone rispetto al betametasone.
•I corticosteroidi intra-articolari sono efficaci sul DOLORE e sulla qualità di
vita globale dopo 1 settimana, con efficacia che si mantiene per 2-3
settimane. Dopo, l’efficacia sembra diminuire.
•Sono soprattutto utili nei casi con evidenti segni infiammatori.
•La funzionalità articolare non sembra migliorata.
•L’acido ialuronico o gli ilani, sebbene più lenti nella latenza, sembrano
essere più durevoli rispetto ai corticosteroidi.
•Non è possibile fare differenza tra I diversi glucocorticoidi; il triamcinolone
sembra superiore al betametasone nella riduzione del dolore fino a 4
settimane, ma non vi sono altre differenze.
•Nell’insieme, i corticosteroidi intra-articolari sono efficaci nel trattamento
sintomatico a breve termine dell’OA del ginocchio.
MECCANISMO D’AZIONE
DEI GLUCOCORTICOIDI
• Positivi: induzione della lipocortina (una proteina della
famiglia delle annessine che blocca la PLA2), di IkB, dei
b2R, ACE e NEP, del decoy per IL-1, …
• Negativi: inibiscono importanti fattori di trascrizione, quali
NF-kB e AP1, inibendo l’espressione di molti geni (citochine,
COX-2, nNOS, PLA2, collagenasi, ecc.)
DURATA D’AZIONE DEI GC
IMMUNOSOPPRESSIONE DA GC
AZIONI ANTI-INFIAMMATORIE
E IMMUNOSOPPRESSIVE DEI GC
I GC riducono le manifestazioni dell’infiammazione
per:
•Diminuzione del numero, distribuzione e attività
dei leucociti periferici che solitamente migrano nei
tessuti infiammati (pur aumentando nel sangue!).
•Diminuzione del numero dei monociti, dei linfociti
T e B circolanti.
•Riduzione delle funzioni dei leucociti e dei
macrofagi tra cui la capacità di chemiotassi e di
rispondere ad antigeni e mitogeni
•Diminuzione della produzione di citochine
infiammatorie, di PG e LT, PAF, dell’istamina
•Riduzione della produzione di anticorpi
•Riduzione dell’infiammazione cronica e delle
reazioni autoimmuni.
MECCANISMO DEGLI EFFETTI
ANTI-INFIAMMATORI DEI GC
•
•
•
Ridotta sintesi citochine
Interazione con fattori di trascrizione, con inibita
attivazione di NF-KB sia con meccanismo diretto
(interazione proteina-proteina) che indiretto (stimolata
espressione dell’inibitore IKBα
α)
Stimolata produzione di lipocortina 1 con diminuita
attività delle PLA2, e quindi diminuita sintesi di
EICOSANOIDI
Sono state descritti vari tipi di PLA2:
1. PLA2 extracellulare, a basso peso molecolare (14 kDa) che
viene secreto da varie cellule coinvolte
nell’infiammazione. Pare coinvolto nella liberazione di
acido arachidonico utilizzato dalla PGHS1 (costitutiva)
2. PLA2 intracellulare, ha un peso molecolare di 85 kDa ed è
presente a livello citosolico. Libera acido arachidonico per
la PGHS2 (inducibile)
LINEE GUIDA PER LA TERAPIA
INFILTRATIVA
OA: PROGRESSIONE DEL DANNO
DANNO ALLA
CARTILAGINE
PROGRESSIONE
DELLA MALATTIA
OA: MECCANISMI PATOGENETICI
NUOVE PROSPETTIVE TERAPEUTICHE
Le recenti acquisizioni sulla patogenesi del danno
cartilagineo nell’osteo-artrosi hanno individuato nuovi siti di
intervento terapeutico:
• Inibizione della iNOS (NO aumenta l’attività delle MMP,
inibisce la sintesi della matrice ed induce l’apoptosi nei
condrociti).
•Terapia con citochine antinfiammatorie
•Inibizione citochine pro-infiammatorie
•Inibizione delle metalloproteinasi
•Calcitonina
•Lubrificanti:
SAPL (Surface active Phospolipids)
DPPC (L-alfa-dipalmitoyl-fosfatidil-colina)