LA RESPIRAZIONE
CELLURARE
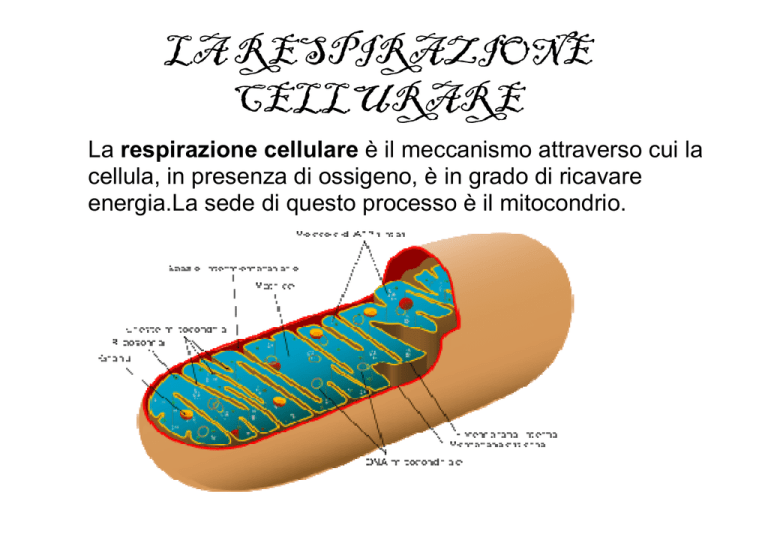
La respirazione cellulare è il meccanismo attraverso cui la
cellula, in presenza di ossigeno, è in grado di ricavare
energia.La sede di questo processo è il mitocondrio.
I mitocondri (dal greco”mitos”,filo
e“condros”corpuscolo)generalmente definiti”la
centrale elettrica della cellula”
sono degli organuli endocellulari che presentano una
forma bastoncellare o a fagiolo con un diametro di 0,5
µm ed una lunghezza di 1-2µm.Morfologicamente i
mitocondri sono caratterizzati da una membrana esterna
e da una membrana interna.le due membrane
delimitano
due compartimenti che sono chiamati camera esterna e
matrice.La camera esterna è lo spazio compreso tra le
due membrane,la matrice è , invece,lo spazio delimitato
dalla membrana interna.
La membrana interna presenta delle invaginazioni,che
si estendono nella matrice,denominate creste
mitocondriali.Le due membrane differiscono fra di
loro per la composizione chimica,infatti la
membrana esterna e caratterizzata da un maggiore
contenuto di lipidi rispetto alle proteine mentre la
membrana interna risulta essere costituita
maggiormente da proteine ed inoltre è
caratterizzata dalla presenza di cardiolipina,un
fosfolipide raro che d’altra parte è del tutto assente
in quella esterna.
Nella matrice sono contenuti ribosomi e molecole
circolari di mtDNA che sono molto simili a quelli
delle cellule procariotiche e la loro presenza
permette ai mitocondri la sintesi di proteine che
rendono questi organuli semi-autonomi rispetto alla
cellula stessa.Tra le sostanze che essi possono
sintetizzare autonomamente sono comprese le
proteine del comlplesso Fo-F1 ATPsintetasi
Fo è un complesso proteico che svolge la funzione di
canale di transito per protoni,F1 catalizza la reazione di
sintesi dell’ATP,che costituisce la moneta energetica,a
partire da ADP+Pi.
Cosa avviene nel processo
di respirazione cellulare?
All’interno dei mitocondri avvengono delle reazioni
redox,che producono energia,nelle quali un composto
(riducente) trasferisce elettroni ad un altro composto
(ossidante).In queste reazioni gli elettroni si spostano
da composti che li legano a se ad alti livelli energetici
a composti che li legano a livelli energetici sempre più
bassi fino ad arrivare all’accettore finale che è
l’ossigeno il quale,con l’aggiunta di due protoni
H+,formerà H2O.
Un ruolo molto importante che consiste nel trasporto
degli elettroni fino all’accettore finale ,che abbiamo
detto essere l’O2,lungo la catena respiratoria è svolto
dai cofattori NAD+ e FAD,che veicolano gli elettroni
riducendosi a NADH+H+ e FADH2.
NAD(NICOTINAMMIDE ADENIN DINUCLEOTIDE)
FAD(FLAVIN ADENIN DINUCLEOTIDE)
Le molecole che ,ossidandosi,consentiranno ai
mitocondri di produrre ATP sono i carboidrati,i lipidi,le
proteine e gli acidi nucleici.Poichè sono molecole
relativamente grandi prima di entrare nei mitocondri
subiranno delle particolari modificazioni che
differiscono a seconda della natura chimica.I
carboidrati vengono idrolizzati in monosaccaridi,le
proteine in amminoacidi che successivamente
verranno deaminati(-NH2),I lipidi scissi in glicerolo e
acidi grassi.Tali modificazioni prendono luogo nel
citoplasma,ed inoltre i monosaccaridi sono soggetti ad
un’ulteriore trasformazione che porta alla formazione
di piruvato( CH3-CO-COOH) e che prende il nome di
glicolisi.
LA GLICOLISI
Essa dunque consiste nel
processo di ossidazione di un monosaccaride con
formazione di due molecole di piruvato che si realizza
in dieci tappe.
Reazione 1
Nella 1°tappa il glucosio viene fosforilato in gluco sio 6-fosfato.
la reazione è catalizzata dall’enzima
esochinasi con consumo di una molecola
di ATP.
Reazione 2
Nella 2°tappa si ha l’isomerizzazione
Del glucosio 6-P in fruttosio 6-P.
Ad opera è l’enzima
Fosfoglucoisomerasi.
Reazione 3
Nel 3°step il fruttosio 6-P viene
ulteriormente fosforilato.L’enzima
catalizzante è la fosfofruttochinasi.
A tal punto la cellula si trova in
difetto di 2 ATP,che sono state usate
per formare una molecola instabile in modo da facilitare la
rottura del legame covalente,infatti la presenza nella molecola di
due radicali fosforici legati al C1 e al C6,che sono all’esterno
dell’anello,fa si che gli elettroni vengano attratti dai due fosfati.
Ciò indebolirà il legame tra gli atomi di C3 e C4,favorendo la
rottura della molecola e la formazione di due molecole a tre
atomi di carbonio:
La (3PGAL)Gliceraldeide 3-fosfato
e il (DHAP)Diidrossiacetone fosfato.
Reazione 4
La 4°fase della glicolisi ,catalizzata dall’enzima a ldolasi,consiste
nella scissione del fruttosio 1,6-bifosfato in gliceraldeide-3-P e
diidrossiacetone fosfato,composti a tre atomi di
carbonio.Tuttavia soltanto la 3PGAL entra nella fase
successiva.
Reazione 5 e 6
Man mano che la 3PGAL viene consumata cedendo 2 elettroni e
e due protoni al NAD+ riducendolo a NADH+H+ formando 1,3
difosfoglicerato ad opera della 3PGAL
deidrogenanasi(REAZIONE 6) ,entra in gioco un
enzima,la trioso fosfato isomerasi,che trasforma il DHAP in
3PGAL.
Reazione 7 e 8
Il 7°step consiste nella defosforilazione del 1-3 dif osfoglicerato
In 3-fosfoglicerato con guadagno di una molecola di ATP,l’enzima
che catalizza la reazione è la fosfoglicerato chinasi.
Successivamente il G3P è soggetto ad un riarrangiamento
catalizzato dalla fosfoglicerato mutasi con formazione di
2-fosfoclicerato.
Reazione 9 e 10
Nella penultima reazione il 2-fosfoglicerato viene disidratato a
fosfoenolpiruvato,reazione catalizzata dall’enzima
Enolasi,infine quest’ultimo composto viene defosforilato dalla
Piruvato chinasi,con guadagno netto di un un ATP per ogni
trioso quindi in totale due; in enolpiruvato che dopo un ultimo
riarrangiamento diventa acido piruvico.
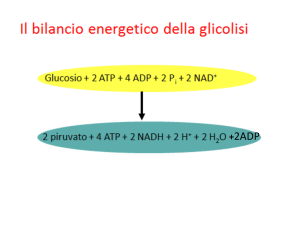
Il resoconto energetico della glicolisi è:
• 2 molecole di ATP e non 4 perché nelle prime fasi si
ha un dispendio energetico pari a 2 ATP
• 2 NADH+H+
• 2 molecole di H2O
Una volta che si ha ottenuto il piruvato vi sono due
possibiltà d’impiego di quest’ultimo a seconda che la
cellula si trovi in condizione di aerobiosi o anaerobiosi.
Se la cellula è in anaerobiosi avviene un processo
denominato FERMENTAZIONE,che consiste nel
processo di riossidazione del NAD+ e del FAD.
La Fermentazione può essere Lattica o Alcolica.
Nella fermentazione lattica il piruvato agisce da
accettore di elettroni e protoni legati al cofattore
NADH+,trasformandosi in acido lattico.Questo tipo di
fermentazione avviene anche in organismi che
normalmente si trovano in condizione aerobica ma
sono in deficit d’ossigeno,es:miocita.
La Fermentazione Alcolica,come nel caso dei lieviti
consta di due tappe.Nella prima l’acido piruvico viene
decarbossilato dalla piruvato decarbossilasi in
acetaldeide con conseguente produzione di CO2,nella
seconda l’acetaldeide viene deidrogenata ad alcol
etilico con conseguente ossidazione del
NAD+(l’enzima che catalizza la reazione è la Alcol
Deidrogenasi).Sia la fermentazione lattica che quella
alcolica sono dei processi che non avvengono nel
mitocondrio ma nel citoplasma.
IL percorso svolto dal piruvato in cellule in aerobiosi e
ben diverso da quello poc’anzi esposto,infatti il piruvati
per poter subire una completa ossidazione deve
entrare nella matrice mitocondriale attraversando le
due membrane.Nella matrice è presente il complesso
multienzimatico della piruvato deidrogenasi,che
contiene più copie di tre enzimi ad attività
catalitica:piruvato deidrogenasi,diidrolipoammide
acetiltransferasi e diidrolipoammide deidrogenasi.
IL complesso multienzimatico della piruvato
deidrogenasi è responsabile della rapida
trasformazione del piruvato in gruppo acetile che
viene rapidemente legato al coenzima A(CoA),una
),
molecola nucleotidica,formando aceti-coenzima A.
Sintesi acetil-CoA=CH3COCOOH+(NAD+)+CoA=>
=>acetil-CoA+(NADH+H+)+CO2
Ciclo di Krebs
Nella matrice sono presenti gli enzimi che consentono la completa
ossidazione del gruppo acetile,derivato dal piruvato,in
CO2,grazie ad una serie di reazioni che vengono indicate
complessivamente come ciclo dell’acido citrico.Il ciclo inizia con
la cessione del gruppo acetile(CH3-CO-)da parte dell’acetil
CoA all’acido ossalacetico(COO¯-CO-CH3-COO¯)che si
trasforma in citrato.il 2°step,catalizzato dall’Acon tasi, consiste
nell’isomerizzazione del citrato in isocitrato,successivamente
l’isocitrato va incontro a decarbossilazione ossidativa(Isocitrato
deidrogenasi) formando α-chetoglutarato,NADH ridotto e una
molecola ci CO2.La reazione successiva molto simile alla
precedente prevede la decarbossilazione ossidativa dell’αchetoglutarato(glutarato deidrogenasi)formando nuovamente
CO2,NADH ridotto e un composto a cui viene aggiunto il CoA
che prende il nome di succinil-CoA.
(dominio catalitico della diidrolipoammide succiniltransferasi,parte del complesso
della α-chetoglutarato deiidrogenasi)
Nella 5 tappa del ciclo che consiste nella trasformazione
del succinil-CoA in succinato,si assiste ad una
fosforilazione diretta del subatrato,inffatti l’energia che
si ottiene dalla rottura del legame fra CoA e la
rimanete parte costituente il succinil-CoA viene usata
dalla succinil-CoA sintetasi per legare un radicale
fosforico ad una molecola di ADP o GDP.Il composto
finale di questa tappa è il succinato.
4°reazione
5°reazione
Il ciclo continua e il succinato viene ossidato dalla
succinato deidrogenasi ,riduncedo 1 FAD a FADH2,e
si forma acido fumarico.
Nella penultima reazione il fumarato
,idratato dalla fumarasi, forma
l’acido malico.Nell’ultima tappa il
malato viene ossidato ad ossalacetato
dalla malato deidrogenasi,producendo una molecola di
NADH ridotto,e il ciclo si chiude.
In ogni ciclo dunque si avrà la liberazione di 2 molecole
di CO2 e la formazione di 3 molecole di
NADH,FADH2,1 di ATP o GTP.Tenendo conto che i
gruppi acetile inseriti nel ciclo sono due per ogni
molecola di glucosio,i prodotti vanno duplicati.Se
consideriamo ulteriormente che le 2 molecole di
piruvato ottenute dalla glicolisi,prima di entrare nel
ciclo di crebs,siano state trasformate in acetil-CoA
formando 2 molecole di CO2 e NADH+H+,la reazione
di ossidazione completa dei prodotti della glicolisi
diventa:
2(CH3-CO-COO¯)+8(NAD+)+2FAD+2ADP+2Pi
6CO2+8NADH+(8H+)+2FADH2+2ATP
SISTEMI SHUTTLE
Le molecole di NADH formatesi nel
citoplasma,in seguito alla glicolisi,
non riescono a passare la membrana
interna per cedere i loro elettroni alla
catena di trasporto,quindi le cellule per recuperare l’energia degli
elettroni conservata nelle molecole di NADH fanno ricorso ai
sistemi navetta.
In alcune cellule i NADH in questione vengono ossidati
a livello della membrana esterna del mitocondrio
cedendo i propri e¯ ad una molecola di DHAP che si
trasforma in glicerolo-3-P.Quest’ultimo attraversa la
membrana interna e si ossida a DHAP riducendo una
molecola di FAD a FADH2.Il DHAP ritorna nel citoplasma ed è
pronto a ricominciare il ciclo.
Con questo tipo di sistema, pur essendo vantaggioso
per la cellula,si ha perdita di energia in quanto nella
molecole di FADH2 gli elettrone si trovano ad un
livello energetico più basso rispetto a quello con cui
sono legati nelle molecole di NADH.
In altri tipi di cellule,come cellule cardiache o
muscolari,le molecole di NADH, provenienti dal
citoplasma,vendono ossidate nel compartimento
intermembranario,in seguito alla trasformazione di un
molecola di ossalacetato in malato; quest’ultimo
attraversa la membrana interna e viene riossidato a
ossalacetato riducendo una molecola NAD+ a NADH.
In questo sistema l’energia viene conservata
integralmente.
CATENA DI TRASPORTO DEGLI e¯
Nella membrana interna dei mitocondri vi sono 4
complessi in grado in grado di trasferire all’ossigeno
gli elettroni trasportati dalle molecole di NADH.
Complesso 1:NADH-CoenzimQ ossidoreduttasi
Complesso 2:succinato-CoenzimaQ ossidorettutasi
Complesso 3:CoenzimaQ-citocromo c ossidoreduttasi
Complesso 4:Citocromo c ossidasi
Ogni complesso è costituito da:
• Enzima principale, che consente il trasferimento degli e¯.
• Gruppi prostetici associati a proteine, che accettono e
cedono gli e¯.
• Proteine strutturali,che nei complessi 1,3 e 4 consentono la
formazione del gradiente protonico nello spazio
intermembranario.
Inoltre vi sono due trasportatori mobili che trasferiscono
gli elletroni da un complesso all’altro.
Il 1°è l’Ubichinone,molecola organica non proteica
il 2°è il citocromo c, una proteina molto piccola a cui è
associato un gruppo prostetico.
L’Ubichinone o Coenzima Q è formato da una struttura
ad anello detta chinone e da una lunga catena
apolare.L’ubichinone pare essere situata nella parte
apolare della membrana interna e, movendosi
liberamente consentirebbe il trasferimento di e¯ e H+
tra i vari trasportatori.
Coenzima Q ossidato
Coenzima Q forma semichinonica
CoenzimaQ ridotto
I gruppi Prostetici che associati alle proteine permettono
il trasferimento di elettrroni sono di 4 tipi:
• Citocromi(a,a3,b,c1),composti caratterizzati da un
anello tetrapirrolico con al centro un atomo di ferro.
Essi passano dallo stato ossidato allo stato ridotto in
quanto l’atomo di Fe centrale,acquistando o cedendo
un elettrone, passa da Fe2+ a Fe3+.
• FAD e FMN(flavin mononucleotide)
• Centri ferro-zolfo,in cui atomi di Fe
e di S sono legati con legami covalenti.
Il complesso formato dai centri Fe-S
e dalle proteine associate costituiscono
Le proteine ferro-zolfo che sono sono la classe di
trasportatori di elettroni mitocondriale più numerosa.
• Centri a rame,dove un atomo di rame,legato ed un
residuo di istidina, cisteina o metionina, permette il
trasferimento di elettroni,passando da uno stato ridotto
Cu+ ad uno stato ossidato Cu2+.
Fosforilazione ossidativa
Nel 1961 Mitchell enunciò la teoria
chemiosmotica che per la prima volta
Metteva in relazione la respirazione cellulare
Con la sintesi di ATP,spiegandone il meccanismo.
Sempre nello stesso anno Racker dimostro che,isolando
le particelle F0 ed F1dell’ATPsintasi,in loro assenza la
Sintesi di ATP non avveniva,nonostante il trasporto di
elettroni si verificasse normalmente.Egli inoltre verificò
che senza trasporto di elettroni,non creandosi il
gradiente protonico,il complesso F0-F1 non sintetizza
ATP;infatti l’uso si sostanze disaccoppianti,che impediscono la
formazione del gradiente, provoca il rilascio dell’energia ceduta
dagli elettroni,durante il loro trasferimento lungo la catena di
Trasporto, sotto forma di calore.
Secondo la teoria chemiosmotica di Mitchell,nelle tappe del
trasferimento di elettroni in cui viene rilasciata energia
libera,quest’ultima viene utilizzata per trasferire protoni dalla matrice
allo spazio intermembranario.IL complesso 1 libera energia
sufficiente per spingere nella camera esterna 4 protoni,mentre i
complessi 3 e 4 consentono la spinta di 2 protoni.Ancora non è ben
chiaro il meccanismo che permette ai complessi 1,3 e 4 di trasferire i
protoni ,ma l’ipotesi più accreditata è quella della modificazione
conformazionale proposta da Boyer,secondo la quale quando un
trasportatore di elettroni si riduce,induce un cambiamento
conformazionale in una delle molecole proteiche associate al
complesso.Tale cambiamento attiva sul versante della matrice un sito
di legame ad alta affinità per un protone;quando il trasportatore sarà
ossidato,il sito di legame del protone si modificherà volgendosi verso
il compartimento intermembrana dove il protone sarà rilasciato in
seguito alla diminuita affinità.Il ritorno dei protoni nella matrice
avviene attraverso la particella F0,ciò provoca il riequilibrio del
potenziale di membrana e la cessione di energia al sistema;tale
energia verrà utilizzata da F1 per sintetizzare ATP.
Per concludere,la quantità energetica che una cellula può ricavare
dall’ossidazione di una molecola di glucosio si può calcolare
tenendo conto che ogni molecola di NADH porta alla sintesi di
2,5 molecole di ATP mentre una molecola di FADH2 forma 1,5
molecole ATP.
ATP da NADH della matrice
ATP da FADH2 della matrice
ATP da ciclo di Krebs
ATP da glicolisi
ATP da NADH
glicolisi(shuttle DHAP)
o ATP da NADH
glicolisi(shuttle a.malico)
8x2,5=20
2x1,5=3
2
2
2x1,5=3
Tot =
30
2x2,5=5
Tot =
32