Prof. Calabrò
8-6-06
CARDIOMIOPATIE
Patologia primitiva del muscolo cardiaco. La cardiomiopatia dilatativa ha come
espressione clinica lo scompenso cardiaco. Si può avere una scompenso perché c’è una
malattia coronaria che ha interessato il muscolo ma è la necrosi dell’infarto che ha
determinato l’alterazione del muscolo, in questo caso dunque la cardiomiopatia non è
primitiva, in tutti i casi in cui non sappiamo perché il muscolo è alterato parliamo di
cardiomiopatia primitiva. Si può avere un’insufficienza mitralica che determina una
dilatazione del ventricolo per la quantità di sangue che rigurgita nel ventricolo
sinistro, ma questa sarà una patologia primitiva della valvola e il muscolo sarà un fatto
secondario. Allo stesso modo possiamo avere una patologia primitiva del muscolo che
allarga la cavità ventricolare, allarga l’ostio della valvola mitrale il che provocherà
un’insufficienza della valvola mitrale stavolta secondaria alla cardiomiopatia (possibile
coinvolgimento secondario delle valvole atrio-ventricolari). Quindi il fatto di trovare
una sintomatologia che può essere anginosa, un’insufficienza valvolare in particolare
della mitrale non è direttamente riconducibile ad una primitiva causa ischemica o
valvolare ma potrebbe anche trattarsi di una primitiva cardiomiopatia con secondario
interessamento delle coronarie o della valvola. Classicamente distinguiamo
cardiomiopatie: dilatative, ipertrofiche, restrittive, aritmogene del ventricolo destro
e specifiche. Poi ci sono tutta una serie di patologie che determinano una
cardiomiopatia dilatativa ma che sono la conseguenza di altre cause, quindi non sono
cardiomiopatie primitive.
DILATATIVA: C’è una dilatazione delle cavità ventricolari, una capacità contrattile
ridotta e in genere c’è un assottigliamento del muscolo.
IPERTROFICA: C’è un’ ipertrofia del muscolo, di parete e in genere c’è una riduzione
della cavità. Quando l’ipertrofia interessa la parete c’è una patologia diastolica quindi
il cuore si contrae bene ma non si dilata bene, la diastole è ridotta. Normale funzione
sistolica, alterata funzione diastolica. La cardiomiopatia ipertrofica può essere
ostruttiva e non ostruttiva a seconda se l’afflusso di sangue dal ventricolo verso
l’aorta avviene normalmente o è ostacolato, ostruito all’interno della cavità stessa del
ventricolo.
RESTRITTIVA: C’è un muscolo non particolarmente aumentato, una cavità non
particolarmente ridotta, ma la patologia del muscolo è tale che non c’è una capacità
diastolica adeguata, c’è una compliance ridotta così come nel caso di una pericardite
costrittiva che impedisce la dilatazione completa del muscolo cardiaco. La
cardiomiopatia è la stessa cosa perchè intrinsecamente queste fibre non hanno la
capacità di avere una diastole adeguata. È una ridotta distensibilità, quindi diastole,
delle camere ventricolari.
dei ventricoli per infiltrazione miocardia.
ARITMOGENA: Patologia subentrata negli ultimi 20 anni specifica solo del muscolo
del ventricolo destro (nella stragrande maggioranza dei casi della zona
dell’infundibolo, sotto la valvola polmonare) che si presenta non omogeneo, si dice un
scaricato da www.sunhope.it
muscolo “a stila” perché presenta una serie di sarcomeri impilati uno sull’altro, dove la
caratteristica clinica non è tanto l’insufficienza cardiaca e lo scompenso ma quello
dell’aritmia. Questo cuore ha la capacità per questa anomalia muscolare di generare
aritmie gravi, tachicardie ventricolari, fibrillazione ventricolare, morte.
DILATATIVA
È la cardiomiopatia più frequente ed è dovuta alla dilatazione di uno o di entrambi i
ventricoli e alla ridotta funzione sistolica. Nella maggior parte dei casi è dilatata solo
una camera cardiaca in particolare il ventricolo sinistro. Ha un’incidenza che è sotto ai
10 per 100000/anno e con una prevalenza del 36 per 100000. Come si misura la
funzione sistolica? La funzione sistolica è il movimento del ventricolo, considerando il
ventricolo sinistro significa un avvicinamento tra la parete libera del ventricolo
sinistro e il setto interventricolare. L’esame che ci fa capire come si avvicinano queste
due strutture è l’ecocardiogramma M-mode che ci fa misurare la distanza tra il setto
e la parete posteriore del ventricolo sinistro e da ciò ricaviamo la grandezza del cuore
e l’escursione in fase sistolica e in fase diastolica. In questo modo si calcola la
frazione di eiezione, cioè la quantità di sangue che viene eiettata in ogni sistole.
Quando diciamo che queste patologie sono primitive è perché in realtà non ne
conosciamo la causa (idiopatiche). Negli ultimi tempi si sta studiando molto l’aspetto
genetico di queste patologie, soprattutto della dilatativa e si sta ricavando qualche
informazione più precisa (dell’ipertrofica già conosciamo qualcosa in più, alcune forme
sono di origine ereditaria). Presumibilmente ci sono dei fattori genetici che alterano il
sistema immunitario e ciò può influire su alcune fasi della storia clinica del pz. Se per
esempio il pz ha un’infezione virale (un’influenza, una miocardite) si può sviluppare un
interessamento anche del muscolo cardiaco e quindi si può avere una ridotta funzione
dello stesso nella fase acuta della malattia che, in caso di persistenza del virus e in
presenza di un’alterazione del sistema immunitario, può determinare una condizione di
dilatazione muscolare più stabile e quindi una cardiomiopatia dilatativa. È presumibile
dunque che ci sia un fattore genetico di base che predispone alla patologia,
probabilmente deve intervenire un fattore stimolante che può essere anche una
banale infezione. Ho visitato poco fa un ragazzo di 30 anni, canottiere, quindi con
un’ottima capacità fisica, che da 15 giorni ha un po’ di affanno, la notte prima del
ricovero ha avuto dispnea più consistente e un senso di costrizione alla bocca dello
stomaco. Ha una tachicardia accelerata con un ritmo di galoppo, dei rumori secchi al
torace. L’eco mostra un cuore di 7 cm mentre normalmente è di 4 o 5 con
un’escursione del 30% mentre normalmente è del 55%. Nella storia non c’è nulla di
recente forse 3 mesi prima, a marzo, c’è stata un’influenza, una febbricola che è
durata 4 o 5 giorni, passata inosservata perché il pz continuava a lavorare e a fare
attività sportiva. Probabilmente ci troviamo di fronte a questa patologia perché a
marzo c’è stato l’episodio acuto dal quale si sviluppa una miocardite a causa
dell’assenza di intervento terapeutico e oggi abbiamo un’alterata funzione miocardica.
scaricato da www.sunhope.it
È una patologia molto seria, grave e delicata perché quando ha questo tipo di storia ti
trovi di fronte persone che fino al giorno prima svolgevano una vita perfettamente
normale. Se c’è una ridotta funzione contrattile c’è una ridotta gittata per cui
aumenta il volume telesistolico, quest’ ultimo provoca un allungamento della fibra
miocardica e quindi una capacità di risposta, quando questa supera i 2,5 non avremo
una capacità di risposta adeguata ma avremo una riduzione della contrattilità. Se
aumenta il volume telesistolico aumenta anche la resistenza all’escursione e quindi lo
stress di parete (Legge di Frank-Starling) e questo, vuoi per l’aumento del sangue,
vuoi per lo stress di parete provoca una dilatazione ventricolare progressiva che
aumenta la ridotta funzione contrattile.
RIDOTTA FUNZIONE
CONTRATTILE
DILATAZIONE
VENTRICOLARE
RIDOTTA GITTATA
SISTOLICA
AUMENTO DELLO
STRESS DI PARETE
AUMENTO DEL
VOLUME TELESISTOLICO
AUMENTO DEL
VOLUME TELESISTOLICO
LEGGE DI FRANK-STARLING
scaricato da www.sunhope.it
Questa patologia ha un andamento non solo cronico ma evolutivo, con i farmaci si
cerca di ridurre tutti questi effetti ma la maggior parte delle volte si arriva al
trapianto. In questa patologia il cuore non va incontro ad ipertrofia perché la causa
primitiva non è l’aumento delle resistenze e lo stress di parete ma il deficit del
muscolo. Quindi anche se ci si aspetterebbe un aumento dello spessore del muscolo ciò
non avviene perché le fibre sono primitivamente interessate dalla patologia e non sono
in grado di andare incontro ad ipertrofia (non come nella stenosi aortica in cui il
problema è l’aumento della resistenza e del lavoro mentre il miocardio è sano e le
fibre possono ipertrofizzarsi). Questo è un cuore con un ventricolo sinistro di aspetto
globoso, dilatato, con una parete non particolarmente assottigliata (ci sono però forme
di dilatativa in cui la parete è davvero molto sottile perché queste sono fibre che non
sono in grado di ipertrofizzarsi).
Se facciamo un taglio per un’analisi istologica vediamo che
non c’è più il normale arrengement, la normale architettura
della fibrocellule miocardiche ma ci sono tutta una serie di
fenomeni degenerativi, infiltrativi a seconda della patologia
che ha interessato il miocardio. Abbiamo detto che i sintomi
principali sono quelli dello scompenso perché il cuore non è in
grado di avere una gittata adeguata e ciò determina il fatto
che non arriva bene sangue alla periferia e che c’è stasi venosa polmonare e sistemica.
Quindi ridotta gittata, il pz accusa facile affaticabilità, dispnea da sforzo, astenia.
Abbiamo già parlato in altra sede delle classi NYHA (bisogna rivederle). IL 75-85%
dei pazienti si presenta in classe funzionale NYHA III-IV.
NYHA I
NYHA II
NYHA III
NYHA IV
Un cuore dilatato, con un ipocontrattilità andrà ad incidere su determinati organi: ci
sarà ridotta gittata nel circolo polmonare, nel circolo cerebrale e così via,
analizziamoli uno alla volta. Se non giunge bene sangue al circolo cerebrale il pz potrà
avere un primitivo giramento di testa, poi un senso di stanchezza fino a non
connettere più bene, ad avere le farfalline (giuro ha detto proprio così…) davanti agli
occhi e all’alterazione dello stato di coscienza. Se non arriva bene sangue alla
scaricato da www.sunhope.it
periferia l’alterazione si sentirà al polso, il pz reagisce con un ipertono simpatico e ciò
porterà ad una vasocostrizione periferica, ad un polso piccolo, frequente per la
sopraggiunta tachicardia e alternante cioè che si sente a volte più forte e a volte più
debole. Non arriva bene sangue al rene, avremo un diminuito flusso renale, una
filtrazione glomerulare ridotta e di conseguenza una ritenzione idro-salina (di sodio e
acqua) il che provoca edema soprattutto agli arti inferiori. Nelle forme molto
avanzate c’è edema cronico che è indurito il che provoca anche ulcere cutanee; nelle
forme non molto avanzate il segno tipico è dato dalla “fovea”? Il pz presenterà stasi
nel circolo venoso sistemico quindi aumenta la pressione nel ventricolo destro,
aumenta la pressione nell’atrio destro, nella vena cava e quindi nelle vene sistemiche.
Il pz presenterà dunque giugulari turgide e se andassimo a misurare con un ago nella
giugulare la pressione venosa sarebbe aumentata. L’ipoperfusione e l’astenia sono
legate invece alla bassa gittata. L’ipertono simpatico determina sudorazione e
vasocostrizione che porterà a sua volta a pallore e cianosi. Questi segni sono molto
importanti perché in base ad essi si può valutare l’entità dell’ipertono simpatico del pz.
Se infatti analizziamo un pz scompensato, con fegato aumentato, giugulari turgide,
affanno ma perifericamente caldo vuol dire che non presenta una vasocostrizione
adeguata; se invece il pz insieme a tutti questi sintomi presenta anche pallore
periferico, estremità fredde o addirittura sudorazione vuol dire che ha un ipertono
simpatico molto forte perché evidentemente l’insufficienza cardiaca è molto grave.
Peraltro ne parleremo quando tratteremo le cardiopatie congenite, nello scompenso
del bambino piccolo (neonato o primo anno di vita) questi sono i sintomi principali, il
bambino infatti non presenta edemi ma sudorazione perché cerca di risolvere la
ritenzione idrica eliminando liquidi in questo modo e non accumulandoli
perifericamente (il pallore è il primo segno dello scompenso nel bambino piccolo). Per
quanto riguarda il polmone sappiamo che non c’è una buona espulsione e quindi c’è una
stasi anche nel piccolo circolo. Si può avere addirittura una situazione di trasudazione
e quindi edema polmonare o versamento pleurico. Molto più frequentemente però la
stasi del piccolo circolo e quindi dei capillari e delle vene polmonari determina un
allargamento delle vene che così comprimono dall’esterno le aree bronchiali il che
porta a stenosi bronchiale estrinseca e aumento della pressione nel circolo arteriolare
bronchiale. L’aumentata pressione determina trasudazione di liquido dai vasi bronchiali
e quindi ostruzione bronchiale anche intrinseca. Per cui in una prima fase si sentiranno
rumori bronchiali secchi, come da espiro forzato, perché c’è una compressione dei
bronchi dall’esterno per il turgore delle vene e dall’interno per la trasudazione del
circolo bronchiale; si instaurerà una cattiva ossigenazione e quindi cianosi.
scaricato da www.sunhope.it
L’elettrocardiogramma non fornisce molti dati significativi, ci aiuta per la tachicardia
e poi a seconda della patologia si avrà un muscolo più o meno rappresentato: in V5 e V6
l’aspetto tipico è caratterizzato da una piccola Q, una R alta e una piccola S invece qui
vediamo che la R è piccola e ciò è esplicativo della scarsa rappresentanza delle forze
elettriche del muscolo del ventricolo sinistro.
All’ eco vediamo un ventricolo dilatato, globoso, con una parete molto sottile. L’ Rx
torace mostra un ventricolo sinistro aumentato. Lo studio emodinamico prevede di
effettuare una coronarografia per escludere che la cardiomiopatia sia secondaria ad
un’ischemia miocardia. Un pz con ischemia presenterà infatti ugualmente un cuore
dilatato, con parete assottigliata, ipomobile, ipocontrattile. In caso di pz giovane
(quello di cui parlavamo prima: trentenne, canottiere, con una sintomatologia da
scaricato da www.sunhope.it
scompenso, un cuore con parete sottile e dilatato) la coronarografia possiamo anche
evitarla perché difficilmente la sua patologia sarà dovuta ad un’ischemia miocardia,
qualora la terapia non dovesse rispondere si farà anche la coronarografia. Questa
dispositiva mostra le diverse terapie da somministrare a seconda dello stadio NYHA in
cui si trova il pz. Un pz dilatato, scompensato lo trattiamo innanzitutto con fattori che
riducono le resistenze periferiche (ACE-inibitori), poi andiamo a ridurre la ritenzione
idrica (diuretici), andiamo ad aumentare la contrattilità (digossina) e andiamo ridurre
il tono simpatico (β-bloccanti) se ancora non risponde aggiungiamo al classico diuretico
un antialdosteronico che aumenta la diuresi, riduce la quantità di aldosterone e la
ritenzione idrica.
Il pz di cui parlavamo prima stanotte ha avuto per la prima volta una fibrillazione
atriale, quindi devo supporre, anche in assenza di sintomi acuti, che la condizione
morbosa sia presente da al massimo 1 anno (non come nella stenosi mitralica in cui la
fibrillazione si presenta tardivamente, dopo 15-20 anni, perché la patologia ha un
andamento cronico e quindi l’organismo inizialmente cerca di adattarsi alla dilatazione
atriale) perché la patologia ha esordio acuto e l’organismo è impreparato a questa
nuova e improvvisa condizione così l’atrio dilatandosi facilita la nascita di foci ectopici.
Nel caso specifico questo pz ha una ridotta capacità contrattile del ventricolo
sinistro, ha un aumento della pressione telediastolica del ventricolo sinistro e ha un
aumento della pressione in atrio sinistro, il tutto è avvenuto in maniera così acuta che
questa distensione dell’atrio sinistro ha trovato una muscolatura non preparata e
quindi ha avuto una fibrillazione dovuta ai foci ectopici che si sono formati. Quando c’è
una stenosi mitralica l’atrio comincia ad ipertrofizzarsi un po’ e poi sempre di più fin
quando anche qui si arriva alla sopportazione massima. Se per esempio c’è un pz con
insufficienza mitralica di grado medio dovuta ad un infarto della parete libera
dell’atrio sinistro che gli ha provocato una necrosi all’attacco del muscolo papillare, in
quella fase acuta la patologia è severissima perché mi trovo un’ insufficienza mitralica
insorta così rapidamente che il muscolo atriale, il circolo polmonare ecc. non riescono
ad adattarsi alla nuova condizione.
La patologia ha una prognosi molto severa con una mortalità del 31% ad 1 anno dalla
diagnosi e del 64% a 5 anni della diagnosi.
FORME SPECIFICHE
• ALCOLICA: la patologia è reversibile se l’apporto di alcool è ridotto o abolito.
• DIABETICA: il diabete provoca un’alterazione di tutto il circolo coronario,
dell’innervazione miocardia e del metabolismo energetico che portano ad una
degenerazione del muscolo.
IPERTROFICA
Ipertrofia del ventricolo sinistro. Nell’ipertesione sistemica e nella stenosi aortica c’è
un’ipertrofia del ventricolo sinistro, facciamo allora l’eco e vediamo l’ipertrofia della
parete e la andiamo a misurare, come facciamo a capire se è una patologia secondaria
scaricato da www.sunhope.it
alla stenosi aortica, all’ipertensione o se è una cardiomiopatia primitiva ipertrofica? La
differenza sta nel fatto che mentre nell’iperteso e nella stenosi, cioè nelle patologie
in cui l’ipertrofia è dovuta allo stress di parete e all’aumento delle resistenze,
l’ipertrofia è omogenea in tutto il ventricolo sinistro (concentrica), nella
cardiomiopatia l’ipertrofia è asimmetrica e prevalente nella parete settale. L’
incidenza è 2,5/100.000 anno, la prevalenza: 20/100.000 anno. In oltre il 50% dei casi
si è dimostrato che è una patologia ereditaria con trasmissione autosomica dominante.
Questa diapositiva mostra un esempio di cardiomiopatia ipertrofica, quello indicato
dalla freccia è il setto.
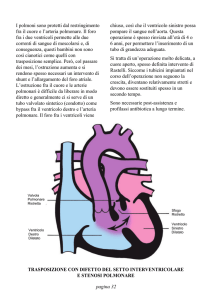
La cardiomiopatia ipertrofica può essere ostruttiva e non
ostruttiva a seconda della presenza o meno di un’ostruzione a
livello sottovalvolare al passaggio di sangue dal ventricolo
sinistro all’aorta per effetto dell’ipertrofia settale che crea
un ostacolo alla via di efflusso del ventricolo sinistro e un
accavallamento del lembo anteriore della mitrale col setto
interventricolare. La distinzione tra le ostruttive e le non
ostruttive si effettua in base alla presenza di un gradiente
pressorio subaortico o medioventricolare. È importante documentare la storia della
patologia che è diversa per l’ipertrofica ostruttiva e non ostruttiva.
DIFFERENZE DI PRESSIONI INTRAVENTRICOLARI
Le forme con ostruzione medioventricolare sono piu’ rare ma piu’ gravi delle forme
con ostruzione subaortica, mentre le forme di ipertrofia apicale non sono ostruttive.
Un ruolo fondamentale viene assunto dal lembo anteriore mitralico (lam) nella genesi
del gradiente all’efflusso ventricolare sinistro ed alla insufficienza mitralica con il suo
movimento anteriore in sistole (sam). Il sam e causato dall’effetto venturi del flusso
ematico anterogrado nel tratto di efflusso del ventricolo sinistro sul lam.
scaricato da www.sunhope.it
L’ipertrofia del setto è la più frequente ma esistono altre forme come quella apicale
e quella medioventricolare che è la più rara (l’ipertrofia della zona centrale della
parete ventricolare provoca un restringimento del ventricolo che sembra così
costituito da due camere, nella fase sistolica c’è un intrappolamento del sangue nella
zona apicale a causa dell’ostruzione che è a questo livello).
Qui vediamo come il lembo anteriore della valvola mitrale venga richiamato verso il
setto ipertrofico creando un’ostruzione all’eiezione di sangue in aorta. Il ventricolo
non è in grado di espellere il sangue senza un ulteriore sforzo.
Istologicamente le fibre miocardiche
perdono
completamente
la
loro
architettura, non si presentano più
parallele ma disarticolate (disarray), il
che provoca un’ inadeguato scorrimento
e contrattilità. Essendo una patologia
muscolare, da ipertrofia del muscolo, la
disfunzione
è
essenzialmente
diastolica.
Fisiopatologicamente
l’ipertrofia
provoca ostruzione che a sua volta ridurrà l’apporto ematico al circolo coronario
provocando ischemia miocardia (quindi uno dei sintomi della cardiomiopatia ipertrofica
è l’angina). L’ipertrofia provoca una disfunzione diastolica (alterato rilasciamento),
tutto questo porta a fenomeni di bassa gittata e ischemia miocardia ma lascia anche
scaricato da www.sunhope.it
una stasi importante nel circolo venoso polmonare per cui l’atrio sinistro si può
ingrandire e dilatare e provocare così aritmie atriali (fibrillazione atriale,
extrasistolia atriale). Quest’ ipertrofia legata al disarray può portare a fenomeni di
aritmie anche ventricolari con gravi conseguenze (sincope, arresto cardiaco). Il rischio
di andare incontro a conseguenze gravi aumenta se c’è familiarità.
Le forme ostruttive possono essere di due tipi: ostruzione di base o sotto sforzo, per
distinguerle si fa fare al pz la prova da sforzo e l’holter per vedere se ci sono aritmie.
Il pz che ha dunque una disfunzione della fase diastolica accusa dispnea, angina,
lipotimia per scarso sangue che arriva al cervello, astenia per scarso sangue in
periferia, presincope, cardiopalmo, fibrillazione atriale (che compare tardivamente),
soffio sistolico eiettivo (è un soffio mesosistolico cioè che sentiamo quando il
ventricolo eietta il sangue in aorta e qui incontra un ostacolo mentre nella presistole il
ventricolo è in fase di contrazione isovolumetrica e non ha ancora eiettato sangue).
Sono pz che di solito non presentano gravi sintomi, quando però compaiono vuol dire
che la patologia sta avanzando progressivamente. (49,50)
Questo elettrocardiogramma ci segnala che c’è un’ipertrofia perché vediamo una R
alta in V1-V2-V3 (ipertrofia settale), onde T invertite giganti da V4 a V6 (ipertrofia
apicale), un tratto S-T sottoslivellato, stirato e una P che non è negativa ma non è
neanche normale.
scaricato da www.sunhope.it
L’holter che dovrebbe essere eseguito per 72 ore consecutive, può mostrare
l’eventuale presenza di aritmie ventricolari o sopraventricolari, utile per la
stratificazione prognostica dei pazienti con CMPI (valuto il pz in base ai fattori
forniti dalla sua storia che incidono sul rischio della sua patologia e in base a fattori
epidemiologici per arrivare al suo livello di prognosi). L’Rx del torace non serve alla
diagnosi. L’ecocardiografia è importante, per dichiarare che il pz soffre di
cardiomiopatia ipertrofica il setto deve essere superiore ad 1,3 (normalmente è 0,91). Il SAM (septal anterior movement) è quello che si vede all’eco relativo al
movimento del lembo anteriore della mitrale a causa dell’ipertrofia settale, se c’è
siamo ancora più sicuri che si tratta di una CMPI. L’ Eco M-mode: SIV/PP> 1,3. L’Eco Bmode effettua una stima più precisa della distribuzione dell’ipertrofia e della
compromissione della geometria endocavitaria. Col doppler misuriamo: il gradiente
pressorio all’efflusso vs con caratteristica configurazione a sciabola, il rigurgito
mitralico correlato al SAM, il tempo di eiezione vs prolungato, il pattern mitralico da
alterato rilasciamento, il pattern mitralico di tipo restrittivo. L’ esame emodinamico
quando è presente un severo rigurgito mitralico è utile per la conoscenza delle
pressioni intracavitarie nel pianificare la terapia, serve inoltre per escludere
aterosclerosi coronarica nei pazienti con angina. Ponendo un catetere in aorta, a
partenza dalla femorale, troviamo una pressione sistolica di 120 e una distolica di 80;
nel ventricolo la sistolica è 120, la diastolica 0-5, ma se la sistolica aumenta (160) si
forma un gradiente di 40 rispetto all’aorta e dunque c’è un’ostruzione media della
valvola aortica. Se il pz ha una stenosi aortica la pressione sistolica ventricolare è 160
mentre nell’aorta la pressione è 120 quindi c’è un gradiente pressorio di 40 che
valutiamo ponendo il catetere nel ventricolo e spingendolo pian piano in aorta fino a
che troviamo il cambiamento di pressione. Nella cardiomiopatia ipertrofica ostruttiva
c’è il lembo anteriore della mitrale che si ripiega sul setto provocando un’ostruzione,
troviamo quindi nel ventricolo una pressione sistolica di 160 e nell’aorta di 120, come
facciamo allora a distinguerla da una stenosi aortica? Saliamo pian piano col catetere
e vediamo dov’è la differenza di pressione: se nel ventricolo la pressione è 120 la
stenosi è sottovalvolare aortica; ma come facciamo a sapere che siamo sotto la valvola
aortica? Lo sappiamo perché nel ventricolo troviamo una sistolica di 160 ed una
diastolica di 4-5 mmHg.
scaricato da www.sunhope.it
Il decorso della CMPI e’ variabile: evoluzione verso la cardiomiopatia dilatativa,
frequente la morte improvvisa. La prossima slide mostra la terapia da effettuare in
caso di CMPI.
CARDIOMIOPATIA RESTRITTIVA
(slides del prof.)
INTRODUZIONE
Gruppo di affezioni miocardiche caratterizzate da:
• alterazioni del riempimento diastolico, senza anomalie della funzione sistolica
(eccetto che nelle fasi tardive) con possibile interessamento delle valvole atrioventricolari.
• Il profilo clinico ed emodinamico e’ indistinguibile dalla pericardite costrittiva.
• La ridotta funzione diastolica è dovuta ad una aumentata rigidità delle pareti
ventricolari che può essere primitiva o secondaria all’infiltrazione di sostanze
estranee.
scaricato da www.sunhope.it
ASPETTI MACROSCOPICI
• severa dilatazione ed ipertrofia degli atri
• modico aumento del peso
• assenza di anomalie della volumetria ventricolare
ASPETTI MICROSCOPICI
• fibrosi interstiziale endo e perimisiale che incapsula focali fascicoli miocardici
e singoli cardiociti
• focale disorganizzazione spaziale delle fibre miocardiche che perdono il loro
normale arrangiamento parallelo (“myocardial disarray”)
IPOTESI EZIOPATOGENETICHE
• malattia familiare, a trasmissione autosomica dominante, talora associata a
blocco a-v di grado variabile e ad una alteazione dei muscoli scheletrici
• Cooke et al. hanno descritto una forma di cardiomiopatia restrittiva primitiva
associata alla sindrome di Noonan
• risultato di una mutazione spontanea
FISIOPATOLOGIA
La Cardiomiopatia restrittiva è caratterizzata da normale funzione sistolica in
presenza di una compliance ventricolare molto ridotta con un modesto volume
diastolico. Il pattern restrittivo di riempimento ventricolare è dal punto di vista
fisipatologico un elemento critico.
scaricato da www.sunhope.it
DIAGNOSTICA STRUMENTALE
ECG
• Anomalie della fase di ripolarizzazione
• Blocco di branca (più spesso sinistra)
• Ingrandimento atriale sn (onda P mitralica)
ECOCARDIOGRAFIA
1) normali/ridotte dimensioni del ventricolo sn
2) spessori parietali normali/lievemente aumentati
3) funzione sistolica del ventricolo sn normale/lievemente ridotta
4) dilatazione di entrambi gli atri, aspetto “a mongolfiera” del cuore
5) pattern mitralico di tipo restrittivo
6) Insufficienza mitralica e tricuspidalica di grado almeno moderato
EMODINAMICA
• pattern di riempimento ventricolare a dip-plateau della pressione diastolica
ventricolare: riempimento accelerato in protodiastole cessa in meso e telediastole
caratteristica comune alla pericardite costrittiva.
CATETERISMO
Se sono presenti:
• grande differenza di pressione diastolica tra i due ventricoli e tra la pressione
venosa centrale e la pressione polmonare di incuneamento
• alta ipertensione polmonare ed aumentate pressioni diastoliche ventricolari sn
È piu’ probabile che si sia in presenza di una cardiomiopatia restrittiva che non di una
pericardite costrittiva
scaricato da www.sunhope.it
DIAGNOSI
DIFFERENZIALE
COSTRITTIVA
ECOCARDIOGRAFICA
CON
PERICARDITE
CARDIOMIOPATIA RESTRITTIVA
FORME SPECIFICHE
AMILOIDOSI
• miocardio compatto ed indurito
• cavita’ ventricolari ridotte, se c’e’ aumento di spessore delle pareti
• dilatazione in fase finale della malattia
• ecocardiografia: aspetto a vetro smerigliato
• prognosi: severita’ in rapporto allo spessore di parete
ENDOMIOCARDITE FIBROPLASTICA DI LOEFFLER
IN FASE ACUTA: infiltrato cellulare eosinofilo ed arterite
DOPO UN ANNO: deposizione trombotica stratificata
POI: fibrosi con cavita’ obliterate per l’ispessimento endomiocardico
Endomiocardiofibrosi senza eosinofilia
Stesso quadro in assenza di eosinofili
EMOCROMATOSI
Miocardio ventricolare ispessito-disfunzione diastolica
NEL TEMPO: aumento di volume del cuore-insufficienza congestizia
SARCOIDOSI
Infiltrazione granulomatosa del miocardio.
Ecocardiografia: fibrosi iperecogena basale e medio-ventricolare aritmie, alterazioni
della conduzione a-v
scaricato da www.sunhope.it
DISPLASIA ARITMOGENA DEL VENTRICOLO DX
• Cardiomiopatia caratterizzata da sostituzione fibro-adiposa della parete libera
del Ventricolo dx.
• Si manifesta frequentemente in eta’ giovanile.
scaricato da www.sunhope.it
PROFILI CLINICI
SEGNI PROGNOSTICI SFAVOREVOLI
scaricato da www.sunhope.it