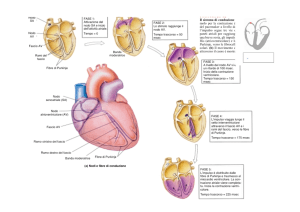
La pressione nelle camere cardiache varia durante il ciclo
cardiaco, ed è la differenza di pressione a spingere il
sangue dagli atri nei ventricoli e da questi nelle arterie. E’
perciò importante che questa direzionalità del flusso venga
mantenuta.
Le valvole si aprono e si chiudono passivamente in base alla spinta del flusso ematico
Muscolo cardiaco
Cellule muscolari striate con fibre contrattili organizzate in sarcomeri; un solo nucleo;
Le singole cellule muscolari cardiache si ramificano e si collegano con le cellule vicine
tramite le loro estremità per formare una rete complessa. Le giunzioni cellulari sono regioni
specializzate note come dischi intercalari. Esse sono costituite da membrane interdigitate
collegate da desmosomi che mantengono unite tra loro cellule adiacenti. Inoltre i dischi
intercalari presentano giunzioni comunicanti permettendo il movimento diretto di ioni da una
cellula all’altra. Queste giunzioni collegano elettricamente le cellule in modo che le onde di
depolarizzazione diffondono rapidamente.
Il segnale per la contrazione del miocardio non proviene dal sistema nervoso ma da cellule
miocardiche specializzate dette cellule autoritmiche definite anche pacemaker, perché
controllano la frequenza cardiaca.
Organizzazione multi-cellulare
= Giunzioni gap
Il battito cardiaco è avviato da potenziali d’azione che originano dalle cellule
pacemaker e non dipendono dalla stimolazione nervosa. Queste cellule
autoritmiche sono concentrate nel nodo senoatriale e nel nodo
atrioventricolare.
Tuttavia, il sistema nervoso autonomo è in grado di esercitare un’attività
regolatrice, modulando la frequenza e la forza di contrazione del muscolo
cardiaco.
Proprietà dei miociti cardiaci:
-eccitabilità
-conduttività
-contrattilità
-ritmicità
Miocardio atriale (eccitabilità e conduttività)
Miocardio ventricolare o miocardio di lavoro (eccitabilità e contrattilità)
Sistema specifico o di conduzione (conduttività e ritmicità)
Accoppiamento eccitazione-contrazione
La contrazione del miocardio può essere graduata. La forza
generata dal miocardio è proporzionale al numero di ponti
trasversali che dipende dalla quantità di calcio legato alla
troponina. Se dal LEC entra una quota addizionale di calcio,
molto più calcio sarà rilasciato dal reticolo sarcoplasmatico e
maggiore sarà la forza generata dal muscolo.
3Na Na
Na
Sarcolemma
Na
NCX
ATP
RyR
Ca
Ca
2K
ATP
3Na
PLB
ATP
ICa
SR
T-Tubule
Ca
by D.M . Bers
Ca
NCX
3Na
Contraction
Cyt
Na
3Na Na
Na
Sarcolemma
Na
NCX
ATP
RyR
Ca
Ca
2K
ATP
3Na
PLB
ATP
ICa
SR
T-Tubule
Ca
by D.M . Bers
Ca
NCX
3Na
Cyt
Na
3Na Na
Na
Sarcolemma
NCX
ATP
Na
RyR
Ca
Ca
2K
ATP
3Na
PLB
ATP
ICa
SR
T-Tubule
Ca
by D.M . Bers
Ca
[Ca]i
NCX
3Na
AP
(Em)
Contraction
Cyt
Na
Il PLB inibisce l’attività della pompa
La fosforilazione del PLB libera la
pompa
da
questa
inibizione,
aumentando
la
velocità
di
riassorbimento e di accumulo del Ca2+
nel reticolo sarcoplasmatico.
Ciò rende più veloce e precoce il
rilasciamento
del
miocardio
abbreviando la durata della
sistole a vantaggio della diastole
e consentendo l’accumulo di
una maggiore quantità di Ca2+
nel reticolo sarcoplasmatico che
si traduce in un maggiore
rilascio dagli “store” e quindi in
una maggiore forza contrattile
durante la sistole.
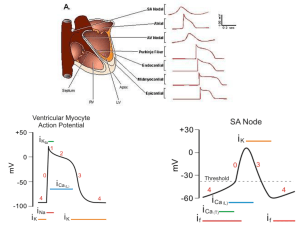
Potenziale d’azione del muscolo cardiaco
Vmr si mantiene stabilmente ad un
valore -80/-90mV da precludere
l’insorgenza di pda in risposta a
segnali di debole intensità che
potrebbero interferire col ritmo
cardiaco fisiologico. La soglia
d’insorgenza del pda è infatti così
elevata da poter essere superata
solo dall’intenso stimolo naturale che
origina nel nodo seno atriale.
L’ingresso di calcio durante la fase 2 prolunga la durata del potenziale d’azione miocardico. Ciò impedisce
che si verifichi una contrazione tetanica. Questa è una caratteristica importante per la funzione del
cuore perché il miocardio tra una contrazione e l’altra deve rilasciarsi per permettere ai ventricoli di
riempirsi di sangue.
PdA del muscolo ventricolare
Potenziale di membr.
del muscolo ventricolare (mV)
Muscolatura
ventricloare
l
0
l
l
l
-50
l
200 msec
Potenziale di riposo (-80 / -90 mV)
Attivazione rapida, Na+-dipendente
Plateau Ca2+-dipendente
Ripolarizzazione K+-dipendente
Contrazione
NaV
CaT
CaL
KA
KV
KIR
Il tetano non può verificarsi a livello del miocardio perché il periodo refrattario e la
contrazione terminano quasi contemporaneamente a causa del potenziale d’azione di
lunga durata. Quando si ha un secondo potenziale d’azione, la cellula miocardica è già
rilasciata e, di conseguenza, la sommazione non può verificarsi.
Il lunghissimo “plateau” del pda dei miociti ventricolari è funzionalmente
importante per due buone ragioni:
a) mantenendo depolarizzata la membrana,
la rende ineccitabile per tutta la sua durata
(perché mantiene inattivati i canali del Na+).
In altre parole: durante il plateau, il cuore si
trova in uno stato di refrattarietà assoluta,
quindi per tutta la durata della contrazione
(della sistole) non può essere nuovamente
eccitato.
Abbiamo visto che la situazione è molto
diversa da quella che si ha nel muscolo
scheletrico, nel quale la refrattarietà assoluta
termina ancor prima che inizi la contrazione.
b) il Ca2+ che entra attraverso i canali (L) della membrana plasmatica attiverà il
“Ca-activated Ca-release” del reticolo sarcoplasmatico, quindi la contrazione del
cuore;
Quattro importanti caratteristiche elettriche dei
potenziali d’azione cardiaci
Depolarizzazione spontanea (potenz. pacemaker)
Innervazione neuronale non richiesta
Propagazione tra le cellule
Sincizio elettricamente accoppiato
Assicura un’attività ritmica continua
Fase di plateau lunga nei miociti (~200ms)
Assicura una forte contrazione
Periodo di refrattarietà lungo nei miociti
Previene la sommazione di scosse muscolari semplici
Potenziale d’azione nelle cellule pacemaker:
Le cellule miocardiche autoritmiche generano p.a. spontaneamente in assenza di uno stimolo dal SN.
Il potenziale di membrana di queste cellule è instabile,
parte da -60 mV e lentamente sale verso il valore soglia.
Ogni volta che il potenziale pacemaker depolarizza la
cellula portandola al valore soglia, parte un potenziale
d’azione. Alla base del potenziale pacemaker vi sono i
canali If che si aprono a valori di potenziali negativi e
permettono il passaggio di Na e K. La membrana si
depolarizza, i canali If si chudono e si aprono i canali per
il Ca di tipo T, l’ingresso di calcio depolarizza
ulteriormente la membrana portandola al valore soglia. A
questo punto si aprono i canali per il Ca di tipo L,
responsabili della fase ascendente del potenziale
d’azione
Potenziale d’azione del nodo SA
È un potenziale d’azione
al Ca2+!!!!!
Potenziale di membr.
del nodo SA (mV)
Nodo SA
Depolarizzazione lenta e
Ca+2-dipendente
0
Ripolarizzazione
K+-dipendente
-50
200 msec
Non c’è potenziale di riposo
(prepotenziale)
È un pda del Ca.
CaT
CaL
KV
Funny
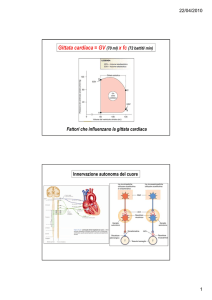
I neurotrasmettitori del sistema nervoso autonomo modulano la frequenza cardiaca
Gli effetti del
parasimpatico sono
normalmente
prevalenti su quelli
simpatici, per cui si
dice comunemente
che il cuore è
costantemente
mantenuto sotto un
“freno” vagale.
L’aumento della permeabilità al Na e al Ca durante la fase del potenziale pacemaker
accellererà la depolarizzazione e quindi la frequenza cardiaca. La diminuzione della
permeabilità al Ca o l’aumento della permeabilità al K diminuirà la velocità di
depolarizzazione rallentando così la frequenza cardiaca.
Si avrà un aumento della velocità della depolarizzazione spontanea ed una diminuzione
del livello di ripolarizzazione per cui la soglia per l’insorgenza del potenziale d’azione
viene raggiunta più rapidamente.
La velocità della depolarizzazione spontanea diminuisce e si avrà una iperpolarizzazione
della membrana, con conseguente allontanamento del potenziale di membrana dal livello
di soglia per l’insorgenza del potenziale d’azione.
IL SISTEMA DI CONDUZIONE DEL CUORE
Le cellule pacemaker sono concentrate nel nodo senoatriale, localizzato nella parte
superiore dell’atrio destro in prossimità dello sbocco della vena cava superiore, e nel nodo
atrioventricolare, posto vicino alla valvola tricuspide in prossimità del setto interatriale.
Le cellule del nodo SA hanno una attività spontanea intrinseca più elevata di quelle del
nodo AV e, poiché i due nodi sono connessi da fibre di conduzione, è il nodo SA ad attivare
la scarica del nodo AV e quindi di tutto il cuore, stabilendone così il ritmo, cioè la
frequenza a cui il cuore batte.
-Un potenziale d’azione inizia nel nodo SA.
Da qui gli impulsi si dirigono al nodo AV
mediante
le
vie
internodali,
che
rappresentano il sistema di conduzione
che si dirama attraverso gli atri.
-L’impulso viene condotto alle cellule del
nodo AV che trasmettono i potenziali
d’azione
meno
velocemente,
di
conseguenza
l’impulso
viene
momentaneamente rallentato (di circa 0.1
s). Ciò permette agli atri di completare la
loro contrazione prima che abbia inizio la
contrazione ventricolare.
-Dal nodo AV l’impulso viene condotto al
fascio atrioventricolare e da qui nelle due
branche del fascio di destra e di sinistra
che conducono lo stimolo al ventricolo di
destra e di sinistra
-Dalle due branche, gli impulsi viaggiano
attraverso
una
estesa
rete
di
ramificazioni dette fibre del Purkinje, che
diffondono
attraverso
il
miocardio
ventricolare.
Potenziale d’azione del nodo AV
È un potenziale d’azione
al Ca2+!!!!!
Nodo AV
Potenziale di membr.
del nodo AV (mV)
l
l
l
0
nodo SA
l
l
-50
nodo AV
200 msec
Simile al nodo SA
Segnaritmo latente
Depolarizzazione lenta,
Ca+2-dipendente
Conduzione lenta (ritardo)
Ripolarizzazione K+dipendente
Flusso dell’attività elettrica
cardiaca (potenziali d’azione)
Nodo SA
Andatura (stabilisce il ritmo cardiaco)
Muscolo atriale
Contrazione
Nodo SA
Nodo AV
Nodo AV
Ritardo
Fascio AV
Fibre del Purkinje
Rapide, distribuite uniformemente
Muscolo ventricol. Contrazione
Fibre di
Purkinje
●I potenziali d’azione sono generati a livello del nodo seno-atriale (nodo SA) e si
propagano rapidamente da una cellula all’altra. L’onda di depolarizzazione è seguita
da un’onda di contrazione che passa prima attraverso gli atri per poi trasferirsi ai
ventricoli.
● Il segnale elettrico passa dal nodo SA al nodo atrio-ventricolare (nodo AV)
attraverso la via internodale, per poi proseguire nel fascio AV, nelle due branche
del fascio, nelle fibre del Purkinje terminali e, infine, nelle cellule miocardiche
contrattili dei ventricoli.
●I setti cartilaginei tra atri e ventricoli impediscono il trasferimento diretto
dell’impulso tra atri e ventricoli. Ciò impedisce che la contrazione ventricolare
parta dalla parte superiore dei ventricoli. In tal caso, il sangue verrebbe spinto in
basso e verrebbe intrappolato a livello del fondo del ventricolo.
●Il nodo SA stabilisce il ritmo del battito cardiaco. Se il nodo SA non funziona
correttamente, altre cellule autoritmiche del nodo AV assumono il controllo
della frequenza.
Un elettrocardiogramma, ECG, è la registrazione dell’attività elettrica del cuore effettuata
con elettrodi posizionati sulla superficie cutanea.
Triangolo di Einthoven
L’onda P corrisponde alla depolarizzazione degli atri; il complesso QRS, rappresenta la
progressione dell’onda di depolarizzazione nei ventricoli; l’onda T, rappresenta la
ripolarizzazione dei ventricoli. La ripolarizzazione atriale non è rappresentata da nessuna
onda specifica ma è inclusa nel complesso QRS.
Gli
eventi
meccanici
del
ciclo
cardiaco
iniziano con lieve
ritardo rispetto
ai
segnali
elettrici.
La
contrazione
atriale inizia
nell’ultima
fase
dell’onda P e
continua
durante
il
tratto PR.
La
contrazione
ventricolare
inizia subito
dopo l’onda
Q
e
continua
fino all’onda
T.
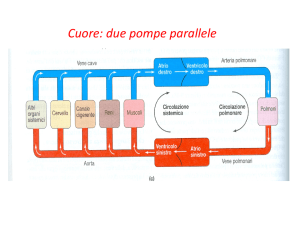
CICLO CARDIACO
È il periodo di tempo compreso tra l’inizio
di un battito cardiaco e l’inizio del successivo
●Un ciclo cardiaco comprende la fase di contrazione (sistole) e di rilasciamento
(diastole).
●La maggior parte del sangue entra nei ventricoli quando gli atri sono rilasciati.
Solo il 20% del riempimento ventricolare è dovuto alla contrazione atriale.
●Le valvole AV impediscono il reflusso di sangue negli atri. Le vibrazioni
associate alla chiusura delle valvole AV causano il primo tono cardiaco.
●Durante la contrazione ventricolare isovolumica, il volume di sangue nel
ventricolo non cambia, ma la pressione aumenta. Quando la P nel ventricolo
supera quella arteriosa, le valvole semilunari si aprono ed il sangue viene spinto
nelle arterie.
●Quando i ventricoli si rilasciano, la P intra-ventricolare diminuisce e le valvole
semilulari si chiudono, provocando il secondo tono cardiaco.
Gittata sistolica = quantità di sangue pompata da un ventricolo durante
una contrazione.
Gittata cardiaca = quantità di sangue pompata da un ventricolo nell’unità di tempo
(volume di sangue pompato nell’unità di tempo).
Gittata sistolica = EDV-ESV 135mL-65mL=70mL
Gittata cardiaca = frequenza cardiaca x gittata sistolica
72 battiti/min x 70 mL/battito
5040 mL/min
CICLO CARDIACO
È il periodo di tempo compreso tra l’inizio
di un battito cardiaco e l’inizio del successivo
Ritorno venoso
Valore medio della
pressione aortica che
si registra durante il
ciclo cardiaco.
PAM = Pdiast + 1/3 (Psist – Pdiast)
PAM = 80 mm Hg + 1/3 (120-80 mm Hg)
PAM = 93 mm Hg
Il sangue dal cuore sinistro si porta nelle arterie sistemiche. La pressione generata dalla
contrazione del ventricolo sinistro viene accumulata nelle pareti elastiche delle arterie e
lentamente rilasciata dal loro ritorno elastico. Questo meccanismo permette di mantenere
una pressione propulsiva continua che sostiene il flusso sanguigno durante la fase di
rilasciamento ventricolare.
Il flusso sanguigno totale a qualsiasi livello della circolazione è uguale alla gittata cardiaca.
Volume di eiezione ventricolare
SV = EDV – ESV
Frazione di eiezione
FE = SV / EDV
SV = 130 mL – 60 mL = 70 mL
FE = 70 mL / 130 mL = 0.54
La frazione di volume telediastolico espulsa dal ventricolo durante un
battito cardiaco è detta Frazione di eiezione
Gittata cardiaca = Gittata sistolica x Frequenza cardiaca
È la velocità con la quale il ventricolo pompa sangue ed è espressa in L/min
Gittata sistolica = EDV-ESV 135mL-65mL=70mL
Gittata cardiaca = frequenza cardiaca x gittata sistolica
72 battiti/min x 70 mL/battito
5040 mL/min
Gittata cardiaca = Frequenza cardiaca x Gittata sistolica
Controllo estrinseco
Gittata cardiaca
Controllo intrinseco
La frequenza cardiaca è sotto il controllo antagonista del SNA. L’attività
parasimpatica rallenta la frequenza cardiaca; l’attività simpatica l’aumenta. Il
controllo tonico della frequenza cardiaca è dominato dal parasimpatico. Per cui
l’aumento della frequenza cardiaca si può avere sia diminuendo l’attività del
parasimpatico, sia attivando l’ortosimpatico.
I neuroni simpatici innervano anche il
sistema di conduzione aumentando la
velocità di conduzione dei pa e quindi
accelerando la contrazione
ventricolare che parte prima e
prosegue più rapidamente riducendo
la durata della sistole
Gli effetti dell’adrenalina, che viene
secreta dalla midollare del surrene e
giunge al cuore per mezzo del
torrente circolatorio, sono simili a
quelli del simpatico. Inoltre aumenta
la velocità di conduzione del
potenziale d’azione attraverso le
fibre muscolari cardiache.
Poiché l’aumentata attività del simpatico è associata ad un’aumentata secrezione di adrenalina,
l’azione dell’ormone rinforza gli effetti dello stimolo nervoso simpatico.
Anche gli ormoni tiroidei, l’insulina e il glucagone influenzano l’attività cardiaca, in
genere aumentando la forza di contrazione cardiaca.
La gittata sistolica, cioè la quantità di sangue pompata dal ventricolo a ogni
contrazione, è direttamente correlata alla forza generata dal miocardio
durante la contrazione: più elevata è la forza, maggiore sarà la gittata
sistolica.
La forza della contrazione muscolare è influenzata da 2 parametri:
1.Lunghezza della fibra muscolare all’inizio della contrazione
(che dipende dal volume di sangue nel ventricolo all’inizio della contrazione(EDV)
2.Contrattilità miocardica
(che dipende dall’interazione del calcio con i filamenti contrattili)
Legge di Starling, relazione lunghezza tensione.
La forza generata dalla contrazione del miocardio è direttamente correlata alla lunghezza
del sarcomero: quando questa aumenta (fino ad una lunghezza ottimale) anche la tensione
aumenta. Se una quota aggiuntiva di sangue passa nei ventricoli, le fibre muscolari si
allungano e quindi si contraggono con maggiore forza, spingendo fuori più sangue.
Relazione lunghezza-tenzione, legge di Frank-Starling
Relazione lunghezza-tensione:
Curva di Starling
Il EDV è determinato a sua volta dal
ritorno venoso che è influenzato da:
Pompa muscolare
Pompa respiratoria
Innervazione ortosimpatica delle vene
….2.Contrattilità miocardica
(che dipende dall’interazione del calcio con i filamenti contrattili
La contrazione del miocardio
può essere graduata. La forza
generata dal
miocardio
è
proporzionale al numero di
ponti trasversali attivi che
dipende dalla concentrazione
del calcio intracellulare.
Effetto inotropo positivo
delle catecolamine
Oltre ad aumentare la forza,
le catecolamine accorciano la
durata
della
contrazione
cardiaca
Il PLB inibisce l’attività della pompa
La fosforilazione del PLB libera la
pompa
da
questa
inibizione,
aumentando
la
velocità
di
riassorbimento e di accumulo del Ca2+
nel reticolo sarcoplasmatico.
Ciò rende più veloce e precoce il
rilasciamento
del
miocardio
abbreviando la durata della
sistole a vantaggio della diastole
e consentendo l’accumulo di
una maggiore quantità di Ca2+
nel reticolo sarcoplasmatico che
si traduce in un maggiore
rilascio dagli “store” e quindi in
una maggiore forza contrattile
durante la sistole.
Un altro meccanismo per aumentare la concentrazione del calcio nel
citosol è quello di impedire la sua rimozione dalla cellula. Ciò si può
ottenere somministrando glicosidi cardioattivi come la digitossina e
il composto correlato ouabaina che agiscono deprimendo l’attività
della pompa Na/K . Il gradiente di concentrazione del Na
diminuisce diminuendo l’energia potenziale per il trasporto attivo
secondario sostenuto dal Na (scambiatore Na/Ca). L’incremento
risultante della contrazione del calcio nel citosol determina una
contrazione miocardica più potente.
Per questo motivo la digitale viene usata per l’insufficienza
cardiaca che è la condizione in cui il cuore non è in grado di
contrarsi efficacemente.
Frazione di eiezione, F
F = [GS/EDV]x100
GS, gittata sistolica
EDV, volume telediastolico