Il metabolismo del glicogeno
Copyright © 2013 Zanichelli editore S.p.A.
La demolizione del glicogeno
Concetti chiave
• Il glicogeno, la forma di immagazzinamento del glucosio nei mammiferi, è
un polimero ramificato.
• La mobilizzazione del glucosio nel fegato coinvolge una serie di reazioni
che dal glicogeno portano a glucosio-1-fosfato, glucosio-6-fosfato e infine
a glucosio.
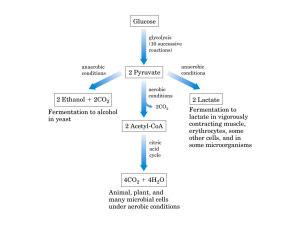
Schema generale del
metabolismo del glucosio
Struttura del glicogeno
Struttura ramificata del glicogeno
Granulo di glicogeno
Il cofattore PLP della fosforilasi
L'enzima deramificante del glicogeno
Scheda 16.2: Le malattie
da accumulo di glicogeno
La demolizione del glicogeno
Punto di verifica
• Elencate le fonti metaboliche e i destini del G6P.
• Descrivete la struttura di una molecola di glicogeno. Qual è il vantaggio
della sua struttura ramificata?
• Elencate i tre enzimi coinvolti nella degradazione del glicogeno e
descrivete i tipi di reazioni che catalizzano.
• Elencate gli attivatori e gli inibitori della glicogeno fosforilasi. In che modo
la fosforilazione influenza la sua attività catalitica?
La sintesi del glicogeno
Concetti chiave
• La sintesi del glicogeno nel fegato coinvolge una serie di reazioni che da
glucosio portano a glucosio-6-fosfato, UDP-glucosio e, infine, a glicogeno.
• L'UDP-glucosio è una molecola attivata.
• Il glicogeno viene allungato a partire da un innesco costruito dalla
proteina glicogenina su se stessa.
Le vie opposte di sintesi e di
degradazione del glicogeno
Diagramma di processo del
meccanismo di reazione della
UDP-glucosio pirofosforilasi
La reazione catalizzata
dalla glicogeno sintasi
L'enzima ramificante del glicogeno
La sintesi del glicogeno
Punto di verifica
• Perché le vie opposte biosintetiche e degradative devono utilizzare
almeno un enzima differente?
• Elencate i tre enzimi coinvolti nella sintesi del glicogeno e descrivete i tipi
di reazioni che catalizzano.
• Qual è la fonte di energia per la sintesi del glicogeno?
• Descrivete il ruolo della glicogenina.
Il controllo del metabolismo del glicogeno
Concetti chiave
• I processi opposti di demolizione e di sintesi del glicogeno sono regolati
reciprocamente da interazioni allosteriche e modificazioni covalenti degli
enzimi chiave.
• Il metabolismo del glicogeno è fondamentalmente sotto il controllo di
ormoni quali l'insulina, il glucagone e l'adrenalina.
FEEDBACK negativo e positivo
La glicogeno fosforilasi è un enzima allosterico modificabile tramite fosforilazione
Il sistema enzimatico di interconversione
della glicogeno fosforilasi
I principali sistemi di
fosforilazione/defosforilazione nel
metabolismo
del glicogeno
L'ormone polipeptidico glucagone
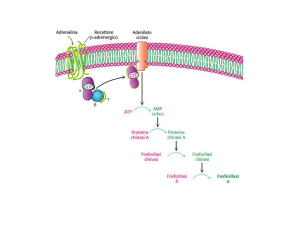
Controllo ormonale del
metabolismo del glicogeno
Il controllo del metabolismo del glicogeno
Punto di verifica
• Riassumete gli effetti dell'AMP e del G6P sulla glicogeno fosforilasi e
sulla glicogeno sintasi.
• Riassumete gli effetti della fosforilazione e della defosforilazione sulla
glicogeno fosforilasi e sulla glicogeno sintasi.
• Perché un sistema di fosforilazione/defosforilazione permette una
regolazione più sensibile di un processo metabolico rispetto a un semplice
sistema allosterico?
Il controllo del metabolismo del glicogeno
Punto di verifica
• Disegnate un grafico che illustri come una chinasi e una fosfatasi
possono regolare le attività di due enzimi che catalizzano processi opposti.
• Quali sono le differenze nella regolazione del metabolismo del glicogeno
tra il fegato e il muscolo?
• Riassumete gli effetti dell'insulina, del glucagone e dell'adrenalina sul
metabolismo del glicoeno.
• Quali sono gli effetti intracellulari del cAMP?
Il ciclo dell’acido citrico
Copyright © 2013 Zanichelli editore S.p.A.
Una panoramica del ciclo dell’acido ciclico
Concetti chiave
• Il ciclo dell’acido citrico è un processo catalitico a molte tappe che
converte i gruppi acetile derivati dai carboidrati, dagli acidi grassi e dagli
amminoacidi in CO2,producendo NADH, FADH e GTP.
Schema generale del metabolismo
ossidativo dei carburanti metabolici
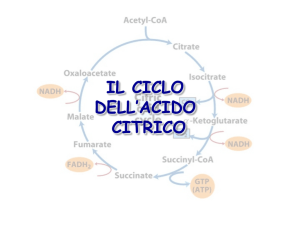
Le reazioni del ciclo dell’acido citrico
Una panoramica del ciclo dell’acido citrico
Punto di verifica
• Spiegate perché il ciclo dell’acido citrico è considerato il punto di
smistamento del metabolismo cellulare.
• Quali sono i substrati e i prodotti della reazione netta corrispondente a un
giro del ciclo dell’acido citrico?
La sintesi dell’acetil-CoA
Concetti chiave
• La piruvato deidrogenasi è un complesso multienzimatico che catalizza
una reazione in cinque fasi in cui il piruvato rilascia CO2 e il rimanente
gruppo acetile viene legato al coenzima A.
• La sequenza di reazioni richiede i cofattori TPP, lipoammide, coenzima A,
FAD e NAD+.
Il complesso multienzimatico della
piruvato deidrogenasi
Organizzazione strutturale del
complesso della PDH
Il complesso della PDH del
B. stearothermophilus
La reazione 1 catalizzata dall’E1 del
complesso della PDH
I cofattori del complesso della PDH
Le reazioni catalizzate dal complesso
della PDH
La sintesi dell’acetil-CoA
Punto di verifica
• Riassumete i vantaggi forniti dai complessi multienzimatici.
• Scrivete la reazione complessiva catalizzata dal complesso della piruvato
deidrogenasi.
• Descrivete le cinque reazioni catalizzate dal complesso multienzimatico
della piruvato deidrogenasi.
• Quali cofattori sono necessari? Quali di questi sono gruppi prostetici?
Gli enzimi del ciclo dell’acido citrico
Concetti chiave
• Gli otto enzimi del ciclo dell’acido citrico catalizzano le reazioni di
condensazione, isomerizzazione, ossido-riduzione, fosforilazione e
idratazione.
• Due reazioni producono CO2, una reazione produce GTP e quattro
reazioni generano i coenzimi ridotti NADH o FADH2.
Reazione 1: la citrato sintasi
Citrato sintasi
PDBids 1CTS e 2CTS
Reazione 2: l’aconitasi
Reazione 3: l’isocitrato deidrogenasi
rilascia la prima molecola di CO2
Reazione 3: l’ossidazione
NAD+-dipendente produce
la prima molecola di NADH
Reazione 3: la decarbossilazione
Reazione 4: l’a-chetoglutarato
deidrogenasi è simile al complesso della
PDH—produzione della seconda
molecola di NADH
Reazione 5: Succinil-CoA sintetasi,
fosforilazione a livello del substratosintesi della molecola di GTP
Reazione 6: la succinato deidrogenasi
produce FADH2
Il malonato è un inibitore competitivo
della succinato deidrogenasi
Il gruppo prostetico FAD è legato
covalentemente alla succinato
deidrogenasi
Reazione 7: la fumarasi
Reazione 8: la malato deidrogenasi
produce la terza molecola di NADH
Gli enzimi del ciclo dell’acido citrico
Punto di verifica
• Disegnate le strutture degli otto intermedi del ciclo dell’acido citrico e
indicate il nome degli enzimi che catalizzano le loro interconversioni.
• Quali tappe del ciclo dell’acido citrico rilasciano CO2 come prodotto della
reazione? Quali tappe producono NADH o FADH2? Quali tappe producono
GTP?
• Scrivete le equazioni nette dell’ossidazione del piruvato, del gruppo
acetile dell’acetil-CoA e del glucosio a CO2 e H2O.
La regolazione del ciclo dell’acido citrico
Concetti chiave
• Il fabbisogno energetico regola il ciclo dell’acido citrico agendo a livello
della tappa catalizzata dalla piruvato deidrogenasi e delle tre tappe che
controllano la velocità del ciclo.
• I meccanismi di controllo dipendono dalla disponibilità dei substrati,
dall’inibizione da parte dei prodotti, dalle modificazioni covalenti e dagli
effetti allosterici.
I prodotti del ciclo dell’acido citrico
Gli elettroni vengono convogliati nella
sintesi di ATP
Le modificazioni covalenti nella
regolazione dell’E1
3 enzimi funzionano in condizioni
lontane dall’equilibrio
Regolazione del ciclo dell’acido citrico
La regolazione del ciclo dell’acido citrico
Punto di verifica
• Quante molecole di ATP si possono generare dal glucosio se il ciclo
dell’acido citrico è attivo?
• Quali sono le tappe di regolazione del flusso nel ciclo dell’acido citrico?
• Descrivete il ruolo dell’ADP, del Ca2+, dell’acetil-CoA e del NADH nella
regolazione della piruvato deidrogenasi e del ciclo dell’acido citrico.
Le reazioni correlate al ciclo dell’acido citrico
Concetti chiave
• Il ciclo dell’acido citrico fornisce i metaboliti per la gluconeogenesi, la
sintesi degli acidi grassi e la sintesi degli amminoacidi.
• Gli intermedi del ciclo dell’acido citrico possono essere riforniti da altre
vie metaboliche.
• Alcuni organismi utilizzano il ciclo del gliossilato, una variante del ciclo
dell’acido citrico, per la conversione netta dell’acetil-CoA in ossalacetato.
Funzioni anfiboliche del ciclo
dell’acido citrico
La biosintesi del glutammato
La biosintesi dell’aspartato
Le reazioni anaplerotiche riforniscono il
ciclo dell’acido citrico di intermedi
Le reazioni correlate al ciclo dell’acido citrico
Punto di verifica
• Spiegate come un ciclo catalitico può fornire precursori per altre vie
metaboliche senza impoverirsi contemporaneamente di intermedi.
• Quali intermedi del ciclo dell’acido citrico possono essere usati
direttamente nella gluconeogenesi? Quali possono essere usati per la
biosintesi degli acidi grassi? Quali possono essere convertiti direttamente
in amminoacidi?
• In che modo la cellula rigenera l’ossalacetato, l’a-chetoglutarato e il
succinil-CoA?
• Descrivete le reazioni del ciclo del gliossilato. Quali sono i due enzimi
che sono unici di questa via? Che cosa fa questa via?
Il trasporto di elettroni e la
fosforilazione ossidativa
Copyright © 2013 Zanichelli editore S.p.A.
Schema generale del metabolismo
ossidativo dei carburanti metabolici
Il mitocondrio
Concetti chiave
• Una membrana interna altamente ripiegata e molto ricca in proteine
separa la matrice mitocondriale dalla membrana esterna.
• Le proteine di trasporto sono necessarie per importare nei mitocondri
equivalenti riducenti, ADP e Pi.
Il mitocondrio
La membrana interna è ricca di proteine
Il trasporto degli elettroni
Concetti chiave
• L’energia libera del trasporto degli elettroni dal NADH all’O2 può
alimentare la sintesi di circa 2.5 molecole di ATP.
• I trasportatori di elettroni sono disposti nella membrana mitocondriale in
modo che gli elettroni passino dai complessi I e II, attraverso il coenzima
Q, al complesso III e da qui, attraverso il citocromo c, al complesso IV.
• Il complesso I a forma di L trasferisce elettroni dal NADH al CoQ
attraverso una serie di centri ferro-zolfo e trasloca quattro protoni nello
spazio intermembrana.
Il trasporto degli elettroni
Concetti chiave
• Il complesso II trasferisce gli elettroni dal succinato al CoQ ma non
contribuisce al gradiente protonico transmembrana.
• Gli elettroni sono trasferiti dal complesso III al citocromo c e attraverso il
ciclo Q vengono traslocati due protoni.
• Il complesso IV accetta gli elettroni dal citocromo c riducendo l’O2 a H2O
e trasloca due protoni per ogni coppia di elettroni trasferiti.
La catena di trasporto degli elettroni
mitocondriale
Potenziali di riduzione dei componenti
della catena di trasporto degli elettroni
I centri ferro-zolfo
Il gruppo prostetico con attività redox
del braccio periferico del Complesso I
Thermus thermophilus
PDBid 2FUG
Traslocazione di protoni nella
batteriorodopsina
Batteriorodopsina
PDBid 1C3W
Scheda 18.1: I citocromi sono proteine
con gruppi eme che trasportano elettroni
Il Complesso III
Complesso III di
lievito
PDBid 1KYO
Il citocromo c
Il Complesso IV
Omodimero della citocromo c ossidasi di cuore bovino
PDBid 1V54
La fosforilazione ossidativa
Concetti chiave
• La teoria chemiosmotica spiega come un gradiente protonico
possa collegare il trasporto degli elettroni alla sintesi dell’ATP.
• L’ATP sintasi è costituita da un componente F1 che catalizza la
sintesi dell’ATP tramite un meccanismo di variazione della propria
capacità di legame.
• Per ogni due elettroni che entrano nella catena di trasporto degli
elettroni sotto forma di NADH e riducono un atomo di ossigeno,
sono prodotte approssimativamente 2.5 molecole di ATP.
L’accoppiamento del trasporto degli
elettroni alla sintesi dell’ATP
Modello dell’F1F0-ATPasi
F1F0-ATPase
PDBid 1JNV, 2A7U e
1B9U
Modello dell’F1F0-ATPasi
Rotazione ATP-dipendente dell’anello c
nell’F1F0-ATPasi
Rotazione ATP-dipendente dell’anello c
nell’F1F0-ATPasi