UNIVERSITÀDIPISA
DIPARTIMENTODIFARMACIA
CorsodiLaureaSpecialisticainChimicae
TecnologiaFarmaceutiche
TesidiLaurea:
PROGETTAZIONEESINTESIDIMODULATORIALLOSTERICIDEL
RECETTORECANNABINOIDECB1
Relatori:
Prof.ssaClementinaManera
Candidata: SaraNencini
Dott.ssaFrancescaGado
N°matricola441646
SettoreScientificoDisciplinare:CHIM–08
ANNOACCADEMICO2015–2016
Indice
Introduzionegenerale
• Storiadellacannabis 1
• Descrizionebotanica 3
• Cannabinoidi
6
• Sistemaendocannabinoide
8
− Recettoricannabinoidi
9
− Endocannabinoidi
13
− Biosintesiecatabolismodegliendocannabinoidi 14
• Meccanismiditrasduzionedelsegnale
17
• Ligandidisintesideirecettoricannabinoidi
21
• Usiterapeutici 30
Introduzioneallapartesperimentale 34
• DerivatidelPSNCBAM-1 42
Partesperimentale
55
75
Bibliografia Introduzionegenerale
Storiadellacannabis
LaCannabisèunadellepiùantichepiantepsicoattivemaiconosciute.Nelcorsodellastoria,
dall’Asiaall’Europa,dalleAmericheall’Africa,milionidiuominihannosfruttatolesuefibre
comemateriaprimaperitessutielacarta,hannousatoisuoisemiperlaproduzionediolio
e combustibile ed hanno apprezzato i suoi principi attivi per scopi medici e religiosi. Per
quantoconcernegliusimedici,essifuronoapprofonditidaiCinesichenetrascuraronoperò
glieffettiprovocatidallasuaassunzione.Essil’assumevanoinformadidecottopercurare
dolori interni di vario tipo come la stipsi, gotta e reumatismi; inoltre la fumavano per
alleviare il mal di denti e per curare lacerazioni del cavo orale. In Italia l’inizio della
coltivazione della canapa (esclusivamente a scopo tessile) è legato all’espansione delle
repubblichemarinare,nellequalierautilizzataperlafabbricazionedicordeeveleperle
navidaguerra.Solosuccessivamente,lemoltepliciproprietàdellacanapafuronosfruttate
nell’usodomesticoeperlaproduzionedioggettidiartigianatocheancoraoggisitrovano
sulmercato(peresempioletovagliedicanapatipichedellaRomagna).InEuropa,invece,
l’uso della canapa come psicotropo inebriante ha cominciato a diffondersi in seguito alla
campagnad’EgittodiNapoleonedel1798.Isuoisoldatinontrovandoalcolicicominciarono
adassumerehashishelaportaronoconloronelrientroinpatria.Sitrattadiunadiffusione
comunque assai modesta, restando l’uso ricreativo confinato in ambiti molto ristretti. Lo
stesso può dirsi della sua diffusone negli Stati Uniti dove, dove l’uso a fini ricreativi era
pressochè sconosciuto ai “bianchi”, essendo, ancora agli inizi del Novecento, patrimonio
quasiesclusivodelleminoranzemessicaneeafroamericane.Proprioinvirtùdiquestasua
scarsadiffusionediuso,finoagliinizidelsecoloscorsolaCannabisnonhadestatoparticolari
clamori.Apartiredaiprimiannidel1900,però,ilconsumodialcunedroghecominciaad
essere percepito come un’azione immorale. Quest’idea nasce negli Stati Uniti, in modo
sorprendentementerepentino,perpoipropagarsi,altrettantorapidamenteoltreoceano.
Leprimesostanzeadessereproibitesonoiderivatidell’oppioelacocaina.Inizialmente,
dunque,laCannabissembraresistereall’ondataproibizionista.Tuttaviaconl’approvazione
delMarihuanaTaxActnel1937,anchelacannabisfiniscenella“listanera”dellesostanze
proibite.Lacanapadiventaquindiimprovvisamenteunadrogapericolosae,nelgirodipochi
anni,sirafforzal’ideacheisuoiderivatisianoaddiritturalaviad’accessoprivilegiataalla
“tossicodipendenza”ealconsumodieroinaecocaina.Questanuovafase,inevitabilmente
coinvolgerànonsoltantolevicendedella“Cannabisdroga”,maanchequelledella“Cannabis
farmaco”. L’uso quindi non medico dei derivati della Cannabis comincia ad essere
severamentepunito,maintempimoltobreviciòarrivaacoinvolgeredirettamenteanche
l’uso terapeutico. Le case farmaceutiche vi si allontanarono tra il diciannovesimo e
ventesimosecolopoichésidiresseroversol’oppioenuovianalgesicisintetici,tantochenel
1941laCannabisscomparedallafarmacopeastatunitense.ÈcosicheilMarijuanaTaxAct
noncondizionòsoltantodrasticamentelastoriafuturadellaCannabiscomedrogaecome
farmaco,maneimpedìanchelostudioinambitoscientifico,proprioinunafaseincuile
potenzialitàterapeutichedellapiantacominciavanoadattrarrel’interessedidiversimedici
ericercatori.InEuropa,invece,ilregimefascistalamisealbandocome“drogadeinegrie
nemici della razza” e piano piano questa pianta assunse solo un aspetto negativo fino a
rimaneresoltantounadrogad'abuso.Negliultimianniperò,inseguitoanumerosistudi,
l’utilizzo della Cannabis a scopo terapeutico è stato tutelato, tanto che farmaci da essa
ottenutisonooraincommercio.1,2
Descrizionebotanica
LaCannabisèunapiantaarbustivaacicloannuale,originariadell’Asiacentraleeoccidentale,
macoltivatadatempiimmemorabiliinvaripartidelglobo.Crescespontaneamenteopuò
esserecoltivatainareetemperateetropicali(Figura1).
LatassonomiaincludelaCannabisnellafamigliadelleCannabaceeoCannabinacee,ordine
Urticalis(piantesialegnosecheerbaceeconfioripocoappariscenti).Leprimeclassificazioni
botaniche della Cannabis risalgono al XVIII secolo dove il primo botanico/naturalista a
parlarne fuCarl Linnaeus, che consideral’interogeneredellaCannabiscomeunasingola
specie indivisa: la Cannabis sativa L. Successivamente un altro botanico del tempo, D.E
Janichewskydistinsetrespecie:
• Cannabissativa(volg.Canapa),altafinoa3metriedallaformapiramidale;
• Cannabisindica(volg.Canapaindiana),piùbassadellaprecedenteeconunmaggior
numerodiramiefoglie;
• Cannabisruderalis(volg.Canaparussa,ruderaleoamericana),altaalmassimomezzo
metroeprivadirami.
InultimoicanadesiSmalleConquistripreserolaclassificazionediLinneo,definendouna
solaspeciedicannabis,presentantedellevarianti:c.sativa(usataperfibraeolio)euna
varietàindianac.indica(ustaperlaresinadallaqualesiestraggonoicannabinoidi).3
Lacannabisèun’erbadioicaafustierettidi2-3metri,piùomenoramificatieispidi.Le
foglie sono picciolate, per lo più alterne, palmato-composte con 5-7 segmenti ineguali,
lanceolati,ellitticiedentati.Almicroscopiosonovisibilideipelidirivestimentounicellulari,
ricurvi,conapiceappuntito,dicuialcunimostranolapartebasaleingrossata,contenente
cistoliti (depositi di carbonato di calcio). Sono presenti anche peli ghiandolari (tricomi)
costituiti da uno stipite pluricellulare, più o meno lungo, e da una testa pluricellulare
globosadi8-6cellule.Èdaquesteghiandole,poconumerosesullefoglieeparticolarmente
abbondantisullebratteedelleinfiorescenzefemminili,chesiricavalaresinariccadiprincipi
attivi (cannabinoidi di interesse farmacologico). Il frutto è una noce di 2,5-3,5 mm di
lunghezza,liscia,grigiastrachematurainautunnoecontienesolitamenteunsoloseme.I
fiori, generalmente riuniti in infiorescenze, sono unisessuali, raramente ermafroditi e
mancanodipetali.Ifiorimaschiliportantilostame,sonoriunitiinracemiascellari,con5
sepalie5stami.Ifiorifemminiliportantiipistillisonoriunitiinspigheglomerulate,disposte
acoppieall’ascelladiunabrattea;sonocostituitidauncaliceurceolatochecircondal’ovario
uniovulato. È dal calice che in caso di fecondazione comincia a formarsi il seme. Il fiore
comparel’estateel’impollinazioneavvieneadoperadelvento.
Nella canapa sono stati evidenziati numerosi composti: un olio essenziale, flavonoidi,
zuccheri, acidi grassi, composti fenolici, diidrostilbeni, composti azotati e i cannabinoidi.
Quest’ultimipresentiappuntosullefoglie,esoprattuttosullebratteedelleinfiorescenze
femminilidovesitrovanoleghiandolecontenentilaresina,vengonoclassificatiinfunzione
dellalorostrutturaeseneconosconocircasettanta.
Iprincipalisonoilcannabidiolo,ilcannabinoloeiltetraidrocannabinolo.Perpoterliestrarre
ènecessariosfregareitricomiperfarfuoriuscirelaresina.4,5
Figura1.Illustrazionedicannabissativa.
Cannabinoidi
Ilterminecannabinoidisiriferivainpassatoalgruppodicomposticontipicastruttura
C21 presenti nella Cannabis sativa. La moderna definizione, basata maggiormente
sullachimicasinteticaesullafarmacologia,comprendestruttureaffini,oognialtro
compostocheinteragiscaconirecettoricannabinoidi.Èstatopropostodiutilizzareil
terminefitocannabinoidipericompostinaturali-vegetali;mentreendocannabinoidi
pericompostinaturali-umaniediligandiendogenideirecettoricannabinoidi.
Ifitocannabinoidinaturalisonoidrocarburiaromaticicontenentiossigeno.6
Iprincipalisono(Figura2):
• Δ9-Tetraidrocannabinolo(Δ9-THC)
• Δ8-Tetraidrocannabinolo(Δ8-THC)
• Cannabinolo(CBN)
• Cannabidiolo(CBD)
• Cannabigerolo(CBG)
• Cannabicromene(CBC)
OH
OH
OH
O
Delta-9-THC
Delta-8-THC
OH
OH
HO
HO
Cannabigerolo (CBG)
Cannabinolo (CBN)
O
HO
Cannabidiolo (CBD)
Cannabicromene (CBC) Figura2.Immaginedeiprincipalifitocannabinoidi.
Tra i fitocannabinoidi, il composto principale dotato di attività biologica è il delta-9tetraidrocannabinolo (abbreviato Δ9-THC). Esso è responsabile dell’attività psicotropa
riscontratadurantel’assunzionedicannabis.6IlΔ9-THCèunolioviscosorosso-marroncino,
concentrato nella resina della pianta. I cannabinoidi strutturalmente correlati al THC
possonoessereconsideratideidibezopiranisostituiti,oppuredeiterpenoidisostituiti,ciò
che cambia è la numerazione chimica (Figura 3). In pratica è usata esclusivamente la
numerazionedibenzopiranica.
11
7
9
1
8
10
OH
1
10a
7
6a
6
2
5
3
4
2
10b
OH
1'
2'
3'
3
13
12
6
O
4'
5
4
3'
1'
(a)
10
5'
8
9
O
6'
5'
1''
3''
5''
(b)
Figura3.Numerazionedibenzopiranica(a)eterpenoide(b).
SistemaEndocannabinoide
IlSistemaEndocannabinoide(ECS)èuncomplessosistemabiochimicochesvolgeimportanti
funzioni regolatorie in tutto il corpo ed è coinvolto in un numero sempre crescente di
processifisiologiciepatologie.7IlSistemaEndocannabinoidehainfattiunruoloimportante
neiprocessifondamentalidellosviluppo.Ilrilasciodeicannabinoidiendogenicontrollala
plasticità sinaptica, ovvero, la capacità del sistema nervoso di modificare l’efficienza del
funzionamento delle connessioni tra neuroni (sinapsi), di instaurarne di nuove e di
eliminarne alcune in molte aree cerebrali comprese la neocorteccia, l’ippocampo, il
cervelletto,eiganglidellabase.Ilsignalingendocannabinoidehaunruolofondamentale
nellesinapsiconunchiarocontinuumd’azione,dallostabilirsidellesinapsinell’inizio del
neurosviluppo,allafunzionedellesinapsinelcervelloadulto.Ilsistemaendocannabinoide,
infatti,èpresentenelSistemaNervosoCentralefindalleprimefasidisviluppocerebrale,ed
esso possiede un ruolo rilevante nell’organizzazione cerebrale durante la vita pre e
postnatale. Recenti evidenze indicano che gli endocannabinoidi intervengono durante il
neurosviluppo.Essisonocoinvoltinelcontrollodellaneurogenesi,nellaproliferazionedei
progenitorineurali,nellamigrazioneenellaspecificazionefenotipicadeineuroniimmaturi,
influenzandolaformazionedicomplessinetworkneuronali.8
IlSisemaEndocannabinoideècostituitoda:
• recettoricannabinoidiCB1eCB2;
• endocannabinoidi;
• enzimideputatiallabiosintesiecatabolismodiquestiligandi.
RecettoriCannabinoidi
Irecettoricannabinoidivengonocosìdefinitiinquantorispondonoasostanzederivantidalla
cannabisedaltricompostiadessistrutturalmentecorrelati.Dallascopertadelprincipale
componentepsicoattivodeipreparatiabasedicannabis,ovverodelΔ9-THC(avvenutanel
1964)9, solo agli inizi degli anni ’90 si giunse all’identificazione e alla caratterizzazione
molecolaredelprimorecettorecannabinoide,denominatoCB1.10
IrecettoricannabinoidisonounaclassedirecettoriaccoppiatialleproteineG.Presentano
un’unicacatenapolipeptidicacheattraversaper7voltelamembranaplasmaticaportando
la porzione ammino-terminale sul versante extracellulare e quella carbossilica su quello
intracellulare. Oltre ai 7 domini transmembrana sono presenti 3 loops intracellulari e 3
extracellulari11(Figura5).
Figura5.StrutturadeirecettoriCB.
IprincipalirecettoricannabinoidisonoilrecettoreCB1eilrecettoreCB2chefuscoperto
successivamente (Figura 6). Il recettore CB1 è stato clonato dalla corteccia cerebrale di
ratto12,dacervelloetesticoliumani13edalcervelloditopo14.Essomostraun’omologianella
sequenzaaminoacidicatralespecie,chevadal97%al99%.IlrecettoreCB1umano(hCB1)
ècostituitodaunacatenapolipeptidicadi472amonoacidi(473nelrattoeneltopo).Una
variantedelrecettoreCB1èstataisolataanchedalpolmoneumanoedèstatadenominata
CB1A.15
Figura6.ImmaginedeirecettoricannabinoidiCB1eCB2.16
Il recettore CB2 è stato invece clonato da cellule leucemiche umane HL-60 (himan
promyelocytic leukaemia cells)17 ed è costituito da una sequenza di 360 aminoacidi e
presenta anch’esso sette domini transmembranali. Il recettore CB2 rispetto all’hCB1,
presentaundominioammino-terminalepiùcorto,dovenonvièsostanzialeconservazione.
L’omologia nella sequenza aminoacidica tra CB1 e CB2 è del 68% per quanto riguarda i
domini transmembranali, e solo del 44% per quanto riguarda la totalità della proteina.17
L’attivazionedelrecettoreportaall’inibizionedell’adenilatociclasi.IlrecettoreCB1modula
anchecanaliionici,inducendoadesempio,l’inibizionedeicanalidelCa+2 el’attivazionedi
quellidelK+.Icannabinoidihannoanchedimostratodimodularediverseviedisegnalazione
che sono più direttamente coinvolte nel controllo della proliferazione cellulare e della
sopravvivenza, tra cui chinasi segnale-regolata extracellulare (ERK), MAP-chinasi (MAPK),
fosfatidilinositolo3-chinasi(PI3K)/Akt.18,19
I recettori CB1 sono predominanti nell’encefalo (Figura 7), e la loro attivazione produce
effettisullacircolazioneelapsiche,similiaquellicausatidall’ingestionedicannabis,cosa
chenonavvieneconlastimolazionedeirecettoriCB2.Essisitrovanoprincipalmentealivello
delleterminazioninervosediencefalo,midollospinaleesistemanervosoperifericodove
inibisconoilrilasciodialtrineurotrasmettitori,masonopresentiancheinalcuniorganie
tessutiperifericitracuighiandoleendocrine,leucociti,milza,cuore,apparatoriproduttivo,
urinarioegastrointestinale.Cosìlaloroattivazioneproteggeilsistemanervosocentraleda
sovrastimolazione o sovrainibizione da parte di neurotrasmettitori. Nell’encefalo sono
espressi particolarmente in quelle regione responsabili del movimento (gangli basali,
cervelletto),dellamodulazionedeldolore(alcunezonedelmidollospinale,sostanzagrigia
periacquiduttale)6edelcomportamentoalimentare20.Riguardoaquest’ultimovannocitate
dueaeree,ilmesolimbicodovevengonomodulatilagratificazioneeilpiacerederivatinon
solo dall’assunzione di cibo appetitoso ma anche di alcool, nicotina e di alcune droghe,
ipotalamo, nei nuclei del quale sono localizzati i neuroni che producono neuropeptidi
anoressizzanti ed oressizzanti in grado di controllare l’apporto alimentare.20 La loro
espressioneinvecealivellodeltroncoencefalicoèbassa,ilchepuòspiegarelamancanzadi
mortalitàacutacannabis-correlata.6
Figura7.DistribuzionedeirecettoriCB1nelcervello.Leareeindicateconipuntininerisonoquelle
incuimaggiormantesilegailcannabinoideesogenoTHC.Fonte:NIDA.
I recettori CB2 sono espressi principalmente a livello periferico, nelle cellule
immunocompetenti,tracuiileucociti,lamilzaeletonsille,ilmidolloosseoematopoietico
maanchenelpancreas.8Recentementebasseconcentrazionisonostateidentificateanche
nel SNC, in particolare sulle cellule gliali e microgliali.21 Tali recettori quindi, svolgono
un’attività immunomodulatoria attraverso il rilascio di citochine, molecole proteiche
responsabilidellerisposteinfiammatorie.8Recentemente,oltreairecettoriCB1eCB2,sono
statitrovatialtrirecettoriingradodiinteragireconilSistemaEndocannabinoide.Traquesti
citiamo il GPR119 (espresso principalmente nel tratto digestivo) e il GPR55 (espresso
principalmentenelSNCenelleossa),cheappartengonoallafamigliadeirecettoriaccoppiati
alleproteineG;mentreilTRPV1orecettorevanilloideditipo1(localizzatosoprattuttonel
SNC)èuncanalecationicononselettivo.
Quest’ultimo è stato ampiamente studiato per il coinvolgimento nella nocicezione. Studi
recenti suggeriscono un’intensa interazione tra sistemi vanilloidi e endocannabinoidi in
diversefunzionicomportamentalifracuil’ansia.22IlrecettoreTRPV1nonèidentificatocome
unrecettorepericannabinoidipoichénonèattivatodamolecolecheagisconoalivellodi
talesistema.18
Endocannabinoidi
L’identificazione dei recettori cannabinoidi fu seguita dalla scoperta dei loro ligandi
endogeni: gli endocannabinoidi. Nell’encefalo gli endocannabinoidi agiscono come
neuromodulatori. Tutti gli endocannabinoidi sono derivati di acidi grassi polinsaturi,
differenziandosicosì,nellastrutturachimica,daifitocannabinoidi.6
Tragliendocannabinoidisinoadoraidentificaticisono(Figura8):
• Anandamide(N-arachidonoiletanolamide,AEA)
• 2-arachidonoilglicerolo(2-AG)
• 2-arachidonylgliceryletere(noladinetere)
• O-arachidonil-etanolamina(virodamina)
• N-arachidonoil-dopamina(NADA)
Anandamide e NADA non si legano solo ai recettori cannabinoidi ma condividono con la
capsaicina,unprincipioattivocontenutonelpepe.Essihannolacapacitàdistimolareanche
i recettori vanilloidi (TRPV1). Anandamide e 2-AG costituiscono i due primi
endocannabinoidiadesserestatiisolatieperquestosonoancheipiùstudiatifinoadora.A
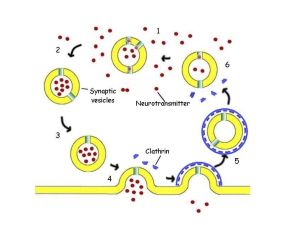
causa della loro natura lipidica gli endocannabinoidi non vengono immagazzinati nelle
vescicole sinaptiche come accade per altri neurotrasmettitori monoamminici, ma sono
sintetizzati “on demand” (solo quando necessario) dai neuroni, in seguito alla
depolarizzazionedellamembranaeall’aumentointracellularedeilivellidelCa2+.6
Figura8.Strutturechimichedegliendocannabinoidi.
Biosintesiecatabolismodegliendocannabinoidi
L’anandamide è stata identificata e isolata nel 1992 nel cervello di maiale (Devane et al.
1992),subitodopolascopertadeirecettoriCB1erappresentalaprimamolecolaendogena
individuata,ingradodilegarsiselettivamenteadessi.23Sitrattadiunderivatoammidico
dell’acidoarachidonico,componentedellemembranecellulari.Deveilsuonomeallaparola
Sanscrito“ananda”chesignifica“beatitudine”.8L’Anandamideèbiosintetizzataapartireda
un precursore fofsfolipidico di membrana, l’N-arachidonoil-fosfatidiletanolammmina
(NArPE)tramiteduefasi(Figura9,A):laprimaèresponsabiledellaformazionediNArPEper
trasferimentodiunaporzionedell’acidoArachidonicodallaposizionesn-1dialtrifosfolipidi
al gruppo amminico della fosfatidiletanolammina.24,25 Questo processo è catalizzato
dall’enzimaN-aciltransferasi(NAT).25IlrilasciodiAEAdaNArPEècatalizzatodaunaspecifica
fosfolipasiDN-acilfosfatidil-etanolammina(NAPE-PLD).26Ilprecursoreprincipaleinvecedel
2-AGèildiacil-glicerolo(DAGs)(Figura9,B)chederivaperlamaggiorpartedall’idrolisidel
fosfatidilinositolo27 ad opera della fosfolipasi C, oppure, in certe cellule, dall’idrolisi
dell’acido fosfatidico28, catalizzata dallo stesso enzima. Gli enzimi che catalizzano tali
processisonodueDAGlipasisn-1selettive,denominateDAGL-αeDAGL-β.29
Figura9.(A)BiosintesiAnadamide;(B)Biosintesi2-AG.
Una volta espletata la loro azione biologica, gli endocannabinoidi vengono ricaptati dalla
cellulaperpoiesseredegradatimedianteidrolisioossidazionedapartedienzimispecifici.
La degradazione di anandamide (Figura 10) avviene ad opera del FAAH o acido grasso
ammide idrolasi, un enzima di membrana intracellulare appartenente alla famiglia delle
serina-idrolasicheconsentediotteneremassimaattivitàapH9.Èampiamentedistribuito
intuttoilcorpo,conleconcentrazionipiùelevatenelcervelloenelfegato,essoidrolizza
l'AEAinacidoarachidonicoeetanolammina.30 IlFAAH,tuttavia,èingradodiriconoscere
unavarietàdiammididiacidigrassi,mailsuosubstratopreferitoèl'anandamide.18Questo
enzima è presente nei compartimenti somato-dendritici dei neuroni dei terminali
postsinapticiesi esprime maggiormentenelcervelletto,ippocampoeneocortecciamaè
assenteneineuronipresinaptici.Ineffettièstatapropriolasualocalizzazioneneineuroni
postsinapticichehafattopensarenel1998chel'anandamidepotessefunzionarecomeun
messaggero retrogrado.31 Il FAAH catalizza, in vitro, anche l'idrolisi del legame estereo
dell'acido 2-AG. Tuttavia tale processo è meno importante in vivo, dato che il 2AG viene
idrolizzatodaunaltroenzima,lamonoacilglicerololipasi(MAGL),enzimaidentificatonel
1976edèritenutoilprincipaleresponsabiledell'idrolisidellegameestereodel2AG18(Figura
10).E'altamenteespressosiaalivellocentraleneineuronipre-sinaptici,astrociti,ecellule
glialichealivelloperiferico,indiversitessutienelsistemaimmunitario.Ulteriorienzimidi
idrolisi del 2-AG sono ABHD6 e ABHD12, proteine integrali di membrana.16 Sono state
identificatedueisoformedelFAAH:FAAH1eFAAH2.Entrambesonoproteineintegralidi
membrana.FAAH1èstatopropostopercontenereunC-terminalesulfrontecitoplasmatico,
mentreilC-terminalediFAAH2siaffacciasullume.FAAH1èstatoclonatodadiversespecie,
tracuitopi,rattiedesseriumani,èmaggiormenteespressoalivellocentrale,neitesticoli,e
nel piccolo intestino. Il FAAH2, al contrario, non si esprime nei roditori ed è l'isoforma
predominante trovata nel tessuto cardiaco.32 Inoltre, enzimi della cascata dell’acido
arachidonico,comeleciclossigenasi2(COX-2)elalipossigenasiedancheenzimideltipo
citocromoP-450 possono intervenire in vie alternative di inattivazione degli
endocannabinoidi.33 L’ossidazione dell’anandamide catalizzata dalla COX-2, seguita
dall’azione di varie prostaglandina sintetasi, può condurre a prostaglandin-etanolammidi
(conosciute come “prostamidi”)34 che sono resisitenti all’idrolisi.35 Similmente il
metabolismo del 2-AG ad opera di COX-2 può portare a prostaglandin-glicerolo-esteri (o
gliceril-prostaglandine)36,37unodeiquali,lagliceril-prostaglandinaE2nonvieneidrolizzata
daFAAHoMAGL.38
L’ossigenazione di anandamide e/o 2-AG può avvenire anche in vitro, ad opera di
lipossigenasi,adareicorrispondentiidroperossieidrossi-derivati.39,42
Figura10.Immaginedelladegradazionedegliendocannabinoidi.16
Meccanismiditrasduzionedelsegnale
Una volta rilasciati, gli endocannabinoidi sintetizzati possono viaggiare in direzione
retrogradalungolafessurasinaptica,legandosiancheairecettoricannabinoidisuiterminali
presinaptici.8EntrambiirecettoriCB1eCB2sonoprincipalmenteaccoppiatiaproteineGi/o
(tramitelasubunitàα).IldominiointracellulareC-terminaledelrecettoreCB1èimportante
perl'accoppiamentoallaproteinaG.43
LaproteinaGèuneterotrimerocomprendenteunasubunitàα,eundimerobeta-gamma
(βγ). In condizioni basali la subunità α lega il GDP ed è ancorata al dimero βγ ma, nel
momento in cui il recettore viene attivato dal ligando, si crea un'alterazione
conformazionale che causa una dissociazione della subunità α dal complesso βγ e un
cambiamento del GDP che diviene GTP. Molti recettori accoppiati a proteine G hanno la
capacitàdiaccoppiarediversisottotipidiGα,suscitandointalmodorispostediverse.Questo
potrebbeindicarecheillegamediunparticolareligandoinduceunaconformazioneGPCR
chefavoriscel'attivazionediunospecificosottotipoGα44(Figura11).
Figura11.GPCRs:attivazionedellasubunitàGαi/o.
I ligandi agonisti per i recettori CB attivano molteplici vie di trasduzione del segnale
principalmenteattraversol'attivazionediquesteproteineGallequaliirecettoristessisono
accoppiati.
Entrambi i recettori se attivati causano l’inibizione dell’adenilato ciclasi e quindi la
conversione di ATP in AMP ciclico (cAMP) con conseguente diminuzione dei livelli di
quest’ultimo.19CiòpuòdeterminareadesempiolafosforilazionedellaproteinachinasiA
(PKA),cheasuavoltaregolal’aperturadeicanalidelK+ ditipoA.Inoltrel'attivazionedei
recettori CB causa la stimolazione delle proteine chinasi “mitogen activated” (MAPK),
importante per molte funzioni cellulari come la crescita, la trasformazione e l'apoptosi43
(Figura12).
Figura12.Immaginedeiprocessiderivantidall’attivazionedeirecettoriCB.16
Tipici eventi intracellulari Gi/o-mediati, accoppiati esclusivamente all’attivazione dei
recettori CB1 (Figura 13), sono rappresentati dall’inibizione dei canali del Ca2+ voltaggiodipendenti(VGCCs)dimoltitipi(inclusoicanaliP/QNeL)edallastimolazionedeicanalial
K+ DI TIPO Kir (inward rectifying)45-47 causando una iperpolarizzazione delle membrane.
L’inibizioneol’attivazionedicanaliionicièunadelleconseguenzeprincipalicherisultadal
legamedegliendocannabinoidiailororecettoriCB1.Recentistudihannodimostratocheun
aumentodiCa2+intracellularecausadepolarizzazionedellemembranecellulariinnescando
labiosintesieilrilasciononvescicolaredellemolecoledegliendocannabinoidilocalizzatia
livellodellemembraneneuronalipostsinaptiche.Gliendocannabinoidicosìliberatipossono
funzionaredamessaggeriretrogradi,legandosiairecettoriCB1presinanpticieinibendocosì
il rilascio di altri neurotrasmettitori (GABA, glutammato, dopamina, acetilcolina,
noradrenalina).8
Figura13.Ilsistemaendocannabinoideendogeno.
Inoltre, vi sono evidenze sempre maggiori della capacità dei CB1-agonisti (inclusi
endocannabinoidicomeanandamidee2-AG)distimolaredirettamente:
1. L’idrolisidelfosfatidil-inositolo-difosfato(PIP2)adoperadellaPLC-β(fosfolipasiC-β),
conilconseguenterilasciodiinositolo-1,4,5-trifosfato(IP3)elamobilitazionedaCa2+
dal reticolo endoplasmatico (ER), attraverso meccanismi Gq/11-mediati o Gi/0mediati.48-51
2. Lamodualzione,attraversoGi/0,dellacascatadisegnalemediatadallafosfoinositide3-chinasi (PI3K) che può essere di tipo positivo o negativo a seconda del tipo di
cellula52-56influenzandocosìlasuccessivaviaAkt/proteinchinasiB.
UnaltromeccanismoditrasduzionedelsegnaledescrittoperentrambiirecettoriCB1eCB2
è rappresentato dal rilascio di ossido nitrico (NO)57-59 con conseguente attivazione della
guanilato ciclasi ed aumento dei livelli di cGMP60,61, mentre il recettore CB2 risulta
accoppiatoancheaunaumentodelrilasciodiceramide.45
Ligandidisintesideirecettoricannabinoidi
Datal’importanzafisiologicadelsistemaendocannabinoidesonostatisintetizzaticomposti
ingradodiattivareall’incircaconlastessapotenzadeiligandiendogeniirecettoriCB1e
CB2, allo scopo di modularne l’azione. Tali composti in base alla loro attività funzionale
vengonoclassificaticomeagonisti,antagonisti,agonistiinversiemodulatoriallosterici.Gli
agonistileganoeattivanofortementeilrecettoregenerandounarispostabiologica;mentre
l’agonistainversoproduceesattamenteuneffettodisegnooppostoaquellodell’agonista.
Gliantagonistinonsonoingradodiindurrediperséunarispostabiologica,malegandosi
con alta affinità al recettore inibiscono l’effetto dell’agonista endogeno, che agisce
attraversolostessorecettore.Imodulatoriallosterici,infinesileganoaunparticolaresito
del recettore, chiamato appunto allosterico, e distinto da quello attivo modificandone e
regolandonecosìl’attività.
AgonistideirecettoriCB
GliagonistideirecettoriCBpossonoesseresuddivisiin4classisullabasedellalorostruttura
chimica:62,63
• Cannabinoidiclassici(Figura14).Sonocompostidibenzopiranici,siaderivatinaturali
cheanaloghisintetici.Gliesempipiùimportantisono:ilΔ9-THCchesilegaconuguale
affinitàairecettoriCB1eCB2comportandosidaagonistaparzialesuentrambi,anche
sepresentaunamaggioreefficaciasulrecettoreCB1.Fulaprimamolecolanaturale
estrattadallapiantadellacannabis64,dalpuntodivistaterapeuticosimostròutilein
chemioterapia come antiemetico, ma anche come analgesico e stimolante
dell’appetito.Tuttavia,ilsuousoèstatoproibitoacausadeglieffettiindesideratia
livello centrale, come euforia e alterazione della memoria dovuti all’attivazione in
particolar modo del recettore CB1.65 Il Δ8-THC ricalca il derivato precedente per
quantoriguardal’affinitàrecettorialeel’efficacianell’attivareilrecettoreCB1;l’HU210èinveceuncannabinoideparticolarmentepotente,icuieffettifarmacologiciin
vivo risultano di lunga durata (molto probabilmente a causa della presenza della
catenalateraledimetileptilica,alpostodiquellapentilicapresentenelTHC).
CH 3
CH 3
OH
OH
H 3C
H 3C
H 3C
H 3C
Delta-9-THC
Delta-8-THC
OH
OH
N
H
O
HU-210
Figura14.Strutturachimicadialcunicannabinoidiclassici.
• Cannabinoidinonclassici(Figura15).SonoanaloghibicicliciotriciclicidelTHC,incui
è stato rimosso l’anello piranico. L’esempio tipico è il CP-55940, agonista
cannabinoide considerevolmente più potente del THC ed ampiamente utilizzato
comeriferimentoneitestdilaboratorio.
OH
OH
HO
CP-55940
Figura15.Strutturachimicadialcunicannabinoidinonclassici.
• Amminoalchilindoli(Figura16).IlprototipodiquestaclasseèilWIN-55212,chein
alcuni studi ha dimostrato possedere un’affinità per i recettori CB2 leggermente
superiorerispettoaquellaperirecettoriCB1.
O
N
O
N
O
WIN-55212
Figura16.Strutturachimicadiunamminoalchilindoli.
• Eicosanoidi (Figura 17). I composti più studiati di questa classe sono i già citati
Anandamidee2-AG.L’anandamidericalcailTHCnelcomportarsidaagonistaparziale
su enrambi i recettori e per il fatto che mostra un’efficacia inferiore sul recettore
CB2.62
Figura17.Strutturachimicadialcunieicosanoidi.
AgonistiCB1selettivi
IprimiagonistiCB1selettivisonostatisviluppatiproprioapartiredall’anandamide,lacui
leggeraselettivitàperilrecettoreCB1èstatasignificativamenteincrementatainserendoun
gruppometilicosulcarbonioinposizione2,R-(+)-metanandamide(Figura18).Inoltre,tale
modificastrutturaleconferisceunanotevoleresisitenzaall’azioneidroliticadiFAAH,percui
laR-(+)-metanandamideeilsuociano-analogoO-1812possonoconsiderarsideglianaloghi,
metabolicamentestabili,dell’anandamide.
Altri agonisti CB1- selettivi con elevata efficacia, ma non resistenti alle FAAH, sono la
arachidonil-2-cloroetilammina(ACEA)elaarachidonil-ciclopropilammide(ACPA).
O
O
CH 3
NH
OH
NH
Cl
ACEA
R-(+)-Metanamide
O
NH
ACPA
Figura18.StrutturachimicadialcuniagonistiCB1selettivi.
AgonistiCB2selettivi
Diquestaclassenefannoparte(Figura19)JWH-133,uncannabinoideclassico,HU-308,un
cannabinoidenonclassico,JWH-015unamminoalchilindolo.
HO
O
O
N
O
O
JWH-133
HU-308
JW-015
Figura19.StrutturachimicadialcuniagonistiCB2selettivi.
Antagonisti/AgonistiinversiCB1selettivi
Ilprincipalecompostodiquestaclasseèildiarilpirazolo(Figura20)SR14176A(Rimonabant).
Esso blocca l’azione di vari agonisti dei cannabinoidi in vivo. Altri composti sono AM251,
AM281,LY320135,essipossonotuttiabloccarel’attivazionedeirecettoricannabinoidiCB1
agonista-indottainmodocompetitivo.Alcunidiessisonogiàstatiimpiegatiinterapiacome
agentianti-obesitàoperiltrattamentodidisordinimetabolici(dislipidemia,diabeteditipo
II), sebbene il loro uso è stato successivamente proibito a causa degli effetti collaterali
psichiatrici (ansia e depressione). Altri possibili usi terapeutici potrebbero includere:
steatosiepatica,abusodialcoolenicotina,ricadutenelcasodidipendenzadaeroinae/o
cocaina,schizofrenia,osteoporosi,morbodiParkinson,malattiadiAlzheimer.Sonoincorso
ulteriori studi allo scopo di sviluppare antagonisti/agonisti inversi CB1 selettivi che siano
incapaci di entrare nel cervello e quindi potenzialmente privi degli effetti indesiderati
centralimaancorautiliperiltrattamentodeidisordinimetabolici.66
Alcuni antagonisti competitivi dei recettori CB1 sono stati sviluppati in modo da essere
sprovvistidiqualsiasicapacitàrilevabilenell'indurresegnidiagonismoinversoalivellodei
recettoriCB1quandosomministratidasoli.Unesempiodiunantagonista,dettoantagonista
"neutro"èNESSO327,essoèunanalogostrutturalediRimonabantepresentaun’affinità
nettamentemaggioresuiCB1rispettoaiCB2.Questicompostipossonoesserepiùutilicome
“strumenti”farmacologici,rispettoagliagonistiinversi,inquantoproduconoeffettisoloin
presenzadielevatilivellidiendocannabioidi.
O
O
H
N
H
N
N
N
N
N
N
Cl
Cl
Cl
Cl
Cl
Cl
AM251
SR141716A
O
O
O
N
H
N
N
C N
N
N
O
O
O
Cl
I
O
Cl
LY320135
AM281
Figura20.Strutturachimicadialcuniantagonisti/agonistiinversiCB1selettivi.
Antagonisti/AgonistiinversiCB2selettivi
TraicompostipiùpotentichebloccanoirecettoriCB2rispettoaiCB1c’èAM630(Figura21).
Questocompostoèconsideratounagonistainversopiuttostocheantagonistaneutrodei
recettori CB2, perché quando somministrati da soli, possono produrre effetti
cannabinomimeticiinversineitessuticheesprimonoirecettoriCB2.63
OMe
O
N
I
N
O
AM630
Figura21.Strutturachimicadiunantagonista/agonistainversoCB2selettivi.
ModulatoriallostericideirecettoriCB1
Imodulatoriallostericisonocompostichelegandosialsitoallostericodelrecettorealterano
leproprietàdisegnalazionedelrecettorestessoedelligandoortosterico,modificandone
l’affinitàdilegame,l’efficaciaepotenzafunzionale.Rientranoinquestacategoria:
• Derivatiindolici:tracuiOrg27569(Figura22)cheèstatoilprimocompostocontali
proprietàadessereidentificato.67
Me
N
Cl
NH
N
H
O
Org27569
Figura22.StrutturachimicadiOrg27569.
• Derivatiureici:tracuiPSNCBAM-1(Figura23)chesicomportacomeunantagonista
allostericoneisaggiconAMPc.67
Cl
O
NH
N
NH
N
Figura23.StrutturachimicadiPSNCBAM-1.
• Modulatori allosterici endogeni del recettore CB1: (Figura 24) tra cui Lipoxin A4
coinvoltonellaregolazionedelsistemaimmunitarioepotentemediatoreendogeno
anti-infiammatorio;Pregnenolonesintetizzatoinvecedirettamentedalcolesterolo.67
Me
HO
OH
O
H
COOH
H
Me
H
HO
OH
Pregnenolone
Lipoxin A4
Figura24.StrutturachimicadialcunimodulatoriallostericiendogenidelrecettoreCB1.
• Modulatori allosterici misti del recettore CB1: appartiene a questa classe il
Cannabidiolo(CBD)chesicomportasiacomeunagonistadeirecettoriCB2checome
unNAMneiconfrontideiCB1(Figura25).67
CH 3
OH
HO
CBD
Figura25.StrutturachimicadelCBD.
Usiterapeutici
I cannabinoidi sono noti soprattutto per i loro effetti sulle funzioni del sistema nervoso
centrale. Essi producono euforia, alterazioni nella cognizione, analgesia, hanno proprietà
anticonvulsivanti, regolano la temperatura corporea, il sonno e l’appetito68 (Figura 26).
Tuttavia,icannabinoidipossiedonoancheattivitàimmunomodulanteeantiinfiammatoria.
Molte malattie del sistema nervoso centrale tra cui il morbo di Alzheimer, il morbo di
Parkinson,lasclerosimultiplaelademenzacoinvolgonoprocessiinfiammatori,causando
unasovraespressionedicitochineealtrimediatoridell’infiammazionenelsistemanervoso
centrale. Pertanto i cannabinoidi posso essere dei potenziali agenti terapeutici coinvolti
nellemalattieneurologiche.
Figura26.CoinvolgimentodelSEinalcunecondizionifisiopatologiche.
RuolodeirecettoriCBnellaNeuroprotezione
EvidenzesperimentalihannosuggeritounruolodeirecettoriCBnellaNeuroprotezione.La
barriera emato-encefalica (BEE) è un importante struttura del cervello, essenziale per la
neuroprotezione.ÈstatovistochelaBEEeicannabinoidicondividonoglistessimeccanismi
dineuroprotezione:irecettoriCB1proteggonodall’eccitotossicitàedallamortecellulare,i
recettori CB2 dall’infiammazione, quindi da tutti quei processi che danneggiano anche la
BEE. I recettori CB hanno dimostrato di migliorare l’integrità della BEE, in particolare
ripristinandolatenutadellegiunzionistrette,mac’èancoramoltaincertezzecircalecascate
di segnalazione sottostanti. Il meccanismo più studiato di neuroprotezione coinvolge gli
effetti antiinfiammatori del recettore CB2 che protegge il cervello impedendone la
neuroinfiammazione;mentreilrecettoreCB1èstatoimplicatonellaprotezionecontrola
mortecellulareindottadaunasovrastimolazioneeccitatoriadirecettori,accompagnatadal
rilasciodicalcio(eccitotossicità).69,70
Effettianti-emetici
La chemioterapia può indurre nausea e vomito, il trattamento inefficace di questi effetti
collaterali hanno spinto gli oncologi, alla fine del 1970 ad approfondire le proprietà
antiemetichedeicannabinoidi.71Ilprimoagonistacannabinoide,Nabilone(Cesamet),cheè
unanalogodelΔ9-THCvenneautorizzatonel1981perlasoppressionedellanauseaedel
vomitoindottidachemioterapia.Piùtardi,ancheDronabinol(sinteticodelΔ9-THC)èentrato
incommercio,comeMarinol,coneffettiantiemetici.
Stimolazionedell’appetito
Pazienti che soffrono di fasi avanzate di infezione da cancro o HIV subiscono spesso una
graveperditadipesoeappetito.Inoltre,incasodiAIDSecachessia(perditadipesoestremo)
questopuòessereaccompagnatodadiarreacronicaedebolezza.72Studicontrollatihanno
dimostratocheilTHCsomministratoperviaoralestimolal’appetitoerallentalaperditadi
pesocronicaneipazienticontumorieAIDS.SièvistocheiltrattamentoconDronabinol
tendeva a stabilizzare il peso. Marinol è stato infatti autorizzato come stimolante
dell’appetitonel1992.
Obesità
Il recettore CB1 sembra regolare l’attività dei neuroni dopaminergici nel sistema
mesolimbico, provocando la modulazione dei comportamenti edonistici mediati dalla
dopamina;interagisce,inoltre,conneuropeptidicomelamelanocortinaepeptidiintestinali
comelagrelinachestimolal’assunzionedicibo.73Èstatodocumentatochel’antagonismo
farmacologico selettivo del recettore CB1 migliora le “anomalie” dei lipidi associati
all’obesità. Dopo il buon risultato ottenuto in vari studi clinici, il più noto bloccante CB1,
SR141617A,anchechiamatoRimonabant(commercialmentenotocomeAcomplia)èstato
approvato in Europa nel 2006 per il trattamento dell’obesità, mentre non ha ricevuto
l’approvazionenegliStatiUnitieCanadapermotividisicurezza.Nonostanteisuoieffetti
positivi sul peso corporeo, l’Agenzia Europea per i Medicinali (EMEA) nel 2008 ha
raccomandato la sospensione di Rimonabant a causa degli effetti avversi riscontrati in
pazienti che ne fanno uso, come una maggiore incidenza al suicidio e di depressione.74
Rimonabant rimane comunque uno strumento sperimentale estremamente prezioso.
Quindi,c’èunurgentebisognodiunanuovastrategiachecondividal’efficaciariconosciuta
delRimonabantcontrol’obesità,ildiabeteditipoIIeneifattoridirischiocardiometabolici,
manonlasuaapparentecapacitàdiprodurresegnidiansia,depressioneetendenzesuicide
inalcunipazienti.Unapossibilesoluzioneaquestoproblema,cheèattualmenteoggettodi
studi, potrebbe essere quella di usare un Modulatore Allosterico Negativo che blocca
selettivamenteleazionimediatedelrecettoreCB1diunosolodegliendocannabinoidi.Così
facendosiandrebberoadeliminareglieffettipsicotropinegatividerivantidall’attivazione
delrecettoreCB1.
Doloreneuropatico
Èunaformadebilitantedidolorecronicoresistentealtrattamento,causatadaundannoal
sistemanervoso.Essopuòderivaredalesionideinerviperiferici,dastatidimalattiacomeil
diabete, dal virus dell’immunodeficienza umana (HIV) e dalla sclerosi multipla. Il dolore
neuropatico riamane un importante problema clinico perché risponde poco alle terapie
disponibili.Icannabinoidisonostativalutatiinstudicliniciperlasoppressionedeldolore
acutopostoperatorioeneuropatico.75
In Italia il primo farmaco a base di cannabinoidi approvato è stato il Sativex per il
trattamento della spasticità muscolare causata da sclerosi multipla nei pazienti che non
avevano riscontrato benefici da altri trattamenti per la spasticità o avevano riportato
eccessivieffetticollaterali.Sativexèunospraysub-lingualecontenentequantitàugualidi
THC e CBD, in cui CBD ha lo scopo di ridurre il metabolismo del THC prolungandone di
conseguenzal’emivita.