~-~~
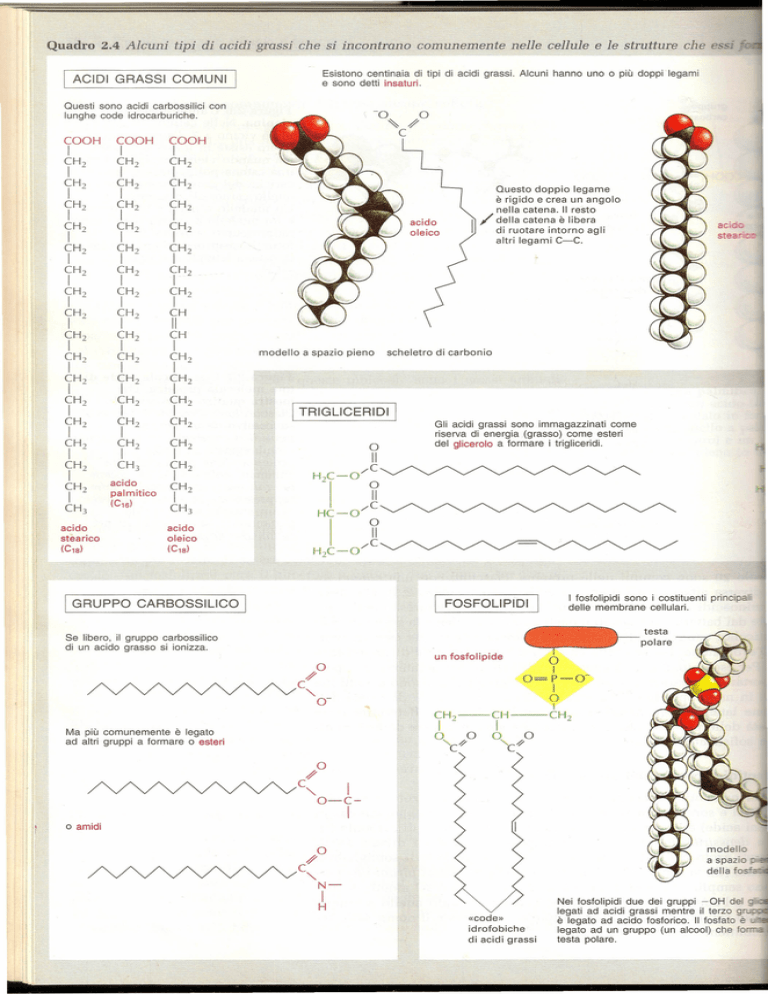
Quadro 2.4 Alcuni tipi di acidi grassi che si incontrano comunemente nelle cellule e le strutture che e si
I
Esistono centinaia di tipi di acidi grassi. Alcuni hanno uno o più doppi legami
e sono detti insaturi.
ACIDI GRASSI COMUNI
Questi sono acidi carbossilici
lunghe code idrocarburiche.
COOH
I
COOH
I
COOH
I
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH
CH2
CH2
CH
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH2
CH}
CH2
CH2
acido
palmitico
(C'6)
CH2
I
l
l
l
l
l
l
l
l
l
l
l
l
l
l
l
CH}
l
l
l
l
l
l
l
Questo doppio legame
è rigido e crea un angolo
nella catena. Il resto
della catena è libera
di ruotare intorno agli
altri legami C-C.
acic
stea--
l
l
l
l
l
l
l
l
l
l
I GRUPPO
/
l
l
acido
stèarico
(C, a)
con
l
l
Il
l
modello
a spazio pieno
scheletro
di carbonio
l
l
l
I TRIGLICERIDI I
Gli acidi grassi sono immagazzinati
come
riserva di energia (grasso) come esteri
del glicerolo a formare i trigliceridi.
l
l
l
l
CH}
acido
oleico
(C,a)
CARBOSSILICO
I
I fosfolipidi sono i costituenti
delle membrane cellulari.
I
FOSFOLIPIDI
@~
Se libero, il gruppo carbossilico
di un acido grasso si ionizza.
':')-----
principa,
testa
polare
O
un fosfolipide
I
O=p-OI
O
I
CH2--CH--CH2
l
Ma più comunemente
è legato
ad altri gruppi a formare o esteri
O
O
'C l'
/
l
O
O
'C l'
O
C"
O-C-
I
I
o amidi
«code»
idrofobiche
di acidi grassi
Nei fosfolipidi due dei gruppi -OH del _ legati ad acidi grassi mentre il terzo g
_
è legato ad acido fosforico. Il fosfato è
legato ad un gruppo (un alcool) che fOJr":C
testa polare.
-si formano
lIPIOICI
--
I
I POLISOPRENOIOI
una testa idrofilica
e una coda idrofobica.
!lO
lunghe catene
polimeriche di isoprene
-----f
~
0-
I
O=P-O-
I
In acqua possono formare un film
superficiale o formare piccole micelle.
acido
stearico
O
rcssono formare aggregati più grandi tenuti insieme da forze idrofobiche:
grosse gocce sferiche
asma delle cellule.
I fosfolipidi e i glicolipidi formano doppi strati lipidici
autosigillanti che sono la base di tutte le membrane cellulari.
:10
t
200 nm
o più
~
4nm ---I
I---
I lipidi sono definiti come le molecole delle cellule
insolubili in acqua ma solubili in solventi organici.
Due altri tipi comuni di lipidi sono gli steroidi
e gli isoprenoidi. Entrambi sono composti da unità
di isoprene.
CH3
'\
C-CH=CH2
,f'
CH2
Gli steroidi hanno una struttura comune ad anelli multipli.
::. cipali
isoprene
D
OH
O
-
erolo - si trova in molte membrane
testosterone
- ormone steroide maschile
=>1011
- idi, questi composti sono costituiti da una regione idrofobica,
::~e lunghe code idrocarburiche, e da una regione polare,
caso contiene uno o più residui di zuccheri e non fosfato.
H
OH
residuo
di zucchero
C-NH
I
regione idrofobica
Il
O
un glicolipide
semplice
dolicol fosfato - usato
per il trasporto di zuccheri
attivati nella sintesi
associata a membrane
di glicoproteine e di alcuni
polisaccaridi.
I
Quadro 2.5 I 20 amminoacidi coinvolti nella sintesi delle proteine
I
I GLI AMMINOACIDI
IISOMERI
La formula generale di un amminoacido
I~
gruppo~H
amminico
N
L'atomo di carbonio Ci. è asimmetrico,
l'esistenza di due isomeri speculari
(o stereoisomeri), D e L.
è
atomo di carbonio
il ct>=
Ci.
C-OOH
I
I
OTTICI
~
gruppo carbossilik--/
gruppo della
R
catena laterale
R è in genere una delle 20 diverse catene laterali.
A pH 7 sia il gruppo amminico che quello carbossilico
sono ionizzati.
H
@
I
I
8
H N-C-COO
2
R
'1
LEGAMI PEPTIDICI
Le proteine consistono
D
1
Gli amminoacidi sono uniti comunemente
chiamato legame peptidico.
esclusivamente
di L-amminoacidi.
legame peptidico: i quattro atomi di ciascun rettangolo grigio -_
una unità planare rigida. Non c'è alcuna libertà di rotazione al legame C-N
da un legame ammidico,
H20
H
H
-,
I
N-C-C
/
H
I
O
,/'
-,
R
-,
H
+
R
,/'
I
-,
N-C-C
/
OH
H
J
O
I
H
H
O
R
I
Il
I
N-C-C-N-C-C
I
/
OH
H
-,
H
R
I
I
H
H
O
,/'
-,
OH
SH
ammino o
N-terminale
Le proteine sono lunghi polimeri
di amminoacidi uniti da legami
peptidici e vengono sempre scritte
con l' N-terminale a sinistra.
La sequenza di questo tripeptide
è His Cys Val.
I
-,
H
+H
O
N-~-~-N-~-C-~-~-COO-
I
I
3
I
CH2
C
/
HN
V
CH2
H
~
DI AMMINOACIDI
Gli amminoacidi comuni sono
raggruppati secondo le caratteristiche
della loro catena laterale
acida
basica
polare priva di carica
non polare
1
I CATENE
Quindi: alanina = Ala = A
BASICHE
I
Il
O
I
/
CH
~
CH3
1
istidina
arginina
(Lvs, o K)
H
Questi 20 amminoacidi hanno
abbreviazioni sia a tre lettere
che a una lettera.
LATERALI
lisina
-N-C-C-
.>
Questi due legami singoli, su entrambi i lati dell'unita _rigida hanno un alto grado di libertà rotazionale.
I
HC=NH+
I FAMIGLIE
carbossi o
C-terminale
H
CH3
CH
I
H
H
O
I
Il
(His,
(Arg, o R)
H
-N-C-
I
I
H
CH2
I
CH2
I
CH2
I
CH2
I
NH3
+
0-
I
I
C
I
/C
HN
/~C=
molto basico
perché la sua
carica positiva
è stabilizzata
dalla risonanza.
Questi atomi di azoto un'affinità relativamente
per un H+ e sono s parzialmente positivi a ::-
I
LI ACIDE
I CATENE LATERALI NON POLARI I
acido glutammico
I
-C-
I
H
O
I
I
Il
alanina
I
(Ala,oA)
CH2
I
C
ç -,
O
I
- = His
= lIeu
o
ç
-c -,
= Lys
- = Leu
OH
H
O
I
Il
I
I
CH3
"
isoleucina
H
O
I
Il
H
O
I
Il
-N-C-C-
I
I
CH2
"I
"CH
/
CH
3
CH3
3
fenilalanina
(Pro, o P)
(Phe, o F)
H
O
H
O
I
Il
I
Il
I
-N-C-C-
'"
-.
/
CH2
glutammina
O
Il
-C-C-
H
O
I
Il
-N-C-C-
I
I
H CH,
I H2
\
\
istidina
His,
O
H
O
I
Il
n
(Trp, o W)
H
O
I
Il
H
O
I
Il
O
H
O
I
Il
I
Il
(Tyr, o Y)
-N-C-C-
I
H
: - e polare
8
-N-C-C-
I
1:-
I
CH
HC=NH+
\
I
I
H
CH2
oj
N
H
tirosina
H
I
I
I
CH2
I
I
CH
-N-C-C-
S-CH3
I
/C"'"
I-i
H
(Thr, o T)
CH2
2)'
triptofano
CH2
treonina
I
metionina
I
ç -,
O
NH2
ammidico non sia carico
_ è polare.
-C-C-
H
-N-C-C-
~
H)
I
CH2
(Met, o M)
CH2
I
C
/
-N-C-C-
CH2
(in realtà un
imminoacido)
(Gin, o Q)
I
H CH
/ 3
CH
CH2
I
=RALI POLARI PRIVE DI CARICA
I
H CH
/ 3
CH
CH3
CH
-nossi o
Il
-N-C-C-
prolina
:~rminale
O
I
(lIeu, o I)
H
S = Ser
T = Thr
V=Val
W=Trp
Y = Tyr
H
(Leu, o l)
I
M = Met
N =Asn
P=Pro
Q= Gin
R = Arg
G)
valina
-N-C-C-
"a in ordine alfabetico:
O
(Val, o V)
leucina
ca ene laterali polari prive di carica sono
-.e e sono in genere all'esterno delle proteine,
- . di amminoacidi non polari tendono
: il all'interno. Gli amminoacidi con catene
sono molto polari e sono quasi sempre
- e proteiche.
~ = Gly
(Gly,
-N-C-C-
0-
H
e
glicina
H
I
CH2
0-
Il
I
H
-N-C-CH
O
I
-N-C-C-
(Glu, o E)
O
H
,
H
I
L________ Y
OH
H
O
I
Il
-N-C-C-
I
I
H CH2
I
cisteina
(Cvs, o C)
SH
Cisteine appaiate permettono la formazione di legami disolfuro nelle proteine.
o
\I
C
HC/
~NH
HC~
/C~
Il u I
N
H
uracile
Le basi sono composti ad anello che contengono
azoto, o purine o pirimidine.
~O
: ,}
C
N~
(~~3J
N
N
PURINE
PIRIMIDINE
I
FOSFATI
D
I
I NUCLEOTIDI I
I fosfati sono normalmente uniti al gruppo
ossidrilico in C5 del ribosio o del deossiribosio.
Sono comuni i mono-, i di- e i trifosfati.
LEGAME FRA BASE
E ZUCCHERO
Un nucleotide consiste di una base contenente
azoto, uno zucchero a 5 atomi di carbonia
e uno o più gruppi fosfato.
legame
BASE
o
Il
-O-P-O-CH
I
I
o
O
0-
N91i'~
come
nell'AMP
~
Il
-O-P-O-P-O
I
Il
0-
o
O
O
Il
Il
I
I
I
0-
0-
o
Il
-O-P-O-CH
I
2
0-
4
o
0-
Il
-O-P-O-P-O-P-O
L-/
come
nell'ADP
I
0-
FOS:ATO
come
CH2 nell'ATP
I
OH
La base è legata
allo stesso atomo
di carbonio (C1) usato
nei legami zucchero-zu
OH
Sono le subunità
degli acidi nucleicl.
Il fosfato rende un nucleotide
carico negativamente.
D
I ZUCCHERI I
HOC~H
CS'
uno zucchero
a 5 atomi di carbonia
O
V=~
<:»
~"H"'~
~"H"'~
~-D-RIBOSIO
usato nell'acido
ribonucleico
se ne usano
due tipi
OH
OH
HO~H
~-D-2-DEOSSIR
usato nell'acido
deossiribonucle
Ciascun carbonio numerato dello zucchero di un nucleotide
è seguito da un segno primo ('); si parla quindi di «carbonio
5 primo» ecc.
OH
H
=
e
---__
TURA
I
l'
nomi possono
UCLEOSIDE
I
con ondere,
. . ..
ma le abbreviazìon!
I nucleotidi si abbreviano con
tre lettere maiuscole. Qualche
ABBR.
base
.
sono chiare.
esempio:
BASE + ZUCCHERO = NUCLEOSIDE
o
Il
/C
<,
"<,
~
NH
G I
~C
adenosina
A
guanosina
G
citidina
C
uridina
U
timidina
T
AMP
dAMP
UDP
ATP
= adenosina monoloslato
= deossiadenosina
monoloslato
= uridina diloslato
= adenosina triloslato
base
BASE + ZUCCHERO + FOSFATO = NUCLEOTIDE
N
D
~ FRA BASE
ERO
Il
- niti da un legame
~ gli atomi di carbonio 5' e
" nucleici. La sequenza
€O "di in un acido nucleico
cc-evìata nel codice ad una
_-----A-C-A,
con l'estremità 5'
. tra.
NUClEOTIDI
1
HANNO MOLTE ALTRE FUNZIONI
Trasportano
energia
chimica
O
nei loro legami
O
acido-anidride
facilmente
idrolizzabili.
O
Il
Il
Il
-O-P-O-P-O-P-O-CH
I
I
I
ico
I
0-
0-
esempio:
ATP (o
2
0-
IDI)
OH
OH
OH
2
Si combinano
H
H
O
con altri gruppi
H
H
O
per formare
H CH3 H
HS-~ -~ -N -~ -~ -~ -N -~ -~ .,
I
OH
H
I
H
I
H
I
H
I
H
esempio:
3
I
H
I
I
-~ -0-
I
HO CH3 H
coenzima
Sono usati come molecole
coenzimi.
O·
O
~-0-
~-O -C~
0-
0-
I
~NJN>
I
2
A (CoA)
segnale
O
OH
specifiche
all'interno
30SI0
-ell'acido
eico
NJ:N
OH
della cellula.
H2
3' O
<D
I
-O-p=O
I
I
O
esempio:
AMP ciclico
5' CH2
(cAMP)
O-~
O=P
3' OH
estremità
3' della catena
I
0-
N
O
OH
{