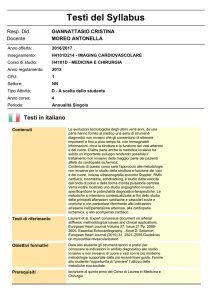
HEART FAILURE: “NEW DEFINITION”
Congestive heart failure represents a complex
clinical syndrome characterized by abnormalities of
left ventricular function and neurohumoral
regulation which are accompanied by effort
intolerance, fluid retention and reduced longevity
J Intern Med. 1996 239: 327-33.
HEART
FAILURE
REDUCED CARDIAC OUTPUT
ELEVATED CARDIAC
FILLING PRESSURE
RENIN
SYMPATHETIC NERVOUS
SYSTEM ACTIVATION
ANGIOTENSIN I
VASOCOSTRICTION
ANGIOTENSIN II
Na+ AND WATER
RETENTION
ALDOSTERONE
CARDIAC
REMODELLING
Goodman & Gilman’s, XI edition 2006
FARMACI UTILIZZATI NELLA TERAPIA DELLO
SCOMPENSO CARDIACO CONGESTIZIO
ACE inibitori
Antagonisti dei recettori AT1 della AII
β bloccanti (si inizia la terapia a dosi basse)
Antagonisti dell’aldosterone (spironolattone, eplerenone)
Diuretici (tiazidici prima, diuretici dell’ansa
nelle fasi avanzate)
Glicosidi cardioattivi (digossina)
Vasodilatatori
ACE-I
Benazepril
Captopril
Delapril
Enalapril
Fosinopril
Lisinopril
Quinapril
Ramipril
Zofenopril
Beta-bloccanti
Bisoprololo
Carvedilolo
Nebivololo
Antagonisti dei recettori
dell’aldosterone
Spironolattone
Canrenone
Eplerenone
ARBs
Candesartan
Valsartan
Losartan
Digossina
Vasodilatatori diretti e inodilatatori nelle forme acute
Diuretici
d’azione
a
diversa
intensità
HEART
FAILURE
Inotropic agents,
digoxin
REDUCED CARDIAC OUTPUT
digoxin
RENIN
β blockers
ANGIOTENSIN I
ELEVATED CARDIAC
FILLING PRESSURE
SYMPATHETIC NERVOUS
SYSTEM ACTIVATION
vasodilators
ACE inhibitors
VASOCOSTRICTION
ANGIOTENSIN II
Na+ AND WATER
RETENTION
AT1 receptor
antagonists
diuretics
ALDOSTERONE
eplerenone
CARDIAC
REMODELLING
Goodman & Gilman’s, XI edition 2006
A review of heart failure treatment.
Guyatt GH, Devereaux PJ. Mt Sinai J Med. 2004
Heart failure is a common and costly medical condition. Ischemic heart
disease and hypertension account for most cases of heart failure in
developed countries. Estimates of the one-year mortality rates for patients
with New York Heart Association (NYHA) Class II, III, and IV are 10%,
20%, and 40%, respectively.
Angiotensin-converting enzyme (ACE) inhibitors reduce mortality of
heart failure patients by approximately 25% (odds ratio 0.77, 95% CI 0.67
0.88). Larger doses of ACE inhibitors are more effective in preventing
hospitalization than are lower doses.
Angiotensin II receptor blockers (ARBs) are an alternative for patients
who cannot tolerate ACE inhibitors because of their side effects (e.g.,
cough). Evidence for benefits of using combination of ACE inhibitors and
ARBs is encouraging, but requires further study. For patients who cannot
tolerate either ACE inhibitors or ARBs, vasodilator therapy with
hydralazine and nitrates will probably provide benefit.
Diuretic therapy, while a mainstay of heart failure treatment, is primarily
used for symptom relief. There is also evidence that spironolactone
reduces mortality (relative risk reduction 30%, 95% CI 18 40%) for patients
with NYHA class III and IV heart failure.
When administering spironolactone to heart failure patients, monitoring for
hyperkalemia is essential.
After two centuries of use, randomized controlled trials have finally
demonstrated that digoxin is effective in preventing hospitalizations
(relative risk reduction 28%, 95% CI 21 34%).
There is now overwhelming evidence that β-blockers are safe for heart
failure patients but that they reduce the risk of death for these patients by
approximately 30%.
Inoltre sono fondamentali nella terapia farmacologica dello scompenso cardiaco
i farmaci anticoagulanti e/o antiaggreganti, le statine e gli ipoglicemizzanti:
TERAPIA ANTIAGGREGANTE
ASPIRINA
in tutti coloro con patologia cardiovascolare accertata (inclusi i diabetici): è
raccomandato un trattamento cronico con 75-150 mg/die di aspirina
in soggetti asintomatici con SCORE > 10% ed in trattamento antiipertensivo
efficace
CLOPIDOGREL
in soggetti intolleranti all’aspirina
in aggiunta all’aspirina nelle sindromi acute coronariche per 9-12 mesi
TERAPIA ANTICOAGULANTE
WARFARIN o ACENOCUMAROLO
in pazienti a rischio tromboembolico
in pazienti con fibrillazione atriale
Eur Heart J 2007, 28: 2375
Beta-blocking agents are now, in conjunction with ACE inhibitors, the
cornerstone of treatment for HF (CIBIS II 1999; COPERNICUS 2002;MERITHF 1999; SENIORS 2005).
Also of note are findings that the aldosterone inhibitors spironolactone
(RALES 1999) and eplerenone (Zannad 2011) and the angiotensin receptor
blockers valsartan (Cohn 2001) and candesartan (CHARM 2003) have
beneficial long-term effects in HF.
All of these agents appear to be effective in groups of participants with
substantial levels of digoxin usage: 73%in the spironolactone trial (RALES
1999), 27%in the eplerenone study (Zannad 2011), 67% in the valsartan trial
(Cohn 2001), 43% in the candesartan trial (CHARM 2003), and more than
50% in some beta-blocker trials (CIBIS II 1999; Packer 2001), with
demonstrable continuing effectiveness in participants already receiving
digitalis.
ANTAGONISTI DEI RECETTORI PER L’ALDOSTERONE
Role of aldosterone in cardiovascular disease
Structure
of
the
selective
aldosterone-receptor
antagonist
eplerenone.
The
9,11-epoxy
group
gives
eplerenone
its
improved
selectivity
over
spironolactone
In addition to classical effects (red) that raise blood pressure, such as
promoting sodium and water retention, which are mediated through
the action of aldosterone on its receptors in the kidney, aldosterone
also has deleterious effects (grey) thought to be mediated through its
actions on receptors in the heart, blood vessels and brain.
NEJM, 2003
β-BLOCCANTI
I primi studi che hanno dimostrato l’efficacia di diversi β-bloccanti nello
scompenso cardiaco di entità lieve-moderata:
Carvedilolo:
The Effect of Carvedilol on Morbidity and Mortality in Patients with Chronic Heart
Failure. NEJM 334:1349-1355, 1996
Bisoprololo: The Cardiac Insufficiency Bisoprolol Study II (CIBIS-II): a randomised trial. Lancet. 353:
9-13, 1999
Metoprololo:
Effect of metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomised
Intervention Trial in Congestive Heart Failure (MERIT-HF). Lancet 353: 2001-7, 1999.
L’efficacia del carvedilolo è stata confermata anche in soggetti con scompenso
cardiaco di grado severo: Effect of carvedilol on survival in severe chronic heart failure. NEJM
344:1651-8, 2001.
Recentemente è stato dimostrato che il nebivololo è efficace nello scompenso
cardiaco: Data From SENIORS (Study of Effects of Nebivolol Intervention on Outcomes and
Rehospitalization in Seniors With Heart Failure): Beta-Blockade With Nebivolol in Elderly Heart Failure
Patients With Impaired and Preserved Left Ventricular Ejection Fraction. J Am Coll Cardiol 53:2150–8,
2009
Lo studio SENIORS ha documentato l’efficacia e la buona tollerabilità del
nebivololo anche negli anziani
The main finding of the present study is that
the effect of the b-blocker nebivolol seemed to
be of similar magnitude between HF patients
with impaired EF and patients with preserved
EF.
Although the SENIORS trial was not powered
to show a statistically significant effect of
nebivolol in the EF subgroups, the HRs are
similar with no apparent evidence of interaction
in any subgroup analysis, which supports the
hypothesis that there is a similar beneficial
effect in patients with impaired and preserved
EF.
The current study provides the first largescale data for a potentially beneficial effect of bblockade in HF patients with a preserved EF,
and is the only one in elderly HF patients.
Time-dependent effects of metoprolol on left ventricular ejection fraction
in patients with heart failure.
The improvement in function with
chronic therapy cannot be attributed
to a direct hemodynamic effect, and
likely reflects a beneficial effect of
treatment on the biology of the
myocardium.
In patients with severe left ventricular dysfunction, the initial administration of a low
dose of metoprolol caused an immediate depression in ejection fraction (day 1).
However, over time and despite uptitration of metoprolol to full therapeutic levels,
ejection fraction returned to baseline (1 month), and by 3 months was significantly
higher than at baseline. In the group given standard therapy, ejection fraction did
not change significantly.
Dose-dependent effect of carvedilol on left ventricular ejection fraction
In the U.S. Carvedilol Trials Program, a subgroup of patients were randomized to
placebo or carvedilol in the standard dose (25 mg twice per day bid), or in a
reduced dose of 12.5 or 6.25 mg twice per day. After 6 months of treatment, left
ventricular ejection fraction increased with all 3 doses of carvedilol, but not with
placebo.
The increase in ejection fraction was strongly related to the dose of carvedilol.
These data emphasize the importance of titrating doses of b receptor antagonists
to the target or the highest tolerated dose.
L’attivazione simpatica è stata considerata come
una delle principali cause di declino progressivo della funzione
cardiaca e di prognosi infausta del paziente scompensato
Il blocco degli “effetti cardiotossici” delle catecolamine ad opera dei β bloccanti si
manifesta con
Attività anti-ipertensiva
Attività anti-ischemica
Riduzione liberazione di renina
Aumento della struttura e funzione ventricolari per:
riduzione frequenza, prolungamento del riempimento diastolico e del tempo di
perfusione coronarica
Ridotta richiesta d’ossigeno
Miglioramento metabolico per inibizione della lipolisi
Up-regulation dei recettori β e loro “risensitizzazione”
Ridotto stress ossidativo
Azioni antiaritmiche
GLICOSIDI CARDIOATTIVI
DIGOSSINA
anello lattonico
insaturo
O
O
CH3
CH3
residui glicosidici
CH3
O
CH3
O
CH3
O
La prima pubblicazione sull’uso dei glicosidi cardioattivi
nella terapia dello scompenso risale al 1785 ad opera di W.
Withering: ”An account of the foxglove and some of its
medical uses: with pratical remarks on dropsy, and other
diseases”.
anello lattonico
insaturo
O
O
CH3
CH3
tevezia (oleandro giallo)
mughetto
residui glicosidici
CH3
O
oleandro
digitalis purpurea
GALENO:
Tutti coloro che bevono questo
rimedio
staranno
rapidamente
meglio, eccetto coloro nei quali non
è efficace, che moriranno
CH3
O
CH3
O
La prima pubblicazione sull’uso dei glicosidi cardioattivi
nella terapia dello scompenso risale al 1785 ad opera di W.
Withering: ”An account of the foxglove and some of its
medical uses: with pratical remarks on dropsy, and other
diseases”.
Ricordati che il miglior medico è la
natura: guarisce i due terzi delle malattie
e non parla male dei colleghi.
Sarcolemmal exchange of Na+ and Ca 2+ during cell
depolarization and repolarization
• Na+ and Ca2+ enter the cardiac myocyte via the
Na+ channel and the L-type Ca2+ channel during
each cycle of membrane depolarization, triggering
the release, through the ryanodine receptor (RyR),
of larger amounts of Ca2+ from internal stores in the
sarcoplasmic reticulum (SR).
• The resulting increase in intracellular Ca2+
interacts with troponin C and activates
interactions between actin and myosin. The
electrochemical gradient for Na+ across the
sarcolemma is maintained by active transport of Na+
out of the cell by the Na+,K+-ATPase.
•The bulk of cytosolic Ca2+ is pumped back into
the SR by a Ca2+-ATPase, SERCA2. The remainder
is removed from the cell by either a sarcolemmal
Ca2+-ATPase or a high capacity Na+-Ca2+
exchange protein, NCX.
REGOLAZIONE FISIOLOGICA DELL’INGRESSO
DI CA++ NELLA MIOCELLULA CARDIACA
Harvey e Champe, Zanichelli ed.
Meccanismo d’azione della digitale
Esistono diverse isoforme a
bassa affinità : a1
ad alta affinità: a2
a livello delle fibre di
conduzione è stata isolata una
terza isoforma: a3
Harvey e Champe, Zanichelli ed.
La digossina si lega preferenzialmente alla forma fosforilata della pompa.
Un’elevata [K+] extracellulare favorisce la defosforilazione della subunità α
L’affinità della digitale per la ATPasi Na+/K+
è quindi fortemente aumentata dalla riduzione di [K+] extracellulare
EFFETTI CARDIOVASCOLARI
EFFETTI DIRETTI
• ATTIVITA’ INOTROPA POSITIVA
• STIMOLAZIONE DELL’ATTIVITA’ ELETTRICA (con un meccanismo
non ancora completamente noto)
• CONTRAZIONE
DELLA
MUSCOLATURA
LISCIA
DELLE
ARTERIOLE
EFFETTI INDIRETTI
• ATTIVITA’ ELETTRICA sui nodi SA e AV
• RISPOSTE RIFLESSE del sistema simpatico e del sistema endocrino
EFFTTO DELLA DIGITALE SUL POTENZIALE D’AZIONE
IN UNA CELLULA DI PURKINJE
20
+
0
-
50
POSTDEPOLARIZZAZIONE
RITARDATA
Na+ K+ Ca++ Ca++ Ca++
100
Na+ K+
• riduzione della durata del PA
• aumenta la pendenza della fase 2
• aumenta la pendenza della fase 4
Effetto della digitale a concentrazioni terapeutiche nell’ECG
Si possono osservare diverse modificazioni:
- La più precoce è a carico dell’onda T, che
può subire diverse modifiche: dall’appiattimento
all’inversione (che può simulare un attacco
ischemico o una pericardite), sia la comparsa di
onde T anomale, per esempio con un picco nella
parte terminale (in circa il 10% dei pz)
- Accorciamento del tratto Q-T, per la riduzione
-del tempo di ripolarizzazione ventricolare
-Comparsa di una depressione del
segmento ST, con formazione di una curva tipica
- Comparsa talvolta di aumento dell’onda U
EFFETTI DIRETTI SULL’ATTIVITA’ ELETTRICA
Le osservazioni sono state fatte sulle fibre del Purkinje:
A dosi terapeutiche:
Diminuzione della durata del PA, soprattutto a causa
dell’accorciamento della fase 2 (plateau).
Aumento della pendenza della depolarizzazione della
fase 4.
La salita del potenziale d’azione
(fase 0) inizia da un potenziale meno negativo
AUMENTO DELL’AUTOMATICITA’
EFFETTI INDIRETTI
SISTEMA COLINERGICO VAGALE
EFFETTO BRADICARDIZZANTE
• per aumento degli impulsi vagali efferenti
• diminuzione della sensibilità delle fibre di conduzione agli impulsi
simpatici
• diminuzione dell’attivazione riflessa del simpatico
L’aumento dell’attività vagale sembra essere il risultato di una
interazione del farmaco a vari livelli del sistema nervoso:
sensibilizzazione dei barocettori arteriosi
aumento dell’attività afferente nei nervi del seno carotideo
aumento dell’eccitabilità delle fibre efferenti del ganglio nodoso e dei
nuclei vagali centrali
SISTEMA SIMPATICO CATECOLAMINERGICO
Nei nodi SA e AV, dosi terapeutiche di digitale determinano una
diminuzione della sensibilità alle catecolamine.
Inoltre, il miglioramento delle condizioni emodinamiche determina
una riduzione dell’attività simpatica ed una diminuzione della sintesi
di renina.
ATTENZIONE:
un’intossicazione
digitalica
determina
un
potenziamento dell’attività efferente simpatica, probabilmente per
attivazione dell’AREA POSTREMA del midollo allungato.
EFFETTI ELETTRICI SUL CUORE
bilancio fra effetti diretti ed indiretti
FIBRE ATRIALI
Si hanno effetti DIRETTI ed INDIRETTI con attività opposta. A concentrazioni
terapeutiche prevalgono gli effetti indiretti vagali
NODO SA
E’ direttamente sotto il controllo del vago e quindi prevalgono gli effetti indiretti (effetto
cronotropo negativo)
NODO AV
E’ sensibile agli effetti indiretti vagali. L’acetilcolina provoca un certo grado di
iperpolarizzazione delle cellule del nodo e quindi viene ridotta l’ampiezza e la velocità di
formazione del potenziale d’azione.
Il periodo refrattario risulta notevolmente allungato, può portare anche a blocco AV.
SISTEMA DI HIS
Non è molto sensibile al vago e più sensibile al sistema simpatico, quindi:
diminuzione della velocità di conduzione per diminuzione della sensibilità alle
catecolamine.
FIBRE VENTRICOLARI
A dosi terapeutiche non si hanno modificazioni significative.
A dosi tossiche si possono avere aritmie fino a fibrillazioni ventricolari.
FARMACOCINETICA
dose digitalizzante
os
e.v.
dose di mantenimento
os
e.v.
DIGOSSINA
DIGITOSSINA
0.75-1.25 mg
0.5-1 mg
0. 8-1.2mg
non usata
0.125-0.5 mg (sembra ottimale
0. 05-0.3mg
una dose attorno a 0.,125 mg/die)
0.25 mg
assorbimento intestinale
< 40-100% (75%)
90-100%
legame alle proteine
plasmatiche
25%
95%
emivita
1.6 giorni
7 giorni
via di eliminazione
escrezione renale del
farmaco immodificato
metabolismo epatico
escrezione renale
concentrazione plasmatica
efficace
0.5-2 ng/ml
10-30 ng/ml
EFFETTI COLLATERALI
delirio, alterazione dei sogni
affaticamento, confusione, astenia
alterazione della visione dei colori
nausea, vomito, dolore addominale
effetti proaritmogeni fino a fibrillazione ventricolare
ATTENZIONE ALLE INTERAZIONI
CON ALTRI FARMACI
ATTENZIONE ALLA
IPOPOTASSIEMIA, soprattutto per
concomitante somministrazione di
diuretici
INTOSSICAZIONE DIGITALICA
INTOSSICAZIONE ACUTA
Nausea e vomito sono prevalenti rispetto alla tossicità
cardiaca. Si possono osservare aritmie (tachicardia) in
genere non gravi
INTOSSICAZIONE CRONICA
predominano sintomi non specifici, quali astenia,
alterazione della visione dei colori, ma soprattutto ARITMIE
GRAVI
INTOSSICAZIONE DIGITALICA
The difficulty in diagnosing patients with digitalis intoxication
can be attributed to several factors:
- signs, symptoms and electrocardiogram manifestations
often can be attributed to the underlying disease process for
which the drug is prescribed;
- a narrow therapeutic window of digoxin resulting in marked
variability in the sensitivity of individuals to the drug;
- the lack of any dysrhythmia diagnostic of toxicity.
It is believed that chronic toxicity occurs in 4–10% of patients
on digitalis, yet is suspected in only 0.25% of the cases.
The Journal of Emergency Medicine, 2001
MODIFICAZIONI DELL’ECG DA INTOSSICAZIONE DIGITALICA:
- Depressione marcata del tratto ST
- Curva T piatta, negativa o bifasica
- Accorciamento dell’intervallo QT
- Aumento di ampiezza dell’onda U
- Prolungamento dell’intervallo P-R
Alterazioni del ritmo:
Bradiaritmie
Bradicardia sinusale
Blocchi AV
Tachiaritmie
Tachicardia giunzionale
Tachicardia atriale
Ectopie ventricolari
Tachicardia ventricolare
Contrazioni
Ventricolari
premature
Tachicardia parossistica
atriale
The results of the present meta-analyses further strengthen the concept that
digoxin has beneficial effects in treating patients with CHF who remain symptomatic
despite therapy with ACE-I, β-blockers, and diuretics, and has both clinical efficacy
and the ability to reduce hospitalizations.
Although some authors have stated that the agent is of limited value, adequate
control of symptoms in patients with CHF may be difficult to achieve through use of
diuretics, ACE-I, and b-blockers alone, and additional clinical gains can often be
made by adding digitalis to the regimen.
The significant rise in other cardiac deaths possibly due to arrhythmias warrants
cautious use in patients at risk for such events.
La digossina riduce la mortalità ad 1 anno e
l’ospedalizzazione
nei
pazienti
con
insufficienza cardiaca cronica, in terapia con
ACE inibitori e diuretici, indipendentemente
dalla digossinemia. Am J Cardiol. 103(1):82-7, 2009
La
digossina
riduce
l’
ospedalizzazione a due anni dei
pazienti con scompenso cardiaco,
sia sistolico che diastolico. Am J Cardiol.
102:1681-6, 2008
IVABRADINA
Capostipite di una nuova classe di farmaci anti-ischemici con meccanismo d’azione
innovativo. Lo sviluppo del farmaco deriva da una scoperta italiana che ha identificato a
livello cardiaco i canali If responsabili della modulazione della frequenza cardiaca
Ivabradine exerts its effect by inhibiting an important pacemaker current (If) in the
sinoatrial node [6–9]. Ivabradine produces dose-dependent reductions in heart rate in
experimental animals [10–13] and healthy volunteers [14] and in patients with chronic
stable angina [15]. In conscious dogs, ivabradine reduces heart rate without any negative
inotropic effect, both at rest and during treadmill exercise [13]. Cardiology 2003;100:149–155
Trattamento della coronaropatia
Trattamento sintomatico dell’angina pectoris cronica stabile negli
adulti con coronaropatia e normale ritmo sinusale. Ivabradina è
indicata:
• negli adulti che non sono in grado di tollerare o che hanno una
contro–indicazione all’uso dei beta–bloccanti
• o in associazione ai beta–bloccanti nei pazienti non
adeguatamente controllati con una dose ottimale di beta–bloccante
e
la
cui
frequenza
cardiaca
sia
>
60
bpm
Trattamento dell’insufficienza cardiaca cronica
Ivabradina è indicata nell’insufficienza cardiaca cronica in classe
NYHA da II a IV con disfunzione sistolica, in pazienti con ritmo
sinusale e la cui frequenza cardiaca sia ≥ 75 bpm, in associazione
con la terapia convenzionale che include il trattamento con un beta–
bloccante o nel caso in cui la terapia con un beta–bloccante sia
controindicata o non tollerata (vedere paragrafo 5.1).
Trattamento della coronaropatia
La dose iniziale abituale raccomandata di ivabradina è di 5 mg due volte al
giorno. Dopo 3-4 settimane di trattamento, la dose può essere aumentata a
7,5 mg due volte al giorno in funzione della risposta terapeutica.
Se, durante il trattamento, la frequenza cardiaca a riposo si riduce in modo
persistente al di sotto di 50 battiti al minuto (bpm) oppure se il paziente riferisce
sintomi collegati a bradicardia come capogiro, affaticamento o ipotensione, il
dosaggio deve essere ridotto, considerando anche la possibile dose di 2,5 mg
due volte al giorno .
Il trattamento deve essere interrotto se la frequenza cardiaca si mantiene sotto
i 50 bpm oppure se persistono i sintomi di bradicardia
Trattamento dell’insufficienza cardiaca cronica
Il trattamento deve essere iniziato solo nei pazienti con insufficienza cardiaca
stabile.
La dose iniziale abituale raccomandata di ivabradina è di 5 mg due volte al
giorno. Dopo due settimane di trattamento, la dose può essere aumentata a 7,5
mg due volte al giorno, se la frequenza cardiaca a riposo si mantiene
continuativamente sopra i 60 bpm, o diminuita a 2,5 mg due volte al giorno se
la frequenza cardiaca a riposo si mantiene continuativamente sotto i 50 bpm o
in caso di sintomi correlati a bradicardia quali capogiro, affaticamento o
ipotensione. Se la frequenza cardiaca è compresa tra 50 e 60 bpm, si deve
mantenere la dose di 5 mg due volte al giorno.
IVABRADINA - FARMACOCINETICA
Assorbimento: L’ivabradina è rapidamente e quasi completamente assorbita dopo
somministrazione orale con un picco plasmatico raggiunto in circa un’ora, in
condizioni di digiuno.
Presenta un elevato effetto di I passaggio
Distribuzione: si lega alle proteine plasmatiche per circa il 70%.
Metabolismo: Esteso metabolismo epatico ed intestinale per azione del CYP3A4. Il
principale metabolita attivo è il derivato N–demetilato (S18982), con una
concentrazione di circa il 40% di quella della molecola madre. Anche il metabolismo di
questo metabolita attivo coinvolge il CYP3A4.
L’ivabradina ha una bassa affinità per il CYP3A4, non mostra induzione o inibizione
clinicamente rilevante del CYP3A4 ed è perciò improbabile che modifichi il
metabolismo o le concentrazioni plasmatiche di substrati del CYP3A4. Al contrario,
potenti inibitori ed induttori possono modificare sostanzialmente le concentrazioni
plasmatiche dell’ivabradina.
Eliminazione: ha un’emivita di circa 11 ore. L’escrezione dei metaboliti avviene in parti
uguali con le feci e le urine. Circa il 4% di una dose orale è escreto immodificato nelle
urine
PRINCIPALI EFFETTI COLLATERALI
Bradicardia
Cefalea (soprattutto nei primi 2 mesi)
Disturbi visivi
fenomeni luminosi (fosfeni), descritti come una aumentata luminosità
transitoria in un'area limitata del campo visivo5.
I fosfeni si sono manifestati generalmente entro i primi 2 mesi di terapia e
nella maggioranza dei casi (76%) si sono risolti durante il trattamento.
In animali trattati con ivabradina sono state osservate variazioni reversibili
della funzione retinica, da attribuire alla interazione del farmaco con la
corrente Ih attivata per iperpolarizzazione, presente nella retina, omologa
con la corrente pacemaker cardiaca If.
TRATTAMENTO DELLO SCOMPENSO ACUTO
Pz scompensato ricoverato per ritenzione di fluidi:
I sintomi prevalenti sono dispnea ed edemi periferici
Trattamento farmacologico con:
DIURETICI i.v.
VASODILATATORI diretti (nitroprussiato e.v.
nitrati organici)
Pz scompensato ricoverato per ridotta gittata cardiaca: (fase molto
avanzata della malattia)
I sintomi prevalenti sono astenia, alterazione dello stato di veglia,
azotemia
Trattamento farmacologico con:
FARMACI INOTROPI POSITIVI i.v.
Dopamina
Dobutamina
Inibitori delle fosfodiesterasi: Inamrinone e Milrinone
FARMACI INOTROPI POSITIVI: DOPAMINA
Effetto sul rene: effetto diuretico
e natriuretico
Effetto sui vasi: vasodilatazione per azione dei recettori D1,
sono particolarmente sensibili i vasi renali, mesenterici e coronarici
Dopamina in infusione continua viene utilizzata nel trattamento dello
scompenso acuto e induce:
A basse dosi: fino a 2 µg/kg/min (azione solo sui recettori DAergici)
Aumento della velocità di filtrazione glomerulare
Aumento del flusso ematico renale
Aumento dell’escrezione di Na+
A dosi più elevate: 2-5 µg/kg/min
Effetto inotropo positivo diretto per attivazione dei recettori β
cardiaci
A dosi alte: 5-15 µg/kg/min
Vasocostrizione per attivazione dei recettori α
FARMACI INOTROPI POSITIVI: DOBUTAMINA
La dobutamina è strutturalmente simile alla dopamina,
ma non interagisce con i recettori dopaminergici.
E’ un agonista dei recettori α e β.
La sua struttura chimica è importante in quanto l’isomero L è un
antagonista dei recettori α, mentre l’isomero D è un agonista.
Per quanto riguarda i recettori β, entrambi gli isomeri sono agonisti,
anche se l’isomero D è circa 10 volte più potente dell’isomero L.
In clinica viene usata la forma racemica e gli effetti terapeutici sono il
complesso risultato dell’interazione della dobutamina con entrambi i
recettori adrenergici.
Per un meccanismo d’azione non ancora completamente chiarito,
l’infusione di dobutamina induce prevalentemente un effetto inotropo
positivo, piuttosto che cronotropo positivo.
Le resistenze periferiche vengono poco modificate,
probabilmente per un bilancio fra l’effetto di
vasocostrizione
(recettori
α)
e
quello
di
vasodilatazione (recettori β).
La dobutamina ha un’emivita di circa 2 minuti e
quindi deve essere somministrata in infusione
continua: 2-3 mg/kg/min.
E’ indicata, come la dopamina, per il trattamento a
breve termine di uno scompenso cardiaco acuto.
FARMACI INODILATATORI:
INIBITORI DELLE FOSFODIESTERASI
Non in commercio in Italia
Inamrinone (Amrinone)
Milrinone (25-75 µg/kg in 10’-20’)
A livello cardiaco: cAMP
intracellulare favorisce la
contrattilità, inducendo un
effetto inotropo positivo
A livello periferico: cAMP
induce vasodilatazione dei
vasi di resistenza e di
capacitanza, riduzione del
pre-carico e del postcarico
Judy Cheng, 2006