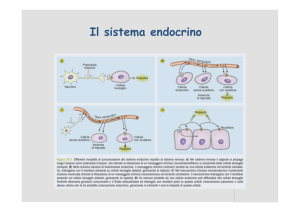
Sistema Endocrino
concetti generali
OMEOSTASI
• Nel 1929, Walter Cannon coniò il
termine omeostasi (= la tendenza
dell’organismo a mantenere lo
Stato Stazionario)
• Studiò:
– Effetti dello stress e degli stimoli
emozionali sui processi digestivi
– La funzione di emergenza delle
ghiandole surrenali nel
controbilanciare condizioni
stressorie
Walter B. Cannon
1871-1945
Cannon, W.B. The Wisdom of the Body, New York, W.W. Norton and Co., 1932
Comunicazione, Integrazione e
Omeostasi
• neuronale (elettrica, tranne il segnale chimico nelle
sinapsi)
• endocrina/immunitaria (chimica, tranne l’eccitabilità
elettrica delle cellule)
Queste categorie non si escludono né divergono, ma
sono rappresentative di un continuum.
I sistemi di controllo chimico
secrezione
mediatore
chimico
recettore e
trasduzione
Messaggio
intracellulare
VARIABILE
CONTROLLATA
recettore e
trasduzione
Cellula Endocrina
TARGET
Messaggio
intracellulare
RISPOSTA
NEURONE
neurotrasmettitore
Anatomia
delle
ghiandole
endocrine
Ghiandole
e
Secrezioni
Cellule e Ghiandole Endocrine
• Ormoni nel sangue.
• Ghiandole singole.
– Tiroide, Ipofisi, Surreni
• In altre ghiandole
– Isole di Langerhans nel Pancreas.
• Cellule singole (Sistema Neuroendocrino
Diffuso)
– Cellule Enteroendocrine (APUD) sparse lungo il
tratto digerente e respiratorio.
Organi con porzioni endocrine
• Cuore
(cellule specializzate parete
atriale e setto interventricolare)
•
•
•
•
Rene (Apparato Iuxta Glomerulare)
Testicoli (Cellule di Leydig)
Ovaio (Cellule della granulosa)
Placenta
Ghiandole
Endocrine
Ipofisi
• Anteriore
– Adenoipofisi
– Pars anteriore
• Posteriore
– Neuroipofisi
– Pars nervosa
• Intermedia
– Pars intermedia
IPOTALAMO
PEDUNCOLO
CHIASMA
OTTICO
Ipofisi Anteriore
• Struttra tipica
ghiandole
endocrine di
origine epiteliale.
• Cellule attive
– Cromofile (A e B)
• Cellule inattive
– Cromofobe (C)
• Acidofile
– Somatotrope circa la
metà delle cellule dell’AI.
Ormone della crescita-GH
– Mammotrope/Lattotrope
circa il 20%, aumentano
in gravidanza. Prolattina
Ipofisi
Anteriore
• Basofile
– Corticotrope circa il 20%.
Corticotropina-ACTH
– Tireotrope circa il 5%.
Tireotropina-TSH
– Gonadotrope circa il 5%.
Gonadotropine-Ormone
luteinizzante LH,Ormone
follicolo stimolante FSH
Capillari
Fenestrati
Ipofisi Posteriore
• Assoni non mielinati delle
cellule neurosecretorie
– OSSITOCINA
– VASOPRESSINA
– Corpi cellulari sono
nell’ipotalamo
• Pituiciti
– Circondano gli assoni,
simili per struttura e
funzione alle neurogliali
del SNC.
• Capillari piccoli e
fenestrati
Pancreas esocrino
200x
450x
Isolotti di Langerhans
• Aggregati di cellule
– Colorazione più chiara delle
cellule acinari
– Fino a 3000 cellule
• Cellule Alfa, Beta e Delta
– Secernono glucagone,
insulina e somatostatina
rispettivamente
• I capillari decorrono
all’interno dell’isolotto
Ghiandola surrenale
12x
Ghiandole
Surrenali
• Corticale
– Glomerulare,
Fascicolata, Reticolare
– Mineralcorticoidi,
Glucocorticoidi,
Androgeni
• Midollare
– Adrenalina e
Noradrenalina
– Origine Neuroectoderma
Zona glomerulare
Zona fascicolata
Zona reticolare
Midollare
20x
Zona glomerulare
• Gruppi di cellule con nuclei
grandi e densi
• Abbondante sER
• Mineralcorticoidi
• Aldosterone
– Regola il sistema reninaangiotensina nel rene
128x
Zona Fascicolata
• Cellule chiare organizzate in fasci
– Spongiociti
• Citoplasma appare vacuolato perché
ricco gocce lipidiche
• sER, Mitocondri sferici
• Ormoni glicocorticoidi
– Cortisolo, sotto controllo Ipotalamo
– Metabolismo dei carboidrati
– Piccole quantità di ormoni sessuali,
androgeni
Zona Reticolare
• Cordoni di cellule che
formano una rete.
• Secernono androgeni
• Meno lipidi che nella
fascicolata più colore.
• Mitocondri allungati con
meno creste tubulari.
• Granuli di Lipofuscina
• Spessore varia a
seconda delle condizioni
fisiologiche.
Caratteristiche delle cellule
secernenti steroidi zona reticolare
1. Colesterolo
accumulato in gocce
lipidiche
2. Abbondante Reticolo
Endoplasmatico liscio
3.Mitocondri particolari
• creste tubolari
• sferici
Midollare del Surrene
• Cellule cromaffini
Granuli che si colorano di
giallo-marrone
• Sali di cromo
• Citoplasma granulare
• Basofilo
• Secernono
Adrenalina e
Noradrenalina
198x
Tiroide
12x
Tiroide
• Strutturata in follicoli
– Ormoni accumulati
all’interno
• Secernono T3, T4
• Tiroglobulina aiuta
accumulo ormoni
• Cellule Parafollicolari
– Cellule chiare
– Secernono
calcitonina
240x
Follicoli Tiroidei
Tiroide
• Dimensione delle
cellule varia a
seconda dello stadio
funzionale
• rER
• Eso- ed endocitosi
Ghiandola in attivita’
670x
Cellule parafollicolari C
480x
Ghiandola in quiescenza
100x
Paratiroidi
• Cellule principali
– Granuli di secrezione,
granuli di glicogeno,
lipofuscina
– Sia chiare che scure
• Cellule ossifile
–
–
–
–
–
eosinofile
Abbondanti mitocondri
Funzione ignota
No granuli di secrezione
Aumentano con l’età
Cellule di Leydig
(cellule interstiziali nei testicoli)
• Secernono
Testosterone
• Abbondante sER
caratteristico delle
cellule secernenti
steroidi
Cellule Enteroendocrine (APUD)
• Epitelio cubico
semplice e
colonnare
• Epitelio dello
stomaco, del tenue
e del crasso
• Secernono ormoni
quando rilevano la
presenza del cibo
• “Comunicano” al Pancreas, al
Fegato ed alle altre cellule
dell’epitelio intestinale quando
iniziare la digestione
Ormoni
•
•
•
•
Presenti nel sangue in tracce (10-15-10-9 M), generano profonde
alterazioni intracellulari
Classificazione funzionale:
– Endocrino: origina in una ghiandola e agisce su una cellula-bersaglio
distante
– Paracrino: origina in una ghiandola e agisce su una cellula-bersaglio
contigua
– Autocrino: agisce sulla stessa ghiandola nella quale origina
– Feromone: trasmesso tra cellule di organismi differenti
Agiscono attraverso recettori e secondi messaggeri
– Per ormoni steroidei
– Per ormoni tiroidei
– Per ormoni non-steroidei e non-tiroidei
Interazioni ormone-recettore analoghe a substrato-enzima:
– Saturabili
– Altissima affinità (KD=10-6-10-9 M)
– Specificità alta ma non assoluta
– Suscettibili di inibizione
31
Sintesi, accumulo e
rilascio degli
ormoni peptidici
preprohormone
1. Sintesi del
Preproormone nel RE
2. Rilascio, nel RE della
sequenza segnale del
preproormone formando
un proormone inattivo
3. Transito del
proormone dal RE al
Golgi
4. Nella vescicola
secretoria enzimi
rilasciano i peptidi attivi
5. Rilascio dell’ormone
nel citosoplasma
6. Secrezione
7. Circolazione
Elaborazione degli Ormoni peptidici
Gli ormoni peptidici sono sintetizzati come preproormoni inattivi che
includono una sequenza segnale, l’ormone e altri frammenti peptidici
aggiuntivi
PreProOrmone
processato
a
ORMONE + Altri peptidi+
Sequenza
segnale
Il prepro-TRH (ormone rilasciante la tireotropina)
contiene 6 copie dell’ormone TRH
Elaborazione degli ormoni peptidici (2)
Gli ormoni peptidici sono sintetizzati come preproormoni inattivi che
includono una sequenza segnale, l’ormone e altri frammenti peptidici
aggiuntivi
Preproopiomelanocortina (POMC) 291 aa
β-lipotropina (91 aa)
(146 aa)
ACTH (39)
Peptide N-terminale(76 aa)
β-endorfina (81 aa)
γ-lipotropina (58)
Nell’adenoipofisi umana vengono liberati come prodotti terminali ACTH,
β-lipotropina, γ-lipotropina, β-endorfina e un frammento N-terminale
(76aa)
Elaborazione degli ormoni peptidici (3)
Gli ormoni peptidici sono sintetizzati come preproormoni inattivi che
includono una sequenza segnale, l’ormone e altri frammenti peptidici
aggiuntivi
Prepro-ANF (151 aa)
fattore natriuretico atriale
Vasodilatante (37 aa)
Fattore kaliuretico (21 aa)
Stimolatore del Na a lunga durata (30)
Fattore natriuretico atriale (28 aa)
Elaborazione degli ormoni peptidici (4)
Gli ormoni peptidici sono sintetizzati come preproormoni inattivi che
includono una sequenza segnale, l’ormone e altri frammenti peptidici
aggiuntivi
Proinsulina (84 aa)
Peptide C
(di connessione)
S
S
S
S
S
S Catena A (21)
S
S
S
S
insulina
S
S
Catena B (30)
TRASPORTO E METABOLISMO
DEGLI ORMONI PROTEICI
Una volta secreti gli ormoni proteici hanno una breve emivita
plasmatica
La maggior parte degli ormoni peptidici, come l’ACTH, l’ormone
paratiroideo (PTH), l’insulina, il glucagone, l’ADH, il TRH, il
GnRH, l’ormone rilasciante la corticotropina (CRH), agiscono
rapidamente e vengono degradati rapidamente, con un’emivita
plasmatica di 3-7 min
Sebbene possano essere degradati da proteasi
circolanti, la tappa iniziale della principale via
di degradazione degli ormoni proteici è
rappresentata dal legame dell’ormone con
il recettore di membrana cellulare
Gli ormoni glicoproteici hanno un’emivita
plasmatica più lunga; l’hCG, l’ormone
peptidico più glicosilato, ha un’emivita
plasmatica di ≈4ore
Sebbene la maggior parte degli ormoni
peptidici circoli a basse concentrazioni come
frazione non legata, alcuni ormoni, come i
fattori di crescita insulino-simili, sono legati
a proteine di trasporto del siero.
Tale legame costituisce un serbatoio circolante e
aumenta l’emivita plasmatica
Ormoni steroidei
liposolubili 1
Ormoni liposolubili 2
TRASPORTO E METABOLISMO
DEGLI ORMONI STEROIDEI
Contrariamente agli ormoni proteici, gli
ormoni steroidei non sono immagazzinati
ma vengono secreti appena sintetizzati
Dopo la secrezione in circolo gli ormoni steroidei si
legano a glicoproteine di trasporto prodotte dal fegato
Le glicoproteine di trasporto plasmatiche
costituiscono una riserva di ormone,
protetto dal metabolismo e
dall’eliminazione renale, che può essere
rilasciato alle cellule
Questo serbatoio prolunga notevolmente
l’emivita plasmatica degli ormoni steroidei,
tampona gli incrementi di produzione
ormonale e fornisce ormoni quando la
produzione diminuisce
Principali proteine di trasporto degli ormoni steroidei:
La globulina legante cortisolo e progesterone (CBG)
La globulina legante gli ormoni sessuali (SHBG)
La globulina legante la vitamina D (DBG)
La piccola frazione di ormone steroideo libero,
in equilibrio con quella legata, si lega ai
recettori cellulari.
La frazione libera viene anche metabolizzata,
principalmente nel fegato, in derivati idrosolubili
inattivi
Stimoli diversi possono
influenzare il rilascio
ormonale
L’esempio dell’Insulina L’insulina può essere
rilasciata direttamente a
causa dell’aumento della
glicemia o tramite
stimolazione nervosa
innescata dall’assunzione di
un pasto
Via di controllo complessa che
include ormoni ipotalamici,
ipofisari e periferici
L’esempio dell’ormone della crescita
L’ormone della crescita (GH) secreto
dall’ipofisi anteriore agisce direttamente
su molti tessuti dell’organismo. Inoltre
influenza la produzione epatica di
somatomedine (o fattori di crescita
insulino-simili, IGF-1 e IGF-3), un’altra
classe di ormoni che regola la crescita
Sinergismo
L’esempio della
glicemia
Il grafico
mostra
l’effetto di
vari ormoni sui
livelli
plasmatici di
glucosio
Tempo (ore)
Bioritmi
I recettori
ormonali
e la trasduzione
del segnale
Recettori
• Proteine associate o non alla membrana
• I recettori “riconoscono” le molecole
segnale e le legano in modo specifico
• Legame Recettore-Ligando
Variazioni del comportamento cellulare
Una cellula che esprime un dato
“recettore ormonale” é un bersaglio
(‘target’)
ormone
ormone
canali
1TM
Recettore
di membrana
7TM
N
N
Recettore
nucleare
ormone
E2
T
R
T
E1
cross-talk
Controllo di variabili citoplasmatiche: modulazione a breve termine
Controllo di variabili
nucleari:
modulazione
a lungo termine
1TM
Somatomedine
Insulina, GH, PRL, EPO
Attivina, AMH
Recettore
di membrana
N
7TM
ORMONI PEPTIDICI
(ACTH, ADH, Angiotensina,
Bradichinina, adrenalina,
calcitonina, glucagone,
ossitocina, paratormone, TSH,
TRH….)
STEROIDEI
aldosterone, cortisolo, estradiolo,
progesterone, testosterone
N
Recettore
nucleare
1,25-diOH-colecalciferolo
(7a-) (20-) (22-) (24-) (27-)-OHcolesterolo
T3, T4
57
Recettori (7 segmenti transmembrana)
α
β
•
•
β1
β2
>
>
>
Cuore, aumenta frequenza e forza di
contrazione
Adipociti, aumenta lipolisi
Intestino, diminuisce motilità
>
>
>
Polmone, rilascio della muscolatura
Fegato, aumenta glicogenolisi
Intestino, diminuisce motilità
•
>
>
>
>
•
Guanilato ciclasi – 1
>
α1
Atrio cardiaco, omeostasi dei liquidi
corporei
Endotelio, recettore per NO
α2
>
>
>
>
REC.Tirosin-chinasi a 2 subunità
>
>
>
>
Virus del sarcoma aviario, oncogene
Epidermide, fattore di crescita
Ubiquitario, recettore per insulina
Piastrine, fattore di crescita
•
Iride dell'occhio,
contrazione
Intestino, diminuisce motilità
Ghiandole salivari,
secrezione di acqua e di
potassio
Cellule pancreatiche B,
diminuisce secrezione
Piastrine, causa aggregazione
Cellule adipose, diminuisce
della lipolisi
Stomaco, diminuisce motilità
α?
>
>
>
Arteriole, costrizione
Sfintere della vescica,
contrazione
Organi sessuali maschili,
eiaculazione
58
Proteina G (GTP-binding protein)
Proteina G = α + β + γ
α: unità catalitica
•
•
•
•
•
α -GDP, inattiva
INATTIVO
α -GTP, attiva
αs, stimola l’effettore
α
GDP
αi, inibisce l’effettore
β
γ
>20 isoforme α
Complesso
ormonerecettore
GTP
GDP
ATTIVO
β
γ
Pi
Stimola o inibisce
γ: ancoraggio alla
membrana
•
>6 isoforme γ
β: alta affinità per
subunità γ, affinità
variabile per subunità α
•
>4 isoforme β
Molte proteine G diverse,
grande flessibilità di
risposta
α
GTP
GTPasi
α
GDP
INATTIVO
Effettore
59
Meccanismo dei recettori adrenergici mediato dalla
proteina G
60
Proteine G
Tipo
Gs
Localizzazione
Fegato
Gs
Adipociti
Gs
Rene
Gs
Gi
Gi/Go
Follicolo
Cuore
Neuroni
Gq
Golf
Muscolo liscio
Epitelio naso
Trasducina
Coni e
bastoncelli
Stimolo
Adrenalina,
glucagone
Adrenalina,
glucagone
ADH
LH
Acetilcolina
Endorfine,
oppioidi
Angiotensina
Molecole
odorose
Luce
Effettore
Adenilato ciclasi
Adenilato ciclasi
Effetto
Scissione
glicogeno
Lipolisi
Adenilato ciclasi
Ritenzione
acqua
Adenilato ciclasi
↑ estrogeni
Canale K
↓ forza
Adenilato ciclasi Attivitˆ elettrica
Fosfolipasi C
Adenilato ciclasi
cGMP
fosfodiesterasi
Contrazione
Sensazione
olfattiva
Segnali visivi
61
Secondi messaggeri
cAMP; Fosfatidil inositolo difosfato;
Fosfolipasi A2; Prostaglandine e
leucotrieni;
62
cAMP
Sistema β-adrenergico - proteina Gs
Meccanismo analogo per
GTP → cGMP → GMP
63
Protein kinasi A
attivata da cAMP
Target: residui Ser e Thr
di altre proteine
(fosforilazione)
AUMENTA l’attività di
alcuni enzimi
•
Glicogeno fosforilasi,
citrato liasi, fosforilasi b
chinasi, HMG-CoA
reduttasi chinasi e altri...
DIMINUISCE l’attività di
altri enzimi
•
Acetil-CoA carbossilasi,
glicogeno sintasi,
piruvato deidrogenasi,
HMG-CoA reduttasi e
altri...
64
Fosfodiesterasi (PDE)
termina il segnale di cAMP e cGMP
cAMP → 5’-AMP, cGMP → 5’-GMP
Target di interventi farmacologici
•
•
•
•
•
Metilxantine
Teofilline
Milrinone (cardiotonico)
Attivazione delle piastrine, tono dei muscoli lisci
(broncodilatatori, vasorilassanti etc), contrazione cardiaca
Sildenafil (Viagra)
65
Fosfatidil inositolo difosfato (PIP2)
DAG, Attiva protein kinasi C
IP3 → reticolo endoplasmico
Mobilizzazione di Ca++
66
Sistema fosfolipasi C, PIP2 → DAG + IP3
DAG: protein kinasi C → mitosi → crescita
IP3: rilascio Ca++ da vescicole
Li+ (farmaco per depressione nervosa)
IP3 + ATP → IP4 + ADP risposte prolungate (memoria?)
67
Fosfolipasi - idrolizzano fosfogliceridi generando lipidi
come secondi messaggeri
Fosfolipasi A2 → acido arachidonico (20C, 4 doppi legami)
•
•
Mediatore dell’infiammazione
Precursore degli eicosanoidi (prostaglandine, prostacicline,
trombossani e leucotrieni)
68
Prostaglandine
Derivano da acido arachidonico via cicloossigenasi (COX)
•
•
COX1 costitutivo, inibito da antiinfiammatori steroidei
(cortisone)
COX2 in risposta a mediatori dell’infiammazione (citochine),
inibito da antiinfiammatori non-steroidei (aspirina e ibuprofen)
Agiscono come ormoni (via proteina G)
•
•
•
•
Inattivate nei polmoni
Precursori dei trombossani (coagulazione)
Infiammazione (artrite reumatoide), sensazione di dolore e
apparato riproduttivo
Inibiscono secrezione gastrica (ulcera)
69
Leucotrieni
Derivano da acido arachidonico via lipoossigenasi (LOX)
•
•
•
Deficit di LOX in disordini mieloproliferativi (↑
↑ trombossano),
immunologici e coagulativi
3 tipi di acido monoidroperossieicosatetraenoico (HPETE)
Leucotrieni (LTA4)
> T1/2=4h
> Responsabili di reazioni anafilattiche: contrazione protratta dei
muscoli lisci (trachea e del tratto GI) e aumento della permeabilità
capillare
70
Trombossani
I trombossani sono composti chimici di natura lipidica,
derivati dell'acido arachidonico (o acido 5,8,11,14
eicosatetraenoico) nella via delle cicloossigenasi;
nella forma attiva, sono caratterizzati da un endoperossido
nell’anello penta-atomico tipico delle prostaglandine,
modificato. Sono degli eteri ciclici con un gruppo ossidrile
(OH) legato al C15.
Fanno parte degli eicosanoidi.
TXA2
TXB2
La trasduzione del segnale - Panoramica dei recettori 7TM
Gαβγ
αβγ
AC
7TM
Gαβγ
αβγ
PLC
DAG
cAMP
IP3
PKG
PKC
PKA
cGMP
Ca2+
GC
NO
NOS
CaMK
La trasduzione del segnale - Panoramica dei recettori 1TM
1TM
Ras
JAK
Piccole GTPasi
janusKinase
PI3K
MAPK
Smads
small mother against
decapentaplegic
PKB/Akt
STAT
Recettori ormonali Nucleari
Recettore per la
Vit D3 attivata
VDR
Recettori per gli
Ormoni
Tiroidei
TRα
α
TRβ
β
Recettori
X epatici
LXRα
α
LXRβ
β
Recettori per
gli
Ormoni
Steroidei
AR
ERα
α
ERβ
β
GR
MR
PRa
PRb
I recettori nucleari per gli ormoni steroidei
interagiscono con le proteine hsp
(heat shock proteins)
hsp90
AR
MR
hsp56
hsp56
ER
GR
hsp50
PR
hsp70
hsp56
hsp70
hsp52
hsp70
HSP90 maschera il DNA-BINDING DOMAIN dei
Recettori per gli steroidi
SR
SRE
hsp90
DNA
Attivazione della trascrizione genica operata da recettori
nucleari per gli ormoni steroidei (ER)
hsp50
ER
hsp70
hsp90
E2
hsp50
hsp70
ER
hsp90
ER ER
hsp90
hsp90
hsp50
hsp70
hsp50
hsp70
HAT
ER ER
TATA
Desensitizzazione
recettoriale
Il legame recettore-ormone spesso provoca la rapida
attenuazione della responsività recettoriale
(DESENSITIZZAZIONE)
1. disaccoppiamento recettore-proteine G in
risposta alla fosforilazione del
recettore
2. internalizzazione del recettore
3. down-regulation dei recettori totali a seguito
della ridotta sintesi di mRNA e di proteina, o
della degradazione lisosomiale
1. Il sistema più rapido di desensitizzazione:
il disaccoppiamento recettore-proteine G in risposta
alla fosforilazione del recettore tramite PKA e/o
PKC
P
PKC
α
γ
β
β PLCβ
α
P
PKA
γ
β
AC
1. disaccoppiamento recettore-proteine G in risposta alla
fosforilazione del recettore tramite le GRK (G proteincoupled receptor Kinase)
La fosforilazione tramite GRK spesso
non è sufficiente per inattivare
completamente i recettori; la
completa inattivazione richiede un
componente addizionale, l’arrestina
α
β
γ
α
P P P
β -arrestina
GR
β
γ
La fosforilazione con GRK e il legame di b arrestina può portare alla
internalizzazione del recettore tramite fossette rivestite di clatrina
Desensitizzazione
effector
Risensitizzazione
Riciclo del Recettore
SIGNAL
Internalizzazione
Degradazione
I meccanismi di desensitizzazione dei
recettori 1TM
La proteina oncogenetica Cbl si
lega al recettore fosforilato
tramite il suo dominio SH2 e lo
porta all’ubiquitinazione e alla
degradazione
Feedback
negativo
Stimolo
Iniziale
RISPOSTA
(effetto)
Feedback
positivo
Stimolo
Iniziale
È necessario un
Ciclo di
fattore
feedback
esterno per
inibire il ciclo
RISPOSTA
(effetto)
Adenoipofisi
TSH
Follicolo
di Graaf
Ciclo di
feedback
TIROIDE
T3/T4
estradiolo
IPOTALAMO
Ormone trofico 1 TRH
Adenoipofisi
L’autoregolazione si realizza attraverso il
feedback da parte dell’effetto su un
fattore.
L’autoregolazione può anche essere
ottenuta mediante l’azione di un fattore su
un altro (interazione)
Ormone trofico 2 TSH
Tiroide
Ormone 3 T3/T4
Cellula bersaglio
RISPOSTA
(effetto cellulare)
Nella macchina chimica che è il
vivente l’interazione e la
retroazione sono alla base di tutti i
meccanismi
Esempio di riflesso endocrino - L’ormone paratiroideo Bassa concentrazione plasmatica di Ca2+ (range 2.2 - 2.4 mM)
Cellula Paratiroidea
_
PTH
OSSO
Aumento del
Riassorbimento
Osseo del Ca2+
RENE
Aumento del
riassorbimento
renale del
Ca2+
Produzione di
1,25 di(OH)D3
Aumento dell’
assorbimento
intestinale del Ca2+
Aumento della concentrazione plasmatica di Ca2+
Feedback
negativo
Ipotalamo
La via di controllo della
secrezione del cortisolo
Ipofisi
Il cortisolo è un ormone steroideo
prodotto dalla corticale del
surrene. Il suo rilascio è
controllato dall’ormone trofico
ACTH (ormone adrenocorticotropo o
corticotropina) dell’adenoipofisi.
L’ACTH a sua volta è regolato dal
CRH (ormone rilasciante la
corticotropina) dell’ipotalamo.
Il cortisolo agisce come feedback
negativo su ACTH e CRH.
Feedback
negativo
causato da
cortisolo
esogeno
Anche il cortisolo
esogeno agisce
come feedback
negativo su
ipotalamo e
ipofisi.
In assenza di
ACTH viene
inibita anche la
corteccia
surrenale
La diagnosi di una patologia
delle vie endocrine
complesse dipende dalla
comprensione del feedback
negativo che controlla l’asse
Ipersecrezione primaria
dovuta a problemi
surrenalici
Livelli di CRH
- Bassi
Livelli di ACTH
- Bassi
Livelli di cortisolo - Alti
Ipersecrezione secondaria
dovuta a problemi ipotalamici
Eccessiva secrezione di CRH:
ipersecrezione secondaria di
cortisolo: il feedback negativo
fallisce
Livelli di CRH
Livelli di ACTH
Livelli di cortisolo
- Alti
- Alti
- Alti
Ipersecrezione secondaria
dovuta a problemi ipofisari
Livelli di CRH
- Bassi
Livelli di ACTH
- Alti
Livelli di cortisolo - Alti