UNIVERSITA' degli STUDI di PERUGIA
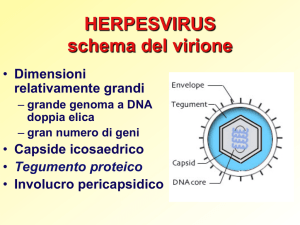
Herpesvirus
Human
HHV-1
HHV-2
HHV-3
HHV-4
HHV-5
Herpes
Simplex-1
Simplex-2
Varicella-zoster
Epstein-Barr
Cytomegalovirus
Virus
alfa
alfa
alfa
gamma
beta
HHV-6
Roseola infantum beta
HHV-7
HHV8
linfotropico
Associato al
Sarcoma di
Kaposi
beta
gamma
Herpes Virus
Alpha-herpesvirus: Herpes simplex di tipo 1 e 2 (HSV-1 e 2)
Virus della Varicella Zoster (VZV/HHV3)
La sede preferenziale di latenza sono le cellule dei gangli
nervosi sensitivi.
Beta-herpesvirus: Citomegalovirus (CMV/HHV5)
Virus erpetici umani 6 e 7 (HHV-6 e 7)
capacità di indurre sincizi.
La sede di latenza: HHV-6 e 7: linfociti T(?); CMV: monociti.
Gamma-herpesvirus: Epstein-Barr (EBV/HHV4)
Virus erpetico umano 8 (HHV8)
Il tropismo è limitato a cellule linfoidi, che sono pure
la sede di latenza (linfociti B)
Herpesvirus: caratteri generali
- genoma: DNA bicatenario
- diametro: 180-200 nm
- simmetria icosadeltaedrica
- capside con 162 capsomeri
- presenza del mantello
- presenza del tegumento
(materiale amorfo tra capside
ed envelope contenente enzimi
virali)
- è inattivato da etere e cloroformio.
La replica è nucleare (al microscopio
visibili “inclusioni” intranucleari)
Peculiarità degli Herpesvirus
- Il genoma codifica per una
DNA polimerasi-DNA dipendente che promuove la
replica virale.
- La replica è nucleare
- Il virus gemma dalla membrana nucleare e viene
liberato per esocitosi.
Gli HSV causano infezioni litiche, persistenti,
latenti e, per l’EBV, immortalizzanti.
Sono ubiquitari, la CMI è richiesta per la risoluzione
Infezioni che si possono stabilire tra
virus e cellula ospite
• Infezioni persistenti (infezioni croniche
non litiche, produttive)
• Infezioni latenti (sintesi di molecole virali
ma senza produzione di virus)
• Infezioni litiche ( lisi della cellula ospite)
• Infezione immortalizzante (infezione che
provoca una replicazione cellulare
incontrollata)
• GENOMA
• Il genoma di tutti gli Herpesvirus è lineare
a doppio filamento
Struttura di HSV-1 e HSV-2
Il genoma codifica per circa 80 proteine
Alcune hanno funzione enzimatica come:
• DNApol-DNAdip
• DNAsi
• timidina chinasi
• proteasi
• ribonucleotide reduttasi (converte i ribonucleotidi in
deossiribonucleotidi)
Molti di questi enzimi sono bersagli degli antivirali.
sul virione sono presenti 11 glicoproteine che hanno
funzioni
•
•
•
•
•
di attacco (gB, gC, gD, gE/gI)
di fusione (gB, gH/gL)
di proteine strutturali
di evasione della risposta immune (gC, gE/gI)
altre funzioni
Ad es. la componente C3 del complemento si lega a
gC e viene cosi eliminata dal siero.
La porzione Fc delle IgG si lega al complesso gE/gI,
Tali attività riducono l’efficacia antivirale degli anticorpi.
Replicazione
• RECETTORE: eparansolfato (proteoglicano)
• ANTIRECETTORE (VAP): glicoproteine virali di
attacco gB, gC, gD, gE/gI
• Dopo l’interazione con l’eparansolfato, localizzato
sulla superficie di molti tipi cellulari, segue una
interazione più stretta con recettori proteici
adiacenti.
.
Da: Nature Reviews I Immunology
•Il montaggio dei nucleocapsidi avviene nel
nucleo e da qui passano
gemmando
attraverso la membrana nucleare nel citoplasma
dove gemmando anche attraverso il reticolo o
attraverso la membrana cellulare esterna.
Replicazione degli
Herpesvirus:
• a) Attacco( cellule epiteliali e
fibroblasti) della gp virale
all’eparansolfato presente
sulla cellula bersaglio.
• b) Penetrazione per
fusione del mantello con
la membrana
citoplasmatica
• c) Il nucleocapside
raggiunge la membrana
nucleare: rilascio del
genoma nel nucleo il DNA
si circolarizza
• d) Trascrizione del
genoma e sintesi delle
proteine virali (3 fasi)
Herpesvirus
e) Sintesi delle proteine
precocissime (alfa) in grado di
legarsi al DNA e importanti per
la regolazione della trascrizione
genica.
• Trascritti associati alla latenza
( LAT ).
f) Sintesi delle proteine precoci
(beta) che sono fattori
trascrizionali compresa la
DNApol-DNAdip.
Il genoma virale viene trascritto da
una RNApol-DNAdip cellulare,
sotto il controllo di fattori
nucleari cellulari e fattori virali.
Herpesvirus
g) Proteine tardive (gamma)
che sono proteine strutturali
l) Assemblaggio nel nucleo
m) Acquisizione del mantello
dal foglietto interno della
membrana nucleare.
n) Liberazione per esocitosi o
per lisi cellulare.
Herpesvirus
Virus a DNA
Per la replica del genoma occorre
DNA polimerasi - DNA dipendente
lreplica del DNA virale avviene analogamente alla
replica del DNA cellulare
• i virus piccoli utilizzano la polimerasi cellulare
• i virus grandi codificano per una polimerasi virale
(adenovirus, herpesvirus)
La trascrizione avviene nel nucleo
Per la sintesi dei mRNA viene usata
RNA polimerasi II - DNA dipendente cellulare
Il nuovo genoma è trascritto dalla RNApol-DNAdip
cellulare (RNA polimerasi II)
La replica del genoma virale avviene non appena
viene sintetizzata la DNApol-DNAdip virale (la DNA
polimerasi virale è il bersaglio degli antivirali).
La replicazione del genoma porta alla trascrizione dei
geni tardivi (g) che codificano per le proteine strutturali
che si assemblano nel nucleo dove vengono
assemblate in procapsidi vuoti, nei quali si inserisce
poi il DNA
Il mantello viene acquisito dal foglietto interno della
membrana nucleare (A) o dalle vescicole del Golgi (B)
Il virus viene rilasciato per esocitosi o lisi cellulare (C).
(B)
(A)
(C)
Ciclo replicativo di HERPES VIRUS
b
a
g
Il DNA virale si circolarizza
e si replica come concatamero
Virus Herpes Simplex
Patogenesi ed Immunità
HSV-1 e 2 inizialmente infettano
cellule mucoepiteliali e fibroblasti
(infezione litica)
e stabiliscono poi una
infezione latente nei neuroni
che innervano l’area infettata.
L’infezione interessa di solito
(ma non esclusivamente):
le parti “alte” del corpo se HSV-1
le parti “basse” del corpo se HSV-2
infezioni da HSV-1 e HSV-2
Patogenesi ed Immunità
Penetrazione del virus attraverso lesioni di cute e membrane
mucose.
Il virus si riproduce alla base della lesione ed infetta
i neuroni innervanti raggiungendo per
trasporto assonale retrogrado i gangli:
• gangli del trigemino per l’HSV-1
• gangli sacrali per HSV-2
dove il virus rimane in forma episomale nel nucleo
Il virus poi ritorna nel sito iniziale di infezione e può rimanere
inapparente o causare lesioni vescicolari. La lesione si
rimargina senza lasciare la cicatrice.
la ricorrenza può essere causata da stress
emozionali, stress fisico, traumi, febbre, ciclo
mestruale, esposizione alla luce solare,,….etc.
In questo caso il virus migra a ritroso lungo il nervo,
causando lesioni a livello cutaneo o mucoso.
La riattivazione è
solitamente meno
Importante e di minore
durata rispetto agli
episodi primari, grazie
alla memoria immunitaria.
La risposta immune
L’immunità innata, con l’IFN-gamma e le cellule NK, è
sufficiente a limitare la progressione iniziale dell’infezione
Le risposte Th1 e i linfociti T-CD8 citotossici (CTL e T Killer)
riescono a distruggere le cellule infettate e a risolvere la
patologia in atto
DH (ipersensibilità ritardata).
Anticorpi neutralizzanti (NT) limitano la sua diffusione, ma non
risolvono l’infezione
In assenza di CMI, l’infezione si può disseminare ad organi
vitali ed al cervello.
Epidemiologia degli HSV-1 e -2
l’HSV è labile, inattivato da ambiente secco, detergenti,
tratto GI.
E’ trasmesso dai liquidi delle vescicole, saliva,
secrezioni vaginali (“il mescolarsi e il combinarsi
di membrane mucose”).
Causano infezioni orali e genitali.
HSV-1: contatto orale, baci, bicchieri, spazzolini, saliva,
dita, cute; il virus penetra attraverso una lesione di
continuo.
L’autoinoculazione può anche causare l’infezione degli
occhi.
HSV-2: contatto sessuale, autoinoculazione, madre-feto.
Eliminazione del virus dalla cervice con le perdite vaginali.
Soggetti a rischio di contrarre infezioni da
HSV
- molto comune - soprattutto
bambini (HSV-1)
- persone attive sessualmente
(HSV-2)
- rischio professionale:
medici, infermieri, dentisti,
ginecologi, persone a contatto con
secrezioni orali e genitali
(patereccio erpetico).
- immunodepressi e neonati per
infezione disseminata
Manifestazioni cliniche delle infezioni da HSV-1
Infezioni primarie: vescicole trasparenti con base eritematosa,
che si trasformano in ulcere e croste.
•
•
•
•
•
•
•
•
•
•
Herpes labiale
Stomatite
Faringite erpetica
Gengivostomatite primaria
Cheratocongiuntivite erpetica
Eczema erpetico
Patereccio erpetico
Herpes gladiatorum
Encefalite erpetica
Herpes neonatale
HSV-1: herpes labiale
Le fasi dell’herpes labiale
• 1° e 2° giorno “fase prodromica” (formicolio)
• 2° e 3° giorno “fase dell’eritema” (prurito e
arrossamento)
• 4° giorno “fase delle vescicole” (comparsa di
vescicole acquose)
• 5° e 6° giorno “fase ulcerosa” (rottura delle vescicole)
• 8°-10° giorno “fase della crosta” (inizio del processo
di guarigione)
Lesioni erpetiche primarie (HSV-1)
Gengivostomatite primaria (bambini di 6 mesi - 3 anni)
lesioni, ulcere, su mucosa buccale, palato, faringe,
gengive, lingua.
Latenza nel ganglio del trigemino.
Gengivostomatite erpetica
Lesioni erpetiche primarie (HSV-1)
Cheratocongiuntivite erpetica
Con ulcere corneali o vescicole palpebrali.
Quasi sempre limitata ad un solo occhio.
Può dare episodi ricorrenti causando
cicatrici permanenti, danno corneale e cecità
Cheratite erpetica
Lesioni erpetiche primarie (HSV-1)
Infezioni cutanee
Patereccio erpetico
Eczema erpetico
Herpes gladiatorum
Patereccio erpetico
Herpes gladiatorum
Herpes gladiatorum
Manifestazioni cliniche delle infezioni da HSV-2
Nei maschi lesioni sul glande o su tutto il pene.
Nelle femmine: vulva, vagina, cervice, area perianale
Sintomi: le lesioni possono essere accompagnate da febbre,
mal di testa, malessere, adeniti inguinali, perdite vaginali,
negli omosessuali proctiti (a carico del retto)
Latenza nei gangli sacrali
Riattivazioni ogni 2-3 settimane.
Herpes genitale della vulva
Herpes genitale del pene
Herpesvirus
La sieropositività verso HSV-2 è correlata con
l’aumento della attività sessuale
.
L’HSV-2 è associato da un punto di vista sieroepidemiologico con il cancro della cervice (come
cofattore per gli HPV).
Altre infezioni da Herpesvirus
Encefalite erpetica (HSV-1)
malattia febbrile acuta. Le lesioni sono limitate ad un
solo lobo temporale. Elevato indice di mortalità
Meningiti (HSV-2)
dopo 10 giorni dall’infezione primaria, febbre elevata,
rigidità nucale, mal di testa, fotofobia, nausea.
Herpes neonatale (soprattutto HSV-2)
Il neonato si infetta per via
transplacentare, perinatale.
Disseminazione del virus
a fegato, polmoni e SNC, in
alcuni casi l’infezione è letale.
Diagnosi di infezione da Herpes simplex
Campioni biologici:
raschiamenti alla base delle vescicole (strisci di Tzanck):
modificazioni cellulari, corpi di Cowdry tipo A
Esame colturale in cellule diploidi umane (HeLa, HEp2,
fibroblasti), cellule renali di coniglio.
Presenza di cellule giganti polinucleate (sincizi)
Effetto citopatico in 24-48 ore.
Immunofluorescenza
PCR: DNA virale in campioni biologici.
Ricerca di anticorpi mediante
differenti metodiche sierologiche
I tests sierologici sono utili per la
diagnosi di una infezione primaria e per studi epidemiologici.
Terapia e profilassi
I farmaci possono essere analoghi nucleosidici o inibitori
della DNA polimerasi.
I farmaci inibiscono la replica virale agendo sugli enzimi
della replica ma non sono in grado di eliminare il virus in
latenza nei gangli sensoriali.
Aciclovir
vidarabina
iododeossiuridina
(cheratite erpetica)
trifluoridina (cheratite erpetica)
famciclovir, valaciclovir, penciclovir
Evitare il contatto con le lesioni.
Uso di guanti, uso di preservativi, parto cesareo. No vaccini.
HSV-3: virus varicella-zoster
(VZV)
VZV:
Caratteri generali
Diametro di 150-200 nm
Simmetria icosaedrica
75 proteine
Il mantello è sensibile all’ambiente secco e ai detergenti.
Si trasmette attraverso le vie respiratorie.
VZV
Patogenesi
La trasmissione attraverso le vie
respiratorie.
L’infezione primaria inizia con l’infezione
delle tonsille e della mucosa
respiratoria, poi vasi linfatici,
viremia, SRE.
Dopo 11-13 gg la seconda viremia,
infezione dei linfociti T, cellule
epiteliali cutanee. A livello cutaneo
causa un rash:
macula, papula, vescicola,
pustola, crosta.
Le manifestazioni sono asincrone.
Febbre e sintomi sistemici si
accompagnano al rash.
Gli Ab limitano l’infezione
La CMI è importante per limitare, la progressione e la
risoluzione
della malattia.
In assenza di CMI, il virus causa maggiori
disseminazioni
(polmoni, fegato, cervello).
Latenza nelle radici dei gangli
dorsali e dei nervi cranici.
Riattivazione, migrazione dai
gangli alla cute
zoster.
Gli Ab limitano la diffusione
della viremia di VZV ma la
CMI è importante per limitare,
la progressione e la
risoluzione della malattia.
In assenza di CMI il virus causa
disseminazioni
(polmoni, fegato, cervello).
L’infezione primaria acuta è
la varicella.
La riattivazione causa
l’herpes zoster
(fuoco di S. Antonio)
nei dermatomeri
innervati.
Latenza nelle radici dorsali
e gangli dei nervi craniali.
La CMI è protettiva.
Soggetti a rischio
• Personale sanitario
• Maestri, insegnanti, personale di scuole e
asili
• Residenti in case di cura
• Soggetti che vivono in ambienti chiusi:
carcerati, personale di sorveglianza, militari,
etc.
Varicella
È una delle 5 malattie esantematiche
infantili insieme a
morbillo
rosolia
Va malattia (Parvovirus B19)
6a malattia o roseola infantum (Herpes tipo 6 e 7)
CLINICA
può essere sintomatica o asintomatica.
Febbre, rash maculo-papulare dopo una incubazione
di 14 gg.
Rash: macule, papule, vescicole, pustole, croste.
Il rash è asincrono; le manifestazioni durano 3-5 giorni.
Il rash è generalizzato: tronco, estremità, testa.
Negli adulti è più grave e si ha una polmonite interstiziale nel
20-30 % di pazienti adulti.
Herpes zoster
Riattivazione di una infezione latente di
varicella.
Dolore acuto nelle aree innervate precede
la comparsa di lesioni.
I’eritema è limitato ai dermatomeri (
regione cutanea innervata).
Lesione maculo-papulare con
base eritematosa, vescicole.
Una complicazione è la nevralgia
posterpetica che persiste per
mesi/anni che si verifica nel 30% dei
pazienti con età > 65 anni che hanno
sviluppato lo zoster.
Un’altra complicazione è lo zoster
oftalmico.
Herpes zoster (“fuoco di S. Antonio”)
Epidemiologia
Il virus è molto contagioso, il 90% circa delle persone
suscettibili hanno contratto l’infezione in casa tra i
familiari.
La malattia ha la trasmissione per via respiratoria o
mediante contatto con vescicole cutanee.
I pazienti sono contagiosi prima e durante i sintomi.
Il 10-20 % delle persone infettate dal VZV sviluppa lo zoster,
l’incidenza è parallela con l’età.
Lo zoster può essere una sorgente d’infezione di varicella in
persone non immuni come i bambini.
Diagnosi (simile a HSV-1 e 2)
Raschiamenti dalle vescicole
IF diretta
Biopsie, secrezioni respiratorie
Strisci di cellule di Tzanck
Esame colturale su fibroblasti
diploidi umani
CPE (dopo 3-6gg), corpi inclusi di
Cowdry tipo A.
Inclusi nucleari, sincizi.
Biopsie per ricercare gli Ag
(Immunofluorescenza per ricercare
gli antigeni di membrana).
PCR.
Test sierologici (ELISA)
VZV
Trattamento, Prevenzione e
Controllo
delle infezioni da VZV
- bambini con varicella:
non si effettua terapia.
- adulti o a pazienti ID con VZV: terapia con aciclovir,
famciclovir, valaciclovir.
Uso di VZIG (immunoglobuline vs. varicella-zoster).
Analgesici,anestetici locali danno sollievo dalla nevralgia
posterpetica che segue lo zoster.
Uso di Vaccino Oka
(a virus vivo ed attenuato).
Virus di Epstein-Barr (EBV)
EBV causa:
• Mononucleosi
infettiva (malattia del
bacio)
• Linfoma di Burkitt
• Carcinoma
nasofaringeo
Linfoma di Burkitt
• È un tumore dei bambini dell’Africa subsahariana in cui c’è deficit delle cellule T
• I linfociti B proliferanti infettati da EBV
Carcinoma faringeo
• Comune tra le popolazioni del sud est
asiatico in particolare nel sud della Cina
Epstein Barr
• Diametro 180-200 nm
2 classi di EBV:
• EBV-A presente nelle
persone immunocompetenti
• EBV-B è isolato in persone
immunocompromesse
• EBV
• codifica per 70 proteine differenti, alcune delle quali sono
espresse nei differenti stadi d’infezioni.
• Le proteine virali prodotte durante una infezione
produttiva sono rilevabili sierologicamente
Marker dell’infezione da EBV
• EBV nuclear antigen (EBNA): Ag nucleare,
marker precoce, gli Ab indotti si sviluppano
tardivamente.
• Ag precoce (EA):
EA-R (citoplasmatico), marker del ciclo litico, gli Ab
Anti-EA-R sono presenti nel Linfoma di Burkitt.
EA-D (citoplasmatico e nucleare). Gli Ab sono presenti
in soggetti con Mononucleosi infettiva.
• Ag capsidico virale (VCA), citoplasmatico. Ag
tardivo, presente nelle cellule produttive;
• Ab IgM anti-VCA sono transitori ( indicano inf
recente) , Ab Anti-VCA IgG sono persistenti.
• EBV Si lega ai linfociti B mediante le
proteine del envelope e si lega al CD21 e
attivazione policlonale dei linfociti
• Tale proliferazione si accompagna ad una
produzione di Ab IgM (Ab eterofili )
evidenziati con la reazione di Paul Bunnel
. L’ingrossamento della milza, fegato tipico
della mononucleosi è dovuto alla
proliferazione dei linfociti B e T attivate.
• Si osserva linfocitosi
Marker dell’infezione di EBV
• ANTICORPI ETEROFILI. Si rivelano
con la reazione di Paul-Bunnel (su globuli
rossi di pecora, cavallo o bovino(
agglutinazione)
Marker precoce in >50% dei pazienti
EBV
• Gli anticorpi hanno un ruolo limitato.
• La risposta delle cellule T (linfocitosi)
contribuisce ai sintomi della Mononucleosi
infettiva.
• Il virus è associato a linfoma e leucemia in
persone con deficit delle cellule T e in
bambini africani (Linfoma di Burkitt) e
con Carcinoma nasofaringeo in Cina.
cellule epiteliali: moltiplicazione virale e rilascio
di virioni
linfociti B: infezione latente senza replicazione
e rilascio di virioni
quando EBV infetta i linfociti B, forma un episoma nel
nucleo della cellula.
Lo stato di latenza è mantenuto dalla proteina EBNA-1
Patogenesi dell’EBV
a) EBV nella saliva --> cellule epiteliali
dell’orofaringe
--> escrezione del virus dalla saliva -->
faringiti.
b) EBV nella saliva --> cellule epiteliali
dell’orofaringe --> proliferazione delle
cellule B --> anticorpi eterofili.
c) EBV nella saliva --> cellule epiteliali
dell’orofaringe --> proliferazione delle
cellule B --> Attivazione delle cellule T
(fegato, linfonodi, milza) -->
Risoluzione --> Linfociti T atipici
(Cellule di Downey).
diagnosi sierologica di mononucleosi: possibili situazioni
Abs anti capsula
Abs tardivi
Mononucleosi infettiva anticorpi eterofili-positiva
Bambini, adolescenti, adulti.
Sintomi:
• febbre
• malessere
• faringiti
• linfoadenopatia
• epatosplenomegalia
• affaticamento
• ostruzione laringea
• rottura della milza
• Complicazioni neurologiche
Epidemiologia dell’EBV
• Mononucleosi infettiva anticorpi eterofilipositiva: trasmissione attraverso la saliva,
contatti stretti (malattia del bacio) o tramite
spazzolini, bicchieri contaminati.
• Linfoma di Burkitt: cofattori (malaria),
predisposizione genetica.
• Carcinoma nasofaringeo: solo in alcune
aree geografiche (Cina), predisposizione
genetica e alimentazione.
Complicazioni neurologiche:
sindrome di Guillian Barrè
Paralisi progressiva agli arti con andamento disto-
prossimale. Può causare complicanze, in particolare
con interessamento dei muscoli respiratori
La sua causa è tuttora ignota, ma è probabilmente
autoimmune
Prevenzione e Controllo
• Nessun trattamento è efficace, nessun
vaccino è disponibile.
• Immunità duratura dopo l’infezione.
• La mononucleosi è benigna nei bambini.