Chimica Organica
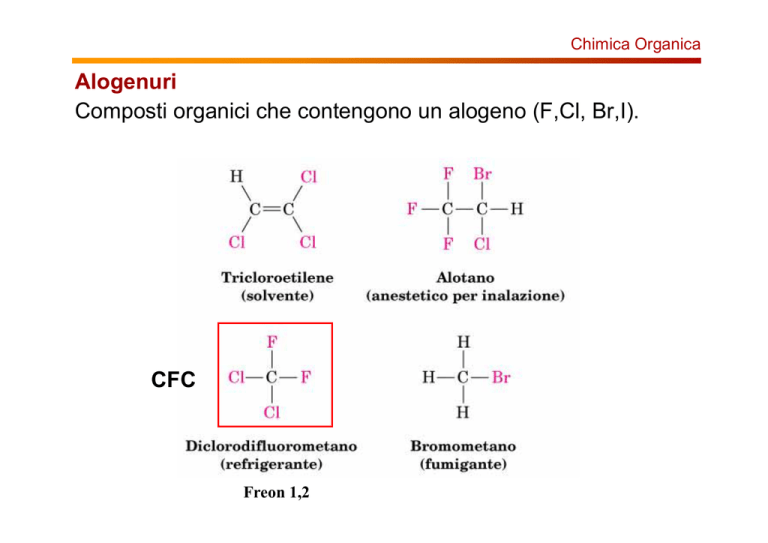
Alogenuri
Composti organici che contengono un alogeno (F,Cl, Br,I).
CFC
Freon 1,2
Chimica Organica
Nomenclatura
Trovare e nominare la più lunga catena di atomi di carbonio.Se è presente un
legame multiplo bisogna scegliere la catena più lunga che lo contiene.
Numerare la catena partendo dall'atomo di carbonio terminale più vicino ad un
sostituente, sia esso un gruppo alchilico o un alogeno.
Identificare e nominare i gruppi e gli atomi di alogeno attaccati a questa catena.
Designare la posizione di ogni gruppo o atomo sostituente con l'appropriato
numero e nome.
Assemblare il nome, elencando i gruppi in ordine alfabetico. I prefissi di, tri, tetra,
etc., usati per designare più di un gruppo dello stesso tipo, non sono considerati ai
fini dell'elencazione in ordine alfabetico.
Chimica Organica
Nomi comuni
nome IUPAC
nome comune
CH2=CHCl
CH2Cl2
CHCl3
Cloroetene
(cloruro di vinile)
Diclorometano
(Cloruro di metile)
Triclorometano
(Cloroformio)
PVC
Parlamento chimico
Chimica Organica
Sintesi di alogenuri
H
H
C
H
C
H
C
HCl
H
H
Cl
H
H
H
C
C
H
R OH
H
C
Br
ClH
C
H
Br 2
H
H
R OH
H
Br
C
H
H
HCl
In alternavita è possibile usare PCl3 o PBr3
Chimica Organica
Polarizzazione del legame carbonio-alogeno
I nucleofili attaccano l’atomo di C povero di elettroni
Chimica Organica
Sostituzione Nucleofilica
Nucleofilo
Gruppo uscente
Chimica Organica
Il meccanismo SN2
Reazione bimolecolare: due reagenti (nucleofilo e
alogenuro) determinano la velocità della reazione.
Inversione della configurazione ad un stereocentro.
Processo a un solo stadio rottura e formazione dei
legami avvengono simultaneamente
Chimica Organica
Effetto dei sostituenti
Chimica Organica
Effetto dei sostituenti
Chimica Organica
Reattività del nucleofilo e bontà del gruppo uscente
I migliori nucleofili sono costituiti
da specie molto basiche e da
atomi grandi e polarizzabili
Il miglior gruppo uscente è quello
che porta alla formazione di
specie più stabili. Il meno basico
o quello privo di carica
Chimica Organica
Il meccanismo SN1
CH 3
H 3C C Cl
CH 3
H 2O
CH 3
H 3C C OH
CH 3
HCl
La reazione avviene con un meccanismo diverso
Chimica Organica
Il meccanismo SN1
Reazione monomolecolare: la velocità
dipende esclusivamente dalla
concentrazione del substrato
Condotta ad uno stereocentro, la reazione
SN1 porta ad una miscela racemica.
Processo a due stadi: 1) la rottura del
legame substrato-gruppo uscente; 2)
formazione legame substrato-nucleofilo
Chimica Organica
Il meccanismo SN1
Chimica Organica
Formazione di una miscela racemica
Se nel corso della reazione si forma una specie con un piano di simmetria,
l’informazione stereochimica è perduta
Chimica Organica
SN1 vs SN2
Tipo di alogenuro
SN1
RCH2X
(primario)
non avviene
altamenta favorita
R2CHX
(secondario)
può avvenire solo
con alogenuri benzilici
e allilici
avviene
R3CX
(terziario)
favorita
non avviene
SN2
Chimica Organica
Eliminazione
Chimica Organica
Il meccanismo E2
R
H
B
R
C
R
H
C
R
C
R
R
δ+
B
Br
C
C
R
R
R
R
X
δ-
R
C
R
Chimica Organica
Regola di Saitzev
Nelle eliminazioni di HX predomina l’alchene più sostituito (il carbonio ibridizzato
sp2 è più elettronegativo)
Chimica Organica
Il meccanismo E1
Chimica Organica
Competizione eliminazione/sostituzione
Le reazioni di eliminazione e sostituzione sono sempre in competizione.
Substrati terziari favoriscono E1/SN1. Substrati primari favoriscono E2/SN2.
Nucleofili debolmente basici favoriscono SN.
Nucleofili stericamente ingombrati (o basi non nucleofiliche) favoriscono E.
Cl
CH3CHCH3 + CH3CH2O-
OCH2CH3
CH3CHCH3
+ CH3CH CH2 + CH3CH2OH
+ Cl-
base forte
O
Cl
CH3CHCH3 + CH3C O-
base debole
O
OCCH3
CH3CHCH3 +
Cl-