LA MEDICINA BIOLOGICA OTTOBRE - DICEMBRE 2000
CLINICAL
M. Corgna
ATTI DEL XV CONGRESSO NAZIONALE DI OMEOPATIA, OMOTOSSICOLOGIA E MEDICINA BIOLOGICA
Milano, 3 giugno - Roma, 10 giugno 2000
SINDROMI
DA IPERANDROGENISMO
NELLA DINAMICA PNEI
DI RISPOSTA A STRESSORI
AFFETTIVI ED AMBIENTALI
ANDROGEN RELATED SYNDROMES IN PNEI RESPONSE TO EMOTIONAL
AND ENVIRONMENTAL STRESSORS
Riassunto. La storia e la mitologia fanno spesso riferimento a donne che si “androgenizzano” per governare nazioni e vincere
guerre, senza perdere gli attributi femminili. Il fenomeno endocrino dell’androgenizzazione femminile, potrebbe anche essere interpretato come risposta di adattamento alla necessità di rivestire ruoli, tradizionalmente maschili, che caratterizzano l’attuale vita
della donna nelle società occidentali. Gli studi sulla differenziazione sessuale potrebbero, inoltre, avvalorare l’ipotesi che l’androgenizzazione nella donna prenda il via “in utero” da un’anomala “programmazione” delle strutture diencefaliche che si ripercuote
sui circuiti neuroendocrini che sostengono la più classica espressione di femminilità: il ciclo mestruale. Le sindromi da iperandrogenismo rappresentano il substrato di problematiche ad impatto profondissimo sull’equilibrio psicofisico della donna. Alopecia,
ipertricosi, sterilità o subfertilità, acne, disfunzioni del desiderio sessuale ed ovaio policistico impegnano giornalmente il clinico.
Gli stressori affettivi ed ambientali possono sinergicamente spostare l’omeostasi endocrina verso uno stato di relativo iperandrogenismo. La crescente esposizione all’inquinamento elettromagnetico, oltre che danneggiare le gonadi, destabilizzerebbe i nostri
organi magnetici e l’epifisi con notevoli ripercussioni sul piano della regolazione gonadica e corticosurrenalica. Un ormone ad effetto androgenizzante a livello ovarico è l’insulina. La recente acquisizione del sinergismo funzionale leptina-insulina potrebbe far
intravedere una relazione tra alcuni quadri dismetabolici, patologie psiconutrizionali e disregolazione ovarica, mentre il tessuto
adiposo assumerebbe, anche, il ruolo di regolazione sessuale. L’Autore conclude con alcune proposte terapeutiche finalizzate alla
modulazione delle sindromi da iperandrogenismo femminile.
Parole chiave: SINDROMI DA IPERANDROGENISMO, INSULINO - LEPTINO RESISTENZA, STRESS ELETTROMAGNETICO
Summary. History and mithology frequently refer to women who resort to “androgenization” in order to rule nations and win
wars. Female androgenization can be interpreted as an adaptation to new “male” roles that women have to play in our society.
Studies on sexual differentiation could cast a light on abnormal priming of diencephalic sites “in utero” which could result in abnormal neuroendocrine circuits altering the most typical expression of female endocrinology: the menstrual cycle. Affective and
environmental stressors together can result in hyperandrogenism. Androgen related syndromes have a strong psychological impact on woman: problems such as alopecia, hypertricosis, sexual desire disturbances, acne, polycystic ovary syndrome face the
clinician daily. Exposure to electromagnetic stressors could destabilize “magnetic organs” and the pineal gland which modulate
reproduction and adrenal activity. Insulin causes androgenization of the ovary. Uptodate data regarding functional insulin-leptin
synergism could represent the link between dismetabolic diseases, nutritional disorders and ovarian disregulation.
Adipose tissue could thus modulate reproduction. The Author suggests some therapeutic guidelines aiming to correct the hyperandrogenism states.
Key words: ANDROGEN RELATED SYNDROMES, INSULIN-LEPTIN RESISTANCE, ELECTROMAGNETIC STRESS
71
LA MEDICINA BIOLOGICA OTTOBRE - DICEMBRE 2000
Le sindromi da iperandrogenismo
rappresentano il substrato fisiopatologico di problematiche ad impatto
profondissimo sull’equilibrio psicofisico della donna. Alopecia, ipertricosi,
sterilità o subfertilità, acne, ovaio policistico, perdita della libido sono solo
alcune delle problematiche cliniche a
cui la psiconeuroendocrinologia e la
medicina biologica cercano di dare
una risposta.
Tra i casi più eclatanti di androgenismo nella storia dell’umanità, quello
della regina egizia Hatshepsut è abbastanza singolare.
Era la primogenita del faraone Tutmosis, uno dei leggendari fondatori
della XVIII dinastia che regnò sull’Egitto dal 1526 al 1512 A.C.
Tutmosis I ebbe anche un secondogenito che era destinato a regnare come suo successore. Dopo la morte
del padre e la prematura morte del
fratello, Hatshepsut dovette unirsi in
matrimonio con un suo fratellastro, figlio di Tutmosis e della concubina
Mutnefret, che salì al trono col nome
di Tutmosis II.
Il breve regno di quest’ultimo diede
alla regina la possibilità di usurpare il
trono del marito ed assumere le sembianze di un faraone, adottandone il titolo. (Fig. 1)
Fino al 1482 A.C., per circa 20 anni,
il faraone Hatshepsut governò un Egitto particolarmente prospero, facendosi
rappresentare nelle vesti di uomo, anche se la propaganda regale dell’epoca tradisce l’originalità dell’evento che
si deduce in un interessante passo del
racconto di una spedizione commerciale organizzata dalla sovrana nella
ricca terra di Punt (costa della Somalia): “Essi (i capi del paese di Punt)
parlano, invocano pace dalla sua Maestà: salute a Te, re dell’Egitto, Sole femmina che brilli come il disco solare”.
Le Amazzoni erano un popolo di
donne guerriere provenienti dalle terre
Caucasiche, che avevano invaso l’Asia
minore, la Tracia, l’Egitto ed altri Paesi.
Erano governate da una regina che si
accoppiava una sola volta all’anno per
diffondere la razza tra una popolazione
maschile vicina, i Gargarei; i figli maschi
venivano uccisi oppure affidati ai padri e
destinati ai lavori servili.
La leggenda narra che veniva loro
tolta una mammella affinché non fosse
d’impedimento nelle attività di guerra:
per questa ragione erano chiamate
Amazzoni (senza mammella).
Capitale del loro paese era Temiscira, vicino a Ponto Eusino. Adoravano
con particolari onori Artemide ed Ares
che era considerato il padre delle
Amazzoni. La loro regina, Ippolita, si distingueva in ogni battaglia proprio perché portava una cintura che le aveva
regalato Ares. Dopo una dura lotta le
Amazzoni vennero sconfitte da Eracle,
cui era stato dato il compito d’impossessarsi della cintura desiderata da
Admeta, figlia di Euristeo (Fig. 2).
Vi sono, inoltre, racconti leggendari
sulla presenza in Sud America di Amazzoni, dalle quali deriverebbe il nome del
grande fiume sudamericano; esisteva,
inoltre, fino al 1894, momento in cui il
Paese venne conquistato dai Francesi,
un esercito di donne nel Dahomey, Africa Occidentale. Sono molti gli esempi
di donne, nella mitologia e nella storia,
che hanno assunto sembianze maschili
per poter governare nazioni o vincere
guerre. Non sappiamo se in queste
donne l’aspetto comportamentale fosse
anche “sostenuto” da un correlato endocrino specifico.
Fig. 1 (sn): Il faraone donna Hatshepsut.
LA DIFFERENZIAZIONE SESSUALE
Fig. 2 (sotto): Amazzonomachia – Copia di opera di Fidia: dettaglio dello
scudo (acropoli di Atene).
72
La differenziazione sessuale non è limitata solo alle gonadi ed ai genitali interni ed esterni: esiste anche una differenziazione dell’encefalo e di alcuni
tessuti periferici.
B.S.Mc Ewen ha dimostrato che il
cervello si comporta come organo sessuale per quanto riguarda il principale
ormone maschile: il testosterone. Il
cervello è in grado di sintetizzare
estradiolo e 5 α diidrotestosterone
(DHT). L’attività della 5 α reduttasi è
spiccata a livello del tronco encefalico
e dell’ipotalamo. La sintesi di estradiolo è legata ad un semplice processo di
aromatizzazione del testosterone (aggiunta di un ossidrile).
LA MEDICINA BIOLOGICA OTTOBRE - DICEMBRE 2000
L’aromatizzazione del testosterone è
massima nell’ipotalamo e minima nella
corteccia cerebrale.
Il sistema nervoso attiva, inoltre, processi biochimici caratteristici delle
ghiandole surrenali: è in grado di
sintetizzare DHEA e pregnenolone.
Il progesterone sintetizzato nel cervello, oltre ad essere responsabile della fisiologica soppressione immunitaria
che si verifica in gravidanza, è in grado
di attivare a livello cerebrale, mediante
la trasformazione in pregnenolone, il
più importante ormone inibitorio, l’acido gammaminobutirrico (GABA).
Diverse ricerche sperimentali hanno
evidenziato che per ogni specie di
Mammiferi, esiste un periodo critico
all’interno del quale l’azione degli ormoni sessuali è in grado di interferire
sulla sessualità del nascituro.
La differenziazione sessuale, che
nella specie umana inizia dopo la sesta settimana di gestazione, è un processo complesso che, in base al programma genetico (cariotipo XY o XX),
interessa il sistema neuroendocrino
nella sua globalità.
Nel maschio le strutture diencefaliche
hanno caratteristiche femminili che si
mascolinizzano durante la vita fetale solo parzialmente ad opera del testosterone prodotto dalla gonade in via di sviluppo. Il DHT e l’estradiolo, infatti, avrebbero un effetto mascolinizzante di gran lunga superiore a quello del testosterone.
Un difetto di “binding” dell’estradiolo cerebrale (necessario perché il feto
di sesso femminile sia protetto dall’effetto androgenizzante dell’estradiolo)
potrebbe essere alla base di una programmazione endocrina femminile in
senso “androgeno”?
La differenziazione sessuale cerebrale è essenziale per sostenere i circuiti neuroendocrini che sono attivi
nella femmina e che si sintetizzano nel
ciclo mestruale. Un difetto in utero della differenziazione sessuale potrebbe,
dopo la pubertà, manifestarsi con la
perdita (da parte dei centri diencefali-
ci) dell’attività secretoria ciclica che
caratterizza l’espressione più classica
di femminilità: il ciclo mestruale.
Per quanto riguarda la corteccia cerebrale, alcuni dati comportamentali dimostrerebbero che il sesso di base sia
maschile nel maschio e nella femmina
e che in epoca post natale avvenga un
processo di demascolinizzazione: in
particolare è stata riscontrata una specializzazione dell’emisfero destro nella
femmina (sensibilità, funzione non verbale, riconoscimento di immagini ed
orientamento) mentre nel maschio esisterebbe una maggiore specializzazione dell’emisfero sinistro (raziocinio, capacità verbali e matematiche).
La determinazione del sesso è legata al sesso gametico (cariotipo maschile o femminile), al sesso gonadico
(gene SRY e AZF), al sesso genitale
ed al sesso psichico.
Il sesso psichico è determinato da
fattori genetici, ambientali, ormonali,
e socio culturali.
A tale proposito ricordiamo due
aspetti fondamentali: l’identità di genere ed il ruolo di genere. L’identità di genere è costituita dal senso di “se stesso”, e quindi dalla percezione sessuata maschile e femminile di se stessi e
del proprio comportamento. Il ruolo di
genere è tutto quello che un individuo
fa o dice per indicare agli altri il grado
della propria mascolinità o femminilità.
In sintesi: il ruolo di genere è l’espressione esteriore dell’identità di genere e
questa è l’esperienza personale del
ruolo di genere.
ne interpretato come una disregolazione del sistema Tchong Mo (gonade-tiroide) funzionalmente legato a Yang
Ming-Grosso Intestino (generatore
dell’energia di mantenimento).
Il meridiano curioso o meraviglioso
Tchong Mo che veicola l’energia ancestrale ha, tra le altre funzioni, anche
quella di controllo del sistema pilifero.
È il primo Meridiano che compare nel
corso della vita embrionale ed ha il
compito di “organizzare” lo sviluppo del
feto. Contribuisce allo sviluppo materiale ed energetico degli organi genitali ed
alla loro nutrizione attraverso il sangue.
I peli sono il sovrappiù del sangue. Il
Tchong Mo è il mare del sangue ed è
quindi responsabile di questa funzione.
Da-Cheng si sofferma sul ruolo “tricogenetico” di questo meridiano ed afferma: “quando il sangue e l’energia
sono in eccesso, la pelle e la carne
sono caldi”. Al contrario, quando è in
eccesso il solo sangue, questo umetta
la cute e provoca abbondante pilosità:
l’eccesso di sangue è un chiaro riferimento all’assenza di ciclo mestruale.
Le mestruazioni “feriscono” i segmenti peribuccali del Tchong Mo da
cui deriva l’assenza di barba e baffi
nella femmina che presenti un regolare
ciclo mestruale.
In effetti gli stati di iperandrogenismo
si accompagnano frequentemente ad
amenorrea, cioè ad eccesso di sangue.
Il fenomeno dell’“androgenizzazione
femminile”, potrebbe anche essere interpretato come adattamento alla necessità di rivestire ruoli, tradizionalmente maschili, che caratterizzano l’attuale vita della donna nelle società occidentali.
AGOPUNTURA
La problematica dell’iperandrogenismo
riguarda anche il sistema del meridiano
curioso o meraviglioso Tchong Mo.
Il sistema Tchong Mo stimola la sessualità intesa come conseguenza normale e conforme dell’ordine del Cielo
e della Terra. L’iperandrogenismo vie-
POSSIBILE RELAZIONE
TRA STRESSORI DI NATURA
AFFETTIVA ED ELETTROMAGNETICA
E STATI DI IPERANDROGENISMO
Molti studi hanno evidenziato che lo
stress elettromagnetico incide diretta-
73
LA MEDICINA BIOLOGICA OTTOBRE - DICEMBRE 2000
mente sulla funzionalità gonadica; tuttavia altri meccanismi possono essere
responsabili di una disregolazione gonadica “indiretta”.
Alterazioni della sintesi di melatonina
si verificherebbero anche nell’ambito
dei 50-60 Hertz, di comune impiego
nelle abitazioni.
Un’attivazione anomala della ghiandola pineale nelle ore notturne per fenomeni rilevanti di dispersione elettrica
(uso di coperte elettriche, materassi ad
acqua riscaldati) può avere ripercussioni sulla salute e sulla fertilità.
Alcuni ricercatori ipotizzano che
l’epifisi sia l’equivalente di un organo magnetico.
Siti ad altissima affinità per la melatonina sono stati riscontrati in molti tessuti biologici; le più alte concentrazioni
si trovano a livello dell’ipofisi, dell’ipotalamo, dell’epididimo e delle surrenali.
La melatonina è stata anche localizzata a livello del nervo ottico, dell’apparato gastroenterico e del sistema
nervoso centrale.
L’azione principale della melatonina
è antiriproduttiva, sebbene non sia noto il sito d’azione.
La melatonina è in grado, infatti, di
sopprimere la risposta delle cellule
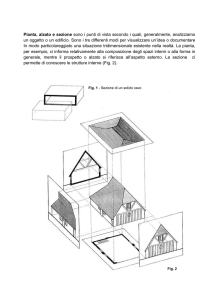
Fig. 3: Possibili modalità d’interazione tra campi elettromagnetici e organismo.
LH secernenti al GnRH in culture di
cellule ipofisarie con possibile inibizione del picco ovulatorio di LH; sono
stati, tuttavia, postulati effetti antigonadotropici mediati dai circuiti nervosi
dopaminergici, serotoninergici e GABAergici.
La melatonina inibisce la sintesi di
cortisolo ed induce un aumento della
sintesi di prolattina.
L’iperprolattinemia è una condizione
androgenizzante. Donne affette da
iperprolattinemia possono mostrare un
aumento del testosterone libero (fino al
doppio dei valori normali), diminuzione
di SHBG e moderato incremento di
DHEAS.
La prolattina, presente nel liquido
follicolare, può bloccare l’effetto stimolante dell’FSH sulla secrezione di
estrogeni da parte del follicolo graafiano in via di sviluppo.
Come gli EMF (Electro Magnetic
Fields) possano influenzare l’organismo
non è completamente documentato
(Fig. 3). I seni etmoidali e sfenoidali presentano alte concentrazione di magnetite. La magnetite è reperibile anche a
livello oculare e nel tessuto cerebrale.
In alcuni esperimenti (Cremel, Bartel; 1983), EMF deboli influenzavano
un enzima specifico necessario alla
sintesi di melatonina, il master hormone in grado di influenzare i ritmi circadiani, il ritmo sonno veglia, la sfera
sessuale, il tono dell’umore e le funzioni immunitarie.
Diversi studi hanno evidenziato che
alcune bande di frequenza favoriscono la fuoriuscita di ioni Calcio dalle
EMF 50/60 Hz
Fenomeno
di risonanza
ciclotronica
74
Fenomeno
dell'efflusso
di ioni Calcio
Interferenza
con gli organi
magnetici
cellule. Tale fenomeno, che prende il
nome di “efflusso di ioni Calcio”, influisce sull’attività proteinchinasica cellulare e su altri sistemi enzimatici che riguardano la replicazione cellulare.
L’interazione costante tra esseri umani e campo magnetico terrestre, inoltre,
potrebbe rappresentare la più interessante scoperta di questo Secolo.
Per il fenomeno di risonanza ciclotronica, la cui spiegazione esula dallo
scopo della presente trattazione, piccole quantità di energia elettromagnetica interagirebbero con il campo magnetico terrestre, provocando imponenti effetti biologici.
EMF ED INFERTILITÀ FEMMINILE
Il grande aumento di infertilità o subfertilità registrato negli ultimi anni potrebbe essere legato ad esposizione
agli EMF.
Dal 10 al 18% degli Americani in età
riproduttiva non sono fertili. L’infertilità
femminile può essere legata ad irregolarità del ciclo mestruale, squilibri ormonali, patologie dell’ovaio, delle tube,
dell’endometrio o del muco cervicale e
poliabortività.
I campi elettromagnetici possono influenzare la fertilità in vari modi. Nel
1988 Goldhaber, Polen e Hiat del Kaiser Permanent Health Group (California), hanno condotto uno studio su
1583 donne gravide. Essi hanno osservato che i soggetti che usavano il
computer (CRT cathode-ray tube) per
più di 20 ore alla settimana presentavano un’incidenza doppia di aborti rispetto a quelli che non lo usavano.
Studi successivi non hanno potuto
confermare questi dati.
Alcuni individui sono più elettrosensibili. L’elettrosensibilità sembrerebbe
più spiccata nella dinamica PNEI del
genotipo fosforico, “atopico”, immunologicamente disreattivo, simpaticotonico. Gli EMF, sommandosi a stressori
cognitivi di tipo psicoaffettivo, potreb-
LA MEDICINA BIOLOGICA OTTOBRE - DICEMBRE 2000
Stressori EM
ed ambientali
Fig. 4 (sn): Stressori di tipo psicoaffettivo ed elettromagnetico possono
attivare alcuni circuiti neuroendocrini con ripercussioni a livello surrenalico.
Attivazione
Surrenalica
Stressori
Psico - Affettivi
bero attivare circuiti neuroendocrini di
gestione dello stress, particolarmente
a livello surrenalico (Fig. 4).
Alcuni studi volti ad esaminare il rapporto tra esposizione ad EMF e risposta da stress hanno evidenziato risultati apparentemente paradossali.
In modelli animali si evidenzia un innalzamento dei livelli ematici di cortisolo. Qualora l’esposizione continui, i
livelli ormonali e la risposta immunitaria si alterano permanentemente.
Stress subliminali potrebbero influire
sulla fertilità e sullo stato immunitario.
Esposizioni, anche di breve durata,
(come l’uso di telefoni cordless) possono causare spikes ormonali nei soggetti più elettrosensibili.
Animali da esperimento di sesso
femminile mostrano risposte allo stress
elettromagnetico di tipo ormonale
(scolorimento del pelo): si deduce (per
estrapolazione) che il sesso femminile
potrebbe essere più colpito dall’esposizione agli EMF anche in termini di
funzione riproduttiva.
Modificazioni del desiderio sessuale
si accompagnano all’ipo o iperfunzionamento di surrene e tiroide. Stati di
iperprolattinemia si associano a perdita del desiderio sessuale.
STATI DI IPERANDROGENISMO
OVARICO
L’insulina è un ormone androgenizzante: stati di iperinsulinemia ed insulinoresistenza possono accompagnarsi
ad iperandrogenismo ovarico.
Fig. 5 (sotto): Sinergismo d’azione
leptina-insulina.
Anabolico
CNS
Catabolico
+
+
–
Segni
di adiposità
insulina/leptina
+
–
Assunzione
di cibo
Dispendio
energetico
+
Metabolismo
Attività fisica
–
Bilancio energetico
+
Depositi
di grasso
L'insulina ha un effetto "androgenizzante" sull'ovaio
Recettori all’insulina e all’IGF1 sono
presenti sulle cellule della granulosa
ed altre cellule dell’ovaio; insulina ed
IGF1 stimolano la steroidogenesi a livello delle cellule della granulosa, tecali e stromali, agendo in sinergia con
FSH ed LH per la stimolazione della
steroidogenesi in vitro. L’insulina aumenta il numero dei recettori all’LH e
l’IGF1 aumenta l’induzione FSH mediata dei recettori all’LH sulle cellule della
granulosa.
L’insulina è stato il primo ormone indicato nel controllo del peso da parte
del S.N.C. Sui neuroni cerebrali che
modulano l’assunzione di cibo sono
presenti i recettori per la leptina e per
l’insulina. Differenti meccanismi sottendono l’associazione di insulina e leptina per il contenuto di grasso corporeo
(Fig. 5).
La leptina (Friedman, 1994) è un ormone prodotto dal tessuto adiposo
ed informa alcuni circuiti cerebrali
di regolazione.
A livello del nucleo arcuato dell’ipotalamo il recettore per la leptina è
espresso in almeno due diverse classi
di neuroni. Una classe esprime NPY
(neuropeptide Y) e AGRP (Agouti Related Protein), due neuropeptidi che
stimolano l’assunzione di cibo. Un’altra
classe esprime POMC, il precursore
dell’α MSH (α Melanocite Stimulating
Hormone) e CART (Cocaine and
Amphetamine Regulated Transcript).
Questi ultimi due peptidi provocano
una diminuzione dell’assunzione di cibo. Altri neuroni con recettori positivi
alla leptina non esprimono nessuna di
queste molecole. I dati clinici disponi-
75
LA MEDICINA BIOLOGICA OTTOBRE - DICEMBRE 2000
bili indicano che la leptina sopprime
l’attività dei neuroni NPY/AGRP e stimola l’attività dei neuroni POMC/CART.
In assenza di leptina i neuroni
NPY/AGRP sono attivati e viene stimolata l’assunzione di cibo. In presenza
di aumentati livelli di leptina, i neuroni
POMC/CART sono attivi e l’assunzione
di cibo è ridotta. Fisiologicamente,
quando un individuo raggiunge un peso stabile, l’attività di questi meccanismi è bilanciata. Le modificazioni nella
concentrazione di leptina, si riflettono
su molti altri organi e sistemi, come la
riproduzione, il sistema immunitario e
la formazione ossea. La leptina rappresenterebbe, dunque, un’importante
molecola di modulazione dello stato
nutrizionale.
L’ipotesi che la resistenza alla leptina possa attuarsi in soggetti insulino
resistenti in sovrappeso è stata suggerita dalla presenza di elevati livelli di
leptina.
Molti meccanismi possono contribuire alla leptino-resistenza. In particolare
un potenziale meccanismo è rappresentato dal deficitario trasporto di leptina attraverso le cellule endoteliali della barriera emato-encefalica: i soggetti
obesi, infatti, presentano livelli cere-
Fig. 6: Patogenesi dell’acne.
brospinali di leptina inferiori a quelli
plasmatici.
La leptino resistenza è chiaramente
documentata nei topi (db/db) e nei ratti (fa/fa).
La leptina e l’insulina agiscono su
meccanismi effettori ipotalamici, sopprimendo i circuiti neuronali cerebrali
anabolici (che stimolano l’assunzione
di cibo e bloccano la spesa energetica) ed attivando i circuiti catabolici
(che inibiscono l’assunzione di cibo
ed aumentano la spesa energetica).
L’ingestione di cibo invia segnali di
sazietà ormonali e neuronali al nucleo
del tratto solitario: un gruppo di cellule
presenti a livello del midollo allungato
riceve i segnali di sazietà e modula i
circuiti effettori centrali leptino ed insulino sensibili, regolando, così, l’assunzione di cibo ed il bilancio energetico.
Condizioni di insulino/leptino resistenza si accompagnano a stati di iperandrogenismo; la correzione degli
stati di insulino/leptino resistenza e
dell’eventuale sovrappeso, si accompagnano a riduzione dei livelli di androgeni circolanti.
Sebbene l’obesità possa contribuire
all’insulino resistenza, anche femmine
non obese possono essere insulino resistenti. L’insulino resistenza, infatti, si
correla al grado di iperandrogenismo;
alcuni studi dimostrano la diminuzione
dell’insulino resistenza parallelamente
alla riduzione dei livelli di androgeni circolanti.
Ipersecrezione sebacea
Ipercheratosi follicolare
ACNE
Colonizzazione batterica
Infiammazione
76
Le beta endorfine stimolano, in vitro, la cellula pancreatica ß ed hanno
effetto iperinsulinemizzante; gli oppioidi inibiscono la sintesi del GnRH
agendo sul centro generatore di pulsatilità ipotalamico (iperinsulinemia
ed insulinoresistenza nel soggetto
magro?).
In condizioni di iperisulinemia il tessuto adiposo converte i preandrogeni
in testosterone; l’iperinsulinemia si associa a diminuzione delle SHBG, caratteristica degli stati di iperandrogenismo.
È ipotizzabile che il tessuto adiposo
moduli la sessualità anche in funzione
del sinergismo leptina-insulina e della
relativa insulino-leptino resistenza.
L’obesità addominale si associa frequentemente ad anomalie del ciclo
mestruale. La sindrome dell’ovaio policistico è rappresentata da anovularietà, iperandrogenismo ed obesità.
L’obesità è presente solo nel 40 %
delle donne affette da ovaio micropolicistico.
ACNE ED INVECCHIAMENTO
CUTANEO
L’acne è una malattia del follicolo
pilosebaceo i cui principali fattori patogenetici sono: 1) ipersecrezione sebacea, 2) ipercheratosi follicolare, 3)
colonizzazione batterica dei follicoli,
4) insorgenza di processo infiammatorio (Fig. 6).
La seborrea è mediata dall’aumento
degli androgeni. Si ritiene, tuttavia, che
la seborrea sia legata ad esaltata risposta della ghiandola sebacea a normali livelli di androgeni circolanti.
Una particolare attenzione meritano i
sempre più frequenti quadri di acne
tardiva che si osservano nelle giovani
donne. In tali situazioni l’associazione
con ovaio micropolicistico è presente
nel 25-30% dei casi.
I recettori cutanei agli estrogeni sono stati identificati da diversi Autori
LA MEDICINA BIOLOGICA OTTOBRE - DICEMBRE 2000
mediante tecniche di binding con
estradiolo marcato. Negli stati di iperandrogenismo cutaneo con seborrea, affini per certi aspetti a quelli della cute menopausale, l’epidermide
appare assottigliata e disidratata e il
derma ridotto di spessore e meno elastico.
Sul piano strutturale le fibre elastiche
si presentano frammentate con aumento degli spazi interfibrillari che assumono un aspetto “a lacune” completamente vuote oppure ripiene di un
materiale finemente granulare.
Il contenuto collagenico diminuisce
e compaiono alterazioni strutturali del
collagene riguardanti i legami e le interazioni tra le diverse unità della molecola.
I proteoglicani, che svolgono funzioni relative alla resistenza, alla compressione ed al grado di idratazione,
subiscono modificazioni rilevanti; viene
ridotta la componente glicidica dei glicosaminoglicani, giustificando la disidratazione cutanea.
IRSUTISMO
È la presenza di peli in zone considerate primariamente maschili.
Il disordine può essere legato a patologie ovariche, surrenaliche (tra cui
deficit parziale o totale di 11 e 21
idrossilasi o di 3 betaidrossisteroidodeidrogenasi), a dismetabolismo del
tessuto adiposo, obesità, assunzione
di androgeni o derivati del progesterone.
Quando si escludano tutte queste
cause, l’irsutismo si definisce “idiopatico” e conseguente ad aumentata sensibilità dei recettori cutanei agli androgeni secreti in quantità normale.
I tumori androgeno-secernenti sono
relativamente rari anche se la loro presenza deve essere sospettata nel caso
in cui lo stato iperandrogenico si presenti improvvisamente ed evolva rapidamente.
Natrium muriaticum
Sepia
Silicea
Calcarea Phosphorica
Sulphur
Graphites
Nux vomica
Calcarea Carbonica
STATI DI IPERANDROGENISMO
-Injeel
Farmaci
di risonanza
PNEI
ALOPECIA ANDROGENETICA
FEMMINILE
È considerata da alcuni A.A. una vera e propria patologia. Colpisce il 50 %
delle femmine sopra i 40 anni, considerando anche il “diradamento” difficilmente individuabile.
In Letteratura sono presenti vari sinonimi di alopecia androgenetica: alopecia di tipo femminile, calvizie comune
femminile ed alopecia diffusa ormonale.
La recessione bitemporale avviene
al momento della maturazione sessuale nell’80% delle femmine, anche se in
modo meno evidente rispetto alla
maggior parte dei maschi.
L’area a rischio è la parte superiore
del cuoio capelluto. Nelle femmine, tuttavia, si osserva generalmente una diffusa diminuzione in tutta l’area.
Nelle femmine con alopecia androgenetica si può osservare una diminuzione della densità dei capelli in area
frontale, posteriormente all’attaccatura
frontale. La conservazione dell’attaccatura frontale è una differenza fenotipica tra femmine e maschi che presentano alopecia androgenetica. Sebbene Aristotele avesse per primo notato che gli eunuchi non diventavano
LM
Fig. 7: Iperandrogenismo: principali
indicazioni terapeutiche.
calvi, Hamilton (1942) dimostrò la correlazione tra immaturità sessuale e
mancanza di alopecia tipica.
La 5 α reduttasi è responsabile della
conversione del testosterone in DHT
ed è presente in concentrazioni più
elevate nel cuoio capelluto di soggetti
calvi.
Sono stati identificati, a tutt’oggi, almeno due isoenzimi: 5 α reduttasi di tipo 1 e di tipo 2 con diverso Km per il
testosterone, diverso pH e diversa
sensibilità agli inibitori della 5 α reduttasi. Nelle femmine, il 50/60 % del testosterone è prodotto dalla conversione periferica di preormoni che sono,
essi stessi, androgeni deboli.
L’affinità del DHT per la globulina legante gli ormoni sessuali (SHBG), la
cui sintesi aumenta grazie agli estrogeni, supera di tre volte quella del testosterone e dell’estradiolo. La carenza di ferro è spesso associata all’alopecia androgenetica.
77
LA MEDICINA BIOLOGICA OTTOBRE - DICEMBRE 2000
TERAPIA BIOLOGICA
DELLE SINDROMI
DA IPERANDROGENISMO
L’approccio terapeutico biologico alle sindromi da iperandrogenismo femminile è complesso.
Distinguiamo due quadri fondamentali di iperandrogenismo in due Gruppi
di pazienti (Fig. 7).
Nel primo Gruppo, lo stato di iperandrogenismo si associa spesso a stati
iperprolattinemici, amenorrrea, disturbi
compulsivi dell’assunzione di cibo, disreattività immunitaria, vulnerabilità a
stressori di tipo affettivo ed elettromagnetico. Si presume che in queste pazienti sia aumentato il tono oppioide
(condizione di insulino resistenza del
soggetto magro ?).
Si ritiene appropriata, in questo ca-
so, la prescrizione di Pulsatilla, Sepia,
Silicea, Natrium muriaticum e Calcarea
Phosphorica. Vi è poi un secondo
Gruppo di femmine in cui l’iperandrogenismo si associa a problematiche
dismetaboliche, ipercolesterolemia,
turbe dell’omeostasi glicemica, obesità
addominale, insulino resistenza ed
iperinsulinemia. È frequente il riscontro
della classica sindrome dell’ovaio policistico, intesa come associazione di
iperandrogenismo, alterazioni del ciclo
mestruale, obesità, anche in assenza
di alterazioni anatomiche evidenziabili.
In questi casi è consigliata la prescrizione di Calcarea Carbonica,
Thuja, Graphites, Sulphur e Nux vomica.
In tutte le pazienti (soprattutto in
quelle appartenenti al primo Gruppo)
si deve prestare particolare attenzione
alla valutazione dello stress elettroma-
IPERINSULINEMIA
ED INSULINO/LEPTINO RESISTENZA
MEDULLA OBLONGATA SUIS
HYPOTHALAMUS SUIS
CORPUS PINEALE SUIS
PANCREAS SUIS
ADEPS SUILLUS
Syzygium compositum
Momordica compositum
Fig. 8 (sopra): Modulazione degli stati di insulino/leptino resistenza.
Thallium aceticum-Injeel f.
Thallium sulphuricum-Injeel f.
gnetico, sia in termini di esposizione
ambientale diurna che notturna.
A tale scopo si dovranno esaminare
alcuni parametri.
Per quanto riguarda la radioattività,
la Legge prevede che la popolazione
non debba essere esposta a valori superiori a 5 mSv/anno. A ciò contribuisce anche la radioattività naturale
emessa dal suolo: in Alto Adige, ad
esempio, è di circa 1 mSv/anno mentre nel Lazio è di circa 1,8 mSv/anno;
gli effetti patogeni si manifestano già a
2,6 mSv/anno.
Per i campi elettromagnetici, alle
basse frequenze domestiche (50-60
Hz), la Legge prevede che a 50 cm.
dalla fonte (es. elettrodomestici) non
siano registrabili emissioni superiori
a 100 µTesla, mentre innumerevoli
studi segnalano effetti patogeni già a
0,20 µTesla (elettrodotti ad alta tensione).
Per i segnali a radio frequenza (emittenti FM, ripetitori TV e telefonici), trasmessi cioè nell’etere, il limite è stato
fissato dalla Legge n. 381/98 a 6
Volt/metro (sembra dimostrato che
l’esposizione pluriennale a questo limite non provochi alcuna conseguenza).
Alcuni esperimenti indicano che il limite entro cui non si può rimanere
esposti per 24 ore, non deve superare
i 25 Volt/metro.
La correzione degli stati di
insulino/leptino resistenza si avvale, olCrinis humanus-Injeel
ALOPECIA ANDROGENETICA
Fig. 9 (dx): Terapia della alopecia androgenetica.
78
ORGANOTERAPICI:
Ovarium suis
Cutis suis
LA MEDICINA BIOLOGICA OTTOBRE - DICEMBRE 2000
tre che del controllo del peso corporeo, anche dell’utilizzazione di alcuni
organoterapici come Hypothalamus
suis, Corpus Pineale suis, Pancreas
suis, Adeps suillus e Medulla oblongata suis (Fig. 8).
Utili i farmaci omotossicologici a tropismo pancreatico come Syzygium
compositum e Momordica compositum;
in particolare il Syzygium, Mirtacea originaria della Malesia, aumenterebbe il
numero dei recettori all’insulina.
Per ottenere una stabilizzazione del
tono oppioide sarà utile l’assunzione di
melatonina 4CH-15CH, serotonina D6D30, triptofano D6-D30 e ACTH D6D30.
La modulazione degli stati di iperandrogenismo si avvale dell’organoterapia: Ovarium suis, Corpus luteum suis,
Glandula suprarenalis suis (da valutare
la scelta della singola diluizione D200
ad effetto inibente sull’organo) e nosodi quali Ovarialcyste-Injeel, Tuberculinum-Injeel, Acne nosode (Staufen
Pharma). Utilissima l’applicazione di
creme contenenti diluizioni decimali di
estrogeni e fattori di rivitalizzazione
cellulare.
Nelle alopecie androgenetiche, infine, si valuterà la possibilità di terapie
domiciliari o mesoterapiche con: Cutis
suis-Injeel, Crinis humanus-Injeel, Ovarium suis-Injeel, Thallium aceticumInjeel forte e Thallium sulphuricumInjeel forte (Fig. 9).
LETTERATURA
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
15.
16.
17.
CONCLUSIONE
18.
Ho cercato di esaminare la complessa problematica delle sindromi da iperandrogenismo femminile alla luce delle recenti acquisizioni.
La Terapia Biologica, priva di effetti
collaterali cerca di correggere il substrato neuroendocrino di queste sindromi ad impatto profondo sull’equilibrio psicofisico femminile.
19.
20.
21.
22.
BARBIERI R.L., MAKRIS A., RANDALL R.W. et Al. - Insulin stimulates androgen accumulation in incubations
of ovarian stroma from women with hyperandrogenism.
J Clin Endocrinological Metabolism 62 904-910, 1986.
BLACKMAN C.F. et Al. – Effects of ELF (1-120 Hz) and
modulated (50hz) RF fields on the efflux of calcium
ions from Brain Tissue in vitro. Bioelectromagnetics 6,
1985 (1-11).
BLACKMAN C.F. et Al. – Calcium efflux from brain tissue: Power density versus Internal field intensity dependencies at 50 MHz Rf. Radiation Bioelectromagnetics 1, 1989 (277-283).
BOTTACCIOLI F. – Psiconeuroimmunologia. Red Edizioni, 1995.
CONWAY G.S., HONOUR J.W., JACOBS H.S. – Heterogeneity of the polycicstic ovary syndrome: clinical,
endocrine and ultrasound features in 556 patients. Clin
Endocrinol (OXFL 30: 459 - 70, 1989).
CORGNA M. – Le sindromi atopiche cutanee nella dinamica PNEI. La Med. Biol. Luglio-Sett. 1995. pagg.
31-36.
CORGNA M., MINAUDO V. – Controllo dello stress
elettromagnetico domestico nel progresso terapeutico. La Med. Biol., Gennaio-Marzo 2000. pagg. 25-30.
DUNAIF A., GRAF M. – Insulin administration alter gonadal steroidal metabolism independent of changes in
gonadotropin secretion in insulin resistant women with
the polycistyc ovary syndrome. J Clin Invest 83, 23-29,
1989.
DUNAIF A., SCOTT D., FINEGOOD D. et Al. – The insulin sensitizing agent troglitazone improves metabolic and reproductive abnormalities in the polycistyc
ovary syndrome. J Clin Endocrin. Metab 81:32993306, 1996.
EHRMAN D.A., BARNES R.A., ROSENFIELD R.J. –
Polycistic ovary syndrome as a form of functional ovarian hyperandrogenism due to a dysregulation of androgen secretion. End Rev 16:322-343, 1995.
FELIG P., BAXTER J., FRIEDMAN L. - Endocrinology
and metabolism. MacGraw Hill, 1995.
GIVENS J.R., KURTZ B.R., KITABCHI A.E. et Al. – Reduction of hyperinsulinemia and insulin resistance by
opiate receptor blockade in the polycystic ovary syndrome with acanthosis nigricans. J Clin. Endocrinol.
Metab 64, 377-382, 1987.
LUHESHI G., GARDNER J., RUSHFORTH D., LOUDON A., ROTHWELL N. – Leptin actions on food intake and body temperature are mediated by IL-1.
Proc. Natl Acad. Sci. USA 96, 7047-7052 (1999).
MAFFEI M. et Al. – Leptin levels in human and rodent:
measurement of plasma leptin and ob RNA in obese
and weight-reduced subjects. Nature Med. 1, 11551161 (1995).
MAVROMATATAKI M. – Mitologia greca e culto Ed
Haitali, 1997.
MC EWEN B.S. – Endocrine effects on the brain and
their relationship to behaviour in G.J Siegel Basic Neurochemistry, Raven Press, New York Ved, 1994.
MOLLER D.E., FLIER J.S. - Insulin resistance mechanisms, syndromes and implications. N Eng J Med 325:
938-948,1991.
PASQUALI R., CASIMIRRI F., VENTUROLI S. et Al. Insulin resistance in patients with polycistic ovaries: its
relationship to body weight and androgen levels. Acta
endocrinologica (Copenh) 104 110-116, 1983.
PASQUALI R., ANTENUCCI D., CASIMIRRI F. et Al. –
Clinical and hormonal characteristics of obese amenorrheic women before and after weight loss. J
Clin.Endocrin. Metab 68: 173-179, 1989.
PERSINGER M.A. LUDWIG H.W, OSSENKOPP K.P. –
Physiological effects of extremely low frequency Electromagnetic fields : a review. Perceptual and motor
Skills 36 (1973).
POLK C. – Biological effects of low level low frequency
electric and magnetic fields IEEE. Transactions on
Education vol 34 n° 3 Aug 1991.
PORETSKY L. – On the paradox of insulin induced hyperandrogenismin insulin resistant states. End Rev 12,
313, 1991.
23. PORTE D. J., WOODS S., BASKIN D., SEELEY R.,
SCHWARTZ M. – Obesity, diabetes and the central
nervous system. Diabetologia 41, 863-881 (1998).
24. PUIGSERVER P. et Al. – A cold-inducible coactivator
of nuclear receptors linked to adaptive thermogenesis.
Cell 92, 829-839 (1998).
25. QU D. et Al. – A role for melanin-concentrating hormone in the central regulation of feeding behaviour. Nature 380, 243-247 (1996).
26. RIFELLI G. – Sessuologia clinica. Masson, 1996.
27. SCHWARTZ M. W., PESKIND E., RASKIND M., BOYKO
E. J., PORTE D. Jr – Cerebrospinal fluid leptin levels: relationship to plasma levels and to adiposity in humans.
Nature Med. 2, 589-593 (1996).
28. SCHWARTZ M. W. et Al. – Specificity of leptin action
on elevated blood glucose levels and hypothalamic
neuropeptide Y gene expression in ob/ob mice. Diabetes 45, 531-535 (1996).
29. SCHWARTZ M. W. et Al. – Evidence that plasma leptin
and insulin levels are associated with body adiposity
via different mechanisms. Diabetes Care 20, 14761481 (1997).
30. SCHMID F. – La Medicina Biologica. Ipsa Ed., 1991.
31. STANLEY B. G., KYRKOULI S. E., LAMPERT S., LEIBOWITZ S. F. – Neuropeptide Y chronically injected
into the hypothalamus: a powerful neurochemical inducer of hyperphagia and obesity. Peptides 7, 11891192 (1986).
32. THERIAULT G., GOLDBERG M., MILLER A.B. et Al. –
Cancer risks associated with occupational exposure
to magnetic fields among electrical utility workers in
Ontario and Quebec, Canada and France 1970-1989.
Am Epidem 1994. 139 550-572.
33. WERTHEIMER N., LEEPER E. – Adult cancer related to
electrical wires near the home. International Journey of
Epidemiology 1982. 11; 345-335.
34. YEN S.S.C. – The polycystic ovary syndrome. Clin Endocrinol (OXF)12 177-208, 1980.
Per riferimento bibliografico:
CORGNA M. – Sindromi da iperandrogenismo nella dinamica PNEI di risposta a stressori affettivi ed ambientali. La Med Biol, Ottobre-Dicembre
2000, pagg. 71-79.
Indirizzo dell’Autore:
Prof. Maria Corgna
– Specialista in Endocrinologia
– Docente e Membro del Direttivo
Scientifico A.I.O.T.
– Docente al Corso Biennale di Perfezionamento sui Prodotti di Origine
Naturale, c/o Università degli Studi
della Calabria
– Tutor in Omeopatia accreditato
dall’Ordine dei Medici di Roma
European Hospital
via Portuense, 700
00151 Roma
Email: [email protected]
Giugno 2000
79