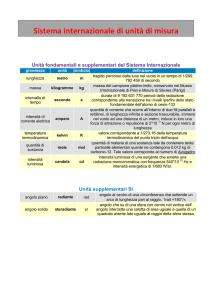
Temperatura e Calore
La materia è un sistema fisico a “molti corpi”
• Gran numero di molecole (NA=6,02·1023)
interagenti tra loro
• Descrizione mediante grandezze “macroscopiche”
(valori medi su un gran numero di particelle):
• Pressione
• Volume
• Temperatura
• Il legame con le grandezze “microscopiche” è di
tipo statistico.
Temperatura
• Rappresenta la 5a grandezza fondamentale (t,T);
• E` in correlazione con altre grandezze fisiche:
•
•
•
•
•
volume di un corpo;
pressione di un gas;
viscosità di un fluido;
resistività elettrica;
.....
Proprietà
termometriche
⇒ T è la misura dello “stato termico” di un sistema fisico
• Principio dell’equilibrio termico: “due corpi posti a
contatto raggiungono, dopo un certo tempo, la medesima
temperatura”.
• Viene misurata con il termometro:
Dilatazione termica: V(t) = Vo (1 + αt)
α=coefficiente di dilatazione termica
In un tubo:
h(t) = h o (1 + βt)
°C
100°
50°
0°
Scale termometriche
°C
K
°F
Scala normale o Celsius o C
0° ⇔ 100° H2O
200°
400°
100°
300°
0°
212°
273°
32°
200°
–100°
100°
–200°
–273°
373°
t
0°
T
scale centigrade
te
Scala Farenheit o F
9
t ( o F) = 32 o + t ( o C)
5
tf
–148°
–328°
Scala assoluta o Kelvin K
–459.4°
T (K) = t (o C) + 273,15
Unità di misura del S.I.
∆T ( K) = ∆t ( C)
o
Interpretazione microscopica
Nella materia (N = numero di molecole ≈ Na=6,02·1023):
• Moto di “agitazione termica” di atomi e molecole:
moto disordinato (gas)
vibrazioni intorno alle posizioni di equilibrio (solidi)
⇒ energia cinetica Ek
• Energia potenziale e di legame:
⇒ energia potenziale Ep
La temperatura di un corpo è correlata al livello
medio di agitazione termica nella materia
Nota: si definisce energia interna U di un sistema la quantità:
U = ∑ particelle ( Ek + E p )
U è quindi funzione della temperatura.
Calore
Due corpi messi a
contatto si portano
alla stessa
temperatura
Trasferimento di energia interna dal
corpo più caldo a quello più freddo.
Si dice che tra i due sistemi vi è stato
scambio di calore
Il calore (Q)
• è l’energia interna dei sistemi trasferita nei processi termici;
• può essere ceduto o assorbito da un corpo.
• Unità di misura (S.I.): Joule (J)
• Unità pratica di misura: caloria (cal)
è la quantità di calore necessaria ad innalzare la temperatura
di 1g di H2O da 14,5 o C a 15,5 o C.
L’equivalente meccanico della caloria è : 1 cal = 4,186 J
Nota: 1000 cal = 1 kcal = 1 Cal
Calore Specifico e Capacità Termica
La quantità di calore Q da fornire ad un corpo di massa m
affinchè la sua temperatura passi da T1 a T2 è
Q = c ⋅ m ⋅ (T2 − T1 ) = c ⋅ m ⋅ ∆T
c = “calore specifico”
C = c·m = “capacità termica”
• quantità caratteristica di ogni
materiale (vedi tabella...)
• dipende dalla massa dell’oggetto
• Unità di misura (S.I.): J/kg·K
(molto utilizzata cal/g·o C )
Ricorda:
• Unità di misura (S.I.): J/K
(molto utilizzato cal/o C o kcal/o C
∆T (Kelvin) = ∆t (Celsius)
Esempio:
1 cal/g·oC = 1 cal/g·K = 4,186·103 J/kg·K
Calore specifico di alcune sostanze a temperatura
ambiente
c
c
materiale (cal/g·oC) materiale (cal/g·oC)
acqua
1,0
glicerina
0,58
alluminio
0,22
ferro
0,83
alcool
0,55
rame
0,09
ghiaccio
0,5
mercurio
0,03
corpo umano
0,83
aria
0,23
Equilibrio Termico
Due corpi a temperature t1 e t2
(t2 > t 1) sono posti in contatto
termico, isolati dall’ambiente
circostante
Dopo un certo tempo, i due corpi
raggiungeranno una temperatura
intermedia di equilibrio tf
Applicando la conservazione
dell’energia si ottiene la
temperatura di equilibrio tf
Q1 = Q2
c1 ⋅ m1 ⋅ (t f − t1) = c2 ⋅ m2 ⋅ (t2 − t f )
t1
tf
Q1
Q2
t2
tf
c1m1t1 + c2 m2 t2
tf =
c1m1 + c2 m2
Trasformazioni di fase
Corrispondono a transizioni tra i tre diversi stati
di aggregazione della materia
solido
liquido
solidificazione
fusione
condensazione
evaporazione
liquido
gas
• Avvengono a temperatura costante, caratteristica della
sostanza in esame;
• Sono accompagnate da
- assorbimento di calore (endotermiche)
- liberazione di calore (esotermiche)
Nota: anche le trasformazioni chimiche sono trasformazioni
endotermiche o esotermiche !
Calore latente
Fusione ed evaporazione sono processi endotermici. Il calore
Q necessario alla fusione (evaporazione) di una massa m è:
Fusione
Q = kf m
T = costante
kf = calore latente di fusione
es.
Evaporazione
kf (H2O) = 80 cal/g
Q = ke m
T = costante
kf = calore latente di evaporazione
es.
ke (H2O) = 606,5-0.695·t cal/g
Alla temperatura corporea t=37 o C:
ke (H2O) = 580 cal/g
Calorimetri
Sono strumenti utilizzati per la misura della quantità di calore Q.
Questa viene ceduta ad un corpo di capacità termica nota C. Misurando
l’aumento di temperatura ∆T si ottiene:
Q = C· ∆T
La misura deve essere eseguita in contenitori
dalle pareti isolanti (vaso Dewar):
• Intercapedine vuota
⇒ conduzione e convezione
• Pareti speculari riflettenti
⇒ irraggiamento
Calorimetri
Il calorimetro delle mescolanze è utilizzato per determinare il
calore specifico incognito cx di un oggetto di massa m .
Questo viene introdotto a temperatura T2 in un recipiente
contenente una massa mH2O di acqua a temperatura T1 .
All’equilibrio si ottiene:
cx ⋅ m ⋅ (T2 − Te ) =
= cH 2O (mH 2 O + ∆m) ⋅ (Te − T1 )
Te = temperatura di equilibrio
∆m = equivalente in acqua del calorimetro:
tiene conto del calore assorbito dalle
pareti del recipiente e dall’agitatore
(è un dato fornito dal costruttore).
Bomba Calorimetrica
Serve per misurare il calore prodotto dalla combustione degli alimenti.
La combustione viene innescata attraverso
contatti elettrici.
Il calore Q sviluppato nella combustione può
essere ricavato misurando l’innalzamento di
temperatura ∆T dell’acqua
Q = cH2OmH2O ∆T
Nota:
per applicare le misure ottenute al corpo umano occorre tenere presente che
• nel corpo umano le proteine vengono metabolizzate solamente fino a prodotti
intermedi (acido urico, ammoniaca) che vengono eliminate con le egesta;
• alcune sostanze ingerite (es. cellulosa) non vengono assorbite.
Bomba Calorimetrica
Si definisce calore di combustione (o potere calorico) di un alimento il
contenuto energetico per unità di massa che viene rilasciato nel
processo di combustione:
• si esprime comunemente in kcal/gr;
• può essere determinato con la bomba calorimetrica.
Esercizio: calcolare il potere calorico del pane sapendo che quando
10g di pane vengono combusti in una bomba calorimetrica
contenente 500g di H2O alla temperatura di 17 o C, la
temperatura finale dell’acqua è di 90 o C.
[R. 3,65 kcal/g]
TERMODINAMICA dei SISTEMI BIOLOGICI
CORPO UMANO t ≈ 37°C ∆t ≈ 0
produzione energia
∆U ≈ 0
processi esotermici
ossidazione di : • carboidrati C
• grassi G
• proteine P
METABOLISMO DEL CORPO UMANO
TERMODINAMICA dei SISTEMI BIOLOGICI
produzione energia
processi esotermici
• Q interna
∆U > 0
•Q
ambiente
• L esterno
• L interno
∆U < 0
CORPO UMANO t ≈ 37°C
⇒ macchina a energia interna
η(%) = 100 L = 100 L
∆U
Q–L
∆t ≈ 0
∆U ≈ 0
(convenzione segni)
Esercizio: Supponiamo che un organismo vivente si comporti come una
macchina termica. Se l’ambiente esterno si trova alla
temperatura di 17 o C, quale dovrebbe essere la temperatura
interna affinche il rendimento sia del 20% ?
[R: 90 o C]
Processi metabolici
Esempio: ossidazione del glucosio:
C6H12O6 + 6O2 ⇒ 6CO2 + 6 H2O + 686 kcal
Si ottiene facilmente:
•
calore di combustione = 686kcal/180g = 3,8 kcal/g
•
volume di O 2 consumato (NTP: T=0o C, p=1 atm) = 6·22,4l = 134,4l
•
volume di CO 2 prodotto (NTP: T=0o C, p=1 atm) = 6·22,4l = 134,4l
•
Quoziente Respiratorio (Q.R.) = V CO2/VO2 = 1
•
Equivalente calorico dell’O 2 (anche chiamato equivalente
respiratorio o potere calorico):
KO2 = 686 kcal/134.4l = 5,1 kcal/litro
Contenuto energetico medio ed
equivalente calorico delle principali
macomolecole alimentari
Calore di combustione
[kcal/g]
Q.R =
Equivalente
VCO2
calorico [kcal/l]
= ——
O2
CO2
VO2
Prodotti di
ossidazione
Macromolecole
Bomba calorim.
Ossidazione
dell’organismo
Carboidrati
4,1
4,1
5,05
5,05
1,0
H2O + CO2
Proteine
5,4
4,2
4,47
5,57
0,8
H2O + CO2 + urea
Lipidi
9,3
9,3
4,74
6,77
0,7
H2O + CO2
4,83
5,89
0,82
Valore medio
Nota:il valore medio si riferisce alla media pesata degli
equivalenti calorici rispetto al contenuto di un pasto
standard (10% protidi, 25% lipidi e 60% glicidi).
Tasso Metabolico
Il tasso metabolico (metabolic rate MR) o potenza metabolica
rappresenta la quantità di energia consumata dal corpo nell’unità
di tempo.
− ∆U
MR =
∆t
• Si esprime in Watt (anche kcal/h, kcal/giorno, ...)
• Può essere misurato attraverso la misura del volume di ossigeno
VO2 consumato dal soggetto in un tempo ∆t
MR = kO2 ⋅
VO2
∆t
dove kO2 rappresenta l’equivalente calorico medio dell’ossigeno
relativo al pasto consumato.
Spirometro
Il volume di ossigeno consumato da un soggetto in un dato tempo può
essere determinato con uno spirometro.
Campana a
tenuta stagna
La pendenza della
retta ottenuta
rappresenta il
numero di litri di
ossigeno consumati
in un minuto
Assorbitore
di CO2
Valvole
Nota:il volume V di ossigeno ottenuto va convertito al volume V o in
condizioni normali (NTP: To=273K, po =1 atm) di ossigeno secco:
Vo =
T
( p − pH 2 O ) ⋅ V ⋅ 273 K
T ⋅ 1atm
= temperatura durante le misura;
pH2O = pressione di vapore saturo alla temperatura T.
Determinazione dell’equivalente calorico medio
Nel caso in cui sia sconosciuto il miscuglio metabolico, si può
determinare l’equivalente calorico medio kO2 misurando separatamente
VO2, VCO2 e la quantità di azoto presente nelle urine:
• il 16% dell’azoto presente nelle proteine si trova nelle urine
⇒ si determina il contenuto proteico dei cibi
• si elimina da V O2 e V CO2 la parte dovuta
all’ossidazione delle proteine e si calcola il Q.R.
dovuto all’ossidazione di carboidrati e lipidi. La
frazione di carboidrati e grassi può essere ottenuta
per interpolazione lineare.
• l’equivalente calorico kO2 è quindi la media ponderata degli equivalenti
calorici delle varie sostanze contenute nei cibi.
Nota: nella pratica si usa il valore medio corrispondente al pasto standard
(errore max ≈ 10%).
Energia fisiologica minima
Anche chiamata tasso metabolico basale (basal metabolic rate MBR) o
potenza metabolica basale è la potenza utilizzata dal corpo per le sole
funzioni vitali:
•
•
•
•
completo riposo;
digiuno da almeno 12 ore
temperatura ambiente t=20o C
tranquillità psichica
Il MBR diminuisce con l’età:
Per persone adulte di media
statura si ha circa:
MBR/m = 1,2 W/kg (uomo)
MBR/m = 1,1 W/kg (donna)
Condizioni di
metabolismo basale
Energia fisiologica minima
Gran parte dell’energia fisilogica minima viene dissipata sotto forma di
calore:
MBR ∝ superficie corporea
La produzione di energia per unità di superficie è quindi relativamente
costante:
Topo:
40 W/m2
Uomo:
50 W/m2
⇐ valore di riferimento (indice metabolico)
Elefante: 100 W/m2
Esempio: sogetto sano, Superficie corporea = 1,7 m2, massa = 70 kg
MBR= 84 W
consumo giornaliero: 7,3 MJ = 1735 kcal
MBR/massa = 1,2 W/kg
Nota: per calcolare la superficie S si può utilizzare la formula empirica
S(m2) = 0,202×massa(kg)0,425 ×altezza(m)0,725
Energia fisiologica minima
Contributi dei vari organi al metabolismo basale di un soggetto di 70 kg.
energia
consumata
(kcal/giorno)
M.B.
(%)
cuore
117
7
polmoni
35
2
reni
180
10
fegato e milza
470
27
cervello
325
19
muscoli scheletrici
310
18
rimanente
298
17
Totale
1735
100
Organo
Esercizio: un soggetto ha una superficie corporea S=1,2 m2 ed indice
metabolico pari a 33 kcal/(h·m2). Trovare
• l’energia consumata in un giorno;
[R: 950 kcal]
• la velocità di consumo dell’ossigeno in litri/h assumendo
un potere calorico dell’O2 pari a 4,63 kcal/l.
[R: 8,5 litri/h]
Attività fisica
Quando viene svolta una attività fisica, la potenza metabolica aumenta
⇒ lavoro meccanico prodotto;
⇒ aumento del ritmo cardiaco e respiratorio ed altri fabbisogni interni;
⇒ calore prodotto nelle attività muscolari.
Potenza
metabolica/massa
Attività
Dormire
[W/kg]
1,1
Potenza
metabolica/massa
Attività
[W/kg]
Pedalare
7,6
Giacere sveglio 1,2
Spalare
9,2
Sedere eretto
1,5
Nuotare
11,0
Stare in piedi
2,6
Spostare mobili 11,0
Camminare
4,3
Sciare
15,0
Rabbrividire
7,6
Correre
18,0
Esercizio: quanta energia interna è utilizzata da un uomo di 65 kg che
va in bici per due ore ?
[R: 850 kcal]
Se l’energia deriva dal metabolismo dei grassi, quanti grassi
consuma?
[R: 91 g]
Supponiamo che con una dieta di 3600 kcal/giorno il peso
della persona rimanga stabile. Se l’uomo decide di perdere
5kg andando in bici 2 ore ogni giorno, quanto tempo impiega
a raggiungere lo scopo?
[R: 55 giorni]
Se l’uomo riduce la dieta a 2800 kcal/giorno, quanto tempo
impiega a dimagrire di 5 kg?
[R: 58 giorni]
Efficienza
L’efficienza con cui viene utilizzata l’energia chimica degli alimenti
nelle attività fisiche puo essere definita come il rapporto tra la
potenza meccanica e la differenza tra la potenza metabolica in atto e
la potenza metabolica basale:
L
100
∆t
e=
%
∆U ∆U
−
∆t
∆t basale
Attività
e (%) Attività
e (%)
Nuotare in superficie
2
Girare una ruota
13
Spalare
3
Salire una scala
23
Nuotare sott’acqua
4
Pedalare
25
Sollevare pesi
9
Camminare in salita
30
Esercizio: con una efficienza del 25% un uomo compie un lavoro
dissipando 20 kcal. Calcolare il lavoro compiuto
[R: 5kcal]
Esercizio: Una donna di 20 anni e m=50 kg scala in 4 ore una montagna
alta 1000 m. La sua potenza metabolica durante questa
attività è di 7 W/kg.
Quale è la differenza tra la potenza metabolica durante
questa attività e la potenza metabolica basale ?
[R: 295 W]
Quanto lavoro compie la donna durante l’ascesa ?
[R: 4,9·105 J]
Quale è la potenza erogata ?
[R: 34 W]
Quale è l’efficienza ?
[R: 11,5 %]
Trasmissione del calore
meccanismi di trasmissione del calore
convezione
PROPAGAZIONE MEDIANTE TRASPORTO DI MATERIA
conduzione
PROPAGAZIONE SENZA TRASPORTO DI MATERIA
irraggiamento
EMISSIONE DI ONDE ELETTROMAGNETICHE
(RADIAZIONE TERMICA)
evaporazione (sistemi biologici)
Convezione
Meccanismo di propagazione tipico dei fluidi, in cui il trasporto
di calore è associato al trasporto di materia.
Esempi:
• Radiatore in una stanza;
• Acqua in una pentola;
• Nei sistemi biologici: sangue e linfa.
fornello
In generale, la quantità di calore Q scambiata in un certo tempo è
proporzionale alla superficie S del radiatore ed alla differenza di
temperatura ∆T tra radiatore e stanza:
Q ∝ S ⋅ ∆T
Conduzione
Meccanismo di propagazione del calore nei solidi
Q
S
S
= K (T2 − T1 ) = K ∆T
t
d
d
S
T1
Q
T2
K = conducibilità termica
d
A temperatura ambiente:
MATERIALI DIVERSI K (kcal m–1 s–1 °C–1)
rame
9.2 10–2
pelle secca 0.6 10–4
ghiaccio 5.2 10–4
polistirolo 9.3 10–6
acqua
1.4 10–4
aria
5.5 10–6
Irraggiamento termico
Trasmissione di calore per emissione di onde elettromagnetiche da
parte di un corpo a temperatura T. Avviene anche nel vuoto !
Esempi:
• Energia solare;
• Animali a sangue caldo emettono onde infrarosse;
• Corpi arroventati emettono luce.
Intensità della radiazione:
I=
Q
S ⋅ ∆t
Ogni corpo irradia ed assorbe calore
dall’ambiente circostante. Si ha:
I = I irradiato − I assorbito
≈ K ⋅ (Ta − Tb ) = K∆T
(W/m 2 )
I = σ T4
legge di Stefan
legge di Wien
λImax = 0.2897 (cm)
T
intensità spettrale emessa
(Wm–2 µm–1) I
109
108
107
106
105
104
103
102
10
1
(watt m–2)
10000°K
6000°K
spettro visibile(400-700 nm)
4000°K
1000°K
1 10 102 103 104 105 106
λ (nm)
Evaporazione
Meccanismo adottato nei sistemi biologici
Calore latente di evaporazione H2O
(t = 37°C) ≈ 580 cal g–1
• Processo endotermico
⇒ passaggio di calore dal corpo al
liquido che evapora;
• Non dipende dalla differenza di temperatura ∆T.
Esempio
evaporazione di 100 g H2O
58 kcal = 242.5 kJ
metabolismo basale = M.B. ≈ 50 kcal ora–1 m–2
(minima quantità di energia per garantire le funzioni vitali)
Metabolismo del corpo umano
Uomo
Organismo omotermo
∆U ≈ 0
t ≈ 37°C ∆ t ≈ 0
ossidazione di : • carboidrati C
• grassi G
• proteine P
• Q interna
∆U > 0
•Q
∆U < 0
ambiente
produzione energia
processi esotermici
Il corpo deve cedere calore all’ambiente per mantenere
costante la temperatura corporea
Trasmissione del calore nel corpo
umano
• conduzione
trasmissione interna ed esterna
contatto tra organi interni
contatto superficie cutanea con aria e vestiti
• irraggiamento
trasmissione esterna
emissione termica
• convezione
trasmissione interna
diffusione con distribuzione omogenea
Inefficaci se ∆T=0
esempio: inefficaci
se la temperatura
ambiente è
maggiore della
temperatura
corporea
del calore interno tramite sangue
• evaporazione
trasmissione esterna
sudorazione e respirazione
H 2O (t = 37°C)
≈ 580 cal g–1
Efficace anche se ∆T=0
più efficace se
l’ambiente esterno è
secco
Termoregolazione corporea
perdita di calore
kcal
ora
100
perdita totale
evaporazione
50
conduzione
irraggiamento
o 22°
26°
30°
34°
°C
t
Bassa temperatura ambiente (T<< 37 o C):
• vasocostrizione
• brividi, pelle d’oca
Alta temperatura (T ≥ 37 o C) o sforzo fisico:
• vasodilatazione
• sudorazione
Processi
regolati
dall’ipotalamo