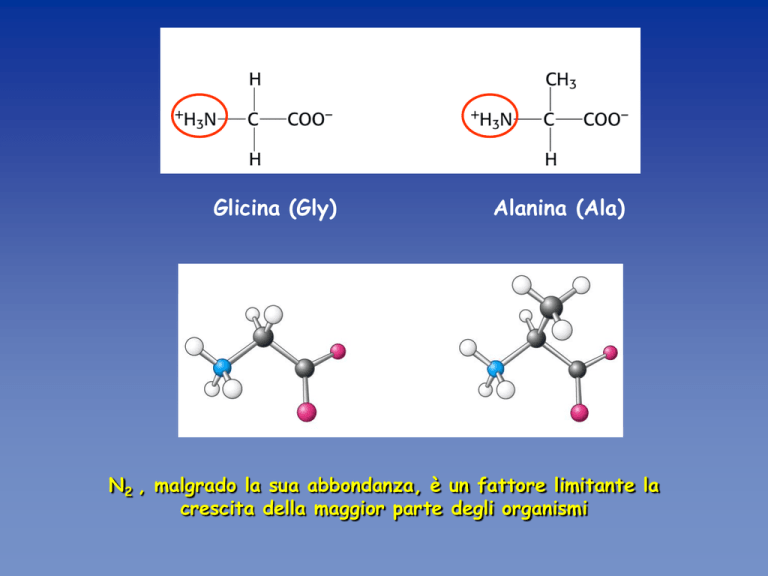
Glicina (Gly)
Alanina (Ala)
N2 , malgrado la sua abbondanza, è un fattore limitante la
crescita della maggior parte degli organismi
La digestione delle proteine
endopeptidasi
HO
R
HO
R
R
H3+N -C-C-NH-C-C-NH-C-C-NH-C-C-NH-C-COO-
R
HO
HO
R
H2 O
H3+N -C-C-NH-C-C-OR
R
HO
H O
H
R
R
+NH -C-C-NH-C-C-NH-C-COO3
R
HO
esopeptidasi
(aminopeptidasi)
HO
H
esopeptidasi
(carbossipeptidasi)
amino acidi
dipeptidi
tripeptidi
Digestione e assorbimento delle proteine
Secrezione di HCl
cellula
parietale
Digestione
H+
ATP
H+
K+
Cl-
stomaco
duodeno
aminoacidi liberi
intestino
peptidasi
aminopeptidasi
aminoacidi liberi
enterocita
sangue
pepsina
pepsinogeno
Cl-
Assorbimento
peptidi
HCl (pH 2)
K+
pancreas
autocatalisi
-
HCO3 (pH8)
enterochinasi
tripsinogeno
tripsina
tripsina
chimotripsinogeno
chimotripsina
proelastasi
elastasi
procarbossipeptidasi
carbossipeptidasi
Non essenziali
Essenziali
Alanina
Arginina
Asparagina
Istidina
Aspartato
Isoleucina
Cisteina
Leucina
Glutammato
Lisina
Glutammina
Metionina
Glicina
Fenilalanina
Prolina
Treonina
Serina
Triptofano
Tirosina
Valina
Con la dieta dobbiamo assolutamente assumere
proteine per rifornirci degli aminoacidi essenziali che
non siamo in grado di sintetizzare per non impedire
la sintesi delle proteine endogene
Proteine alimentari
Proteine tissutali
300g
100g
16g N
Sintesi proteica
Derivati non
proteici
Pool di aminoacidi
liberi
30g
16g N
NH3
chetoacidi
UREA
Purine
Pirimidine
Porfirine
Neurotrasmettitori
Ormoni
Aminozuccheri
Lipidi complessi
Deaminazione degli aminoacidi
COO|
HC-NH2
|
R
-aminoacido
NH3
COO|
C=O
|
R
-chetoacido
Proteine alimentari
Proteine tissutali
300g
100g
16g N
Sintesi proteica
Derivati non
proteici
Pool di aminoacidi
liberi
30g
16g N
NH3
Glucosio
Aa glucogenetici
Tutto l’azoto che non
utilizziamo deve essere
eliminato perché non
abbiamo alcun composto
che abbia un ruolo di
riserva di azoto o di
aminoacidi
UREA
chetoacidi
Purine
Pirimidine
Porfirine
Neurotrasmettitori
Ormoni
Aminozuccheri
Lipidi complessi
Aa chetogenetici
Acetil-CoA
Ciclo
di Krebs
ATP
Corpi chetonici
Deaminazione degli aminoacidi
COO|
H-C-NH2
|
R
-aminoacido
NH3
COO|
C=O
|
R
-chetoacido
Transaminazione
Deaminazione ossidativa
L’ammoniaca è tossica
Basi puriniche
Aminoacidi
NH3
Amine biogene
Nel plasma
[NH3] = 0,1 - 0,2 mg/100ml
(glucosio = 70-100 mg/100ml)
L’ammoniaca viene
portata al fegato per
neutralizzarla
trasformandola in
urea
fegato
urea
L’urea viene escreta
dal rene
rene
escrezione
La catena respiratoria è un complesso organizzato di
trasportatori di elettroni situato nel doppio strato
fosfolipidico della membrana interna del mitocondrio
Il suo ruolo è di permettere la riossidazione dei trasportatori di
idrogeno NADH e FADH2 a spese dell’ossigeno
L’ossidazione del NADH è separata dalla
riduzione dell’ossigeno per permettere un
maggiore recupero di energia
G° = - 52,7 Kcal/mole
NADH (H+) + ½ O2
-
NAD+ + H2O
I componenti della catena respiratoria sono ordinati secondo il loro
POTENZIALE REDOX (E°) da quello più basso (NADH) a quello più alto (O2)
1
2
3
1
2
3
Siti fosforilativi in cui si produce una quantità di energia
sufficiente per fosforilare una molecola di ADP ad ATP
4H+
+
+
+
+
4H+
2H+
+
+
+
+
- - -
+
+
-
L’energia liberata dall’ossidazione del NADH viene
utilizzata per pompare dalla matrice allo spazio
intermembrana un numero definito di protoni
NADH (H+) + ½ O2
-
-
NAD+ + H2O
G° = - 52,7 Kcal/mole
-
spazio intermembrana
matrice
4H+
+
+
+
+
4H+
2H+
+
+
+
+
- - -
+
+
-
H+
I protoni seguendo il loro gradiente rientrano
nella matrice attraverso l’ATPsintasi, il loro
passaggio fornisce la forza necessaria per la
fosforilazione dell’ADP ad ATP
-
-
Teoria chemiosmotica di Mitchell
Il
flusso
di
elettroni
lungo
la
catena
respiratoria
provoca
l’estrusione di protoni H+ dalla matrice nello spazio intermembrana
Si crea un gradiente di pH (alcalino all’interno, acido all’esterno) e
di potenziale elettrico (negativo all’interno, positivo all’esterno)
Gli ioni H+ possono attraversare la membrana mitocondriale interna
soltanto in corrispondenza di specifici canali ai quali è associata
l’ATP sintasi
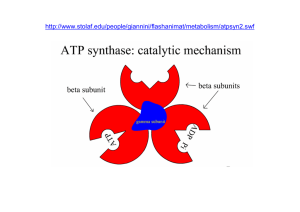
L’ATP sintasi è l’enzima che utilizza l’energia prodotta dalla caduta
di potenziale elettrochimico provocata dal rientro dei protoni nella
matrice per sintetizzare ATP
ADP + Pi
ATP
Rendimento della catena respiratoria
Per ogni NADH ossidato sono pompati verso lo
spazio intermembrana 10 H+
Per ogni FADH2 ossidato sono pompati verso lo
spazio intermembrana 6 H+
Necessari 4 H+ per formare un ATP
10/4 = 2,5 ATP formati per ogni 2 e- donati
da NADH
6/4 = 1,5 ATP formati per ogni 2 e- donati
da FADH2
Glicolisi e ciclo di Krebs: bilancio di reazione
Glucosio + 2ADP + 2Pi +2NAD+
2Piruvato + 2ATP + 2NADH + 2H2O + 2H+
3ATP
2Piruvato + 2 NAD+ + 2 CoASH
2AcetilCoA + 2NADH + 2CO2
5ATP
2Acetil-CoA+6NAD+2FAD+2GDP+2P+2H2O
Si formano 5 ATP per
ogni atomo di carbonio
ossidato
2CoASH+6NADH+2FADH2+2GTP+4CO2
15ATP
30ATP
3ATP
2ATP
b-Ossidazione: bilancio di reazione
Palmitato (C16) + 7FAD + 7NAD+ + ATP
8Acetil CoA + 7FADH2 + 7NADH, 7H+ +AMP + 2Pi
80ATP
10.5ATP
107ATP
17.5ATP
Si formano 6,7 ATP
per ogni atomo di
carbonio ossidato
glucosio
Gli
Glizuccheri
zuccheri sono composti a un livello intermedio di
ossidazione, per questo motivo dalla loro ossidazione si
ricava un po’ meno ATP
Sono però idrosolubili e quindi facilmente catabolizzabili
Sono perciò preferiti da tessuti che devono ottenere
rapidamente ATP, ad esempio il muscolo scheletrico
bianco
Meno ATP ma più rapidamente
acido palmitico
IIgrassi
grassi sono più ridotti degli zuccheri e quindi portano alla
formazione di un maggior numero di molecole di ATP
Sono però insolubili in acqua e quindi più difficilmente catabolizzabili
Sono perciò preferiti da tessuti che devono ottenere maggiori
quantità ATP, ad esempio il muscolo scheletrico rosso o il cuore
Più ATP ma più lentamente