Quattordicesima esercitazione
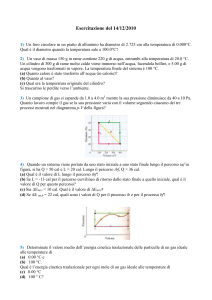
1) 0.2 moli di gas perfetto monoatomico compiono la trasformazione indicata in figura. Calcolare:
a) le temperature TA , TB e TC
b) la variazione complessiva di energia interna nella trasformazione A → B → C
c) il lavoro totale compiuto LA→C
d) il calore complessivamente assorbito (con il relativo segno)
Ris.: TA = TB = 244 K,TC = 915 K; ∆U = 1670 J, L = 500 J; Q = 2170 J
2) 3 ` di elio alla pressione di 15 atm si trovano alla temperatura iniziale di 549 K.
Il gas viene fatto espandere a pressione costante fino al volume di 6 ` e successivamente raffreddato
a volume costante fino a tornare al valore iniziale di temperatura.
a) Quanto vale la pressione finale?
b) Descrivere la trasformazione sopra indicata nel piano PV.
c) Quanto vale la variazione totale di energia interna del gas nell’intera trasformazione
d) Quanto lavoro è stato compiuto in totale dal gas?
e) Il gas ha ceduto o assorbito calore? Calcolare la quantità di calore scambiata nella trasformazione.
Ris.: Pf in = 7.5 atm; ∆U = 0; Lgas = 4.5 · 103 J; Qassorbito = 1.08 · 103 cal
3) Due grammi di azoto (N2 ; P.M.=28) alla temperatura iniziale di 0o C sono posti in un contenitore
di volume pari a 2 `, dotato di una valvola che si apre quando la pressione interna raggiunge
1.5 atm.
a) Quanto vale la pressione iniziale del gas?
b) Quanto vale la temperatura del gas quando la valvola si apre?
c) Quanto calore è stato fornito al gas per raggiungere tale temperatura?
Ris.: Pin = 0.8 atm; T = 512 K; Q = 85 cal
4) Un tubo di sezione 2 dm2 , alto 1 m è chiuso superiormente da un pistone a tenuta perfettamente
scorrevole e di massa trascurabile, mentre l’estremo inferiore è aperto e pesca per 10 cm in una
vasca piena d’acqua. Il sistema si trova a 37o C.
All’inizio il pistone si trova all’estremità superiore del tubo ed il livello
dell’acqua del tubo è uguale a quello dell’acqua nel recipiente.
L
a) Quanto vale il volume occupato dall’aria ed il numero di moli di aria
contenute nel tubo?
Se ad un certo punto si mette un peso sopra il pistone, questo si abbassa e
h
P
anche l’acqua nel tubo scende nel tubo (vedi figura) fino ad una profondità
di 8 cm al di sotto del pelo libero dell’acqua nel recipiente.
b) Quanto vale la pressione assoluta esercitata dal gas?
c) Quanto vale in queste condizioni il volume occupato dal gas (la temperatura rimane costante)?
d) Quanto vale la variazione di energia interna del gas?
Ris.: V = 18 `; n = 0.71 moli; P = 1.021 · 105 P a; Vf in = 17.86 `; ∆U = 0
5) Un recipiente adiabatico avente capacità di 150 cm3 è riempito a metà con acqua (alla temperatura
iniziale di 40o C). Il recipiente viene successivamente riempito aggiungendo olio freddo (densità
0.8 g/cm3 ; temperatura 10o C).
La temperatura finale del miscuglio diventa 25o C. Si calcolino
a) la massa dell’olio e quella del miscuglio
b) la quantità di calore ceduta dall’olio all’acqua
c) il calore specifico dell’olio
olio
o
= Qolio
Ris.: Molio = 60 g, Mmisc = 135 g; Qacqua
ass = 1125 cal; csp = 1.25 cal/g C
ced
6) Un bicchiere contiene 100 cm3 di acqua alla temperatura iniziale di 60o C. Dopo un certo tempo
la temperatura scende fino a 40o C.
Di quanto è cambiata la sua energia interna?
Quanto valgono il calore ed il lavoro scambiati con l’ambiente circostante?
Quali meccanismi possono aver provocato tale scambio? (spiegare)
Quanta acqua (a 80o C) bisogna aggiungere nel bicchiere per portare l’acqua alla temperatura
iniziale?
Ris.: ∆U = 8.36 kJ; L = 0; Q = 2 kcal; m = 100 g
7) Un blocco di ghiaccio di massa 100 g inizialmente a 0o C si trasforma in acqua a 22o C per effetto
di somministrazione di calore.
a) Quanto calore è stato complessivamente necessario? (cal. lat. ghiaccio: 80 cal/g)
Se si trascura l’effetto della modesta variazione di volume del sistema dovuta alla differente
densità di ghiaccio ed acqua cioè se si assume che il processo avvenga a volume costante, si dica:
b) quanto lavoro è stato compiuto o subito dal sistema e quale è stata la sua variazione di
energia interna
c) Quale frazione di tale variazione è attribuibile al cambiamento di energia cinetica delle
molecole d’acqua e quale frazione è invece dovuta al cambiamento di energia potenziale.
Ris.: Q = 10.2 kcal; L ∼ 0; ∆U = 42.6 kJ; cin: ∼ 20%
8) In un cilindro verticale, chiuso superiormente da un pistone scorrevole è contenuto vapor d’acqua
saturo (essendo presente sul fondo una piccola quantità di liquido).
Inizialmente il volume del recipiente è pari a 50 `, la temperatura è di 37 o C e la pressione è pari
a 47 mmHg
Successivamente il pistone viene alzato, mantenendo la temperatura costante, fino al volume di
100 `.
a) Anche la pressione e la densità del gas si mantengono costanti. Sapete spiegarne il motivo?
b) Si calcolino il valore della massa di acqua passata allo stato aeriforme (supponendo valida
la legge dei gas perfetti).
c) Si calcolino infine il valore del calore assorbito dal sistema (λ ev = 540 cal/gr), il lavoro fatto
sul sistema, la variazione di energia interna del sistema, precisando il segno di ciascuna di
tali quantità)
Ris.: m = 2.2 g; Q = 1200 cal; Lest = −Lgas = −310 J; ∆U = 4.7 kJ
9) In una giornata d’inverno viene presa dentro casa e scaldata fino a 20 o C l’aria esterna che si
trova a 0o C e che ha un’umidità relativa del 100%. Qual’è l’umidità relativa dell’aria nella casa?
vap.sat
(Dati: P0vap.sat
= 4.58 mmHg; P20
= 17.55 mmHg)
oC
oC
Ris.: u.r. = 26.1%
10) Quale è la differenza fra gas, vapori non saturi e vapori saturi?
Un cilindro, chiuso inferiormente da un pistone mobile senza alcun attrito
e di superficie pari ad 1 dm2 , si trova nella situazione indicata in figura.
Sul pistone (di massa m = 10 kg) si esercita dall’esterno la pressione
atmosferica.
All’interno del cilindro si trovano una piccola quantità di acqua (comunque
sufficiente a riempire il cilindro di vapore saturo) e azoto (N 2 ) alla temperatura di 90o C
a) Quanto vale la pressione che dall’esterno agisce sul miscuglio contenuto nel cilindro?
b) Se il cilindro è in equilibrio quanto vale la pressione parziale esercitata dal solo azoto?
c) Se inizialmente il pistone si trova ad una quota di 20 cm dalla base superiore del cilindro,
quante moli di azoto sono presenti?
d) Si descriva qualitativamente che cosa avviene quando la temperatura del sistema viene
diminuita a 15o C. Quanto vale la pressione parziale esercitata dal solo azoto?
e) Quanto vale il volume finale?
(Pressione di vapore saturo dell’acqua: Psat (90o C) = 530 mmHg Psat (15o C) = 13 mmHg)
Ris.: Pest = 0.92 · 105 P a; PN2 = 0.22 · 105 P a; nN2 = 0.015 moli; Pf in N2 = 0.9 · 105 P a;
Vf in = 0.4 `