gy
o
tol
ric
t
dia
Pe
a
ep
H
FRA
NC
ES
di
r a LLO
u
a c CIRI
CO
In the last few years, there has
been considerable progress
in the understanding of
the role of primary cilia in
various human diseases.
They sense the extracellular
environment and transduce
signals into appropriate
cellular response thus
directing embryonic
development and organ
function. Defects have
been associated with a
growing number of pediatric
conditions including
a number of complex
syndromes and a few of
organ-specific conditions.
Hepatic ciliopathies are
Congenital Hepatic Fibrosis,
Caroli Syndrome and
Disease.
Key Words
Primary cilium, hepatic ciliopathies,
children, Caroli syndrome,
congenital hepatic fibrosis
14
Le ciliopatie,
diagnosi e gestione clinica
Marco Sciveres
Epatologia Pediatrica e Trapianto di Fegato, ISMETT, University of Pittsburgh Medical Center di Palermo
Il ciglio primario, struttura e funzione
Il ciglio primario (CP) è un organello subcellulare, altamente conservato durante
l’evoluzione, presente in singola copia in numerose linee cellulari. La funzione delle cilia mobili è nota da tempo ma il CP, immobile, è stato considerato a lungo un
organello di secondaria importanza dalla funzione oscura. Tale visione è mutata
negli ultimi dieci anni, in parallelo con il tumultuoso incremento della conoscenza
della sua ultrastruttura e proteomica (contiene almeno un migliaio di proteine) (1,2).
È composto da nove coppie di microtubuli periferici e da un corpo basale che deriva dal centriolo. Si riconosce poi una zona di transizione composta da fibre a forma
di Y che si ancorano alla membrana separando fisicamente e funzionalmente la
porzione ciliare da quella cellulare. Esiste inoltre un sistema di trasporto bidirezionale altamente specializzato che provvede alla corretta localizzazione delle proteine
ed alla loro rimozione.
Il CP può definirsi come un sensore universale che permette alla cellula di rilevare
un ampio spettro di segnali extracellulari, meccanici, chimici, osmotici, termici,
elettromagnetici e di orientare di conseguenza il comportamento cellulare. Esiste
inoltre una stretta connessione con il ciclo di replicazione cellulare. Il riassorbimento del CP permette la liberazione del corpo basale che andrà poi a formare il centriolo maturo il quale, duplicandosi, fornirà gli estremi del fuso mitotico e quindi
l’orientamento spaziale della divisione mitotica (1,2).
Fisiopatologia e spettro clinico delle ciliopatie
Il malfunzionamento del CP ha conseguenze sia di tipo malformativo, se il difetto
agisce in fase embriogenetica, sia di tipo degenerativo, se perturba la capacità di rigenerazione ed omeostasi di un tessuto. Ad esempio la flessione meccanica determina l’aumento della concentrazione intracellulare di Ca attraverso l’apertura dei
canali connessi alla policistina 1 e 2 (mutate nella malattia policistica del rene autosomica dominante). Lo stesso stimolo può avvenire nell’ambito del nodo embrionario per rilevare la corrente di fluido extracellulare che regola l’informazione di lateralità così come nell’ambito del tubulo renale dell’organo adulto per rilevare il flusso
di urina. Le conseguenze saranno estremamente diverse: difetti di lateralità vs formazioni di cisti tubulari (3).
La maggior parte delle ciliopatie può essere definita come “disordine monogenico
recessivo”. La correlazione genotipo-fenotipo è estremamente complessa, in prima
analisi dipende dal gene coinvolto e dalla gravità della mutazione: una missense determina una malattia degenerativa lieve ad insorgenza tardiva, una null una malattia disembriogenetica grave ad insorgenza precoce. Sono poi possibili fenomeni di
allelismo multiplo ovvero mutazioni eterozigoti in geni funzionalmente correlati che
determinano l’insorgenza di malattia così come polimorfismi multipli possono agire
come modificatori del fenotipo.
Esistono malattie d’organo come la fibrosi epatica congenita o l’amaurosi di Leber
e malattie sindromiche nelle quali il quadro clinico è la somma delle singole anomalie, variamente combinate, ma con pattern patologici relativamente monotoni (4).
Giorn Gastr Epatol Nutr Ped 2014; Volume VI(4):14-18
Nel rene e nel fegato prevale la fibrosi e la formazione di cisti, nell’encefalo la malformazione delle strutture della linea mediana, nell’occhio la degenerazione retinica, così come possono comparire malformazioni della gabbia toracica, polidattilia, difetti di lateralità (situs
inversum, malformazioni cardiache), etc. La nefronoftisi, ad esempio può esistere in forma
isolata o come parte di sindromi con differente gravità: dal quadro relativamente benigno
della sindrome di Senior-Loken fino alle forme gravi di Sindrome di Meckel, incompatibili
con la vita già in utero (5).
Nel fegato adulto solo i colangiociti sono dotati di CP. Essi rilevano il flusso biliare, la concentrazione intraluminale di ADP e l’osmolarità della bile (6). L’integrità del sistema ciliare
è inoltre cruciale per consentire il normale sviluppo delle strutture duttali. Il coinvolgimento
epatico in tutte le ciliopatie ha un aspetto comune che è quello della malformazione del piatto duttale.
Durante la vita fetale il piatto duttale è una struttura canalicolare cilindrica indifferenziata
che decorre intorno al ramo venoso portale. L’arresto della maturazione di questa struttura
esita in una corona di dotti periferici malformati nell’ambito di una fibrosi portale densa.
Anche le strutture biliari di più grosso calibro possono mostrare dilatazioni intra o extraepatiche (7).
In Tabella 1 sono elencate le principali ciliopatie con danno epatico ed il loro possibile substrato genetico. Tra le ciliopatie epatiche d’organo si distinguono la fibrosi epatica congenita
(FEC) e la malattia di Caroli (MC) con la sindrome di Caroli (SC) definita come un overlap
tra le due [Figura 1].
Tabella 1 Elenco delle ciliopatie con interessamento epatico. Sia la fibrosi epatica congenita che la
sindrome e la malattia di Caroli sono in realtà quasi sempre associate a vari tipi di nefropatia fibrocistica, più spesso ARPKD (autosomica recessiva), ma anche (ADPKD (autosomica
dominante) o rene a spugna midollare
Malattia
Geni coinvolti
Malattie d’organo
Fibrosi epatica congenita
Sindrome di Caroli
Malattia di Caroli
PKHD1
PKHD1
?
Sindromi complesse
Meckel-Gruber
MKS1, TMEM67, CEP290, RPGRIP1L, CC2D2A
Joubert e disordini correlati (incluso COACH)
Bardet-Biedl
Oral-facial-digital Type I
Condrodisplasia di Jeune
Displasia cranioectodermica
Displasia epatorenale e pancreatica
Ellis-Van Creveld
Mainzer-Saldino
Glomerulocystic kidney disease
Nefronoftisi
AHI1, NPHP1, CEP290, TMEM67, RPGRIP1L,
ARL13B, CC2D2A
BBS1, BBS2, ARL6, BBS4, BBS5, MKKS, BBS7,
TTC8, BBS9, BBS10, TRIM32, BBS12, MKS1,
CEP290
OFD1
IFT80
?
NPHP3
EVC, EVC2
?
HNF-1b
NPHP1, INVS, NPHP3, NPHP4, IQCB1, CEP290,
GLIS2,
RPGRIP1L,
NEK8VI(4):14-18
Giorn Gastr Epatol
Nutr Ped
2014; Volume
15
Pediatric Hepatology
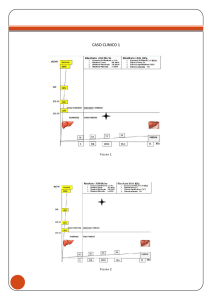
Malformazione piatto
duttale, Fibrosi
Dilatazione vie
biliari extraepatiche
Sindrome di Caroli
Dilatazione vie
biliari intraepatiche
Malattia di Caroli
Cisti del coledoco tipo 5?
Figura 1 Spettro clinico delle ciliopatie epatiche. La cisti del coledoco tipo 5
è una entità controversa, probabilmente parte di questa famiglia di disordini
La fibrosi epatica congenita/sindrome di Caroli
Queste entità, largamente prevalenti nell’ambito delle ciliopatie epatiche, condividono l’anomalia istopatologica della malformazione della placca duttale e la fibrosi massiva. Il fegato è
aumentato di volume, a contorni irregolari, di consistenza dura con ipertrofia del lobo sinistro
ed un margine inferiore quasi orizzontale, spesso apprezzabile appena al di sopra dell’ombelicale trasversa. La splenomegalia è causata dall’ipertensione portale. I dati di laboratorio sono
“inconsueti”: transaminasi, GGT, albumina ed emocoagulazione nella norma, eventuali segni di ipersplenismo (leucopenia e trombocitopenia).
Nella SC il quadro è più complesso, a quanto descritto si aggiungono delle dilatazioni sacculari delle vie biliari intraepatiche, spesso le più periferiche, e talvolta la dilatazione fusiforme del coledoco e delle principali diramazioni (8,9). Una nefropatia fibrocistica si associa
nel 90% dei casi.
La FEC “isolata” è una entità controversa. Il coinvolgimento renale è talvolta evidenziabile solo a livello subclinico. Può coesistere una tipica anomalia del sistema portale: rami
portali intraepatici che decorrono duplicati e paralleli alla periferia degli spazi portali (aspetto “a binario”), forse frutto dell’ostruzione del ramo portale primitivo.
La presentazione in epoca perinatale e neonatale è caratterizzata da un fenotipo grave che
riflette la presenza di un genotipo più sfavorevole. In essa le caratteristiche malformative
predominano e la diagnosi è spesso fatta in utero per la presenza di nefromegalia o cisti
renali e oligoidramnios. È frequentemente associata con ipoplasia polmonare e pneumotorace che richiedono una assistenza ventilatoria prolungata (9). La malattia renale è precoce e severa, vi è ipertensione refrattaria ed insufficienza d’organo precoce. La fibrosi
epatica in questo contesto assume un ruolo di secondo piano, il fenotipo prevalente è quello della SC e la diagnosi è spesso fortemente suggerita dagli elementi clinici e dall’aspetto
d’imaging. La biopsia epatica può non essere necessaria.
Quando invece la presentazione clinica si colloca dopo la prima infanzia, il fenotipo prevalente è quello della FEC paucisintomatica e con malattia renale inapparente o lieve. In
questo caso la biopsia epatica spesso è necessaria per apprezzare le lesioni tipiche (9).
La storia naturale della malattia non è caratterizzata dallo sviluppo di insufficienza d’organo. Le problematiche da gestire sono due: l’ipertensione portale e le colangiti ricorrenti. La prima è legata alla fibrosi ed è presente in entrambe le varianti cliniche. La gravità
16
Giorn Gastr Epatol Nutr Ped 2014; Volume VI(4):14-18
Le ciliopatie, diagnosi e gestione clinica
è variabile così come la propensione alla progressione; a 10 anni di età, tuttavia, il
75% dei bambini ha varici esofagee ed il 25% di essi ha sofferto di almeno un episodio di sanguinamento (9).
La possibilità di andare incontro ad episodi ricorrenti di colangite è strettamente
correlata al fenotipo SC (50% almeno un episodio). Il problema clinico può essere
relativamente lieve, in caso di episodi sporadici, che coinvolgono germi naïve, privi di
significative resistenze agli antibiotici, ma può essere anche drammatico se le dilatazioni biliari vengono colonizzate da germi multiresistenti. In questo caso gli episodi
sono ravvicinati e subentranti e può esistere un rischio quoad vitam.
Altre problematiche minori possono essere la presenza di litiasi all’interno delle dilatazioni biliari, il rischio di colangiocarcinoma che diventa concreto a partire dalla
terza decade di vita e l’ insorgenza di episodi di pancreatite qualora alla dilatazione
fusiforme del coledoco si sommi una malgiunzione dei dotti biliopancreatici con
tratto comune.
La gestione della malattia deve tenere conto della complessità del quadro e della
malattia renale. Le complicanze dell’ipertensione portale possono essere gestite conservativamente in maniera piuttosto agevole, la prognosi nei pazienti con un quadro
di FEC ad esordio tardivo è generalmente buona, la sopravvivenza con il fegato nativo a dieci anni dalla diagnosi supera il 90%. Nei casi di SC, specie se ad esordio
precoce, la prognosi è peggiore: a 10 anni dalla diagnosi il 50% dei bambini ha subito un trapianto di fegato (9). Le colangiti ricorrenti sono di per sé una indicazione
al trapianto: il timing e l’opzione di un trapianto combinato fegato/rene sono ancora
oggetto di discussione. La presenza di infezioni ricorrenti controindica il trapianto di
rene isolato; non è semplice invece valutare il potenziale residuo ed il ritmo di progressione di malattia del fegato e soprattutto del rene (10). La prognosi della nefropatia dipende dalla variante clinica. Nella SC è decisamente peggiore: l’80% dei
casi svilupperà insufficienza renale in età pediatrica. Non vi è inoltre alcuna correlazione tra l’andamento clinico dell’ipertensione portale e la funzione glomerulare:
le due problematiche decorrono parallele ed indipendenti.
La malattia di Caroli
Nel 1958 J. Caroli descrisse per primo la dilatazione congenita delle vie biliari
intraepatiche associata a malattia cistica renale. Questa rara variante (incidenza
1:1000000), caratterizzata da ectasia duttale pura senza altre anomalie epatiche,
è ora definita come “Malattia di Caroli” ed è comunemente attribuita ad un arresto del rimodellamento della placca duttale a livello dei grandi dotti biliari
intraepatici.
Le dilatazioni biliari nella MC sono più prossimali, numerose e molto spesso ospitano formazioni litiasiche: ciò condiziona esordio clinico e storia naturale della malattia. Le colangiti sono infatti la modalità di presentazione più frequente, ma la MC
può essere asintomatica per decadi o essere caratterizzata solo dalla presenza di dolori addominali ricorrenti ed epatomegalia. Possono coesistere quadri di malattia
focale con presenza di parenchima epatico sano: in questi casi il trattamento chirurgico può consistere nella resezione epatica (segmentale o lobare). Il trapianto di fegato viene riservato ai casi di malattia bilobare con ricorrenti colangiti o ipertensione
portale refrattaria.
Bibliografia
1. Hildebrandt F, Benzing T, Katsanis N. Ciliopathies. N Engl J Med 201;364(16):1533-43.
2. Fry AM, Leaper MJ, Bayliss R. The primary cilium: guardian of organ development and homeostasis.
Organogenesis 2014;10(1):62-8.
Giorn Gastr Epatol Nutr Ped 2014; Volume VI(4):14-18
17
Pediatric Hepatology
3. Waters AM, Beales PL. Ciliopathies: an expanding disease spectrum. Pediatr Nephrol 2011;26(7):1039-56.
4. Ferkol TW, Leigh MW. Ciliopathies: the central role of cilia in a spectrum of pediatric disorders. J Pediatr.
2012;160(3):366-71.
5. Hildebrandt F, Attanasio M, Otto E. Nephronophthisis: disease mechanisms of a ciliopathy. J Am Soc
Nephrol 2009;20(1):23-35.
6. Huang BQ, Masyuk TV, Muff MA et al. Isolation and characterization of cholangiocyte primary cilia.
Am J Physiol Gastrointest Liver Physiol 2006;291(3):G500-9.
7. Gunay-Aygun M. Liver and kidney disease in ciliopathies. Am J Med Genet C Semin Med Genet
200915;151C(4):296-306.
8. Alvarez F, Bernard O, Brunelle F et al. Congenital hepatic fibrosis in children. J Pediatr. 1981;99(3):370-5.
9. Rawat D, Kelly DA, Milford DV et al. Phenotypic variation and long-term outcome in children with
congenital hepatic fibrosis. J Pediatr Gastroenterol Nutr. 2013;57(2):161-6.
10.Telega G, Cronin D, Avner ED. New approaches to the autosomal recessive polycystic kidney disease
patient with dual kidney-liver complications. Pediatr Transplant 2013;17(4):328-35.
Corresponding Author
Marco Sciveres
Epatologia Pediatrica e Trapianto di Fegato
ISMETT, University of Pittsburgh Medical Center Italy
Via Tricomi, 1 - 90127 Palermo
Tel. + 39 0912192111
E-mail: [email protected]
Key Points
• La disfunzione del ciglio primario determina un gruppo numeroso ed eterogeneo di malattie.
• Vi è ampia variabilità genetica ma lo spettro clinico comprende un limitato numero di manifestazioni d’organo.
• La malattia fibrocistica del fegato è frequentemente presente ma, se isolata, configura il quadro
della Fibrosi epatica Congenita e della Malattia e Sindrome di Caroli
• I principali problemi clinici sono l’ipertensione portale e le colangiti ricorrenti.
• La gestione è scarsamente standardizzata e va ottimizzata sul singolo paziente.
18
Giorn Gastr Epatol Nutr Ped 2014; Volume VI(4):14-18