Lezione 1
Andrea Vittadini
Dip. di Scienze Chimiche
via Marzolo, 1.
Tel: 049 8275235
Email*: [email protected]
www: http://chimica.unipd.it/andrea.vittadini
*per favore, scrivere da [email protected]
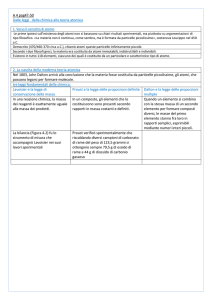
Fig. A Quadrilatero - II piano
SCALE
SCALE
P
T1
Fig. B Quadrilatero - I piano
T2
x
Arrivo
Come si arriva al mio studio (uno dei modi possibili):
1.
2.
3.
4.
Si sale al primo piano del Seminario Chimico di via Marzolo 1 (P nella Fig. A)
Attraverso il secondo tunnel a sinistra (T2) si entra nel secondo piano del “quadrilatero”.
Si segue il corridoio come nella Fig. A fino alle SCALE
Si scende di un piano, si gira a destra e si segue il corridoio come nella Fig. B.
1
Lezione 1
http://www.chimica.unipd.it/andrea.vittadini
Testi di riferimento:
Petrucci et al. “Chimica Generale” Piccin ed.
2
Lezione 1
Oxtoby et al. “Chimica Moderna” Edises ed.
Atkins & Jones. “Principi di Chimica” Zanichelli.
Zanichelli
3
Lezione 1
http://chemwiki.ucdavis.edu/
SCOPO DEL CORSO
-
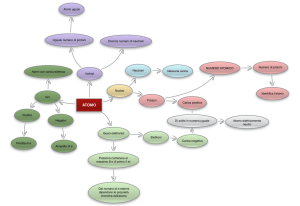
ATOMI E MOLECOLE
Conoscere la struttura dell’atomo.
Comprendere le interazioni fra atomi e molecole: il legame chimico.
Conoscere il sistema periodico degli elementi
Dare un nome ai composti chimici (inorganici)
Scrivere la formula dei composti chimici (inorganici)
Prevedere la struttura e le proprietà molecolari in base alla formula chimica.
-
PROPRIETA’ CHIMICO-FISICHE DELLA MATERIA
Stati di aggregazione e trasformazioni fisiche della materia.
Leggi dei gas.
Proprietà delle soluzioni.
-
TRASFORMAZIONI CHIMICHE
Scrivere le equazioni chimiche;
Utilizzare il concetto di mole per fare previsioni quantitative;
Comprendere il concetto di equilibrio chimico e i fattori che lo governano.
Comprendere il concetto di velocità di reazione e i fattori che la influenzano
(Cinetica chimica).
Trasformazioni con trasferimento di elettroni (Elettrochimica)
4
Lezione 1
A. A. 2006/07
Appello del 29/08/2007
Nome e cognome
Esame di Chimica 1° anno 1° trimestre
_____
numero di matricola
PARTE 1: QUESTIONARIO (RISPONDERE SUL FOGLIO)
1. Quanti protoni ci sono in 208Pb?
□ A 208
□ B 126
□ C 82
□ D 84
2. Quale dei seguenti elementi è un alogeno?
□ A Bismuto
□ B Berillio
□ C Bromo
□ D Boro
3. i. Scrivere la configurazione elettronica completa dei seguenti elementi:
A Zolfo
_____________________
B Potassio
_____________________
ii. Scrivere la configurazione elettronica utilizzando il simbolo del gas nobile
opportuno:
C Cloro
_____________________
D Ferro
_____________________
4. Dire in quale sequenza i seguenti legami sono in ordine di polarità crescente.
□ A O-H, C-H, N-H, F-H
□ B N-H, C-H, O-H, F-H
□ C C-H, N-H, O-H, F-H
□ D F-H, O-H, N-H, C-H
5. Scegliere la descrizione più appropriata per il doppio legame del’etene
(H2C=CH2)
□ A Si tratta di due legami “sigma” paralleli.
□ B Si tratta di due legami “pi greco” fra loro perpendicolari.
□ C Si tratta di un legame centrale “pi greco” con due legami “sigma” laterali.
□ D Si tratta di un legame “sigma” e di uno “pi greco”.
5
Lezione 1
6. Scrivere i nomi dei seguenti composti.
HClO
NH3
KClO4
Fe2S3
_________________
_________________
_________________
_________________
7. Scrivere le formule dei seguenti composti:
acido nitrico
_____________
pentossido di dicloro _____________
acido perclorico
_____________
cloruro di rame (II)
_____________
PARTE 2: ESERCIZI DA SVOLGERE PER ESTESO
8. Prevedere sulla base della teoria dell’orbitale molecolare quale sarà la specie
più stabile (cioè con il legame chimico più forte) tra gli ioni molecolari O2+ e
O2−
9. La sequente reazione avviene in soluzione acquosa basica:
[Fe(CN)6]3− + Cr2O3 Æ
[Fe(CN)6]4− + CrO42−
Scrivere l’equazione bilanciata usando il metodo delle semireazioni.
10. a) bilanciare la seguente reazione:
H2S + O2
Æ
H2O +
SO2
b) Se 4L di H2S vengono fatti reagire con 10L di O2 a T e P costanti, in
condizioni in cui tutte le sostanze coinvolte sono gassose, quale sarà il volume
finale della miscela gassosa?
11. Da dati tabulati, si sa che per un dato processo chimico ΔH° = 40.63 kJ/mol,
ΔS° = 108.8 J/mol·K.
Prevedere se il processo sarà spontaneo a 27 °C.
6
Lezione 1
La Chimica è la scienza che studia la materia
dell’universo, ed in particolare la sua composizione, le
sue proprietà e le sue trasformazioni
Cambiamento fisico: l’identità è conservata
Piccin Nuova Libraria S.p.A.
7
Lezione 1
Cambiamento chimico: l’identità cambia
Δ fisico
vs.
Δ chimico
Tagliare la carta
Bruciare la carta
Sciogliere zucchero
Scaldare zucchero
Sbattere un uovo
Bollire un uovo
Bollire l’acqua
Elettrolizzare acqua
Rompere un vetro
Drogare un vetro
8
Lezione 1
FIGURA 1-3 Classificazione
schematica della
materia
Sostanze,
elementi,
composti,
& miscele
Piccin Nuova Libraria S.p.A.
La chimica moderna
Robert Boyle
“The Sceptical Chymist”
(1661)
1661)
Compie numerosi esperimenti sui gas, elabora
una definizione operativa di elemento, rispolvera le
teorie atomistiche
Antoine Lavoisier
“Traité élémentaire de chimie” (1789)
1789)
Considerato il padre della chimica moderna
(Legge
Legge di conservazione della massa)
massa
John Dalton
“A New System of Chemical Philosophy” (1808)
Teoria atomica e nuova definizione di elemento
9
Lezione 1
La chimica moderna
Robert Boyle
“The Sceptical Chymist”
(1661)
1661)
Compie numerosi esperimenti sui gas, elabora
una definizione operativa di elemento, rispolvera le
teorie atomistiche
Antoine Lavoisier
“Traité élémentaire de chimie” (1789)
1789)
Considerato il padre della chimica moderna
(Legge
Legge di conservazione della massa)
massa
John Dalton
“A New System of Chemical Philosophy” (1808)
Teoria atomica e nuova definizione di elemento
Legge di conservazione della massa
(di Lavoisier)
La massa delle sostanze che si formano in
una reazione chimica è uguale alla massa
delle sostanze che partecipano alla reazione
A1 + A2 + A3 + … ⇒
B1 + B2 + B3 + …
∑ m ( A ) = ∑ m( B )
i
i
j
j
10
Lezione 1
Piccin Nuova Libraria S.p.A.
La chimica moderna
Robert Boyle
“The Sceptical Chymist”
(1661)
1661)
Compie numerosi esperimenti sui gas, elabora
una definizione operativa di elemento, rispolvera le
teorie atomistiche
Antoine Lavoisier
“Traité élémentaire de chimie” (1789)
1789)
Considerato il padre della chimica moderna
(Legge
Legge di conservazione della massa)
massa
John Dalton
“A New System of Chemical Philosophy” (1808)
Teoria atomica e nuova definizione di elemento
11
Lezione 1
John Dalton
Nuova definizione di elemento:
Gli elementi sono fatti di atomi, che
sono indistruttibili (⇒ conservazione
della massa), e identici per lo stesso
elemento.
I composti secondo Dalton
I composti sono fatti di atomi diversi combinati
fra loro in rapporti fissi.
12
Lezione 1
I composti secondo Dalton
I composti sono fatti di atomi combinati fra loro in
rapporti fissi.
Moderni “modelli molecolari” dell’ossido e biossido di carbonio
13
Lezione 1
Dalton
1808
Binnig
Rohrer
1981
Premio Nobel Fisica, 1986
Miscroscopio a effetto tunnel (STM)
I simboli degli elementi
14
Lezione 1
E poi ??
L’esistenza degli atomi sembra ragionevole, ma…
Cosa sono gli atomi?
Come si legano tra loro?
Hanno una struttura interna?
15
Lezione 1
1) L’atomo è piccolo
(∼10-10 m = 1 Å)
2) L’atomo è vuoto!
La maggior parte della massa
e tutta la carica positiva
dell’atomo sono concentrate in
una parte molto ristretta
dell’atomo detta nucleo, di
dimensioni ∼10-15
m
I costituenti dell’atomo
Particella
Massa
carica
e- elettrone
p+ protone
9.109x10-31 kg
1.673x10-27 kg
- 1.602x10 -19 C
+ 1.602x10 -19 C
n neutrone
1.675x10-27 kg
0
16
Lezione 1
Elementi e particelle
Un elemento è
determinato dal numero
dei suoi protoni
(Moseley, 1913)
•X
•Z
Z
X
simbolo dell’elemento
numero atomico = n. di protoni (determina l’identità).
¾ Elemento: è costituito da atomi con lo stesso Z
Elementi e particelle
Un elemento è
determinato dal numero
dei suoi protoni
(Moseley, 1913)
•X
•Z
•A
A
Z
X
simbolo dell’elemento
numero atomico = n. di protoni (determina l’identità).
numero di massa = n. di protoni + n. di neutroni (=n. “nucleoni”)
¾ Elemento: è costituito da atomi con lo stesso Z
¾ Atomi con lo stesso Z ma diverso A si chiamano isotopi
dell’elemento.
17
Lezione 1
Elementi e particelle
Un elemento è
determinato dal numero
dei suoi protoni
(Moseley, 1913)
•X
•Z
•A
•chg
A
Z
X
chg
simbolo dell’elemento
numero atomico = n. di protoni (determina l’identità).
numero di massa = n. di protoni + n. di neutroni (=n. “nucleoni”)
carica dell’atomo = n. protoni – n. elettroni
La caratteristiche chimiche di un atomo (isotopo) cambiano
profondamente modificando il numero dei suoi elettroni.
Unità di misura per la massa
• Unità di massa atomica (u o Da o amu/uma)
=
1
12
m (1 atomo 12C)
= 1.660538782(83) ×10−27 Kg
• Massa (isotopica) di un isotopo AX:
la sua massa espressa in u.
• Massa (isotopica) relativa di un isotopo AX:
M (AX) =
m (1 atomo AX )
1
12
m (1 atomo 12C)
18
Lezione 1
Come si contano gli atomi
(e non solo!)
• Numero di Avogadro:
NA ≈ 6.02214 1023 mol-1
= n. atomi in 12 g di 12C
• 1 NA di particelle è contenuta in
“1 mole” (mol) di sostanza
1 mol = quantità di elemento la cui
massa in g uguaglia numericamente la massa atomica
• “massa molare” di 12C: M(12C) = 12 g/mol
29.8
0%
6.85
%
13.2
2%
0.14
6%
10.0
2%
16.8
4%
23.1
3%
Miscele isotopiche naturali
massa atomica relativa (Ar) di un elemento
Ar (X) = Somma (
abbondanza
fraz. isotopo
Ar(Hg) = 200.59 ⇒
x
massa relativa
isotopo
)
M(Hg) = 200.59 g/mol
19
Lezione 1
FIGURA 2-16 Tavola periodica degli elementi
Piccin Nuova Libraria S.p.A.
Numero atomico Z
FIGURA 2-16 Tavola periodica degli elementi
Massa atomica Ar
Piccin Nuova Libraria S.p.A.
20