Neoplasie degli apparati
genitale e urinario
Ovaio
Vescica
Prostata
Testicolo
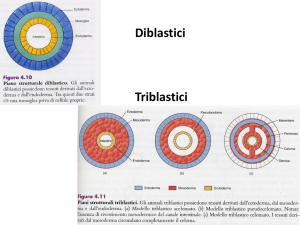
Neoplasie dell’ovaio
Anatomia patologica
Mortalità
Utero
Mammella
Pancreas
Frequenza per 100,000 donne
80
70
Ovaio
Stomaco
Polmone
Colon retto
60
50
40
30
20
10
Ovary
0
1930
1940
1950
1960
anni
1970
1980
1990
1997
Greenlee RT, et al. CA Cancer J Clin 2001;51:15-36.
Diagnosi precoce
La diagnosi precoce è rara, a causa:
Mancanza di metodi di screening, che attualmente non
è raccomandato
Tardiva comparsa di segni e sintomi
Sintomi aspecifici
Può essere utile :
Periodica visita ginecologica con esame pelvico
Ecografia transvaginale
dosaggio del marcatore specifico (CA 125)
in caso di dubbio
Utile nella diagnosi
Non raccomandato per lo screening
Istologia:
cellule di origine delle neoplasie
Classificazione istologica
Papillare sieroso (50% delle neoplasie epiteliali)
Istotipo più comune
Endometrioide (20%)
occasionalmente associato con il carcinoma endometriale
A cellule chiare (4%) e Indifferenziato (15%)
a prognosi peggiore
Neoplasie “borderline” (10%)
a comportamento meno aggressivo
Tumori a cellule germinali
Teratoma
Disgerminoma
Tumori del seno endodermico
Tumori stromali
Tumori a cellule della granulosa
Tumori a cellule di Sertoli Leydig
Caratteristiche cliniche
Le neoplasie epiteliali rappresentano
l’80%-90% delle neoplasie ovariche
Più comune forma di disseminazione:
Esfoliazione di cellule maligne attraverso
superficie epiteliale della capsula ovarica
la
Le cellule maligne circolano
nel fluido peritoneale e nei vasi
linfatici
E’ una malattia essenzialmente addominale e
solo in fase molto avanzata
interessa altri siti.
Diagnosi
radiologica
RMN:
immagine coronale
di cistoadenocarcinoma
ovarico
Stadio I
Stadio IA
Stadio IB
Stadio IC
Stadio II
Stadio IIA
Stadio IIB
Stadio IIC
Classificazione F.I.G.O.
Limitato all’ovaia
Una sola ovaia
Ambedue le ovaie
Tumore sulla superficie ovarica con rottura capsulare o ascite positiva per
cellule neoplastiche o “washing” peritoneale positivo
Estensione pelvica
Estensione a utero o tube
Maggiore estensione pelvica
IIA o IIB con rottura capsulare o ascite positiva per cellule neoplastiche o
“washing” peritoneale positivo
Stadio III
Una o due ovaie con impianto peritoneale oltrea la pelvi o linfonodi
retroperitoneali o inguinali positivi, metastasi sulla glissoniana
epatica; Interessamento del piccolo intestino o omento
Stadio IIIA
Stadio IIIB
Stadio IIIC
Grossolanamente limitato alla pelvi con linfonodi negativi ma documentato
interessamento peritoneale (microscopico)
Come sopra ma < 2 cm; linfonodi negativi
Come sopra ma > 2 cm; o linfonodi retroperitoneali o inguinali positivi
Stadio IV
Metastasi a distanza; versamento pleurico positivo; metastasi epatiche
Fattori prognostici
Stadio FIGO (TNM)
Età
Residuo patologico postchirurgico
CA 125 postchirurgico
Tipo istologico
Terapia
La strategia terapeutica dovrebbe sempre essere
concordata tra chirurgo (specialista) e oncologo
Terapia chirurgica:
Radicale per stadi precoci I e II
Citoriduttiva per stadi III peritoneali
“second look” dopo chemioterapia
Chemioterapia:
Dopo chirurgia citoriduttiva per la malattia residua
(la chirurgia è radicale solo
nello stadio I e II)
Primaria negli stadi localmente avanzati
Sono proponibili varie linee successive
Carboplatino + Paclitaxel
Doxorubicina Liposomiale (CAELIX®)
Topotecan, Gemcitabina, Oxaliplatino, Vinorelbina
Sopravvivenza per stadio
Stadio
Sopravvivenza 5 aa.
I
> 90%
II
∼ 80%
III
15% - 20%
IV
< 5%
Carcinoma della vescica
dell’urotelio
e
VIE URINARIE
Morfologia
EPITELIO
tubuli e dotti del rene
(carcinoma a cellule
chiare)
UROTELIO
pelvi
renale, uretere, vescica, uretra
(carcinoma di epitelio transizionale,
TUMORI DELLE VIE URINARIE
Epidemiologia
DATI DELLA REGIONE PIEMONTE
8000
7000
7826
6940
6000
5000
4000
Prostata
5239
5040
Vescica
Rene
3000
2000
1000
0
1961
266
223
2000
Testicolo
1832
2001
Generalità
Età DI MASSIMA INCIDENZA : 50-70 anni
Fattori predisponenti:
fumo (atipie 50% vs 4%)
esposizione professionale
(coloranti, industria della pelle)
farmaci (ciclofosfamide)
Tempo di latenza: mediana 18 anni
Screening – non previsto ma:
pazienti con storia di lesioni vescicali a basso rischio
sono seguiti con cistoscopie e citologie urinarie
periodiche
Generalità
Localizzati in:
vescica (più frequenti)
pelvi renale, uretere
Spesso multifocali
(“field cancerization”)
Caratteristiche cliniche:
ematuria (80-90%)
sintomi irritativi (frequenza urinaria)
ostruzione (uretere, pelvi renale)
Diagnosi e Stadiazione
ESAMI:
Citologia urinaria
Cistoscopia
Eco/TAC addome
TAC torace
Scintigrafia ossea
Trattamento locale
I chemioterapici endovescicali
(Doxorubicina, Mitomicina)
sono più efficaci nei tumori di basso grado
riduzione delle recidive a breve termine
scarso effetto sulle recidive a lungo termine
efficacia nel prolungamento degli intervalli liberi
scarso effetto sulla durata della sopravvivenza
hanno scarsi effetti collaterali
Il BCG è più efficace nei tumori di alto grado
Riduzione del tasso di recidive e progressione
Prolungamento della sopravvivenza
ha tossicità locale e sistemica maggiore
Carcinoma della vescica infiltrante
La cistectomia radicale è il GOLD STANDARD
per il trattamento delle neoplasie vescicali
infiltranti e superficiali ad alto rischio di recidiva
Ai pazienti con buon performance status e di età
inferiore a 70 anni viene proposto l’intervento
conservativo con neovescica ortotopica
Negli altri casi viene eseguito l’intervento di Bricker
con uretero-neocistostomia cutanea
Non viene più eseguita l’ureterosigmoidostomia
La radioterapia non può essere considerata una
valida alternativa alll’intervento chirurgico
Recidiva e malattia metastatica
risultati della terapia medica
Monochemioterapia :
Cisplatino -> risposte 24%
Paclitaxel -> risposte 46%
Polichemioterapia:
Lo standard attuale è costituito da :
Cisplatino + Gemcitabina
Carboplatino + Gemcitabina (creatinina>1.5)
Risposte complete : 20-22%
Risposte obiettive : 50-60%
Sopravvivenza mediana : 12-13 mesi
Carcinoma della prostata
ANATOMIA
Vescica
Uretra
Pene
Testicolo
Vescicola
seminale
Dotto
ejaculatorio
Prostata
Incidenza e prevalenza per età in Italia
Tasso/100.000
2.500
Incidenza
Prevalenza
2.000
1.500
1.000
500
0
< 50
50 - 54
55 - 59
60 - 64
65 - 69
70 - 74
75 - 79
> 80
Sopravvivenza a 5 anni
in relazione allo stadio
Bianchi
Neri Americani
94
Tutti gli stadi
87
100
98
Locale
32
30
Sistemico
0
20
40
60
%
80
100
Neoplasia ormonodipendente.
Network di regolazione ormonale.
Testosterone
Ipofisi
LHRH
i
en
og
tr
Es
Ipotalamo
Testicoli
LH
Prostata
PRL
AC
TH
Surrene
Cortisolo
Androgeni
surrenalici
Sedi di origine
del carcinoma prostatico
Zona Centrale
5-10%
Zona di Transizione
20%
Zona Periferica
70%
Diagnosi:
Esplorazione rettale
Finalità
–
–
–
–
noduli
consistenza
dimensioni
mobilità
Sensibilità 57-68%
Specificità 44-96%
Segni e sintomi
Malattia precoce
Zona periferica: nessuno
Zona di transizione:
Disuria (frequenza, urgenza, mitto
stentato)
Diminuita forza del mitto
Nicturia
Malattia in progressione locale
Ematospermia
Ridotto volume eiaculato
Impotenza
Malattia avanzata
Dolore osseo
Linfedema
Diagnosi:
algoritmo diagnostico dopo i 50 anni
Indagini I livello
Indagini II livello
Indagini III livello
Esplorazione rettale
PSA
Ecografia transrettale
Frazione PSA libero
Biopsia prostatica
Diagnosi: ecografia transrettale
In presenza di lesione
focale ipoecogena
Sensibilità
86-90%
Specificità
40-60%
Diagnosi: Biopsia Prostatica
indispensabile per la diagnosi di neoplasia
PSA : caratteristiche
Il PSA è un prodotto funzionale secreto dall’epitelio
prostatico normale per lisare il coagulo seminale
Il PSA non è un marcatore cancro-specifico
I livelli di PSA aumentano anche per:
–Adenoma prostatico voluminoso
–Flogosi acuta o cronica
–Visita urologica con o senza esami strumentali.
PSA : valore nelle neoplasie
L’85-90% del PSA totale
è legato all’α-1-ACT
(antichimotripsina)
Rapporto
Libero/Totale
Cut-off: 0,15
Adenoma
Neoplasia
ISTOLOGIA : grading secondo indice di Gleason
Gleason
grado
1
2
3
4
5
Storia naturale
PIN* alto grado
OrmonoLocalmente
Locale avanzato
Metastatico refrattario
TxN0M0
T3-4
Tempo (anni)
*: PIN, prostatic intraepithelial neoplasia
D1.5 D2 D2.5 D3
Terapia
PIN* alto grado
OrmonoLocalmente
Locale avanzato
Metastatico refrattario
TxN0M0
Tempo (anni)
T3-4
Prostatectomia
Radioterapia
‘Watchful waiting’
D1.5 D2 D2.5 D3
Ormonoterapia
Radioterapia
Ormonoterapia
‘Watchful waiting’
*: PIN, prostatic intraepithelial neoplasia
Chemoterapia
Risultati dell’Ormonoterapia
Diagnosi di malattia stadi III/IV
(45% - 55% delle nuove diagnosi di carcinoma prostatico)
TERAPIA ORMONALE
85% Risponde
(PSA riduz. ≥ 50%)
20% raggiunge il
“Disease-Free Status”
e sospende la terapia
80% Risponde parzialmente
e
continua la terapia
Durata mediana della risposta:
3 anni
15% Fallisce
Diventa ormonorefrattario
Sopravvivenza mediana:
6-12 mesi dalla diagnosi
Terapia della malattia avanzata
ORMONOTERAPIA
(Orchiectomia)
LH-RH analoghi :
LEUPRORELIN
GOSERELIN
TRIPTORELIN
BUSERELIN
Antiandrogeni periferici:
TERAPIA SUCCESSIVA
Sospensione del farmaco
antiandrogeno
Ormonoterapia di
seconda linea
(con diverso antiandrogeno)
Chemioterapia
BICALUTAMIDE
CIPROTERONE
FLUTAMIDE
DOCETAXEL
Blocco androgenico totale
(analogo + antiandrogeno)
VINORELBINA
MITOXANTRONE
Carcinoma del testicolo
Tumori germinali e seminoma
del Testicolo
Epidemiologia
3 picchi di incidenza:
Infanzia (fino a 15 anni) : carcinoma embrionario
20-35 anni
>50 aa. : seminoma
nuovi casi: 2-3/100.000/anno in USA
1-2% sono bilaterali
Maggiore frequenza nel testicolo ritenuto
soltanto 1-2% di rischio di insorgenza di un
secondo tumore primitivo nel testicolo controlaterale
Classificazione istologica
Tumori Germinali (90-95%)
Seminoma (35%)
Non-seminoma (65%)
Carcinoma Embrionario (20%)
Teratoma (5%)
Corio-carcinoma (<1%)
Istologia mista (40%)
Tumori Non-germinali (5-10%)
Tumore a cellule di Leydig
Tumore a cellule di Sertoli
Gonadoblastoma
Diagnosi e stadiazione
Ecografia testicolare (tumefazione
dolente)
Orchiectomia- indispensabile per la
diagnosi istologica
Sono vietate le agobiopsie trans-scrotali
Tac addomino-pelvica / toracica /
cerebrale
TC/PET globale corporea
Diagnosi e stadiazione
Markers neoplastici
Fondamentali per la diagnosi
differenziale
e per il monitoraggio
del trattamento
AFP (alfa-fetoproteina)
Tempo di dimezzamento (T½) : 5-7 giorni
Non elevata nel seminoma e nel teratoma puro
B-hCG (beta-coriongonadotropina umana)
Tempo di dimezzamento (T½) : 18-36 ore
Elevata nei non-seminomi
Minimamente elevata in alcuni seminomi
LDH
Indicatore prognostico non specifico, molto attendibile
Trattamento
Stadio I
Orchiectomia Radicale -> osservazione
Guarigione nel 100% dei pazienti
Stadio II
Orchiectomia + linfoadenectomia retroperitoneale
Chemioterapia adiuvante : 3 cicli di BEP
(Bleomicina, Etoposide, Cisplatino)
guarigione nel 98-99% dei pazienti
Stadio III
Con chemioterapia (3 cicli BEP) guarigione nel 70-80%
Stadio IV
Oltre il 70% dei pazienti sono vivi a 5 anni dopo
polichemioterapia con 1-3 linee (BEP – PEI – GEMOX)
Conclusioni
I tumori del testicolo sono guaribili
L’orchiectomia è indispensabile per la diagnosi
I markers tumorali non sono elevati nel
seminoma (Beta-HCG minimamente)
L’autoesame dei testicoli è importante in
pazienti con storia di testicolo ritenuto
Prima della chemioterapia è indispensabile la
crioconservazione del liquido seminale
Nello Stadio I non c’è bisogno di chemioterapia
La Chemioterapia funziona ..!!
Conclusioni
Non c’è bisogno di chiamarsi
LANCE ARMSTRONG
Per avere una buona prospettiva di vita
Quando ci si ammala di un carcinoma del
testicolo, anche se in stadio avanzato
CARMINE, 35 anni, muratore,
residente e curato ad Asti
sposato con 3 figli naturali
15 anni dopo la chemioterapia
(multiple metastasi polmonari bilaterali)
Grazie per l’attenzione !