PANCREAS ENDOCRINO
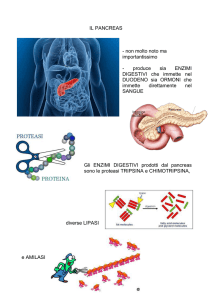
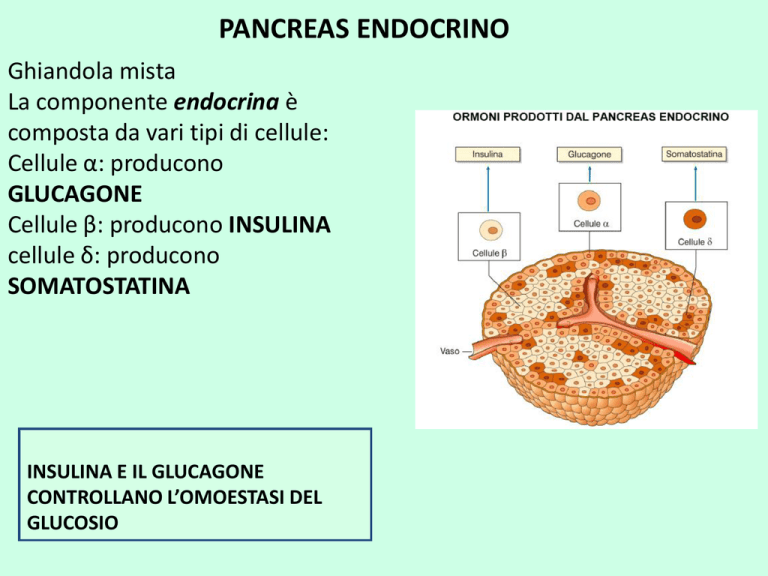
Ghiandola mista
La componente endocrina è
composta da vari tipi di cellule:
Cellule α: producono
GLUCAGONE
Cellule β: producono INSULINA
cellule δ: producono
SOMATOSTATINA
INSULINA E IL GLUCAGONE
CONTROLLANO L’OMOESTASI DEL
GLUCOSIO
SINTESI DI UN ORMONE PEPTIDICO: PREPROORMONE,
PROORMONE, ORMONE+PEPTIDI, SECREZIONE
MECCANISMO D’AZIONE DI UN ORMONE PEPTIDICO
SINTESI DELL’INSULINA: ORMONE PEPTIDICO
• I° Fase: immediata (secondi) insulina
già presente nella cellula
• II° Fase: tardiva dopo “de novo” sintesi
dell’ormone
La secrezione di insulina è regolata mediante un meccanismo a feedback dai livelli di principi
nutritivi apportati con la dieta. La molecola centrale nei meccanismi di regolazione è il
glucosio. Infatti la secrezione di insulina è praticamente nulla quando il glucosio plasmatico è
uguale o inferiore a 50 mg/dl, mentre è massima quando la glicemia è uguale o superiore a 250
mg/dl.
L’ insulina stimola la captazione di glucosio e di aminoacidi da parte dei tessuti, mentre inibisce
la liberazione di glucosio, acidi grassi e aminoacidi e la chetogenesi. L’ effetto netto è
rappresentato dalla diminuzione dei livelli plasmaticidi questi substrati.
MECCANISMO DI SECREZIONE DELL’INSULINA
GLUCOSIO
GLUCOSIO-P
[ATP]/[ADP]
_
K+
SECREZIONE
DEL’INSULINA
[Ca2+]
DV
MECCANISMO D’AZIONE DELL’INSULINA
IL RECETTORE PER L’INSULINA E’ UN TETRAMERO IN CUI LE SUBUNITA’ a
INIBISCONO L’ATTIVITA’ CATALITICA INTRINSECA DELLE SUBUNITA’ b. IL LEGAME
DELL’INSULINA CON LE SUBUNITA’ a RIMUOVE QUESTA INIBIZIONE
REGOLAZIONE MEDIATA DALL’INSULINA
FOSFORILAZIONE SUBSTRATO
RECETTORE INSULINA IRS
FOSFORILAZIONE DELL’ENZIMA FOSFADITILINOSITOLO-3
CHINASI (PI3K) CON ATTIVAZIONE DELLA VIA PI-3k-PkB
FOSFORILAZIONE DELLA PROTEINA LEGANTE I
RECETTORI DEI FATTORI DI CRESCITA GRB2, CON
ATTIVAZIONE DELLA VIA SoS-Ras-MAPK
REGOLAZIONE DEL METABOLISMO
FOSFORILAZIONE SUBSTRATO
RECETTORE INSULINA IRS
ATTIVAZIONE DELL’ENZIMA PI3K CHE
CONVERTE IL LIPIDE DI MEMBRANA PIP2 IN
PIP3
PIP3 SI LEGA ALLA PROTEIN CHINASI B
LA PKB ATTIVATA DALLA PDK1, VA AD
ATTIVARE LE SUE PROTEINE BERSAGLIO
COME LA: GLICOGENO SINTASI CHINASI 3
CHE FOSFORILATA VIENE INATTIVATA E SI
ATTIVA LA SINTESI DEL GLICOGENO
REGOLAZIONE DEL METABOLISMO
LA PDK1 VA A FOSFORILARE ANCHE LA
CHINASI INIBENTE L’APOPTOSI, AKT E QUESTA
FOSFORILA GLUT4, CHE RAGGIUNGE LA
MEMBRANA PLASMATICA E PERMETTE
L’INGRESSO DEL GLUCOSIO
NEL DIABETE INSULINO-RESISTENZA VIENE A
MANCARE PROPRIO QUESTA VIA
REGOLAMENTO DELLA TRASCRIZIONE GENICA
FOSFORILAZIONE SUBSTRATO RECETTORE
INSULINA IRS
QUESTO FOSFORILATO SI LEGA ALLA
PROTEINA GRB2
GRB2 ATTIVA SOS, PERMETTENDO LA
SOSTITUZIONE DI GDP CON GTP NELLA
PROTEINA RAS
RAS ATTIVA ATTIVA LA PROTEIN CHINASI RAF-1
RAF-1 FOSFORILA MEK
MEK FOSFORILA MAPK, CHE ATTIVATA ENTRA
NEL NUCLEOE ATTIVA FATTORI DI TRASCRIZIONE
DI UN GRUPPO DI GENI PER LA DIVISIONE
CELLULARE
PRINCIPALI AZIONI DELL’INSULINA
L’AZIONE PIU’ EVIDENTE DELL’INSULINA E’ QUELLA IPOGLICEMIZZANTE. QUESTO
EFFETTO E’ IL RISULTATO DELL’AZIONE DELL’INSULINA SU MUSCOLO, FEGATO E
TESSUTO ADIPOSO:
1) NELLE CELLULE ADIPOSE E MUSCOLARI AUMENTA LA CAPTAZIONE DEL
GLUCOSIO MEDIANTE UN’AZIONE PERMISSIVA SUL PROCESSO DI TRASPORTO.
QUESTA AZIONE RIFLETTE L’AUMENTO DEL NUMERO DI TRASPORTATORI DEL TIPO
GLUT-4 NELLA MEMBRANA PLASMATICA, IN SEGUITO SIA ALLA TRASLOCAZIONE
DALLE MEMBRANE INTERNE A QUELLE DI SUPERFICIE CHA ALL’AUMENTO DEI
PROCESSI DI TRASCRIZIONE DEL GENE DEL GLUT-4
2) NEL FEGATO STIMOLA LA CAPTAZIONE DEL GLUCOSIO AUMENTANDO LA
FOSFORILAZIONE DEL GLUCOSIO (AUMENTO SINTESI GLUCOCHINASI) E
L’UTILIZZO DEL GLUCOSIO PER LA SINTESI DI GLICOGENO E PER IL METABOLISMO
ENERGETICO
3) NEL MUSCOLO AUMENTA LA SINTESI DI PROTEINE E DI GLICOGENO
4) NEL TESSUTO ADIPOSO RIDUCE LA DEGRADAZIONE DEI TRIGLICERIDI E NE
FAVORISCHE LA SINTESI
glucagone
ormone iperglicemizzante
polipeptide di 29 amminoacidi (PM 3.485)
unica catena lineare che, una volta passata in circolo, si avvolge su se stessa in modo
casuale
la biosintesi avviene in modo analogo all’insulina con formazione di pre-proglucagone (PM 18.000) da cui deriva, per distacco di catene polipeptidiche, di proglucagone (PM 12.000) di 100 aa già parzialmente attivo, da cui deriva l’ormone
attivo
il proglucagone viene sintetizzato anche in certe cellule dell’intestino tenue e
dell’encefalo, ma non viene trasformato in glucagone
si trova accumulato nelle cellule α in granuli secretori dai quali viene liberato per
esocitosi
produzione giornaliera di 100-160 g che determina un livello ematico di 100-150
pg/ml
ha un emivita nel sangue circolante di ~ 6 min
fattori che influenzano la secrezione di glucagone
glucosio ematico: una diminuzione della concentrazione ematica di glucosio stimola la
secrezione di glucagone. Le concentrazioni di glucagone ematico sono più alte a digiuno e
tendono a diminuire dopo un pasto
amminoacidi: stimolano la secrezione di glucagone, in particolare l’arginina. L’aumento sia
di glucagone che di insulina dopo un pasto proteico, funziona come meccanismo protettivo
per garantire che i livelli ematici di glucosio sia mantenuti
acidi grassi: un aumento di acidi grassi circolanti inibisce la secrezione di glucagone
insulina: la glicemia elevata inibisce la secrezione di glucagone in presenza di insulina. Se
l’insulina è mancante, le cellule α non sono in grado di rilevare l’aumento di glucosio
ematico e i livelli di glucagone rimangono alti.
ormoni gastroenterici: gastrina e colecistochinina stimolano la produzione di glucagone,
mentre la secretina e la somatostatina la inibiscono
sistema nervoso autonomo: l’innervazione ortosimpatica del pancreas e un’aumentata
concentrazione di catecolamine surrenali stimola la produzione di glucagone
meccanismo d’azione del glucagone
glucagone
recettore
adenilato
ciclasi
β
γ
GDP
α
proteina G
citosol
GTP
α
GDP GTP
ATP
AMPc
subunità regolatrice
PKA
inattiva
cAMP
PKA attiva
ATP
ADP
fosforilasi chinasi
inattiva
fosforilasi chinasi –PO4
attiva
Ca2+
ATP
glucosio
sangue
glucosio -6-PO4
glicolisi e ciclo di Krebs
ADP
fosforilasi b
inattiva
fosforilasi a –PO4
attiva
glucosio -1-PO4
PO43-
glicogeno
diabete mellito
infezione virale
reazioni immunitarie
anticorpi contro le
cellule β
cellula β
anticorpo contro il recettore
anticorpi contro
l’insulina
difetti nella
sintesi
difetto recettoriale
II messaggero
difetto nella
secrezione
insulina
sangue
trasporto di glucosio
insulino-dipendente
difetto a livello
del recettore
difetto postrecettoriale
risposta
cellula
bersaglio
rappresenta una malattia cronica del metabolismo dovuta alla carenza di insulina oppure
ad una ridotta efficacia di quest’ormone. I difetti possono verificare a vari livelli.
Sintomi:
•
iperglicemia che non si osserva soltanto in situazione postprandiale, ma anche in caso di
digiuno
•
aumento della diuresi (poliuria)
•
aumento della sete (polidipsia) e della fame (polifagia)
•
associati ad una diminuzione del peso corporeo.
Classificazione del diabete mellito
Diabete di tipo 1
una malattia tipicamente AUTO-IMMUNE, anche se esistono
forme “idiopatiche”
il meccanismo principale è la profonda carenza insulinica
interessa essenzialmente bambini e adolescenti
Diabete di tipo 2
iperglicemia legata a insulino-resistenza (= difetto di azione
dell’insulina) + carenza insulinica relativa e progressiva.
interessa essenzialmente l’adulto e rappresenta la forma di
diabete PIU’ FREQUENTE
comune associazione con obesità e altre malattie metaboliche
Altre forme di diabete mellito
• Diabete secondario
– Malattie endocrine,patologie pancreatiche, farmaci..
– Alcune forme sono reversibili
• Malattie genetiche
– Difetti genetici della secrezione o dell’azione dell’insulina
– Sindrome genetiche complesse con diabete
• Diabete gestazionale
– > 30 % sviluppano diabete di tipo 2 nel corso della vita
Il diabete mellito di tipo 1
• Malattia auto-immune caratterizzata da infiltrazione linfocitaria
(linfociti T) delle isole di Langherans pancreatiche, seguita da
progressiva distruzione delle cellule b-pancreatiche e
profonda carenza di produzione insulinica
La carenza insulinica determina l’incapacità delle cellule (in
particolare adipose e muscolari) ad utilizzare il glucosio,
con 2 conseguenze immediate:
1.
Accumulo di glucosio nel plasma iperglicemia marcata
superamento della soglia renale di riassorbimento
glicosuria poliuria poliurodipsia
2.
Utilizzo di fonti alternative di energia
Riserve lipidiche perdità di massa grassa
Riserve proteiche perdità di massa magra
(muscolare)
La cheto-acidosi diabetica
•
Se la situazione precedente continua ad evolvere perché
non diagnosticata in tempo si verificano:
1.
Disidratazione severa per poliuria
ipotensione, tachicardia, torpore..
2.
Produzione massiccia di corpi chetonici
acidosi metabolica (cheto-acidosi) con iperventilazione secondaria
e turbe digestive (vomito..) che peggiorano la disidratazione
•
La cheto-acidosi è una complicanza spontaneamente
fatale del diabete di tipo 1
Fisiopatologia del diabete di tipo 2
• Caratterizzato da 2 elementi essenziali
– Insulino-resistenza: inadeguata utilizazione del glucosio da parte delle
cellule, che non rispondono normalmente alla stimolazione insulinica;
il difetto può essere di tipo pre-recettoriale, recettoriale o postrecettoriale.
– Difetto della b-cellula: anche se inizialmente relativo (la secrezione
insulinica è a lungo conservata), è ormai ammesso che l’insorgenza del
diabete di tipo 2 è legata a una produzione di insulina insufficiente a
compensare la resistenza insulinica
Fattori di rischio per il diabete di tipo 2
•
Il diabete di tipo 2 è il più frequente (> 90 % dei casi di diabete)
•
Tipicamente caratteristico dell’ età matura (> 40 anni), interessa
pazienti sempre più giovani
• Fattori di rischio
–
–
–
–
Familiarità ++ (ereditarietà multigenica)
Età
Obesità
Stile di vita: alimentazione e sedentarietà
• Patologie associate (frequenti)
– Dislipidemia, sindrome metabolica..
Alterazioni biochimiche dei tessuti secondarie
all’iperglicemia cronica
•
Glicosilazione di numerosi proteine cellulari e extra-cellulari
– Emoglobina glicosilata e fruttosamina circolanti (markers di equilibrio glicemico)
– Glicosilazione di collagene e proteine a lunga vita con formazione di complessi
AGE che alterano la matrice vascolare contribuiscono a microangiopatia
/glomerulopatia.
• Stress ossidativo
.
– Aumentata produzione di ione superossido (0 ) a livello della catena respiratoria
mitocondriale, di radicali liberi, con diminuzione di NO
disfuzione endoteliale che favorisce l’ateroma e le sue complicanze.
•
Aumentata produzione di sorbitolo (via dei polioli)
– Glucosio sorbitolo poco diffusibile rigonfiamento cellulare osmotico es:
cataratta
Le complicanze del diabete
• La microangiopatia diabetica
– Alterazioni specifiche del microcircolo
retinopatia, nefropatia e neuropatia diabetiche
• La macroangiopatia diabetica
– Ateromatosi precoce e diffusa complicanze cardiovascolari
• Altre complicanze
– Aumentata sensibilità alle infezioni
– Cataratta
– Piede diabetico