PROGRAMMA DI BIOLOGIA /Scienze della Terra/ Chimica
Anno scolastico 2013/14 classe 4^D e E Scienze Applicate:
SCIENZE DELLA TERRA
La crosta terrestre: minerali e rocce
I costituenti della crosta terrestre
I minerali
Le rocce
Rocce magmatiche
L’origine dei magmi
Le rocce sedimentarie
Le rocce metamorfiche
Il ciclo litogenetico
I fenomeni vulcanici
Il vulcanismo
Edifici vulcanici, tipi di eruzione e prodotti dell’attività vulcanica
Vulcanismo effusivo ed esplosivo
Fenomeni di vulcanismo secondario
I fenomeni sismici
·Lo studio dei terremoti
Propagazione e registrazione delle onde sismiche
La forza di un terremoto : intensità e magnitudo a confronto
Le scale di intensità
Gli effetti del terremoto
Terremoti all’interno della terra
La distribuzione geografica dei terremoti
BIOLOGIA
L’organizzazione del corpo umano
Omeostasi
I processi della vita
Le cavità corporee
I termini dell’anatomia
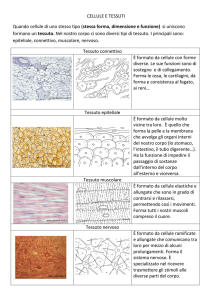
Le cellule e i tessuti
Tessuto epiteliale
Tessuto connettivo
Tessuto muscolare
Tessuto osseo
Tessuto nervoso
Le membrane del corpo
L’apparato tegumentario
La pelle
Gli annessi cutanei
Le funzioni della pelle
L’apparato cardiovascolare
Le funzioni del sangue
I componenti del sangue
L’emostasi
I gruppi sanguigni
La struttura e l’organizzazione del cuore
Il flusso ematico nel cuore
Il battito cardiaco
Il ciclo cardiaco
I fattori che influenzano la frequenza cardiaca
La struttura e le funzioni dei vasi sanguigni
Il flusso ematico nei vasi sanguigni
Vie di distribuzione del sangue
IL TESSUTO NERVOSO:
Panoramica del sistema nervoso
L’istologia del tessuto nervoso
I potenziali d’azione
La trasmissione sinaptica
IL SISTEMA NERVOSO:
La struttura del midollo spinale
Le trentuno coppie di nervi spinali
Le funzioni del midollo spinale
L’encefalo
Le dodici coppie di nervi cranici
Le componenti del sistema nervoso periferico
La struttura del sistema nervoso autonomo
GLI ORGANI DI SENSO
Sensibilità specifica: il senso della vista
Sensibilità specifica: il senso del’udito
L’apparato endocrino
Il lavoro degli ormoni
La ghiandola pineale
L’ipotalamo e l’ipofisi
La tiroide
Le ghiandole paratiroidi
Le isole pancreatiche
Le ghiandole surrenali
L’apparato urinario e l’equilibrio idrosalino
La struttura del rene
Le funzioni dei nefroni
Il percorso dell’urina
L’equilibrio dei fluidi corporei
Gli elettroliti nei fluidi corporei
L’equilibrio acido-base dell’organismo
PROGRAMMA DI CHIMICA
Anno scolastico 2013/14 classe 4^D /E Scienze Applicate
Le proprietà delle soluzioni:
La concentrazione delle soluzioni (%m/m,m/v,V/vMolarità,Molalità,Frazione molare e Normalità)
L’effetto del soluto sul solvente: le proprietà colligative
La tensione di vapore delle soluzioni: la legge di Raoult
L’innalzamento ebullioscopico e l’abbassamento crioscopico
L’osmosi e la pressione osmotica
Le reazioni chimiche
Le equazioni di reazione
I calcoli stechiometrici
Reagente limitante e reagente in eccesso
La resa di reazione
I vari tipi di reazione: sintesi, decomposizione, scambio semplice, doppio
scambio
L’energia si trasferisce
I sistemi scambiano l’energia con l’ambiente
L’energia chimica si trasforma in energia termica e viceversa
Le funzioni di stato
Il primo principio della termodinamica
Le reazioni di combustione
Il calore e l’entalpia di reazione
Le trasformazioni spontanee e non spontanee
L’entropia e il secondo principio della termodinamica
L’energia libera di Gibbs
La velocità di reazione
L’equazione cinetica
I fattori che influiscono sulla velocità di reazione
La teoria degli urti
L’energia di attivazione
Il meccanismo di reazione
L’equilibrio chimico
L’equilibrio dinamico
L’equilibrio chimico
La costante di equilibrio
Il quoziente di reazione
La costante di equilibrio e la temperatura
La termodinamica dell’equilibrio
Il principio di Le Chatelier
Acidi e basi si scambiano protoni
Le teorie sugli acidi e sulle basi
La ionizzazione dell’acqua
Il pH-La forza degli acidi e della basi
Come calcolare il pH di soluzioni acide e basiche
Come misurare il pH
La reazione di neutralizzazione
La titolazione acido base
L’idrolisi
Le soluzioni tampone
Le reazioni di ossido-riduzione
Il numero di ossidazione
Ossidazione e riduzione
Come si bilanciano le reazioni redox
Gli equivalenti e la normalità nelle reazioni redox
L’elettrochimica
La chimica dell’elettricità
Reazioni redox spontanee e non spontanee
Le pile - La scala dei potenziali standard di reazione
Le pile in commercio
L’elettrolisi e la cella elettrolitica
Parabiago 5/6/2014
Firma Alunni
Firma Insegnante