CHIMICA ORGANICA III
CORSO DI LAUREA IN CHIMICA anno accademico 2009-2010
Prof. Daria Giacomini
PROGRAMMA DETTAGLIATO
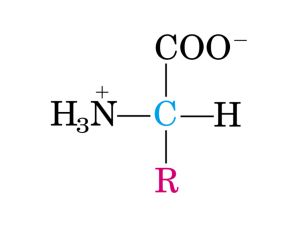
AMMINOACIDI E PEPTIDI
(ref: V.Santagada, G. Caliendo Peptidi e Peptidomimetici)
Le sostanze Naturali: classificazione in metaboliti primari e secondari.
La classe degli amminoacidi, suddivisione in amminoacidi proteinogenici e non proteinogenici. Esempi di alfa,
beta, gamma amminoacidi.
Analisi dettagliata degli Amminoacidi Proteinogenici: presenza e implicazioni nella struttura di proteine
Amminoacidi non polari: Glicina, Alanina (D- ed L-Alanina e beta-alanina), Valina, Leucina, Isoleucina,
Prolina.
Amminoacidi non polari con residui aromatici: Fenilalanina ( L-Dopa, catecolammine-Adrenalina,
Aspartame). Triptofano (Serotonina, Melatonina, Triptamina. Sintesi della gramina attraverso reazione di
Mannich).
Amminoacidi con residui alcolici: Serina (sito attivo degli enzimi, glicosilazione con Nacetilglucosammina, Omoserina). Treonina (Allo-Treonina), Tirosina (tiroxina, modificazioni post-trasduzionali).
Amminoacidi con residui solforati: Cisteina (ossidazione a cistina, denaturazione di proteine, ossidazione
ad acido cisteico e formazione di Taurina, omocisteina, Glutatione) Metionina. Discussione sugli stati di
ossidazione dei composti organici solforati.
Amminoacidi Acidi: Acido Aspartico, Acido Glutammico (Glutammati)
Amminoacidi con residui azotati: Asparagina, Glutammina.
Amminoacidi Basici: Lisina, Arginina( approfondimento su gruppi funzionali guanidina e ammidina DBU,
DBN, creatina e Istamina) Istidina.
Reazioni degli amminoacidi con Ninidrina.
REAZIONI DI AMMINOACIDI
Formazione di Idantoine, tioidantoine, dichetopiperazione e reazione con ninidrina.
PROPRIETA' DI AMMINOACIDI
Proprietà chimico-fisiche degli amminoacidi. Punto isoelettrico ed equazione di Henderson-Hasselbach.
SINTESI DI AMMINOACIDI
Amminazione di -bromo esteri. Esempi: sintesi malonica della leucina, Sintesi di Gabriel della metionina.
Sintesi di Strecker e Strecker modificata.
Amminazione Riduttiva a partire da acido piruvico.
Sintesi asimmetriche di amminoacidi (cenni sulla riduzione enantiselettiva per idrogenazione asimmetrica con
catalizzatori di Nojori). Risoluzione di miscela racemiche.
Sequenziamento di Peptidi: determinazione N-terminale determinazione del C-terminale
SINTESI DI PEPTIDI (ref: Najera C. SynLett 2002, 1388, Albericio et alii. ChemRev 2009, 2455):
Problemi nella sintesi peptidica: Formazione di Azlattoni, Dichetopiperazine ed Idantoine.
Sintesi Lineare e Sintesi Convergente.
Strategia Razionale per la sintesi Peptidica: utilizzo di gruppi protettori.
Definizione di Gruppo protettore, di gruppo protettore permanente e temporaneo.
Protezioni ortogonali, stabilità ortogonale ed instabilità modulata.
Caratteristiche dei gruppi protettori per la sintesi peptidica.
Gruppi protettori della funzione amminica (Boc, Cbz, Fmoc, tritile, benzile -reazione di Birch) condizioni di
inserimento, stabilità ortogonale e rimozione.
Gruppi protettori della funzione carbossilica (esteri metilici ed etilici, benzilici e t-butilici) condizioni di
inserimento, stabilità ortogonale e rimozione.
Gruppi protettori delle funzioni sulle catene laterali degli amminoacidi: strategia della protezione minima.
Attivazione della funzione acido-carbossilico per ilo coupling peptidico (formazione di cloruri acilici, ed
anidridi miste ed esteri attivati).
Reagenti di Coupling peptidico: Carbodiimmidi (DCC, EDC, e promotori DMAP e HBTU).
Esempio di una sintesi in soluzione di un tripeptide.
Sintesi di peptidi in fase solida: ancoraggio su resina (resina di Merrifield e di Wang), strategia Fmoc su fase
solida
CARBOIDRATI
(ref: Brown, Chimica Organica; J.Gorzynski Smith, Chimica Organica)
Definizione e caratteristiche strutturali.
Monosaccaridi: aldosi e chetosi. Albero genealogico dei monosaccaridi derivanti dalla D-gliceraldeide.
Esempi di amminozuccheri. Formazione intramolecolare di emiacetali, strutture piranosidiche e furanosidiche
dei monosaccaridi. Mutarotazione degli zuccheri.
Reazioni dei Monosaccaridi
Riduzione. Analisi e stereochimica degli alditoli.
Ossidazioni con reattivi di Tollens, Feheling e acido iodidrico.
Acidi aldonici, aldarici ed uronici. Lattonizzazione di acidi aldonici ed aldarici.
Trasformazione dell'acido glucuronico in Vitamina C.
Reazioni dei gruppi ossidrilici: formazione di metileteri, acetati e acetonidi.
Formazione di glicosidi. Definizione di aglicone.
Aspetti stereochimici nella formazione di glicosidi. Esempio di sintesi della salicina.
Definizione di Nucleoside, e basi nucleotidiche, esempio di sintesi di un nucleoside.
Disaccaridi. Strutture di Saccarosio, Tetralosio, cellobiosio e Lattosio
Polisaccaridi. Cellulosa, Amido (amilosio e amilopectina)
STEREOCHIMICA
(ref: IUPAC Gold Book, , L.G.Wade J.Chem Edu. 2006, 83(12),1793. A.Ault J.Chem.Edu. 2008, 85 (3) 441. Mislow
J.Am.Chem.Soc. 1984, 106, 3319. E.Eliel, Stereochemistry of organic compounds).
Siti web: www.cem.msu.edu/~reusch/VirtualText/intro1.htm
www.chemgapedia
Approfondimenti su stereocentri, centro, asse e piano di chiralità.
Analisi stereochimica degli alditoli, degli acidi aldarici. e dei cicloesani sostituiti.
Stereochimica dei sistemi Biciclici (fusione trans e cis di decaline e steroidi)
Nomenclatura dei sistemi Biciclici (Anelli isolati, fusi, pontati e spirani).
LIPIDI
(ref: Smith, Chimica Organica)
Definizione e classificazione (lipidi idrolizzabili e non-idrolizzabili).
Cere. Struttura e proprietà.
Triacilgliceroli (Trigliceridi). Trigliceridi semplici e misti. Grassi e Oli. Struttura e proprietà.
Acidi Grassi. Nomenclatura e strutture degli acidi grassi saturi ed insaturi. Reazione di ossidazione degli acidi
grassi
Saponi e Detergenti.
Eicosanoidi. Proprietà e strutture. Biogenesi per ciclossigenazione dell'acido arachidonico. Prostaglandine,
Prostacicline, Trombossani e Leucotrieni.
Terpeni. Caratteristiche strutturali e riconoscimento delle unita' isopreniche.
Esempi di Monoterpeni Sesquiterpeni, Diterpeni e Carotenoidi.
Steroidi. Caratteristiche strutturali, alcuni esempi.
REAZIONI PERICICLICHE
(ref: Smith, Chimica Organica; Norman e Coxon, Principi di Sintesi Organica; Clayden, Greeves, Warren,
Wothers, Organic Chemistry)
Definizione e classificazione delle reazioni pericicliche.
Cicloaddizioni: definizione e differenza con le reazioni di ciclizzazione.
Cicloaddizione [4+2] di Diels-Alder e Cicloaddizione [2+2]
Analisi degli orbitali molecolari (MO) di frontiera (Teoria di Fukui) e regole di selezione per reazioni termiche o
fotochimiche.
Analisi dei reagenti della Diels-Alder: caratteristiche del diene (conformazione e sostituenti) ed esempi dei
dieni più utilizzati. Caratteristiche del dienofilo ed esempi delle molecole più utilizzate.
Stereochimica e Regiochimica della reazione di Diels-Alder.
Esempi di Diels-Alder utilizzate nella sintesi di prodotti naturali e di steroidi.
Elettrocicliche: definizione ed esempi.
Analisi degli MO e condizioni di selezione chiusura conrotatoria e disrotatoria.
Esempi.
Sigmatropiche: definizione ed esempi.
Shift di legame sigma C-H e shift di C-C.
Rezione di Cope e di Claisen.
Sintesi di Fisher dell'indolo.
REAZIONI DI TRASPOSIZIONE (RIARRANGIAMENTI)
(ref: Norman e Coxon, Principi di Sintesi Organica; Clayden, Greeves, Warren, Wothers, Organic Chemistry)
Migrazioni al carbonio elettron deficiente.
Trasposizione di Wagner-Meerwein di carbocationi. Trasposizione Pinacolica
Attitudine migratoria e stereochimica della trasposizione.
Migrazioni all'azoto: Trasposizione di Beckmann con esempi
Migrazioni all'ossigeno: Trasposizione di Bayer-Villiger con esempi.