Università degli Studi del Piemonte Orientale “A. Avogadro”
CORSO DI ALTA FORMAZIONE IN LEGISLAZIONE
ALIMENTARE
Metodi per il rilevamento degli OGM in matrici
alimentari: principi ed i metodi di analisi basati sulla
ricerca del DNA e delle proteine
Dott.ssa Patrizia Cesaro
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Gli Organismi Geneticamente Modificati sono BATTERI,
FUNGHI, VIRUS, PIANTE e ANIMALI le cui caratteristiche
genetiche sono state modificate in laboratorio. In genere UNO O
PIÙ GENI PRESI DA ALTRI ORGANISMI vengono introdotti nel
patrimonio ereditario dell’organismo (DNA) che si vuole
modificare (Definizione giuridica in Direttiva 2001/18/CE).
IL GENE/I INSERITO CODIFICA
PARTICOLARE INTERESSE
PER
UN
TRATTO
DI
Le applicazioni degli OGM investono gli ambiti più disparati; la
MEDICINA, L'ECOLOGIA, IL SETTORE AGRO-ALIMENTARE e
ZOO-TECNICO. Meno conosciuto, ma molto importante dal
punto di vista medico, è il loro utilizzo in campo farmaceutico,
dove hanno consentito la produzione di vaccini sicuri.
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
• Il DNA è la sede
dell’informazione
genetica
• È presente nel
nucleo
di
ogni
cellula
• È identico per
ogni cellula dello
stesso organismo
• Successione
di
nucleotidi contenti
le basi azotate A, T,
CeG
• Numero di geni
variabile a seconda
dell’organismo
• Diversi
livelli
organizzazione
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
TUTTE LE PIANTE OGGI COLTIVATE SONO GENETICAMENTE MODIFICATE
o GENETICAMENTE MIGLIORATE
Il principale obiettivo del miglioramento genetico delle piante coltivate è
quello di ottenere varietà con caratteristiche PRODUTTIVE, QUALITATIVE e
di RESISTENZA AGLI STRESS migliori di quelle varietà già disponibili sul
mercato.
METODOLOGIE USATE:
• incrocio
SELEZIONE
• mutagenesi (uso di radiazioni che provocano mutazioni)
SELEZIONE
• trasferimento genico
SELEZIONE
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
COMPONENTI DI UN COSTRUTTO O CASSETTA DI
ESPRESSIONE PER OTTENERE PIANTE GM
promotore
GENE
terminatore
ELEMENTI REGOLATORI DELLA TRASCRIZIONE E TRADUZIONE:
- promotore e terminatore
- sito di legame per il ribosoma
GENE: - gene di interesse
- gene reporter
- marcatore di selezione
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
METODI PER IL RILEVAMENTO DEGLI OGM
NEGLI ALIMENTI (DETECTION)
1. RICERCA DELLE PROTEINE
2. ANALISI DEL DNA
Qualunque sia la tecnica utilizzata,
per garantirerisultati affidabili è
necessario ottimizzarne vari aspetti
legati alla qualità: PROCEDURE,
REAGENTI e STRUMENTAZIONE.
Risulta
pertanto
di
cruciale
importanza la “VALIDAZIONE” dei
metodi.
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
TANTO PIU’ UN PRODOTTO E’ GREZZO TANTO PIU’ E’ FACILE
ISOLARE ED ANALIZZARE L’ANALITA
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Limite consentito <1% (10 volte superiore al limite di rilevabilità
0,1%, che rappresenta la più bassa soglia scientificamente
difendibile per la quantificazione di materiale OGM) 3 motivi:
•
STATISTICA (0,1% la variabilità delle ripetizioni è statisticamente accettabile)
•
TECNICA (0,1% per evitare errori tecnici dovuti al limite di sensibilità di un metodo che in
realtà è 0,01%)
•
CAMPIONAMENTO (una quantificazione affidabile al 0,1% richiede almeno 10000
fagioli di soia, 2,5kg, se si scende a 0,01% occorrerebbero 25kg
di grani)
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
CAMPIONAMENTO
• Gli schemi per il campionamento degli OGM si basano sulle
procedure utilizzate per l’analisi delle micotossine. La direttiva
98/53 (Direttiva 98/53/CE del 16 luglio 1998, GUCE L 201 del
17/7/1998, pag. 93) riguardante il campionamento e l’analisi di
alcuni contaminanti negli alimenti è stata la prima linea guida di
campionamento per gli OGM ed è oggi ancora utilizzata, ma ce ne
sono altre più recenti.
• Il materiale OGM NON ha una distribuzione omogenea, di
conseguenza la rappresentatività del campionamento sta alla base
di tutta l’analisi. Per questo è indispensabile effettuare il prelievo
in modo ACCURATO, cercando di CAMPIONARE DIVERSI PUNTI
DEL PRODOTTO.
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Come si eseguono le analisi?
Tre livelli:
campione
- RILEVAMENTO (presenza/assenza OGM)
- IDENTIFICAZIONE (dell’evento di trasformazione)
RILEVAMENTO
- QUANTIFICAZIONE (determinazione %)
negativo
positivo
IDENTIFICAZIONE
È autorizzato?
< 1%
no etichetta
> 1%
QUANTIFICAZIONE
sì
no
È ILLEGALE
etichetta obbligatoria
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Metodi basati sulla RICERCA DELLE PROTEINE
Il transgene codifica per una PROTEINA
Metodi con un basso LIVELLO TECNOLOGICO si tratta di:
• saggi immunologici BASATI SUL RICONOSCIMENTRO ANTIGENEANTICORPO
• che consentono analisi qualitative e quantitative
• in cui l’analita deve essere conosciuto
9
9
9
Western blot
ELISA
Lateral flow assay
Limiti: - localizzazione della proteina
- le proteine non devono essere degradate
USATI PER IL CONTROLLO DI SEMENTI E MATERIE PRIME
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
IL LATERAL FLOW ASSAY
• Basso costo
• Facilità di esecuzione
NON QUANTITATIVO
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Lateral Flow Strip Protocol
2
1
3
1. Punch leaf disc
2. Add buffer and
grind in tube
3. Insert flow strips
for testing
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
OGM Sì
OGM No
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Limite detection 1seme/1000 semi
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
TEST ELISA
• Analisi quantitativa, alta sensibilità, economico
• Ideale per analisi di laboratorio
• Sono processabili + campioni contemporaneamente
• Possibilità di automatizzare il saggio
• Disponibili kit commerciali
• Sono necessarie proteine NON denaturate
Provette singole o
piastre multipozzetto
Enzyme-labelled Antiantibody antibody
antibody specific
to antigen
Blocking protein
well
Colour Response
Concentration
Dependent
Antigen
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
TEST ELISA: PRINCIPIO del Sandwich
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
TEST ELISA: PRINCIPIO
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Western Blotting
• Test QUALITATIVO altamente specifico
• usato in ricerca
Metodi basati sulla RICERCA DEL DNA
Metodi con un MEDIO-ALTO LIVELLO TECNOLOGICO basati su:
• Polymerase Chain Reaction (PCR end point, PCR quantitativa),
• ibridazione con sonde (Southern blot, microchip GMO)
RILEVAMENTO GENERICO: si utilizzano primers o sonde specifici per sequenze
molto usate per la costruzione di OGM (p35S CaMV, tnos3’ A. tumefaciens, ecc.).
RILEVAMENTO SPECIFICO: si utilizzano primers o sonde per lo specifico evento
di trasformazione (transgene).
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
campione
estrazione DNA
RILEVAMENTO GENERICO (PCR end-point, ibridazione con sonde)
negativo
positivo
IDENTIFICAZIONE - rilevamento SPECIFICO
(PCR end-point, ibridazione con sonde)
È autorizzato?
no
sì
ILLEGALE
< 1%
no etichetta
QUANTIFICAZIONE (PCR quantitativa)
> 1%
etichetta
obbligatoria
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
QUALITATIVA
Verifica DNA estratto (PCR end-point con primers universali per geni di pianta)
Per una buona riuscita dell’analisi sono importanti:
1. CAMPIONAMENTO
2. PREPARAZIONE dell’ANALITA (estrazione e purificazione)
3. ANALISI QUALITATIVA e QUANTITATIVA dell’ANALITA
L’OBIETTIVO PRIMARIO DEI METODI DI ESTRAZIONE È QUELLO DI
OTTENERE DNA CON IL PIÙ BASSO LIVELLO DI DEGRADAZIONE
POSSIBILE
Es.: ESTRAZIONE DNA
2. Preparazione dell’analita: metodi di estrazione: CLASSICI (CTAB)
COMMERCIALI (resine brevettate)
COMBINATI
3. Analisi qualitativa e quantitativa del DNA: lettura allo spettrofotometro (260 e 280 nm)
Quantità: 1 unità assorbanza 260nm = 50 µg ds DNA/ml
Qualità (purezza): rapporto assorbanza 260nm/280nm (1,7-1,9)
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
METODI DI RILEVAMENTO GENERICO E SPECIFICO
M +ve
• Southern Blot
•
•
•
•
•
•
Frammentazione del DNA dell’OGM mediante
digestione enzimatica
corsa e separazione dei frammenti su gel d’agaroso
trasferimento del DNA su membrana di nilon
incubazione con la sonda molecolare
sviluppo mediante autoradiografia
M
Corso di Alta Formazione in Legislazione Alimentare
-ve
M
P32 labelled
probe
Alessandria 21 maggio 2010
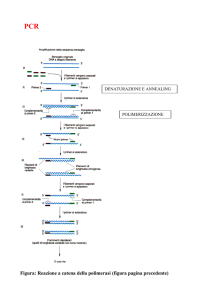
• PCR end-point
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Rendimento teorico di molecole di DNA che si
formano a partire da una singola molecola stampo:
N° molecole finali = N x 2C
N= n° di molecole iniziali
C= n° cicli
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
PCR FRAGMENT CONFIRMATION
FALSI NEGATIVI:
FALSI POSITIVI:
amplificazione di un gene di pianta per verificare la
presenza del DNA nel campione analizzato
- digestione enzimatica dell’amplificati
- ibridazione con sonde specifiche (southern blot)
- sequenziamento
- PCR con primers interni al frammento amplificato
(NESTED PCR)
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
ESEMPIO: RICERCA SOIA GM
Primer per le-1 ¼ 118bp
Primer per transgene ¼ 169bp
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
campione
estrazione DNA
RILEVAMENTO GENERICO (PCR end-point, ibridazione con sonde)
negativo
positivo
IDENTIFICAZIONE - rilevamento SPECIFICO
(PCR end-point, ibridazione con sonde)
È autorizzato?
no
QUALITATIVA
Verifica DNA estratto (PCR end-point con primers universali per geni di pianta)
sì
ILLEGALE
< 1%
no etichetta
QUANTIFICAZIONE (PCR quantitativa)
> 1%
etichetta
obbligatoria
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
METODI DI QUANTIFICAZIONE: LA REAL TIME PCR
COS’È:
è una reazione PCR che può essere seguita in tempo reale (mentre avviene);
la quantità di DNA che si sintetizza può essere misurata ad ogni ciclo PCR
pratica
• La crescita esponenziale è limitata
• Segue una crescita lineare
• Il plateau non è correlato alla quantità
iniziale del DNA
La REAL TIME PCR
misura il DNA ad ogni ciclo
Corso di Alta Formazione in Legislazione Alimentare
teoria
PCR
misura il DNA end-point
(saturazione)
Alessandria 21 maggio 2010
PCR quantitativa
• Rilevamento della fluorescenza associata all’amplificazione
• Il prodotto di PCR non viene analizzato su gel di agarosio
• Analisi del prodotto di fluorescenza tramite computer
Plot lineare
Incremento di
fluorescenza
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Chimiche fluorescenti
per PCR Real-Time
LA FLUORESCENZA SI GENERA DURANTE LA PCR PER EFFETTO
DI DIVERSE POSSIBILI REAZIONI CHIMICHE
Le chimiche principali sono basate:
• sul legame di coloranti fluorescenti che si intercalano in modo
aspecifico nella doppia elica di DNA (SYBR Green);
• sia sull'ibridazione di sonde specifiche per il frammento di interesse
marcate con molecole fluorescenti (Dual-labeled (come le sonde
TaqMan) Molecular beacons, Scorpion, sonde FRET (Fluorescence
Resonance Energy Transfer))
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Fluorescenza
Curve di amplificazione
Plot lineare
Cicli di amplificazione
Per ogni campione si ottiene una curva di amplificazione
il cui CT (=Threshold Cycle) è inversamente
proporzionale alla quantità di templato iniziale
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Normalised reporter fluorescence (Rn)
Plot di amplificazione
Linea soglia scelta
d a l l ’ o p e r a t o r e
In maniera da intersecare le
curve di tutti i campioni nella
fase esponenziale
Indica il valore al di
sopra del quale inizia
l’accumulo di un
a m p l i f i c a t o PCR cycle number
Corso di Alta Formazione in Legislazione Alimentare
E’ il ciclo della reazione di
amplificazione in cui il segnale
di fluorescenza del campione
è maggiore rispetto a quello
della linea soglia (Threshold)
Alessandria 21 maggio 2010
Analisi tramite software
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
DNA DI RIFERIMENTO (STANDARD)
STANDARD COMMERCIALI
• OGM
• 0% OGM
È necessario produrre almeno 5 diluizioni dello stesso standard
allo scopo di costruire una curva standard
I campioni da determinare vengono affiancati agli standard ed ai
controlli NEGATIVI (H2O)
È necessario produrre almeno 3 repliche sia per ogni campione sia
per gli standard per aumentare l’affidabilità del risultato
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
STANDARD DI RIFERIMENTO
Un “CALIBRATORE” è una qualsiasi matrice da cui si ottiene
un DNA a percentuale nota di transgene con cui vengono
costruite le curve di taratura. Viene di norma utilizzato
Materiale di Riferimento Certificato (CRM) a percentuale nota
di OGM (w/w); si tratta di farine a granulometria finissima e
controllata, preparate da Institute for Reference Materials and
Measurements (IRMM, Belgio) e commercializzate dalla ditta
Fluka.
Sono disponibili in commercio per l’analisi quantitativa farine
standard a contenuto di OGM pari a 0%, 0,1%, 0,5%, 1%, 2%,
5% per i principali eventi transgenici.
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
CURVA STANDARD
La retta di regressione deve avere un coefficiente correlazione il più possibile
vicino a 1 e un valore di pendenza il più possibile vicino a 3,322. La pendenza
della retta è indice dell’efficienza di reazione
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Quantificazione con METODO DELLA CURVA STANDARD
La quantità di DNA dei campioni deve essere compresa all’interno
della curva degli standard per un calcolo affidabile
Ct
10 1
35
10 2
10 3
unknown sample
10 4
25
10 5
10 6
3500 copies
10 7
15
1
2
3
4
log10 quantity
Corso di Alta Formazione in Legislazione Alimentare
5
6
7
Alessandria 21 maggio 2010
gene endogeno
Corso di Alta Formazione in Legislazione Alimentare
transgene
Alessandria 21 maggio 2010
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Kit commerciali basati sulla tecnica PCR
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
campione
estrazione DNA
RILEVAMENTO GENERICO (PCR end-point, ibridazione con sonde)
negativo
positivo
IDENTIFICAZIONE - rilevamento SPECIFICO
(PCR end-point, ibridazione con sonde)
È autorizzato?
no
ILLEGALE
< 1%
no etichetta
QUALITATIVA
Verifica DNA estratto (PCR end-point con primers universali per geni di pianta)
sì
QUANTIFICAZIONE (PCR quantitativa)
> 1%
etichetta
obbligatoria
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010
LA TECNOLOGIA E LA RICERCA VANNO AVANTI………
Sono disponibili NUOVI METODI SEMPRE PIU’ SOFISTICATI E
PRECISI:
• Biosensori
• Microarray
• Chip
……. MA OCCORRE LA LORO VALIDAZIONE
Corso di Alta Formazione in Legislazione Alimentare
Alessandria 21 maggio 2010