Concetto
periodico
gruppo
periodo
massa
elementi
pa
pf
vm
metalli alcalini
terrosi
alogeni
densita
periodica
periodi
gruppi
pm
pf
pe
raggioatomico
metalli
elettronegativita
gasnobili
elementi
densita
volumemolare
alcalini
alcalinoferrosi
nonmetalli
gassosi
liquidi
valenza
mendeleev
Periodico
Liquido
Gassoso
PE
Densita
PM
Periodi
Gruppi
Elettronegativita
Ossidazione
Configurazione
Ionizzazione
Raggioatomico
Alcalini
Alogeni
Nobili
Acido
Basico
Neutro
Definizioni di Claudia (completate)
Definizione
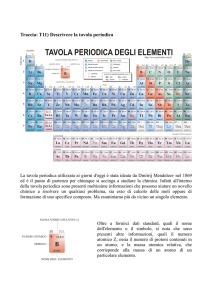
il sistema dove sono riportate tutte le caratteristiche fisiche degli elementi
classificazione degli elementi verticalmente
classificazione degli elementi orizzontalmente
quantità di materia degli elementi
così si possono anche chiamare gli atomi
quantifica il numero di protoni ed elettroni dell'elemento
temperatura massima in cui l'elemento cambia il suo stato fisico
si calcola facendo il rapporto tra massa e densità
i metalli del primo gruppo
i metalli del secondo gruppo
i metalli del settimo gruppo
viene espressa in g/ml
Definizioni di Cesaretti (50%)
lo è una proprietà che varia in maniera ciclica all'aumentare del numero
atomico
le righe orizzontali del sistema periodico
le righe verticali del sistema periodico
la somma di neutroni e protoni
raggiunge i 100°
mezza distanza tra due nuclei
elementi che si ossidano facilmente
capacità di attirare elettroni
gas molto ricchi.....
formano la tavola periodica
Clara ed Elisa
Lo è il Sistema della Tavola degli Elementi chimici
Stato che si ottiene raggiunto il punto di fusione
Stato della materia dove gli atomi sono più lontani
E' la temperatura in cui un elemento raggiunge i 100°C
Pùò essere espressa in g/ml e in g/L
E' la somma di neutroni e protoni
Le linee orizzontali della Tavola Periodica degli Elementi
Le linee verticali della Tavola Periodica degli elementi
Forza che ha un atomo di attrarre a sé gli elettroni
Lo è lo stato di un elemento
1s, 2s, 2p: cosa formano?
Il processo mediante il quale un elettrone viene tolto dall'atomo
E' una dimensione periodica dell'atomo che aumenta da sinistra verso destra
I metalli del primo gruppo della tavola periodica
I nonmetalli del penultimo gruppo della tavola periodica
I gas che hanno sangue blu
PH minore di 7
PH maggiore di 7
PH 7
correzione
Errata
Contesto generico
Errata
Errata
Errata
Err term e def
Errata
Insuff precisione
Errata
Errata
Relazione con SP
Realazione con SP
Troppo vaga
Relazione con SP
Relazione con SP
Superflua
Superflua
periodico
uub
hg
gasnobili
metallialcalini
alogeni
protoni
Pfus
densita
configurazione
periodo
gruppo
mercurio
atomico
elettronegativita
simbolo
stato
ponti
pe
Gattari
è il sistema di Mendeleev
il simbolo dell'ununbio
il simbolo del metallo liquido
gruppo di elementi di alta società
il nome del primo gruppo
penultimo gruppo
vengono indicati dal numero atomico
punto di fusione
proprieta periodica rapporto tra massa e volume
è elettronica quella di Lewis
ce ne sono sette nella tavola periodica
sono le linee sulla tavola periodica
metallo liquido
lo è il raggio
è di pauling
lo hanno tutti in alto a destra
puo' essere solido,liquido e gassoso
lo sono i legami con l'idrogeno
periodico
elementi
raggioatomico
densita
mendeleev
pa
gruppo
numeroatomico
periodo
nobili
valenza
elettroni
configurazione
alogeni
isotopi
nonmetalli
alcalini
fe
elettronegativita
Federica vale
periodico:lo è il sistema degli elementi
elementi:sono contenuti nella tavola periodica
raggio atomico:aumenta dall'alto al basso e diminuisce da sinistra a destra
densità:massa di un volume unitario
mendeleev:ha scritto il primo sistema periodico
pa:peso di un atomo (sigla)
gruppo:le colonne del sistema periodico
numero atomico:parametro che ordina gli elementi
periodo:le righe della tavola periodica
nobili:gas di "sangue blu"
valenza:stato di ossidazione
configurazione:disposizione degli elettroni
alogeni:elementi che formano acidi Hx
isotopi:atomi con stesso numero atomico ma diverso numero di massa
non metalli:elementi a destra della linea nera
alcalini: metalli del primo gruppo
fe:metallo scoperto nell'antichità
elettronegatività:capacità di un atomo di attirare elettroni
idrogeno:il primo fra tutti gli elementi
Periodico
Liquido
Gassoso
PE
Densita
PM
Periodi
Gruppi
Elettronegativita
Ossidazione
Configurazione
Ionizzazione
Raggioatomico
Lambertucci Tomassetti
Lo è il Sistema della Tavola degli Elementi chimici
Stato che si ottiene raggiunto il punto di fusione
Stato della materia dove gli atomi sono più lontani
E' la temperatura in cui un elemento raggiunge i 100°C
Pùò essere espressa in g/ml e in g/L
E' la somma di neutroni e protoni
Le linee orizzontali della Tavola Periodica degli Elementi
Le linee verticali della Tavola Periodica degli elementi
Forza che ha un atomo di attrarre a sè gli elettroni di legame
Lo è lo stato di un elemento
1s, 2s, 2p: cosa formano?
Il processo mediante il quale un elettrone viene tolto dall'atomo
E' una dimensione dell'atomo che aumenta da sinistra verso destra
Ripetuto
Esempio specifico
Scelta errata term
Relazione col SP
Err Senso comune
Relazione con SP
togliere
COMLPETARE
Def errata
Def errata
Più precisa
Relazione con SP
Alcalini
Alogeni
Nobili
Elementi
Transizione
periodo
gruppo
pf
pe
densita
pesoatomico
zeta
Volumemolare
tpe
stato
sostanza
alcalinoterrosi
nobili
massamolare
mendeleev
uma
catione
dodicesima
antimonio
isotopo
I metalli del primo gruppo della tavola periodica
I nonmetalli del penultimo gruppo della tavola periodica
I gas che hanno sangue blu
Ordinati nella tavola periodica
Gli elementi della tavola periodica tra i metalli e i nonmetalli
Tozzi Venturini
Nella tavola periodica sono orizzontali
Ne fanno parte elementi con caratteristiche comuni
periodi
gruppi
pm
pf
pe
raggioatomico
ioni
elettronegativita
gasnobili
elementi
densita
uma
atomo
lewis
metalli
legame
liquidi
energia
Mirko Luchetti & Mirko Cipolletta
1 lo è una proprietà che varia in maniera ciclica all'aumentare del numero
atomico
2 le righe orizzontali del sistema periodico
3 le righe verticali del sistema periodico
4 la somma di neutroni e protoni
5 a temperatura raggiunta gli elementi diventano liquidi
6 temperatura massima di un elemento
7 mezza distanza tra due nuclei
8 possono essere positivi e negativi
9 capacità di attirare elettroni da altri atomi
10 elementi che hanno già l'ottetto
11 formano la tavola periodica
12 la massa di un volume unitario
13 unità di misura delle moli
14 intorno ci girano gli elettroni
15 colui che ha inventato la famosa teoria dei puntini
16 con l'ossigeno formano legami ionici
17 possono essere ionici e covalenti,polari e apolari
18 lo hanno in comune il mercurio e il bromo
19 lo è quando è di prima ionizzazzione
avogadro
20 numero con cui si trova il numero delle molecole
periodico
periodica
configurazione
mole
pa
stronzio
Giovannangeli
sistema di disposizione degli elementi
lo è la tavola di mendeleev
disposizione degli elettroni nei vari orbitali
quantità di sostanza che contiene 6·10²³
peso di elettroni, protoni e neutroni in g/mol u.m.a.
elemento n°38
periodica
Errata
errato
Relaz. SP
Errata
Più precisa
Come varia
ERRATO
Errato
Eliminare
Scelta errata
termine
eliminare
Più preciso
Eliminare
Eliminare
densita
carica
volume
mendeleev
elementi
raggioatomico
massaatomica
covalente
ionico
periodi
nucleo
gruppi
isotopi
boro
periodicita
numero
nome
dimensione
atomo
energia
co
raggio
gruppi
periodi
gasnobili
lantanidi
attinidi
struttura
peb
pesoatomico
pf
densita
ossidazione
elettronegativita
simbolo
numeroatomico
metalli
nonmetalli
gassosi
alcalini
alcalinoferrosi
solidi
liquidi
si trova facendo il rapporto tra massa e volume
quella del nucleo è positiva
si trova facendo il rapporto tra massa e densità
ha inventato il primo sistema periodico
sono ordinati nel sistema periodico
è una dimensione che aumenta scendendo dal gruppo
quella media si trova dalla risultante di tutti gli isotopi di quell'elemento
tipo di legame dei non metalli
tipo di legame di tra un metallo e un non metallo
Righe del sistema periodico
è sta
Belvederesi
lo è una proprietà che varia in maniera ciclica all'aumentare del numero
atomico
grandezza atomica
distingue con esattezza l'elemento
definisce la grandezza di un atomo sulla tavola periodica
la materia è formata da lui
in un elemento è di prima ionizzazione
le prime del comportamento degli ossidi
c'è nel sole ma nell'atomo si dice con 2 parole
si usano per dividere contengono gli elementi che hanno caratteristiche
comuni
si usano per dividere gli elementi secondo il numero atomico
sono descritti come elementi di alto rango nella tavola periodica
Ne fa parte il cerio
Ne fa parte il torio
quella elettronica può essere a duetto o ottetto
è un punto che si raggiunge andando ad alte temperature
come si dice quanto pesa un atomo
il punto che si raggiunge quando si formano elementi gassosi
definizione della quantità
si dice di un elemento che perde elettroni
qualità dell'elemento che precisa quanti eV lo ionizzano
si usa al posto del nome dell'elemento nella tavola periodica
serve a precisare i protoni dell'elemento
se formano legame ionico, uno dei due farà parte dei..
se formano legame covalente saranno
si dice a quegli elementi la cui densità si misura in g/L
lo sono quegli elementi del 1° gruppo
lo sono quegli elementi del 2° gruppo
se quando cadono fanno rumore sono...
elementi splash!
pa
raggioatomico
Orsolini
un numero di avogadro di atomi
spazio occupato da un atomo singolo
forza con cui un atomo attrae gli elettroni di un altro atomo
proprietà che segue un andamento crescente poi decrescente
ciclico
peso massa media degli ogni atomo
la metà del diametro atomico
volumemolare
volume che occupa una mole
mole
volumeatomico
elettronegativita
periodica
Relazione con SP
Errata
Troppo vaga
Eliminare
Cambiare termine
Riportare al SP
Cambiare termine
Senso comune
Senso comune
Errata
Troppo vaga
Non Ripet. termine
Errata – rel con SP
Errata
Relaz. Con metalli
Errata
Eliminare
Semplificare
Eliminare
Eliminare
Eliminare
Relazione con
SP
Relazione con
sp
ei
massamolare
densita
è richiesta per l'estrazione di elettroni
peso di una mole
densità: rapporto tra massa e volume
valenza
temperaturadifusione
quando la si raggiunge si ha un passaggio di stato
nucleo
isotopi
ossigeno
cf
protoni
nucleo: parte più interna dell'atomo
isotopi:
fondamentale per la vita
?
protoni: sono presenti allo stesso numero degli elettroni
mendeleev
metallialcalini
Fu il primo a scoprire la periodicità degli elementi
occupano costituiscono il primo gruppo
periodico
periodica
configurazione
mole
pa
stronzio
densita
carica
Volume Vm
mendeleev
elementi
raggioatomico
massaatomica
covalente
ionico
periodi
nucleo
gruppi
isotopi
boro
Sambuco
sistema di disposizione degli elementi
lo è la tavola di mendeleev
disposizione degli elettroni nei vari orbitali
quantità di sostanza che contiene 6·10²³
pa: peso di elettroni,protoni e neutroni in g/mol
stronzio: elemento n°38
densità: si trova facendo il rapporto tra massa e volume
carica: quella del nucleo è positiva
volume: si trova facendo il rapporto tra massa e densità
mendeleev: ha inventato il primo sistema periodico
sono ordinati nel sistema periodico
è una dimensione che aumenta scendendo nei gruppi
quella media si trova dalla risultante di tutti gli isotopi di
quell'elemento
tipo di legame dei non metalli
tipo di legame di un metallo e un non metallo
righe del sistema periodico
aumenta per ogni gruppo e diminuisce e riaumenta per ogni
periodo
colonne del Sistema Periodico
elementi con uguale numero atomico e diverso numero di
massa
primo elemento dei semimetalli
Eliminare
Relazione con
SP
?
Cambia termine
e def
Collega a SP
?
Collega a SP
?
Def collegata a
SP
Troppo vaga
Errata
Eliminare
Errata
Relaz con SP
Rifare
Errata
Zampetti e Scipioni
Periodico
PF
PE
Lo e' il sistema della tavola l’andamento di alcune
proprietà degli elementi all’aumentare del numero
atomico
E' la temperatura in cui un elemento raggiunge lo stato
liquido
E' la temperatura in cui un elemento raggiunge i 100°ad
1ATM
Densita
Puo' espressa in g/ml oppure g/l
Periodi
Gruppi
PM PA
Simbolo
Nella tavola ne sono presenti 7
Sono indicati in numeri romani ma distinti con A e B
E' la somma di neutroni e protoni
Ognuno ha il suo in alto a destra
Ossidazione
Lo e'lo stato di un elemento
Elettronegativita
Alcalini
Metalloidi
Nobili
Forza di un atomo di attrarre a se elettroni in un legame
Lo sono i metalli del 1°gruppo
Elementi che non hanno ancora deciso da che parte stare
Non si abbassano a formare composti con la plebe, sono
asociali
Diminuisce se aumenta la forza di attrazione attorno al
nucleo
Lo sono solo il Mercurio e il Bromo
Se si incontrano con ossigeni seducenti nascono tante
piccole anidridi
E' elettronica ma non elettrotecnica
A differenza degli altri possono essere covalenti, polari ecc
Non sono famosi come quelli di venezia perche' ad
idrogeno
Costituisce la mina della matita
Raggioatomico
Liquidi
Nonmetalli
Configurazione
Legami
Ponti
Carbonio
Relazione con
elementi SP
Errata e da
mettere in relaz.
Con SP o
eliminare
Relazione con
SP
Aspetti formali
Errata
Formale,
Eliminare
Vaga e
fuorviante
cambiare
Eliminare
eliminare