RECETTORI PER LE CATECOLAMINE
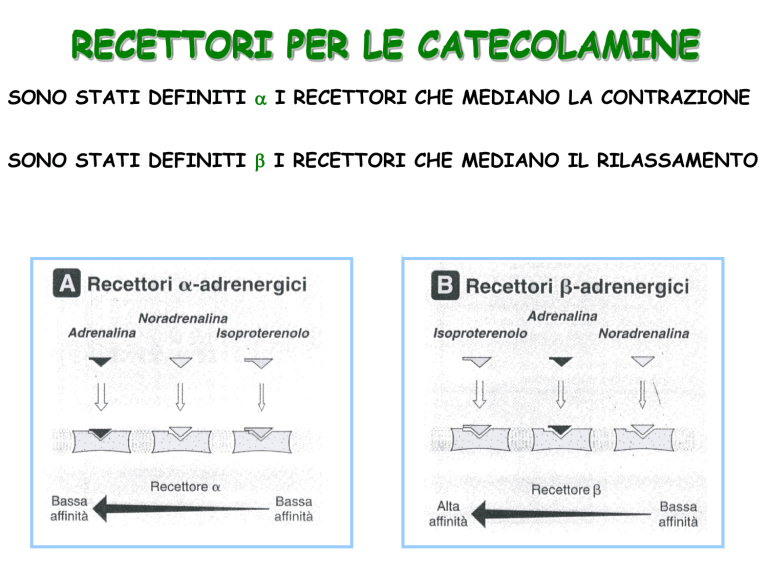
SONO STATI DEFINITI I RECETTORI CHE MEDIANO LA CONTRAZIONE
SONO STATI DEFINITI I RECETTORI CHE MEDIANO IL RILASSAMENTO
RECETTORI PER LE CATECOLAMINE
1980-90 Gli studi molecolari di cloning hanno messo in evidenza l’esistenza di 10
recettori diversi per la NA
In particolare sono state definite due famiglie eterogenee:
1: 1A, 1B, 1C,
1D
2: 2A, 2B, 2c
: 1, 2, 3
RECETTORI PER LE CATECOLAMINE
Studio di tipo farmacologico
Negli anni ‘70 lo sviluppo di farmaci agonisti del recettore ha suggerito
l’esistenza di eterogeneità nell’ambito di questi recettori
Fenossibenzamina: recettori 1 post-sinaptici giunzionali
Clonidina:
recettori 2 pre-sinaptici
recettori 2 postsinaptici extragiunzionali
DISTRIBUZIONE E FUNZIONE DEI RECETTORI
1
MUSCOLATURA LISCIA VASALE
arteriole e vene
contrazione
MUSCOLATURA LISCIA ORGANI
stomaco
rilassamento
intestino: pareti
sfinteri
rilassamento
tratto genito-urinario
contrazione
CUORE
contrazione
contrazione
OCCHIO
muscolo radiale dell’iride
contrazione
FEGATO
glicogenolisi
gluconeogenesi
RECETTORI
Famiglia
1
1
Sottotipi
Trasduzione
1A
IP3/DAG
1B
IP3/DAG
1C
IP3/DAG
1D
?
DISTRIBUZIONE E FUNZIONE DEI RECETTORI
TERMINALI NERVOSI
catecolaminergici
gangli intramurali
dello stomaco
MUSCOLATURA LISCIA VASALE
arteriole:
coronarie, pelle e mucose,
renali
MUSCOLATURA LISCIA ORGANI
stomaco
intestino
RENE
2
inibizione liberazione NA
inibizione liberazione ACh
contrazione
rilassamento
rilassamento
tubuli prossimali
diminuzione escrezione
Na+, k+, Cl-
PANCREAS CELLULE
diminuzione secrezione
insulina
PIASTRINE
aggregazione
RECETTORI
Famiglia
2
Sottotipi
2
Trasduzione
2A
cAMP;
K+
2B
cAMP;
Ca++
2C
cAMP
Ca++
RECETTORI
Famiglia
Sottotipi
Trasduzione
1
cAMP
2
cAMP
3
cAMP
DISTRIBUZIONE E FUNZIONE DEI RECETTORI
(NA=A)
1
CUORE
Nodo SA
Atrio
aumento di frequenza
aumento della contrattilità
Nodo AV
aumento della velocità di conduzione
Hiss-Purkinje
aumento della velocità di conduzione
aumento dell’automatismo
Ventricolo
aumento della contrattilità
aumento della velocità di conduzione
aumento dell’automatismo
aumento dell’automatismo
RENE
Apparato
juxta-glomerulare
aumento della secrezione di renina
DISTRIBUZIONE E FUNZIONE DEI RECETTORI
>
(A NA)
VASI
arteriole: coronarie
muscoli scheletrici
polmonari
renali
gastrointestinali
MUSCOLATURA SCHELETRICA
MUSCOLATURE LISCE ORGANI
stomaco
intestino
bronchi
tratto genito-urinario
FEGATO
2
vasodilatazione
glicogenolisi
rilassamento
glicogenolisi
neoglucogenesi
Effetti dell’attivazione simpatica
DISTRIBUZIONE E FUNZIONE DEI RECETTORI
>
(NA A)
TESSUTO ADIPOSO
3
lipolisi
meccanismo molecolare attivati dai recettori
1 nel cuore
miocardio
effetto inotropo positivo
effetto dromotropo positivo
meccanismi molecolari attivati dalle catecolamine nei vasi
1
2
effetti delle catecolamine sui vasi
variano a seconda dei distretti e sono mediati dai recettori:
1, 2A e 2
distretto cutaneo:
vasocostrizione
1 giunzionali
2A extragiunzionali
muscoli scheletrici:
vasodilatazione
2
rene:
vasocostrizione
1 e 2A
distretto splacnico:
vasodilatazione
2
distretto polmonare:
vasocostrizione
2
effetti renali delle catecolamine
tubulo prossimale
diminuzione del flusso
2A e 2C
diminuzione dell’escrezione
di Na+, K+ e Cl-
apparato juxta-glomerulare
aumento secrezione di renina
1
effetti delle catecolamine sulle muscolature lisce
intestino
rilassamento diretto
2
stomaco
rilassamento indiretto
2A
sfinteri
contrazione
1
bronchi
rilassamento diretto
2
effetti metabolici delle catecolamine
fegato
glicogenolisi
glicogeno
glucosio
secrezione insulina e glucagone
tessuto
adiposo
neoglucogenesi
acidi grassi nel plasma
METABOLISMO DELLE CATECOLAMINE
• RICAPTAZIONE NELLE TERMINAZIONI NERVOSE
• COMT
• TRASFORMAZIONE METABOLICA
• MAO
• sulfotransferasi
• DILUIZIONE PER DIFFUSIONE DALLO SPAZIO
SINAPTICO E LA CAPTAZIONE NEI SITI
EXTRANEURONALI
•Nicotinico
–canale ionico Na+
•Ca2+
–risposta eccitatoria
•rapida
–1 millisecondo
•Muscarinico
–metabotropo
•proteine G
–risposta eccitatoria o
inibitoria
•lenta
Recettori colinergici
Recettore nicotinico
•5 subunità
–2α ,β ,γ ,δ , ε
–differenti sottotipi e
•recettori muscolo scheletrico,
gangli autonomi e SNC
•differente sensibilità a farmaci e
tossine
•tutti attivati da nicotina
–canale per Na+e Ca2+
•1 msec 50.000 Na2+
•potenziale postsinaptico
eccitatorio
Vie colinergiche centrali
•Setto e n. basale di Meynert neocortex,
ippocampo, bulbo olfattorio
–processi cognitivi
•Pontetalamo e striato
–movimento
•Midollotronco encefalico e mesencefalo
•Recettori muscarinici
•Recettori nicotinici
–effetti pre-e postsinaptici
–rilascio neurotrasmettitori
•dopamina, n. accumbens
•glutammato
Effetti dell’attivazione parasimpatica
SISTEMI A PROIEZIONE DIFFUSA
Assoni lunghi e ramificati, che
terminano in più aree cerebrali
contemporaneamente
Gruppi di neuroni con i corpi cellulari raggruppati in
zone precise del SNC
Sistema Motorio
A seconda dell’area in cui viene liberato il neurotrasmettitore, i sistemi a proiezione
diffusa influenzano una specifica attività
Quindi i sistemi a proiezione diffusa:
• influenzano specifiche attività cerebrali
(azione specifica), a seconda della struttura
che vanno a regolare
• influenzano contemporaneamente più aree
cerebrali (azione integrata)
ad es., durante una situazione di pericolo:
aumenta il rilascio di noradrenalina in più aree cerebrali:
pianificazione di
strategie difensive
percezione degli stimoli
sensoriali
attività endocrina e
comportamenti di fuga
apprendimento
risposte
motorie
Sintesi: tutti i neurotrasmettitori classici sono sintetizzati
nelle terminazioni dell’assone (terminali sinaptici)
4: SISTEMI DOPAMINERGICI
1) Sistema Nigro – Striatale:
• contiene il 75 % della dopamina del SNC
• controllo motorio: iniziare movimenti
• Morbo di Parkinson
2) Sistema Mesolimbico:
• percezione sensoriale
• comportamenti motivati (gratificazione e ricompensa)
• apprendimento e memoria
3) Sistema Mesocorticale:
• percezione sensoriale
• funzioni cognitive
• programmazione azioni e comportamenti
• interazione sociale
• apprendimento e memoria
4) Sistema Ipotamo - Ipofisario:
• regolazione della secrezione
endocrina (prolattina, o. crescita):
la dopamina è uno dei fattori
ipotalamici
Recettori dopaminergici
• D1-like
– D1 e D5
– adenilil ciclasi, fosfolipasi C
• D2-like
– D2, D3, D4
– adenilil ciclasi, canali Ca2+
– canali K+
Effetti Centrali Dopamina
• recettori D2 n. accumbens
– movimento
Parkinson
– processi psichici
schizofrenia
– meccanismi di ricompensa
dipendenza
Effetti periferici Dopamina
• Basse concentrazioni
recettori D1
– vasodilatazione renale, mesenterica, coronarica
• Maggiori concentrazioni
recettori β1
– azione inotropa positiva
• Alte concentrazioni
– vasocostrizione, ipertensione
recettori α 1
SISTEMA SEROTONINERGICO
Nuclei del Rafe: nove nuclei, a livello della linea mediana
suddivisi in 2 gruppi:
1) porzione rostrale: nel Ponte e
Mesencefalo, proiettano a tutto il snc
Percezione sensoriale:
Ciclo sonno/veglia:
Comportamento:
Umore
2) Porzione caudale: in Bulbo
Percezione degli stimoli sensoriali
• Nocicezione (lesioni: aumento percezione dolore)
Recettori serotoninergici
Si distinguono in 7 tipi (5-HT1-7), di cui solo per i primi quattro si
hanno buone conoscenze.
I recettori 5-HT1, 5-HT2, 5-HT4 e 5-HT5 fanno parte della superfamiglia
dei recettori accoppiati alle proteine G. Il recettore 5-HT3, invece, è un
recettore-canale controllato da ligando (la serotonina) che permette il
flusso di Na+ e K+ e ha una struttura simile a quella del recettore
colinergico nicotinico.
Il recettore 5-HT1 presenta 5 sottotipi (A, B, D, E, F) tutti accoppiati a
proteine Gi e proteine Go, quindi alla via dell’adenilato-ciclasi, pertanto
riducono la concentrazione di AMP-ciclico (cAMP). Inoltre, almeno uno
dei sottotipi 5-HT1, il recettore 5-HT1A, attiva anche un canale al K+
ligando-dipendente e inibisce un canale per il Ca2+ voltaggiodipendente.
I recettori 5-HT1A si trovano nell’ippocampo e nei nuclei del rafe del
midollo allungato, dove agiscono come autorecettori somatodendritici
inibitori sui corpi cellulari dei neuroni serotoninergici; si pensa
possano essere coinvolti nella termoregolazione.
Come recettori postsinaptici, si trovano anche in regioni
del SNC associate con l'umore e l'ansia, quali
l'ippocampo e l‘amigdala. L'attivazione dei recettori 5HT1A comporta l'attivazione dei canali del potassio
rettificanti anomali (o inward rectifiers), che inducono
iperpolarizzazione e inibizione neuronale.
A livello ipotalamico, questo sottotipo recettoriale è uno
dei principali responsabili della regolazione della sintesi
e della secrezione dell’ormone adrenocorticotropo (o
corticotropina, ACTH.
I recettori 5-HT1B, nel sistema nervoso centrale, sono
espressi ad alti livelli nei nuclei della base, nello striato e
nella corteccia frontale, mentre al di fuori del SNC sono
presenti nei tessuti vascolari.
Hanno una tipica localizzazione presinaptica e
fungono da autorecettori inibitori. Possono anche
avere funzione di eterorecettori e modulare
negativamente il rilascio di altri neurotrasmettitori
quali acetilcolina, noradrenalina, dopamina,
glutammato e GABA.
I recettori 5-HT1D funzionano come autorecettore sui
terminali assonici, inibendo il rilascio di 5-HTI
Questo sottotipo si trova nei vasi sanguigni cranici
(perciò importanti nella patogenesi dell’emicrania) e
ampiamente nella sostanza nigra e nei gangli della
base; potrebbe regolare la velocità di scarica delle
cellule dopaminergiche e il rilascio di dopamina dai
terminali assonici.
I recettori 5-HT1E si trovano nella corteccia cerebrale
e nello striato.
I recettori 5-HT1F si trovano nel cervello e in periferia
Il recettore 5-HT2 presenta 3 sottotipi (A, B, C) che sono
accoppiati alle proteine Gq e G11, quindi alla via della fosfolipasi
C; sono sia presinaptici che postsinaptici.
I recettori 5-HT2A sono ampiamente distribuiti nel SNC, soprattutto nelle zone di terminazione degli assoni
serotoninergici. Elevate concentrazioni di recettori 5-HT2A sono
presenti nella corteccia prefrontale, nel claustro,nel tubercolo
olfattivo, come pure in diversi nuclei originatisi dal tronco
encefalico, nonché nella muscolatura liscia e nelle piastrine.
I recettori 5-HT2B sono stati identificati nel fondo dello stomaco.
I recettori 5-HT2C sono espressi in concentrazione molto elevata
a livello del plesso corioideo dove regola la produzione di
transferrina e del liquido cerebrospinale
Il recettore 5-HT3, a differenza degli altri tipi di recettori
serotoninergici che sono accoppiati a proteine G, è un
recettore-canale attivato dal ligando serotonina che permette
il flusso di Na+ e K+; ha una struttura di membrana simile a
quella del recettore colinergico nicotinico. Appartiene alla
famiglia dei recettori-canale cationici nonché alla classe I
(insieme al recettore nicotinico, al recettore GABA A e al
recettore glicinergico A), quindi è un pentamero e ciascuna
delle cinque catene polipeptidiche attraversa quattro volte la
membrana plasmatica.
Il legame della serotonina su due siti recettoriali determina
l’apertura di un canale permeabile ai cationi Na+, K+ e Ca++ con
conseguente depolarizzazione desensibilizzante.
Questi recettori sono localizzati sulle terminazioni
parasimpatiche nel tratto gastrointestinale e anche nelle
afferenze vagali e splancniche.
Nel sistema nervoso centrale (SNC), invece, vi è una elevata
densità di recettori 5-HT3 nel nucleo del tratto solitario e
nell'area postrema (dove c’è il centro del vomito).
I recettori 5-HT3 presenti nel canale gastroenterico e nel SNC
sono coinvolti nella risposta emetica e costituiscono la base
anatomica per le proprietà antiemetiche degli antagonisti
recettoriali 5-HT3.
Il recettore 5-HT4 è accoppiato ad una proten Gs, quindi alla via
dell’adenilato-ciclasi, ed è ampiamente diffuso in tutto il corpo.
Nel SNC si ritrova nei neuroni dei collicoli superiore e inferiore e
nell'ippocampo.
Nel canale gastroenterico è localizzato sui neuroni (per esempio,
del plesso mesenterico), sui muscoli lisci e sulle cellule
secretorie. Si pensa che nel canale digerente il recettore 5-HT4
sia in grado di evocare la secrezione e facilitare il riflesso
peristaltico.
Sistema Istaminergico
L’istamina deriva dell’istidina per azione della
istidindecarbossilasi. E’ localizzata nella maggior parte dei
tessuti, ma e’ presente ad alte conc. nei polmoni, nel tratto
gastrointestinale. Quella non mastocitaria, si trova negli
istaminociti, nei mastociti e basofili si trova in granuli
intracellulari legata ad una proteina e con una macroeparina.
Il sistema istaminergico origina dai nuclei
tuberomammillari dell’ipotalamo, localizzati nella formazione
reticolare bulbare, pontina e mesencefalica lungo la linea
mediana. I loro assoni eccitano ipotalamo, talamo,
proencefalo basale (colinergico), gangli della base e corteccia
cerebrale (neurotrasmettitore istamina, di derivazioni
amminoacidica).
A livello ipotalamico l'istamina è un regolatore di
altre funzioni, quali il rilascio di vasopressina, di
ossitocina, di prolattina, ACTH e beta-endorfina.
Regola pure il senso di fame e di sete: un aumento
dell'istamina sopprime queste due sensazioni,
mentre antagonisti del recettore H1 agiscono
sull'ipotalamo ventromediale per stimolare
l'appetito
Il livello di attività dei neuroni istaminergici e’ alto nella veglia e
declina nel corso del sonno. Altre funzioni attribuite all’istamina
includono il controllo della fame e della sete e la termoregolazione.
L’inibizione farmacologica dei neuroni istaminergici riduce la veglia e
innesca il sonno (antistaminici)
Quattro tipi di recettori istaminergici:
H1: sono localizzati essenzialmente nel terminale post-sinaptico e
causano eccitazione.
H2 e H3 sono inibitori, rispettivamente post- e presinaptici . Gli H3
sono autorecettori con azione inibitoria su i neuroni che rilasciano
istamina.
H4 Localizzazione prevalente: Midollo osseo, milza, eosinofili,
mastociti, neutrofili. Effetti: modula l'attivazione della risposta
immunitaria. La scoperta di questo sottotipo recettoriale risale al
2001.
Anche questi recettori inibiscono l'adenilatociclasi tramite una Gi.
Anche questi recettori inibiscono l'adenilatociclasi tramite una
Gi. Accessoriamente possono accoppiarsi ad una Go, che regola i
canali del potassio e l'attivazione delle MAP chinasi tramite la PKC.
È stato riportato che possono anche attivare delle proteine G
presenti esclusivamente nelle cellule midollari, la G15 e la G16,
tramite le quali possono agire sulla mobilizzazione del calcio dai
depositi intracellulari.
Il GABA e’ un neurotrasmettitore inibitorio e il suo rilascio nello
spazio sinaptico impedisce all’impulso nervoso di propagarsi nel
neurone postsinaptico.
L’acido glutammico e’ un neurotrasmettitore eccitatorio e consente
quindi allo stimolo nervoso di propagarsi nel neurone postsinaptico.
I neuro peptidi sono costituiti da complesse molecole
proteiche di lunghezza variabile (da 3 a 80 AA) e possono
essere rilasciati sia dai neuroni che dalle cellule
neurosecretrici localizzate in tessuti od organi non nervosi,
quali l’intestino, il cuore e il pancreas. Sono piu’
propriamente detti neuro mediatori in quanto possono
passare direttamente attraverso lo spazio sinaptico, ma
sono anche in grado di diffondere a distanze maggiori
influenzando, per esempio, numerose cellule all’interno di
una certa zona del SNC. La loro azione e’ piuttosto
diversificata in quanto i loro effetti possono variare a
seconda dell’area dell’encefalo in cui vengono rilasciati.
Le endorfine, come gli altri neuro peptidi, hanno
generalmente un’azione inibitoria sui neuroni con cui
stabiliscono un legame. La maggior concentrazione di
recettori per le endorfine si riscontra: