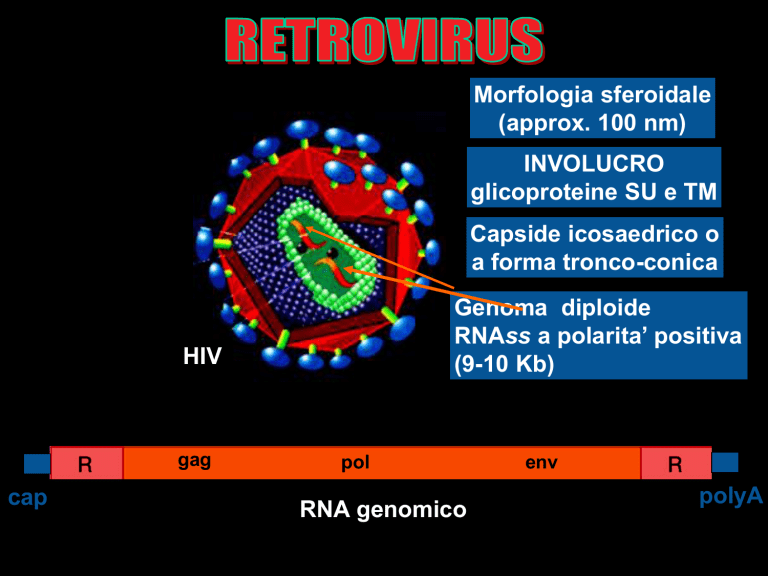
Morfologia sferoidale
(approx. 100 nm)
INVOLUCRO
glicoproteine SU e TM
Capside icosaedrico o
a forma tronco-conica
Genoma diploide
RNAss a polarita’ positiva
(9-10 Kb)
HIV
gag
cap
pol
RNA genomico
env
polyA
vertebrati
alterazioni
del sistema
immunitario
tumori
AlphaBetaGammaEpsilonretrovirus
leucemie
Deltaretrovirus
patologie
neurodegene
rative
Lentivirus
gp120
/NCp7
integrasi
gp41
proteina
nucleocasidica
p9
NC
proteina di matrice
p17
MA
proteasi
p24
CA
RETROTRASCRIZIONE
COMPLESSO DI PREINTEGRAZIONE
Trascrittasi Inversa : RT
RT: DNA polimerasi RNA-dipendente
RT: RNAsi H
RT: DNA polimerasi DNA-dipendente
RT manca di attività “proof reading”
1-10 errori/genoma
DNA PROVIRALE
U3
LTR
R
LTR
INTEGRAZIONE del DNA PROVIRALE
PROCESSAMENTO: le estremità del DNA virale vengono
riconosciute da IN e tagliate per formare idonee
estremità 3’ (avviene nel PIC).
INTEGRAZIONE:
rottura dei legami fosfodiesterici nel DNA dell’ospite (4-6 bp)
Inserimento delle estremità 3’virali (processate)
Enzimi di riparo (della cellula ospite)
L’integrazione è sito specifica per il genoma virale (estremità), ma
casuale nel genoma della cellula ospite
PROMOTORE
PROVIRUS INTEGRATO
PROVIRUS INTEGRATO
PolyA
ATTIVA TRASCRIZIONE
DI HIV-1
RNA polimerasi II
cellulare
Trascritti corti
proteina
TAT
TRASCRIZIONE HIV-1
9.1 kb
pr55 MA
CA
MA
CA
p17
p24
NC
NC
p15
p2
NC p7
p1
p6
MA
CA
NC
PR
PR
p10
RT
RT
p51/66
IN
IN
p31
4.3 kb
Gag-pol e env
mRNA sono tradotti
come poliproteine
processate
successivamente
SU
SU
gp120 TM
gp41
TM
gp160
Ciclo di replicazione
di HIV-1
TRASCRIZIONE di
mRNA e vRNA
SINTESI
PRECURSORI PROTEICI
ASSEMBLAGGIO
sulla plasmamembrana
MATURAZIONE
attività della PROTEASI
a Enfuvirtide (T20)
b inibitori nucleosidici
inibitori nucleotidici
(AZT)
(Tenofovir)
inibitori non-nucleosidici (Nevirapina,
Efavirenz)
c molecole peptidomimetiche in grado di
bloccare il sito catalitico della proteasi
(Ritonavir)
VIRUS a RNAss di POLARITA’ NEGATIVA
RNA virale non è infettante
il genoma virale non può essere tradotto
l’RNA virale è trascritto in mRNA (polarità+)
I virioni contengono una RNA polimerasi RNA-dipendente
virus provvisti di involucro
ORDINE MONONEGAVIRALES
150-300 nm
morfologia: sferico pleomorfica (forme filamentose)
RpRd
trascrittasi e replicasi virale
GENOMA PARAMYXOVIRIDAE
Tr
sequenze intergeniche EIS
TRASCRIZIONE dei PARAMYXOVIRUS
sequenze intergeniche EIS
Modello “Start-Stop
Pol (P+L) inizia la sintesi del mRNA
al terminale 3’
L: RpRd P: recruta L sul templato.
trascrizione della sequenza Leader
la Pol si ferma alla sequenza STOP
la trascrizione ricomincia al 3’ (sequenza
START) del gene N
la trascrizione di N continua fino alla
sequenza STOP
Pol ricomincia la sintesi al 3’ del gene P
mRNA monocistronici
mRNA provvisti di “ cap” e “poly A”
ruolo delle sequenze EIS
SEQUENZE STOP
per
scivolamento
viene
sintetizzata la coda poliA (200nt)
all’estremità 3’ del trascritto
Terminazione del trascritto
SEQUENZE START
5’ “capping” del mRNA
Trascrizione polarizzata
Sequenze EIS
L
PP P
P
3’
End-Intermediate-Start
N
P
M
F
HN
L
5’
Transizione tra trascrizione e replicazione del genoma
dei PARAMYXOVIRUS
bassi livelli di N: favoriscono la sintesi di mRNA
alti livelli di N: la RpRd continua la sintesi di vRNA attraverso le
sequenze EIS
CICLO DI REPLICAZIONE
QuickTime™ and a
GIF decompressor
are needed to see this picture.
virus Sendai
FUSIONE
Trascrizione mRNA
Sintesi di proteine
Trascrizione vRNA
Assemblaggio e
gemmazione
2 Sottofamiglie:
Paramyxovirinae
Pneumovirinae
Genere
Ospite
Specie
Respirovirus
virus parainfluenzale 1-3
virus Sendai
Morbillivirus
virus del morbillo
virus del cimurro del cane
uomo
Rubulavirus
virus della parotite
uomo
Henipavirus
virus Hendra
virus Nipah
Pneumovirus
virus respiratorio sinciziale (RSV)
virus respiratororio bovino
infezione vie aeree superiori
uomo
topo
uomo/equini
uomo/suini
uomo
Virus Respiratorio sinciziale - RSV
•isolato nel 1956
1- infezione delle prime vie aeree
2- infezione delle vie aeree profonde
danno immunomediato
(necrosi ed edema della mucosa
dei bronchi )
grave infezione in età pediatrica
ospedalizzazione nel 30% dei casi
SINCIZI in
cellule epiteliali
infettate con RSV
Virus della Parotite
isolato nel 1945
ospite:uomo
1- replicazione nelle cellule epiteliali delle vie aeree superiori
2- linfonodi locali - distali - organi del SRE
3- infezione delle parotidi (infiammazione
locale=orecchioni)
Complicazioni
orchite (20%; più frequente negli adulti)
virus del Morbillo
•altri sintomi e complicazioni
–otite
–polmonite
–infezioni al CNS (as SSPE, subacute
sclerosing panencephalitis)
febbre alta
Vaccino attenuato
MPR
(trivalente):
Morbillo (Paramyxoviridae),
parotite(Paramyxoviridae),
rosolia (Togaviridae)
15 mesi di età
From Flint et al.,
ASM Press, 2004












