
AVVERTENZA
Il presente materiale didattico viene fornito allo scopo di facilitare la
comprensione degli argomenti trattati e costituire il raccordo tra lezioni e
studio individuale
NON E’ PERTANO DA INTENDERSI COME SOSTITUTIVO DEL LIBRO DI TESTO
Inoltre, nonostante la massima scrupolosità nella preparazione, è pur sempre
possibile che siano presenti inaccuratezze e imprecisioni. E’ quindi necessario
il costante controllo con i testi di riferimento
Si invita a non diffondere, fotocopiare o utilizzare tale materiale per scopi
diversi dalla preparazione individuale dell’esame
Dr Monica MONTAGNANI – CdL Medicina e Chirurgia
Esame Farmacologia – V Anno/II Semestre - Canale LZ
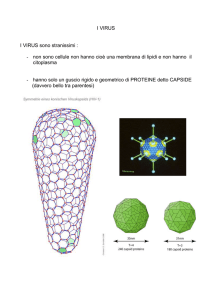
VIRUS
Parassiti intracellulari obbligati
La loro replicazione dipende primariamente dai processi di sintesi della
cellula ospite. I farmaci antivirali dovrebbero bloccare sia l’ingresso che
l’uscita dalla cellula o essere attivi all’interno della cellula ospite.
VIRUS – TAPPE DELLA REPLICAZIONE
Adsorbimento
alla cellula ospite e
penetrazione
1
Uncoating dell’acido
nucleico virale.
4
2
3
5
Assemblaggio delle
particelle virali.
6
3-4 Sintesi delle
proteine regolatorie
precoci
Sintesi del RNA o DNA.
Sintesi delle proteine
strutturali tardive.
Release
dalla
cellula.
FARMACI ANTIVIRALI
• Un farmaco antivirale deve essere altamente
specifico ed efficace.
• Deve essere in grado di interferire con una
infezione in atto
• Deve infine interferire con la replicazione del
virus senza provocare danni alla cellula ospite
PRINCIPALI SITI D’AZIONE DEI FARMACI ANTIVIRALI
VIRUS DI IMPORTANZA CLINICA
VIRUS
Adenovirus
Herpesvirus
Poxvirus
Papillomavirus
Parvovirus
Hepadnavirus
Arenavirus
Coronavirus
Influenzavirus
Paramixovirus
Picornavirus
Retrovirus
Rabdovirus
Togavirus
ACIDO
MALATTIE
NUCLEICO
Infezioni respiratorie e oculari
DNA
Herpes labialis, herpes genitalis,
DNA
encefalite, varicella, herpes
zoster, mononucleosi, retinite
Vaiolo, Vaccino
DNA
Papilloma
DNA
Eritema infettivo
DNA
Epatite B
DNA
Coriomeningite linfocitaria
RNA
Infezioni respiratorie
RNA
Influenza
RNA
Morbillo, infezioni respiratorie
RNA
Poliomielite, infezioni
RNA
respiratorie
Leucemia, AIDS
RNA
Rabbia
RNA
Rosolia, febbre gialla
RNA
MIXOVIRUS – INFLUENZA VIRUS
NA
HA
Il virione dell’influenza contiene:
8 segmenti RNA
che codificano per 10 proteine
Viral RNA
M1
NP
I segmenti RNA complessati con
Nucleoproteine (NP) e con una
M2
RNA-polimerasi
RNA-dipendente trimerica costituiscono
la ribonucleoproteina core, circondata da
uno strato di
proteina matrice (M1)
Emoagglutinina (HA) Neuraminidasi (NA)
M2 (solo influenza tipo A)
Sono tre proteine integrali immerse nel guscio involucro (envelope) virale
derivato dalla membrana plasmatica delle cellule infette.
ANTI INFLUENZA-VIRUS
INIBITORI DELLA PROTEINA M2
Amantadina
Rimantadina
INIBITORI DELL’ENZIMA NEURAMINIDASI
Zanamivir
Oseltamivir
PROTEINA M2
La proteina M2 (presente solo nel virus A)
è coinvolta nella mediazione dell’uncoating virale,
attraverso la sua capacità a formare tetrameri capaci di agire come
canali protonici.
M2
ADAMANTAMINE
AMANTADINA e RIMANTADINA
MECCANISMO D’AZIONE
Agiscono bloccando un canale ionico
formato dalla proteina M2 che attraversa la
membrana virale.
Durante lo stadio iniziale della replicazione
virale il virus è captato in vescicole
endocitotiche, in cui il pH si abbassa per
l’ingresso di idrogenioni.
Gli ioni idrogeno passano attraverso il canale M2 nell’interstizio della particella virale e
promuovono la dissociazione della proteina M1 dai complessi ribonucleoproteine in modo
che le ribonucleoproteine possono entrare nel nucleo cellulare e iniziare la replicazione.
Sia la AMANTADINA che la RIMANTADINA entrano nel canale ionico e bloccano la
penetrazione degli ioni idrogeno che sono necessari per la dissociazione di M1 e
ribonucleoproteine.
AMANTADINA (Mantadan)
ATTRAVERSO L’INIBIZIONE DEI CANALI IONICI M2
INIBISCE LA SPOLIAZIONE DEL VIRUS DELL’INFLUENZA A
SOMMINISTRAZIONE
– entro 24-48 ore dall’infezione
– per 10 giorni ad alte dosi
PROBLEMI TERAPEUTICI
1) L’amantadina non ha effetto contro i virus dell’influenza B (i virus dell’Influenza B
presentano canali ionici con proprietà molto differenti)
2) emersione di mutanti virali
3) tossicità per il sistema nervoso centrale
AMANTADINA (Mantadan)
SPETTRO ANTIVIRALE
Influenza A virus
Parainfluenza virus
Rosolia virus
MECCANISMO D’AZIONE
Riduzione della permeabilità della membrana cellulare
e impedita penetrazione del virus nella cellula
Inibizione dell’ ”uncoating” (svestimento virale)
(legame con la proteina M2)
INDICAZIONI
Profilassi e Terapia dell’influenza tipo A
TOSSICITA’
Insonnia, difficoltà di concentrazione
Neurotossicità (in insufficienza renale)
Nervosismo, Confusione, Allucinazioni, Convulsioni, Coma
RIMANTADINA (Flumadine)
Ha lo stesso spettro antivirale dell’amantadina.
E’ 4-19 volte più attiva dell’amantadina.
FARMACOCINETICA
SOMMINISTRAZIONE
Orale 100 mg x2
ASSORBIMENTO
Biodisponibilità: 96%
DISTRIBUZIONE
Legame proteico: 40%
Volume distribuzione: 720 – 986 L
Emivita plasmatica = 30 ore (24-36)
METABOLISMO
Epatico: ampio
ELIMINAZIONE
Renale: metaboliti immodificata (< 15%)
TOSSICITA’
Disturbi gastrointestinali
NEURAMINIDASI
La Neuraminidasi catalizza il
clivaggio
virale
dell’acido
sialico terminale (acido Nacetilneuraminico)
da
vari
glicoconiugati della superficie
cellulare,
facilitando
la
diffusione del virus influenzale
nel
tratto
respiratorio
e
aumentando la virulenza di
alcuni
ceppi
attraverso
numerosi meccanismi:
Promuove il release del virione dalla cellula ospite infetta
Previene la formazione di aggregati virali dopo il release
Previene l’inattivazione virale da parte del muco respiratorio
Promuove la penetrazione nelle cellule epiteliali respiratorie.
Altera la parte carboidratica dell’ Emoagglutinina.
Promuove la produzione di IL-1 e TNF-alfa
Attiva il TGF- e induce apoptosi cellulare.
INIBITORI DELLA NEURAMINIDASI
ZANAMIVIR (Relenza)
Analogo dell’acido sialico
OSELTAMIVIR
(Tamiflu)
(GS4104)
Profarmaco del GS4071
ANALOGHI DI ACIDO SIALICO, CON SOSTITUZIONE AL 4’ OH CON UN
GRUPPO AMINICO O GUANIDINICO
MECCANISMO D’AZIONE
LEGANDOSI AL SITO ATTIVO DELLA PROTEINA
NEURAMINIDASI (NA) VIRALE - REGIONE MOLTO
CONSERVATA - INIBISCONO IL RILASCIO DEI VIRUS
DELL’INFLUENZA A E B
SOMMINISTRAZIONE
Devono essere assunti molto
precocemente
PROBLEMI TERAPEUTICI
emersione di mutanti virali
OSELTAMIVIR
(Tamiflu)
SPETTRO ANTIVIRALE
Influenza virus A e B
MECCANISMO
Inibitore della neuraminidasi
RESISTENZA
Mutazione della neuraminidasi
FARMACOCINETICA
Somministrazione
Assorbimento
Distribuzione
Metabolismo
Eliminazione
Orale: 75 mg x 2 /die per 5 giorni
Biodisponibilità orale: 75%
Legame proteico: 42% Oseltamivir carbossilato: 3%
Emivita plasm: 1-3 h Oseltamivir carbossilato): 6-10 h
Epatico: idrolisi da esterasi: Oseltamivir carbossilato
Renale: 90% (Oseltamivir carbossilato) FG+ST
INDICAZIONI
Trattamento e prevenzione dell’influenza A e B
TOSSICITA’
Nausea e Vomito
ZANAMIVIR (Relenza)
Analogo dell’acido sialico
SPETTRO ANTIVIRALE
Influenza virus A e B
MECCANISMO
Inibitore della neuraminidasi
RESISTENZA
Mutazione della neuraminidasi
FARMACOCINETICA
Somministrazione
Assorbimento
Distribuzione
Eliminazione
Inalazione: 10 mg x 2 /die per 5 giorni
Biodisponibilità orale: 2%
Biodisponibilità inalatoria: 10-20 %
Volume distribuzione 16 L
Emivita plasmatica: 2 h (ev); 3-5 h (inalazione)
Renale immodificata: 90%
Respiratoria: 4%
INDICAZIONI
Trattamento e prevenzione dell’influenza A e B
TOSSICITA’
Ben tollerato
FARMACI WIN
• inibiscono la penetrazione dei picornavirus
MECCANISMO D’AZIONE: interagiscono con il sito di riconoscimento
della VAP al recettore cellulare
Efficaci in vitro, ma non
in vivo (non sono
utilizzati nella terapia
umana)
From Flint el at Principles of Virology ASM Press



![Lezione 15 Virus [modalità compatibilità]](http://s1.studylibit.com/store/data/000771737_1-84b1cca561c5813066d1b76125338a98-300x300.png)







