Corso di Laurea Scienze Infermieristiche
Principi di Oncologia
Pianificazione Diagnostico-Terapeutica
Prof.ssa Silvia Mezi
Valutazione clinica
…in prima visita con un pz oncologico prima
della programmazione terapeutica
4 domande fondamentali
1. Come sta il paziente?
2. Quale diagnosi ha?
3. Abbiamo tutte le informazioni necessarie per la
programmazione terapeutica (tipo tumore,
caratteristiche biologiche, estensione di malattia …)?
4. Il paziente è informato?
Valutazione clinica
Come sta il paziente?
Anamnesi:
Comorbidità
Storia farmacologica (terapie in atto) / Allergie a farmaci
Sintomatologia (dolore, tosse, dispnea, subocclusione…)
Valutazioni cliniche:
- Età e Condizioni generali (scale di Performance Status /
Scale di valutazione cognitiva)
- Esame Obiettivo (alla ricerca di versamenti pleurici,
ascite, masse palpabili e parametro di malattia …)
- Ematochimici (riserva epatica, renale, midollare) e
markers tumorali
Valutazione clinica
Scale di Performance Status
Valutazione clinica
Scale di Dolore
Scala analogico-visiva (VAS)
Nessun
dolore
Il massimo
dolore
Scala categorica numerica (NRS)
Nessun
dolore
0
1
2
3
4
5
6
7
8
9
10
Il massimo
dolore
Scala semantica (VRS)
Nessun
dolore
Dolore
lieve
Dolore
moderato
The Pain Affect Faces Scale
Dolore
grave
Valutazione clinica
Markers Tumorali
ESPRESSIONE ANTIGENICA
SUPERFICIALE DI PROTEINE
INTRACELLULARI
PRESENTI NELLE CELLULE
TUMORALI
SOSTANZA PRESENTE
NEL SANGUE E/O NEI FLUIDI
BIOLOGICI DI PAZIENTI
AFFETTI DA TUMORE …
MA NON SOLO…
Markers Tumorali
La concentrazione dei marker tumorali (MT) nel siero
dipende da :
• numero cellule produttrici di MT
• caratteristiche biochimiche del MT
• quota di liberazione del MT dalla cellula tumorale
• vascolarizzazione del tumore
• grado di necrosi del tumore
• quota di metabolizzazione del MT
• complessazione con anticorpi
Alcuni esempi di falsi positivi con i MT
CICLO MESTRUALE
AFP HCG MCA CA125
FUMO
CEA TPA TG
ALCOOL
CEA TPA
PER TALE MOTIVO NON SI FA DIAGNOSI SOLO CON I MARKERS
TUMORALI,ma aiutano nella valutazione della malattia!
L'impiego razionale dei mt sierici consiste
nell'interpretare
le loro modificazioni nel tempo
DOSAGGI SERIATI
IN PZ ONCOLOGICI
MT
POSTOPERATORIO
La mancata normalizzazione o l'aumento progressivo dei MT nel
post-operatorio indicano la persistenza di tumore residuo
o la presenza di metastasi
T 1/2 piu' tardivo
Non si ottiene la negativizzazione del MT
MT SIERICI
POST-OPERATORIO
Dopo un intervento chirurgico radicale e' attesa una normalizzazione
del mt indice di remissione clinica completa
CEA
cinetica biesponenziale
100%
50%
5 gg
AFP
14gg
T 1/2 120 ore
120 ore
500 ore
componente rapida
componente lenta
MT SIERICI
FOLLOW-UP
I livelli sierici del MT sono correlati con la presenza e l'estensione
della malattia
VARIAZIONI positive o negative riflettono un aumento
o una diminuzione del numero delle cellule neoplastiche
DOPO UNA FASE DI NEGATIVIZZAZIONE DI UN MT LA
COMPARSA DI CONCENTRAZIONI CRESCENTI INDICA CON
ELEVATA PROBABILITA' LA PRESENZA DI METASTASI
L'INNALZAMENTO DI UN MT PUO' PRECEDERE DA 2 A 10
MESI LA DOCUMENTAZIONE STRUMENTALE DI RECIDIVA
in quanto la massa critica puo' essere inferiore a quella rilevabile con
le metodiche diagnostiche
Nel follow-up e' considerata significativa la PROGRESSIVITA' e la
CONTINUITA'
dell'incremento nel tempo, piu' del valore assoluto del MT
falsi positivi
falsi negativi
Follow-up
vero positivo
patologie infiammatorie
* met. costituite da cell. che
non producono il MT
* ridotta vascolarizzazione
* diametro tumorale non
significativo
dosaggio progressivamente
crescente nel tempo
MONITORAGGIO DELLA RISPOSTA DURANTE
TERAPIA ANTITUMORALE
In corso di trattamento chemioterapico l'entita' della diminuzione o
aumento dei MT correla con la risposta alla cht
MARCATORE
RISPOSTA
Normalizzazione ………………… risposta clinica completa
Diminuzione
………………… risposta parziale
Stazionario
………………….. malattia stabile
Aumento
…………………… progressione di malattia
RC
RP
MS
PD
Valutazione clinica
Quale diagnosi ha?
Solo Radiologica
Il pz in base alle condizioni cliniche può
ricevere trattamenti attivi ?
SI
Ci vuole la diagnosi
istologica
NO
Programmare
Terapia di
Supporto
Valutazione clinica
Abbiamo tutte le informazioni sulla malattia?
Diagnosi Istologica
Verificare se presenti eventuali informazioni biologiche
Valutazione clinica
Valutazione del tumore
Tipo di primitività del tumore
Caratteristiche biologiche del tumore
Estensione del tumore
Valutazione del tumore
TIPO DI PRIMITIVITA’ DEL TUMORE
TUMORI DEL POLMONE
TUMORI DEL TESTICOLO
Squamoso
Non
Microcitoma Microcitoma
Adenoca.
TUMORI DELLA MAMMELLA
TUMORI DEL GROSSO INTESTINO
Ca. Ano Ca. Retto
Non
Seminoma Seminoma
Ca.
Colon
duttale
lobulare
midollare
Tubulare
Valutazione del Tumore
ESTENSIONE DEL TUMORE
Valutazione dell’estensione del tumore
=
STADIAZIONE DELLA MALATTIA
TNM
Dall’esame
istologico
Patologico
pT pN pM
Clinico
cT cN cM
Dopo exeresi
chirurgica
T = estensione del Tumore
N= coinvolgimento Nodale (linfonodi)
M= presenza/assenza di Metastasi a distanza
Dagli esami
strumentali
Pre-exeresi o post
exeresi parziale
chirurgica
Valutazione del Tumore
ESTENSIONE DEL TUMORE
Perché è importante conoscere L’ESTENSIONE?
Perché cambia la prognosi e l’obiettivo terapeutico…
Fattore Prognostico: il TNM
T: TUMOR
N: LYMPH NODE
M: METASTASIS
Lo STADIO di malattia rappresenta un fattore prognostico
TNM come fattore prognostico:
alcuni esempi …
Breast Cancer Survival Rates
Stage
2yr
5yr%
10yr%
%BC
I
100
90
70
60
II
90
70
55
30
III
70
40
30
IV
25
2-5
<1
10
The overall median survival for MBC is <2ys.
50% of women with MBC stage IV will live <2ys.
%BC: incidenza di Breast Cancer suddivisa per stadio
Survival in relation
to presence and extent of regional lymph nodes
Carcinoma Gastrico e Stadiazione
Rischio di ricaduta tumore gastrico:
malattia micrometastatica all’esordio !!!
Stadio
5-years S
I
80%
II
60-70%
III
40-50%
Cambiamento
della prognosi
Gennaio 2010: nuovo TNM nel TUMORE DEL
POLMONE tipo NSCLC
CARCINOMA POLMONARE: SOPRAVVIVENZA PER STADIO
T
pT1N0R0
pT2N0R0
N° pz
OS a 5 aa
pT1a < or =2 cm
1816
77%
pT1b >2 to 3 cm
1653
71%
pT2a >3 to 5 cm
2822
58%
pT2b >5 to 7 cm
825
49%
pT2c >7 cm
364
35%
pT3N0
711
38%
pT4 (any N)
340
22%
pT4 (additional nodule(s) in
the same lobe)
363
28%
pM1 (ipsilateral pulmonary
nodules)
180
22%
cT4-malignant pleural
effusion/nodules
(p < 0.0001)
(p < 0.0001)
2%
J Thorac Oncol. 2007 Jul;2(7):593-602
NSCL: TNM come FATTORE PROGNOSTICO
• La prognosi degli stadi iniziali di malattia dopo resezione chirurgica
radicale è da correlarsi con la stadiazione patologica di malattia:
T
N
Adapted from Mountain CF. Chest. 1986;225 S.
Tumori Colo-Rettali (CRC):
localizzazioni
• Cecum
14 %
• Ascending colon
10 %
• Transverse colon
12 %
• Descending colon
7 %
• Sigmoid colon
25 %
• Rectosigmoid junct. 9 %
• Rectum
23 %
70%
Tumore Colo-Rettale Staging
Stage
Description
0
Intraepithelial; lamina propria invasion
I
Submucosa (T1) or muscularis propria (T2) invasion
II
A: pericolorectal tissue invasion (T3)
B: penetration to visceral peritoneum surface (T4a)
C: invasion/adherence to other organs/structures (T4b)
III
IV
A: T1-T2 + 1-3 regional LN; T1 + 4-6 regional LN
B: T3-T4a + 1-3 regional LN; T2-T3 + 4-6 regional LN; T1-T2 + ≥ 7 regional LN
C: T4a + 4-6 regional LN; T3-T4a + ≥ 7 regional LN; T4b + any regional LN
A: metastasis to 1 organ/site
B: metastases to multiple organs/sites or peritoneum
Edge SB, et al. AJCC cancer staging manual, 7th ed. New York, NY: Springer; 2010.
5-Yr Survival Rates by
Colon Cancer Stage
Stage
I
Observed 5-Yr Survival,%
74.3-78.7
IIA
66.7
IIB
60.6
IIC
45.7
IIIA
64.7-73.7
IIIB
42.1-58.2
IIIC
12.9-32.5
IV
19.2*
*2001-2003 SEER data.
Gunderson LL, et al. J Clin Oncol. 2010;28:264-271. Kopetz S, et al. J Clin Oncol. 2009;27:3677-3683.
Carcinoma del colon:
Stadio III (ogni T,N1-2, M0)
• 50% curati dalla chirurgia
• 7% curati dalla chirurgia+chemioterapia
• 43% ricadono nonostante la chemioterapia
Aumento di sopravvivenza a 5 anni
6-7%
Impact investigators; Lancet 1995.
O’Connell et al; JCO 1997
Lo Stadio: un fattore prognostico nel Ca. del Colon
O’Connor E.S. JCO 2011 Sept 1
ITER DIAGNOSTICO
CORREDO DI SEGNI E SINTOMI
aspecifico
specifico
SOSPETTO DIAGNOSTICO
PROGRAMMI DI SCREENING
indagini di immaging
endoscopiche
In corso di accertamenti
per altre patologie
DIAGNOSI
citologica(fnab)
istologica (tru-cut)
istologica intraoperatoria
La morfologia patologica rappresenta la base
DEFINIZIONE DIAGNOSTICA
istotipo tumorale
diffusione loco-regionale
PREVISIONE PROGNOSTICA
CARATTERIZZAZIONE BIOLOGICA
PROGRAMMAZIONE TERAPEUTICA
ITER DIAGNOSTICO IN ONCOLOGIA
Estensione LOCO-REGIONALE
Estensione SISTEMICA-METASTATICA
Caratterizzazione ISTOLOGICA e
MOLECOLARE
Strategia terapeutica
Valutazione della risposta in corso di trattamento cht
Follow-up
Cancer patient management: Solid tumors
Clinical findings
Biopsy
Cancer diagnosis
Staging/Grading
Therapeutic intention
Therapeutic decision
CT scans
Tumor extent/staging
Tumor extent/staging
Metastatic disease
Extent
Chemotherapy
Hormonal therapy
Targeted therapy
Palliative care (RT-Surgery)
Best supportive care
Localized disease
Resectable
tumor
Operable
patient
Surgery
+ Radiation therapy
+ Chemotherapy
+ Hormonal
Targeted therapy
Nonresectable
tumor
Inoperable
patient
Radiation therapy
Chemotherapy
Hormonal therapy
targeted therapy
Carcinoma della mammella
CA MAMMARIO
Iter diagnostico
Screening MX
diagnosi precoce
MORTALITA'
INCIDENZA DI TUMORI LOCALMENTE
AVANZATI
TUMORI METASTATICI ALLA DIAGNOSI
Il ca della mammella è, anche in fase iniziale, potenzialmente una
malattia sistemica in forma micrometastatica piuttosto che una patologia d'organo
APPROCCIO INTEGRATMULTIDISCIPLINARE
TERAPIA ADIUVANTE
La neoplasia e' ETEROGENEA
malattie con caratteristiche cliniche analoghe possono presentare
risposte ai trattamenti e storia naturale differente
DIVERSITA' BIOLOGICHE E
DIVERSI PROFILI DI ESPRESSIONE GENICA
classificazione molecolare
signature di Amsterdam
La capacita' di sostenere la formazione e la progressione tumorale potrebbe risiedere in una piccola
frazione di cellule tumorali CANCER STEM CELLS (fenotipo CD44 pos./CD24-) potenzialmente
quiescenti anche per lunghi periodi (GO)
Ca della mammella
Estensione locoregionale
-E.O
-MX bilaterale in 3 pr.
Estensione locale
Multicentricita’multifocalita’bilateralita
-ETG con sonda ad alta frequenza
-FNAB-CORE BIOPSY
-RM
Natura della lesione
Diametro
BREAST CANCER
Diagnosis path
Lesione
sospetta
Palpable mass
Cyst
Normal
Nonpalpable
mass
Cyst
aspiration
Biopsy
Needle
localization
•Excisional biopsy
•Core-cutting needle biopsy
Insufficient
evaluation,
rebiopsy
Ductal
carcinoma
in situ
Invasive
cancer
Treatment Path
Lobular
carcinoma
in situ
Benign
Continued
appropriate
screening
Ca della mammella
Estensione sistemica di malattia
Alla diagnosi
Rx torace 2p
Tc torace
Etg epatica
Tc addome-pelvi
Scintigrafia ossea
TC/RM
Rx mirata
Tc cranio / RM cerebrale
sintomatiche
Marcatori tumorali
Funzionalita' epato renale e midollare
solo nelle pz
Ca della mammella
Estensione sistemica di malattia
Tc total body + cranio
Malattia
metastatica
Scintigrafia ossea
Rx mirata
TC/RM
Marcatori tumorali
Funzionalita' epato renale e midollare assetto coagulativo
In corso di trattamento chemioterapico restaging ogni 2-3 cicli di
terapia
per valutare la risposta al trattamento
LESIONI NON PALPABILI
biopsia stereotassica
CHIRURGIA
+/-CHT/HT
RT
NEOPLASIE INIZIALI T1/T2
CHIRURGIA
CHT+/-HT
RT
TUMORI LOCALMENTE AVANZATI
terapia multimodale
CHT Chirurgia +/-RT CHT/HT
TUMORI METASTATICI ALLA DIAGNOSI
TUTTE LE PZ erb B2 positive (3+ )
HERCEPTIN in associazione alla cht/ ADJ per 1 anno
ESTENSIONE SISTEMICA METASTATICA
Nei tumori della mammella di diametro sup. a 1,5 cm il
problema diagnostico/terapeutico e prognostico e ’
rappresentato dal
NUMERO delle MICROMETASTASI e dalla loro
FARMACORESISTENZA
L ’ evento metastatico avviene nei primi 10-20
raddoppiamenti volumetrici.
0,5 cm
27 raddoppiamenti volumetrici
1 cm
30 raddoppiamenti volumetrici
2/3 della sua crescita
RICADUTA DOPO SOLA TERAPIA
LOCOREGIONALE
N+
N+
NN-
RO+
RORORO+
G, Ki 67, Erb B2.
45%
75%
45%
25%
Riduzione del rischio assoluto e relativo di
ricaduta con trattamento adiuvante
Globalmente riduzione del RR del
35%
Ndal 20 al 13%
7%
N+
dal 65 al 42%
23%
FOLLOW-UP
Il diametro del tumore T e la sua estensione ai linfonodi N rappresentano i
FATTORI PROGNOSTICI PRINCIPALI.
Hanno impatto sul tasso di ricaduta l’assetto recettoriale RO, l’indice cinetico,
l’espressione della p53, espressione dell’ erb B2.
DOPO IL TRATTAMENTO INIZIALE UNA FRAZIONE PIU’
O MENO IMPORTANTE DI PZ RICADE (DiseaseFreeSurvival)
Con un tasso di ricaduta max nei primi 3 anni, ancora significativo a 5 anni, possibile
fino a 20 anni
Primi 3 aa
EO
3 mesi
MT
”
MX
1aa/6mesi QUART
RX TORACE
6 mesi
ECO EPATICA
6 mesi
SCINTIGR.OSSEA
1aa
5aa
6 mesi
“
1 aa
1 aa
1 aa
/
dopo 5 aa
6 mesi
“
1aa
/
/
/
Carcinoma del polmone
CA DEL POLMONE
ITER DIAGNOSICO
Sospetto di ca polmonare
RX TORACE
TC TORACE
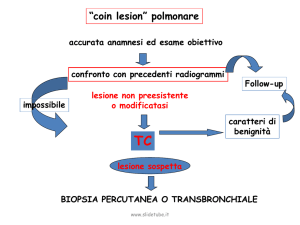
LESIONE PERIFERICA
LESIONE CENTRALE
Biopsia transparietale TC
guidata
Broncoscopia
Toracoscopia
Citologia broncolavaggio
Broncoscopia
Mediastinoscopia
(toracotomia
esplorativa)
ESTENSIONE METASTATICA SISTEMICA
TC TOTAL BODY CON CRANIO
SCINTIGRAFIA OSSEA
FUNZIONALITA' RESPIRATORIA
MT
EMATOCHIMICI
Sono candidati all’intervento chirurgico pz MO
RX TORACE / TC TORACE
TUMORE RESECABILE
T1 T2
Sospetto N2
mediastinoscopia
Lesione surrene
FNAB
Lesione epatica unica FNAB
TUMORE NON
RESECABILE
N2 linf mediastinici
N3 linf controlaterali
Versamento pleurico
T4
NSCLC
ESTENSIONE LOCO-REGIONALE
estensione del tumore primitivo
TC
torace
presenza adenopatie in sede ileomediastinica
infiltrazione della parete toracica
versamento pleurico
noduli polmonari multipli
La valuzione dei linfonodi e’ basata su un criterio
dimensionale PATOLOGICI SE MAGGIORI DI 1 CM
(falsi + 5%- falsi -10/30%) MEDIASTINOSCOPIA
RM
TC-PET
distingue la componente atelettasicada tumore
grado di infiltrazione della parete toracica
NSCLC
LA CHIRURGIA CON INTENTO RADICALE RAPPRESENTA IL
TRATTAMENTO PIU’ EFFICACE
- resecabilita’ del 10-25%
- sono sottoposti a resezione completa pz al I stadio (T1N0)
e stadio II
- pz allo stadio III A (T3 N1) devono essere sottoposti ad un
trattamento cht neoadiuvante
OPERABILITA’
SEDE
DIMENSIONI DEL TUMORE
ISTOTIPO (non microcitoma)
PS
NSCLC
OPERABILITA’
Tumori di diametro minore di 3 cm confinati al parenchima polmonare
Posizione periferica (distanti 2 cm dalla carena)
Atelectasia o polmonite limitata
Non versamento pleurico (T4)
Linfonodi ilari o mediastinici indenni
M0
Il ca polmonare presenta alla diagnosi metastasi subcliniche a dista
L’incapacità dei trattamenti locoregionali di controllare la malatti
La ChT di I linea (palliativa) nel ca
del polmone rappresenta il
trattamento di elezione nei paz con
malattia metastatica, versamento
pleurico, adenopatie sopraclaveari
Ca polmone
Follow up
E.O.
Rx Torace TC
Etg epatica
MT
TC total body
Scintigrafia ossea
OGNI 3 MESI
OGNI 12 MESI
Small Cell Lung Cancer
Malattia limitata
Malattia estesa
Tumore confinato a 1
emitorace con metastasi
ai linfonodi
mediastinici e
sopraclaveari
Metastasi a distanza
Adenopatie mediastiniche
controlaterali o sopraclav.
Versamento pleurico o
pericardico
IL TRATTAMENTO CHT E’ PREVISTO IN TUTTI I
CASI
DI MICROCITOMA
Gli esami di stadiazione sono orientati a selezionare i casi
candidabili a un trattamento RT TORACICO E PROFILATTICO A
LIVELLO ENCEFALICO
30% PZ CON MALATTIA LIMITATA IN RISPOSTA
COMPLETA DOPO CHT
SCLC
•
ESAME GENERALE
EO
Emocromo+esami biochimici
citologia espettorato
test funz. respiratoria
•
ESTENSIONE LOCO-REG
RX torace 2 p
TC torace
broncoscopia
mediastinoscopia
citologia versamento pleurico
biopsia adenopatie sovraclaveari
•
ESTENSIONE A DISTANZA
Scintigrafia ossea
TC total body
TC o RM encefalo
agoaspirato+biopsia osteomidollare
Valutazione della risposta ai
trattamenti
Valutazione della risposta in corso di cht
• LA RISPOSTA AL TRATTAMENTO DEVE ESSERE
VALUTATA OGNI 3 CICLI DI TERAPIA
• IL TRATTAMENTO DEVE ESSERE SOSPESO IN CASO DI
PROGRESSIONE
• LA RISPOSTA AL TRATTAMENTO DEVE ESSERE SEMPRE
VALUTATA CON LA STESSA METODICA
• LA TC DEVE ESSERE SEMPRE TOTAL BODY IN
MALATTIA MET (renali 13%,ovariche50%surrene
5%,GI20%,tiroide20%)
Esami ematochimici
Mt
Eco epatica o TC
Rx torace Tc
Scintigrafia ossea o rx delle sedi met