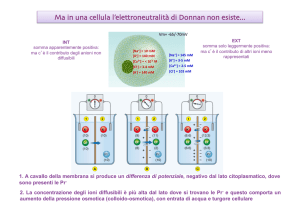
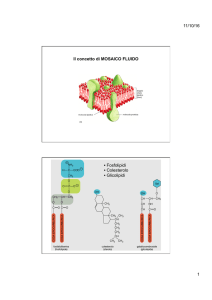
Canali “senza porta” (non gated) o canali di “leakage”
Sono presenti in tutte le membrane cellulari.
Sono sempre nello stato aperto.
Il flusso di ioni che li attraversa è detto “leakage” (perdita) perché tende
a cancellare i gradienti ionici creati ai due lati delle membrane dai
trasporti attivi.
Sono i responsabili della conduttanza di fondo delle membrane (leakage
conductance) che, essendo diseguale per le diverse specie ioniche,
gL=gNa,L+gK,L+gCl,L+gCa,L
(gNa,L≠gK,L≠gCl,L≠gCa,L)
genera quel fondamentale potenziale di diffusione che è il potenziale di
membrana a riposo (resting potential).
Esistono canali di leakage (“leakage channels” o “resting channels”) per
i tre ioni più diffusi nei liquidi organici: Na+, K+, Cl-.
Non se ne sa molto, perché sono stati studiati molto meno dei VOC e
dei ROC
Oltre ad essere fondamentali nel generare il potenziale di
membrana a riposo, i canali di leakage hanno un importante
finalismo:
limitare i gradienti ionici creati dalle pompe ioniche,
che di per sé tenderebbero ad aumentarli fino a livelli eccessivi.
1 - Canali del Na+ “epiteliali” (ENaC)
Il nome viene dal fatto che i dati sulla struttura di questi canali vengono quasi
esclusivamente da quelli presenti nell’epitelio dei tubuli renali (successivamente
anche del colon e degli alveoli polmonari), ma si ritiene che siano presenti in tutte
le cellule, dove darebbero un contributo al leakage di Na+.
Denominazioni alternative: Sodium
channels non-neuronal-1 (SCNN1) e
Amiloride-sensitive Sodium channel
(ASSC).
Oltre che al Na+, il canale è anche
permeabile al Li+ ed ai protoni (H+)
•La molecola è costituita da tre subunità (α, β e γ),
codificate da geni distinti.
•Stechiometria: α2β2γ2.
•Ogni subunità (ca. 700 aa) comprende due segmenti
transmembranari ed un loop extracellulare.
•Ambedue le estremità (-N e –C) pescano nel citosol.
Sono insensibili alla TTX
Sono sensibili all’amiloride, che viene impiegata in Medicina come diuretico.
Importanti per il riassorbimento dell’acqua nel tratto distale dei tubuli renali e nel colon
(dove la sua espressione è stimolata dall’aldosterone e dall’ADH).
Sono anche presenti:
nella membrana baso-laterale dei barocettori aortici.
nei recettori gustativi dell’epitelio linguale, (rivelazione degli stimoli salati (Na+) ed
acidi (H+).
nel pancreas, nell’ovaio e nel testicolo (funzione ignota).
2. Canali del K+ di tipo “leak” (o “2P”)
Vedremo che quella dei canali del K+ è una famiglia straordinariamente numerosa. Questo
è l’ultimo gruppo individuato.
È formato da due subunità disposte in tandem per formare il poro.
Ogni subunità è costituita da 4 STM, con 2 regioni-P.
In un primo tempo sono stati descritti 4 membri del gruppo (TWIK, TREK, TASK e
TRAAK), ma poi si è visto che sono 15.
Uno è sensibile al pH extracellulare, un altro è sensibile all’ac. arachidonico.
3. Canali cationici
Praticamente tutte le cellule sono dotate di canali cationici (che escludono il Cl- ma
lasciano passare tutti i cationi).
Attraverso questi canali (quando siano aperti) entrano Na+ e Ca2+, il K+ esce.
La corrente netta è entrante [I(Na+Ca)inw > I(K)ou].
il potenziale d’inversione è attorno allo zero.
NB I canali cationici sono la principale via di leakage per il Ca2+.
4. Canali del Cl- (CLC)
Sono presenti in tutte le cellule, ma sono numerosissimi nell’organo elettrico della
Torpedine (e di altri “pesci elettrici”), dove sono addensati nella membrana ventrale (non
nervosa) delle elettoplacche. Qui la presenza dei canali CLC ha il significato di stabilire
un contatto a bassissima impedenza tra le elettroplacche (che sono appilate, disposte in
serie), per consentire lo straordinario flusso di corrente (dell’ordine degli Ampère !) che le
attraversa durante la scarica dell’organo elettrico.
E’ appunto dall’organo
elettrico di Torpedo che
è stata estratta e
purificata la proteina
costitutiva di questi
canali,
denominata
CLC-0.
NB.
Dall’organo
elettrico
sono
stati
purificati (e poi clonati
per la prima volta)
anche i recettori-canale
nicotinici.
I canali del Cl- (CLC) sono stati i primi canali clonati, ma hanno strutture molecolari
atipiche rispetto al modulo “classico”.
La molecola è configurabile in 13 α-eliche (D1-D13), molte delle quali (ma non tutte !)
sono STM.
CLC-0 è il capostipite di una grande famiglia di proteine simili, presenti nelle membrane
cellulari di tutti i tessuti.
- CLC-1 è l’isoforma abbondantemente espressa nel muscolo scheletrico, le cui
fibrocellule infatti hanno una elevata gCl
Una mutazione di questa proteina dà la miotonia, riconducibile alla riduzione
della conduttanza al Cl-: vistosa ipertrofia ed ipereccitabilità muscolare,
paradossalmente associate a diminuita capacità contrattile.
- CLC-2 è presente in svariati tessuti.
- CLC-K1 e CLC-K2 sono tipiche del tubulo renale (Kidney), dove consentono il
riassorbimento del Cl- dall’ultrafiltrato (al seguito del Na+, riassorbito
attivamente). .
5. Canali CFTR
Questi “canali” (o trasportatori?) del Cl- sono stati particolarmente studiati, perché il loro
malfunzionamento per errore genetico (ereditario) causa una grave malattia
particolarmente diffusa nei Paesi nord-europei: la fibrosi cistica o mucoviscidosi.
La sigla sta per “Cystic Fibrosis Transmembrane (conductance) Regulator”, il nome che è
stato dato alla proteina associata alla malattia.
CFTR è una grossa molecola
proteica (ca. 1500 aa.) con due
domini
transmembranari
(Membrane
Sub
Domain)
(MSD1 e MSD2), ognuno dei
quali à costituito da 6 STM
(M1..M6, M7..M12).
Ognuno dei due MSD è seguito da un dominio intracellulare predisposto per legare
l’ATP: (Nucleotid Binding Domain) NBD1 e NBD2. Questi contengono una particolare
sequenza “ABC”: ATP Binding Cassette). Inoltre, nell’ansa intracellulare centrale della
molecola, è presente un dominio regolatore (R) che contiene punti di fosforilazione.
CFTR è un canale ionico attivato per via
fosforilativa (dalla PKA, AMPc-dipendente).
Nello stato defosforilato il canale è chiuso; quando
uno solo dei NBDs è fosforilato, il canale
attraverserebbe periodi di apertura brevi, e periodi di
apertura lunghi quanto tutti e due i NBDs sono
fosforilati.
La forma più comune di Fibrosi Cistica (70% dei casi) è dovuta alla delezione di una Phe
in posizione 508 (all’interno di NBD1).
La fibrosi cistica ha esito molto spesso fatale nei primi mesi di vita. Consiste in
un’aumentata viscosità di tutti i secreti esocrini, che diventano poveri di acqua (e ricchi
di Cl-); ciò ostacola il normale flusso dei secreti nei dotti ghiandolari, facilitando anche
l’insorgenza di infezioni.
Particolarmente gravi sono gli effetti sulla secrezione mucosa delle vie respiratorie
(compromissione della ventilazione alveolare) e sulla secrezione esocrina del pancreas
(compromissione della digestione, quindi dell’assorbimento, dei grassi e delle proteine).
La diagnosi precoce si può fare misurando la concentrazione del Cl- nel sudore del
neonato.
3. La Proteina Codificata dal Gene della Fibrosi Cistica:
Cystic Fibrosis Transmembrane Conductance Regulator (CFTR)
Un canale Cl2 insiemi di 6 domini transmembrana
2 “cassette di legame per l’ATP” (“proteina di trasporto ABC ”)
Cl-
est
int
N
ATP
ATP
dominio-R
C
CFTR è un canale al Cl- attivato dalla fosforilazione e dall’idrolisi dell’ATP
est
int
dominio-R
N
protein kinasi A
cAMP-dipendente
ATP
ATP
C
CFTR è un canale al Cl- attivato dalla fosforilazione e dall’idrolisi dell’ATP
Cl-
est
int
N
ADP
O
O-
P
O
O
O
O
P
O
O-
ADP
dominio-R
-O
O
P
O
O
O
P
-O O
O
C
4. CFTR aiuta a controllare il flusso di acqua attraverso gli epiteli
- particolarmente importante è questo processo a livello degli epiteli polmonari -
Cl- lume
Na+
acqua Cl-
superfice
“apicale”
Na+
1. I canali al Na+ degli
epiteli sono di solito
aperti, ma un intenso
flusso di Na+ richiede un
controione.
2. Se il CFTR è aperto,
il Cl- diventa il
controione. Quindi NaCl
fluisce attraverso la
membrana nel lume.
3. l’acqua quindi fluisce
attraverso le cellule per
mantenere la pressione
osmotica costante.
La superfice “basale” (rivolta
verso il sangue) è normalmente
molto permeabile agli ioni
4. Risultato: una
soluzione isotonica di
NaCl fluisce dal sangue
al lume* (o vice-versa)
* nel caso degli epiteli polmonari ciò diluisce
il muco favorendo gli scambi respiratori
5. Cosa c’è di sbagliato nel DF508?
Cl-
est
int
N
dominio-R
La mutazione più comune (70% dei mutanti):
una delezione di un singolo codon (3-nt) in posizione 508
nella ATP-binding cassette #1.
Una fenilalanina è deleta.
C
CFTR-DF508 normalmente non raggiunge la membrana plasmatica;
WT CFTR
CFTR-DF508