FENOMENO FISICO
è reversibile
la composizione della materia non cambia
Ad esempio i passaggi di stato sono fenomeni fisici: con la fusione, un cubetto di ghiaccio si
scioglie a temperature superiori a 0°C, ma la composizione della materia non cambia (si tratta
sempre di molecole di acqua, sia allo stato solido che allo stato liquido). Inoltre facendo scendere
la temperatura al di sotto degli 0°C, l’acqua ritorna allo stato solido, quindi è un fenomeno
reversibile.
FENOMENO CHIMICO
non è reversibile
la composizione della materia cambia
Ad esempio la combustione è un fenomeno chimico: dalla combustione di un pezzo di legna si
ottengono sostanze diverse da quelle di partenza e non si può partire dai prodotti della
combustione per formare il pezzo di legna iniziale!
La chimica studia le trasformazioni che avvengono nei fenomeni chimici.
La chimica come scienza nasce solamente tra il XVIII e il XIX secolo, quando gli scienziati
ripetono in modo ordinato gli stessi esperimenti su tutte le sostanze che hanno a disposizione.
Essi vogliono capire quali leggi regolano il comportamento chimico delle sostanze.
Un ELEMENTO CHIMICO è una sostanza semplice formata da atomi dello stesso tipo, tutti
uguali tra loro.
NOME ELEMENTO
Es.:
SIMBOLO
ferro
Fe
ossigeno
O
idrogeno
H
carbonio
C
azoto
N
zolfo
S
Un COMPOSTO CHIMICO è una sostanza formata da molecole tutte uguali tra loro, ciascuna
formata da almeno due atomi di diverso tipo.
NOME COMPOSTO
Es.
Acqua
Anidride carbonica
Glucosio
FORMULA CHIMICA
H2O
ogni molecola di acqua è formata da 2 atomi di
idrogeno e 1 atomo di ossigeno
CO2
ogni molecola di anidride carbonica è formata da
1 atomo di carbonio e due atomi di ossigeno
C6H12O6
ogni molecola di glucosio è formata da 6 atomi di
carbonio, 12 atomi di idrogeno, 6 atomi di
ossigeno
Gli scienziati tra il Settecento e l’Ottocento vogliono identificare gli elementi chimici,
separandoli dai composti che li contengono e catalogarli in base al loro comportamento nelle
reazioni chimiche. I metodi più importanti che utilizzano per scoprire le leggi fondamentali della
chimica sono:
SINTESI DI COMPOSTI: processo in cui si crea una sostanza facendo reagire i suoi
componenti
ANALISI DI COMPOSTI: processo in cui si usano reazioni chimiche per separare un composto
nelle sostanze che lo compongono
Nel 1870 il chimico russo Mendeleev riesce a classificare gli elementi: costruisce la TAVOLA
PERIODICA. Egli dispone gli elementi in righe orizzontali in base alla loro massa atomica,
partendo dagli elementi con atomi con massa minore, verso quelli con massa maggiore. Questo
ordinamento prosegue nella riga successiva e così via. Le colonne verticali si chiamano GRUPPI, le
righe orizzontali si chiamano PERIODI. All’interno di ogni gruppo si trovano elementi che hanno
proprietà chimiche molto simili tra loro. Ad esempio tutti gli elementi del primo gruppo si
combinano con gli elementi del penultimo gruppo. Gli elementi dell’ultimo gruppo si chiamano GAS
NOBILI o gas inerti perché non formano legami chimici con gli altri elementi.
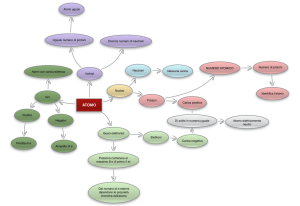
L’ATOMO
Verso la fine dell’Ottocento, gli scienziati scoprono che l’atomo è formato da particelle ancora
più piccole: neutroni, protoni ed elettroni.
Nel nucleo dell’atomo ci sono protoni e
neutroni.
Intorno
al
nucleo
ruotano
gli
elettroni.
Gli elettroni hanno carica elettrica negativa
I protoni hanno carica elettrica positiva
I neutroni non hanno carica elettrica
Un atomo è elettricamente neutro, perché ha la stessa quantità di cariche elettriche positive e
negative che si annullano a vicenda:
il numero di elettroni è uguale al numero di protoni. Il
numero atomico (Z) di un elemento è il numero dei protoni contenuti nel nucleo dei suoi atomi,
che corrisponde al numero di elettroni che ruotano intorno al nucleo.
Numero atomico di un elemento (Z) = numero di protoni = numero di elettroni
Es. il numero atomico dell’idrogeno è 1: significa che ogni suo atomo ha 1 protone ed 1 elettrone.
Es. il numero atomico del carbonio è 6: significa che ogni suo atomo ha 6 protoni e 6 elettroni.
Le proprietà chimiche di un elemento dipendono proprio dal suo numero atomico
Nella tavola periodica gli elementi non sono disposti secondo la massa atomica, ma secondo
il numero atomico!! Mendeleev infatti aveva ordinato gli elementi in base alla massa atomica, ma
aveva dovuto fare alcune eccezione, cioè cambiare di posto alcuni elementi, per far sì che gli
elementi dello stesso gruppo avessero comportamento chimico simile.
Gli elettroni non possono assumere una posizione qualsiasi intorno al nucleo, ma si muovono
dentro gusci concentrici, simili agli strati di una cipolla. Ogni guscio elettronico può contenere un
numero massimo di elettroni:
1. nel primo guscio possono stare 2 elettroni
2. nel secondo guscio 8 elettroni
1
3. nel terzo guscio 8 elettroni
2
e così via…
3
Gli atomi per diventare più stabili, cercano di completare il proprio guscio elettronico più
esterno: possono riuscirci formando legami chimici con gli altri atomi
I legami chimici si formano quando gli atomi cedono, acquistano oppure mettono in comune i
propri elettroni con gli altri atomi.