COMPITO A
PRIMO QUESITO
A) Primo Principio
Q-L = ΔU
Dove Q è la quantità di calore complessivamente scambiata dal sistema con l’ambiente( positva se
assorbita e negativa se ceduta)
L è il lavoro complessivamente scambiato ( positivo se <<uscente >> dal sistema e negativo se
<<entrante>>
ΔU è la variazione di energia interna
B) U è una variabile distato perché non dipende dalla trasformazione ma solo dallo stato iniziale e dallo
stato finale del sistema
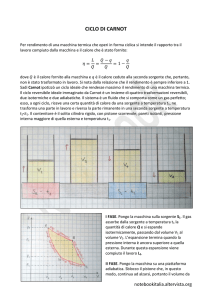
C)La figura a lato rappresenta una trasformazione ciclica di
un gas ideale.
Quali delle seguenti affermazioni sono vere?
Il lavoro compiuto dal gas è positivo nel percorso ABC e
negativo nel percorso CDA
VERO : la prima è un’espansione e la seconda una
compressione)
Il lavoro compiuto dal gas nel percorso ABC è uguale e opposto
compiuto nel percorso CDA
FALSO Le aree sottese dai due diagrammi non hanno uguale valore
a quello
Per compiere l’intero ciclo il gas deve complessivamente ricevere lavoro
dall’esterno
VERO Il lavoro complessivo è positivo ( l’area sottesa dall’arco di curva ABC è
maggiore dell’area sottesa dall’arco di curva ADC)
Per compiere l’intero ciclo il gas deve complessivamente assorbire calore
VERO : poichè ΔU=0, essendo lo stesso iniziale identico allo stato finale, Q =L
La variazione di energia interna relativa al
è uguale a quella relativa al percorso ABC
percorso CDA
FALSO le due variazioni sono uguali e opposte ( ΔU totale=0)
SECONDO QUESITO
In che senso il Secondo Principio della Termodinamica pone dei limiti alle
trasformazioni termodinamiche che vanno oltre a quelli imposti dalla
conservazione dell'energia?
Il Secondo Principio afferma che non esiste alcuna trasformazione termodinamica il cui unico risultato
sia
la conversione in lavoro del calore sottratto ad una sola sorgente termica ( Enunciato di Kelvin)
Il trasferimento di una quantità di calore da una sorgente più fredda ad una sorgente più calda
Pertanto sancisce l’impossibilità di alcuni processi che, pur non contraddicendo il Primo Principio, non
avvengono spontaneamente in natura.
Possono essere realizzati soloin concomitanza di altri effetti collaterali:
una macchina termica trasforma in lavoro una parte del calore assorbito, ma a paatto che restituisca
la parte rimante come calore a temperatura più bassa
Un frigorifero sottrae calore ad un corpo freddo per cederlo all’ambiente, più caldo, a patto di ricevere
lavoro dall’esterno ( in generale sotto forma di energia elettrica)
TERZO QUESITO
Una mole di gas perfetto monoatomico si trova in uno stato iniziale A,
caratterizzato da :
Pressione = 105 Pa
Temperatura = 400K
Il gas viene fatto espandere isotermicamente fino a dimezzare la pressione stato
B) ,poi viene riportato al volume iniziale mediante un’isobara (stato C)e infine è
riportato nello stato A mediante un’isocora
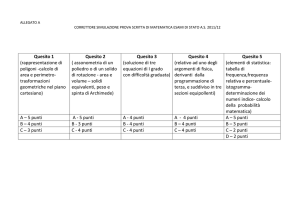
a) Tracciare il grafico del ciclo termodinamico, nel piano PV
b) Determinare i parametri di stato all’inizio e alla fine di ciascuna
trasformazione
c) Calcolare il valore del calore e del lavoro scambiato in ciascuna
trasformazione, indicando il verso dello scambio
Stato A
Stato B
Stato C
AB
BC
CA
TOTALE
Pressione (Pa)
2*10 5
10 5
10 5
Volume (dm3)
16,62
33,24
16,62
Temperatura (K)
400
400
200
Calore (J)
2304,02
assorbito
Lavoro J)
nRT ln(VB/VA)
=2304,02
compiuto
PB(VC-VB)=-1662
ricevuto
0
ΔU(J)
0
642,02
compiuto
0
Cp*(TC-TB)= -4155
ceduto
Cv(TA-TC)=2493
assorbito
642,02
assorbito
3/2 R(Tc-TB)=-2493
3/2 R(TA-TC)=2493
Nella tabella compare il bilancio energetico complessivo, come ulteriore verifica dei risultati
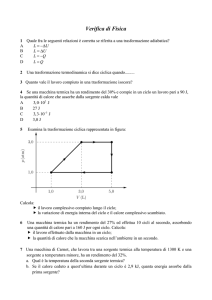
Nella figura a lato è rappresentato un ciclo termodinamico
costituito da due isoterme e due isocore, applicate ad una
mole di gas perfetto monoatomico.
Sapendo che
VA = 10 litr1 e VB = 30 litri
PA =
3 atmosfere e PC = 0,5 atmosfere
Determinare
Il valore di T1 e di T2
Il lavoro e il calore scambiati in ciascuna trasformazione
Il lavoro e il calore scambiati nell’intero ciclo
Applicando le proprietà dei gas perfetti
T2 = PA VA/R = 364,62 K
PD =3 PC =
PB = PA/3 = 1 atm =101 KPa
1,5 atm = 151,5 KPa
AB
Calore (J)
3328,78
BC
Cv(TC-TB)= - 2272,50
CD
T1=T2/2 = 182,31K
Lavoro J)
nRT2 ln(VB/VA) =3328,78
compiuto
0
ΔU(J)
0
3/2 R (TC-TB)=- 2272,50
-1664,40
nRT1 ln(VD/VC)= -1664,40 0
ceduto
ricevuto
DA
Cv(TA-TD)=2272,50
0
3/2 R (TA-TD)= 2272,50
assorbito
TOTALE
1664,38
1664,38
0
assorbito
compiuto
Nella tabella compare il bilancio energetico complessivo, come ulteriore verifica dei risultati
SECONDO QUESITO
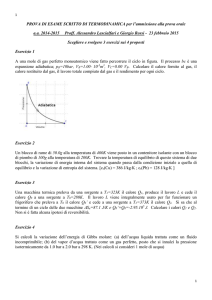
Un gas perfetto subisce una trasformazione ciclica che , nel piano PV , è
rappresentata da un rettangolo il cui contorno è percorso in senso orario.( come in
figura)
Quali delle seguenti affermazioni sono esatte? (Motivare le risposte)
Il lavoro complessivo è
Positivo
X
ciclo percorso in senso orario
Negativo
Nullo
La somma algebrica del calore scambiato è
Positiva
X
Q=L
poichè ΔU =0
Negativa
Nulla
La macchina che esegue questa trasformazione
riceve dall'esterno una quantità di calore Q e la trasforma integralmente in
lavoro
riceve una certa quantità di calore Q dall'esterno che, in parte viene
trasformata in lavoro e in parte va ad aumentare l'energia interna
riceve una certa quantità di calore Q dall'esterno che, in parte viene
trasformata in lavoro e in parte viene ceduta all’ambiente
X la macchina
assorbe calore nelle trasformazioni AB e DA mentre lo cede nelle altre duePertanto assorbe calore, ne converte una parte in lavoro e il resto lo cede
all’ambiente
TERZO QUESITO
VERO O FALSO ? (Motivare le risposte)
Due macchine di Carnot
lavorano tra le stesse temperature T1 >T2
Le due macchine hanno lo stesso rendimento VERO rendimento = (T1-T2)/T1
Le due macchine forniscono lo stesso lavoro FALSO non deriva necessariamente
dall’uguaglianza L/Q1 = L’/Q’1
Le due macchine assorbono la stessa quantità di calore dalla sorgente calda
e cedono la stessa quantità di calore dalla sorgente fredda
FALSO non deriva necessariamente dall’uguaglianza
(Q1-Q2)/Q1 = (Q’1-Q’2)/Q’1
Le due macchine forniscono lo stesso lavoro se e solo se assorbono la stessa
quantità di calore dalla sorgente calda VERO deriva dall’uguaglianza L/Q1
= L’/Q’1
Le due macchine cedono la stessa quantità calore alla sorgente fredda se e
solo se assorbono la stessa quantità di calore dalla sorgente calda VERO
deriva dalle uguaglianze L = L’ quindi Q1-Q2 = Q’1-Q’2