Def. Sono condizioni patologiche che conducono nei soggetti che ne sono affetti
un notevole rischio di contrarre infezioni e di sviluppare malattie autoimmuni o
tumori a causa di alterazioni del sistema immunitario.
Esse sono causate da alterazioni di uno o più meccanismi del sistema
immunitario e possiamo distinguerle in :
Primarie o
congenite
Secondarie
o acquisite
•Presentano un substrato ereditario
•Si ha la mutazione di uno o più geni
•Le alterazioni geniche determinano alterazioni nel funzionamento delle cellule
o della linea umorale sia innata che acquisita
•Le manifestazioni cliniche si presentano sia alla nascita che nella fase adulta
• Si manifestano nella vita postnatale in conseguenza di eventi quali :
•Infezioni virali
•Tumori (in particolare del sistema emolinfopoietico)
•Trattamento con farmaci immunodepressivi
•Carenze alimentari gravi
•Stress prolungati
•invecchiamento
DEFICIT DEL SISTEMA DEL
COMPLEMENTO
DEFICIT PRIMARI
DELL’IMMUNITA’
INNATA
DIFETTI DEI FAGOCITI
LAD
(LEUCOCYTE ADHESION DEFICIENCY)
IMMUODEFICIENZE
EREDITARIE
DEFICITI DELL’IMMUNITA’
SPECIFICA
UMORALE
DEFICIT PRIIMARI
DELL’IMMUNITA’
SPECIFICA
DEFICIT DELL’IMMUNITA’
SPECIFICA
CELLULO-MEDIATA
SCID
(SEVERE COMBINED IMMUNO
DEFICIENCY)
•Sono dovuti a patologie a carico dei geni che codificano per una o più delle proteine che
costituiscono il sistema del complemento
•Sono ereditate con meccanismo autosomico recessivo
•Possono essere coinvolti :
•sia i singoli elementi che costituiscono la cascata enzimatica
( da C1 a C9)
•sia le proteine regolatrici dell’attivazione per via classica o
alternativa (fattori H ed I ed il C1 inibitore)
•Questi difetti provocano :
•Suscettibilità alle infezioni da germi piogeni
•Sviluppo di malattie autoimmuni (Lupus eritematoso)
•Sviluppo di vasculiti ( infiammazione e necrosi dei vasi
,ischemia tissutale..etc)
•Sviluppo glomerulonefriti
Il deficit dell’inibitore di C1 ( C1 INH) è associato ad una trasmissione
autosomica dominante:
•Causa edema angionuritico ereditario malattia che comporta :
•Crisi dolorose da eritemi
•Edema della cute
•Edema delle mucose
Una altro deficit che interessa il sistema del complemento è quello riguardante la
lectina legante il mannosio (MBL) che causa una suscettibilità alle infezioni da
batteri Gram-positivi.
•Un esempio tipico è la malattia cronica granulomatosa
•E’ una sindrome molto rara a trasmissione ereditaria
•Caratterizzata da infezioni batteriche e fungine e formazioni di granulomi in
vari organi del corpo
I fagociti dei pazienti affetti da questa malattia dopo aver fagocitato l’agente
patogeno non riescono ad ucciderlo a causa di un difetto nell’esplosione
respiratoria che comporta scarsa o mancata formazione di derivati reattivi
dell’O2
Gli enzimi che intervengono in tale processo sono la famiglia di nicotinamide
adenina dinucleotide fosfato ridotto (NADPH) ossidasi noti come :
O 2-
O2
•p22
•p67
•p91
•Mieloperossidasi
MPO
NO
H2O2
ONOO-
HOCL
I derivati dell’O2 rappresentano il più potente meccanismo di uccisione microbica
definito killing intracellulare che viene attuato dalle cellule fagocitarie
Si ha un accumulo di fagociti che portano dentro i microrganismi ancora vivi
,determinando cosi la formazione di ascessi multipli e granulomi costituiti da :
•Cellule giganti multinucleate
•Macrofagi
•Linfociti
•Plasmacellule
•Polimorfonucleati
L’incapacità da parte dei leucociti di migrare nei siti dove è richiesta l’interazine con
altre cellule , determina risposte immunitarie inefficaci.
Una forma molto conosciuta è il LAD ( deficit di adesione leucocitaria)
Fra le varie molecole interessate abbiamo :
Integrine CD11 e CD18
che mediano il rapporto di adesione fra leucociti e endotelio vascolare
La LAD è dovuta ad una mutazione genica nel cromosoma 21q22.3 che
porta alla mancanza della catena b2 (CD18)
Le alterazioni che si osservano riguardano :
•Chemiotassi
•Adesione
•Migrazione leucocitaria
•Difetti di attivazione dovuti alla inefficenza di
interazione con le cellule portante l’antigene
Un esempio tipico e la sindrome di Chedeiak-Higashi caratterizzata da :
•Albinismo oculocutaneo parziale
•Infezioni ricorrenti da piogeni
•Aumento del tempo di sangunamento
•Progressivo deterioramento delle funzioni
neurologiche
•E’ presente una mutazione nel cromosoma 1 a livello del gene LYST
•La mutazione determina una incapacità di fusione dei granuli lisosomiali con
conseguente alterata degranulazione e con formazione di vacuoli
citoplasmatici giganti .
•Si osserva nell’85% dei pazienti sviluppo d linfomi
•L’osservazione dei leucociti mostra la formazione di granulazioni giganti
Riguardano sia i meccanismi umorali che quelli cellulari ed in taluni casi
entrambi
Spec.
cellulo
mediata
DEFICIT
PRIMARI
IMM.SPEC.
Spec.
umorale
SCID
Si ha l’incapacità o la ridotta capacità di produrre una o più classi di
immunoglobuline , con la conseguente suscettibilità alle infezioni.
La sindrome che le rappresenta è la agammaglobulinemia di Bruton che
presenta diverse variabili.
E’ causata dalla carenza di BTK o Bruton's tyrosine kinase, una tirosinchinasi
citoplasmatica che nei linfociti B svolge un ruolo importante nella trasduzione
del segnale.
In assenza della chinasi si arresta lo sviluppo dei linfociti B e la sintesi di
immunoglobuline.
La carenza di BTK blocca infatti il riarrangiamento dei geni VDJ per la regione
variabile delle immunoglobuline, e di conseguenza, la sintesi delle stesse.
La riduzione delle gammaglobuline, che rasenta l'assenza completa, rende i
bambini suscettibili alle infezioni batteriche e da enterovirus.
Si ricorda la sindrome di DiGeorge o ipoplasia timica congenita
•Deriva da un anomalo sviluppo branchiale del terzo e quarto
arco branchiale
•E’ caratterizzata da
1. aplasia o ipoplasia timica
2. Ipoparatiroidismo
3. Malformazioni cardiache
•
I pazienti presentano microdelezione del cromosoma
22q11.2 (circa 2 megabasi)
•
Una piccola parte dei pazienti presenta microdelezioni del
cromosoma 10p13-p14
•
I pazienti presentano difetti nei linfociti T e B più o meno
gravi
Vanno ricordate due in particolare :
Sindrome di Wiskott-Aldrick
Ataxia teleangectasica
Malattia ereditata con modalità autosomica recessiva caratterizzata da :
•coreoatetosi che comincia nell’infanzia (Corea :ovvero movimenti
a scatti, molto rapidi; Atetosi :movimenti molto ampi e, nell’esplicarli,
lenti )
•atassia cerebellare progressiva (progressiva difficoltà nella
deambulazione ed in altri movimenti)
•teleangectasia della congiuntiva e della cute (dilatazione delle
piccole arterie )
•Disartria (difficoltà nell’articolare a parola)
•Anomalie dei linfociti T e B
immunodeficienza umorale e cellulare e sensibilità alle radiazioni ionizzanti.
I pazienti affetti vanno soggetti ad:
•Infezioni senobroncopolmonari ricorrenti
•neoplasie linforeticolari e altre neoplasie maligne
L’alfafetoproteina serica generalmente risulta elevata.
La WAS risulta dallemutazioni nel gene che codifica per la
proteina WASP (Wiskott-Aldrich Syndrome Protein).
Il gene WASP è situato sul cromosoma Xp11.22 e codifica per una
proteina di 502 aminoacidi.
La WAS ha una trasmissione recessiva legata al sesso e pertanto
la maggioranza dei pazienti, oltre il 90%, sono maschi che hanno
una mutazione del gene WASP.
La proteina WAS WASP è una proteina citoplasmatica espressa
esclusivamente nelle cellule emopoietiche.
La precisa funzione di WASP non è nota, ma è probabile che essa
intervenga nella trasmissione del segnale all'interno delle cellule e
nella regolazione delle interazioni dell'actina con altre proteine del
citoscheletro consentendo il rimodellamento delle cellule ematiche
in risposta a stimoli esterni
Il percorso differenziativo delle cellule staminali linfoidi in linfociti T e B maturi
prevede numerosi fasi maturative .
L’alterazione di tale processo determina stati di immunodeficienza dovuti
all’assenza dei linfociti B e T maturi .
Se i precursori linfocitari non vanno incontro all’appropriato riarrangiamento dei geni
codificanti per il recettore per l’antigene (TCR) a causa della mutazione del gene
delle ricombinasi (RAG) o del gene deputato al riparo della doppia elica di DNA
(DSRB) non saranno generate cellule T e B mature.
Altri casi di SCID possono riguardare i recettori per le citochine
Nella maggior parte della SCID legata al sesso abbiamo un difetto della subunità
della catena gamma dei recettori delle interleuchine 2,4,7,9,15. questo determina
una interferenza con il segnale di sopravvivenza dei progenitori T
Si possono verificare difetti di espressione di molecole MHC con conseguente
difficoltà di presentazione ai linfociti T dell’antigene.
Mutazioni a carico dell’enzima ZAP-70 (tirosin chinasi) espressa solamente dai
linfociti T e dalle cellule natural killer induce una linfopenia T a causa di un blocco
maturativo timico e alterazioni nella trasduzione del segnale TCR.
Causa una immunodeficienza derivata dalla mancata sintesi di molecole MHC di
classe II.
E’ una forma recessiva di SCID e rappresenta il 5% dei casi .
La forma più comune riguarda le MHC di classe II, con conseguente alterazione
nella presentazione dell’antigene da ciò deriva la mancata selezione dei CD4+ e
la linfopenia T.
Il difetto non è a carico del gene per MHC ma per i fattori trascrizionali tra i quali :
•C II TA(transattivatore di classe II)
•RFX(fattore regolatorio X)
Sono stati identificati 2 agenti eziologici per
l’uomo :
Retrovirus
Hiv-1
Retrovirus
Hiv-2
SIV
(simian
immunodeficinecy
Virus)
HIV 1/2
FIV
( Human
immunodeficiency
Virus)
( Feline
immunodeficiency
Virus)
Immunodeficienze
acquisite
Tipo N
(non M e non O )
A
B
HIV-1
Tipo O (Outlier)
C
D
Tipo M
(main)
HIV
F1
G2
HIV-2
G
Molto simile al
SIV(nelle
scimmie)
K
I tre tipi di HIV-1 M,N,O si suppone derivano dal passaggio del virus similHIV
dallo scimpanzè all’uomo verificatasi in quelle regioni dell’Africa equatoriale che
sembra il luogo di origine del virus.
Tutti i sottotipi del gruppo M sembrano avere origine da un precursore comune
esistito probabilmente prima del 1940.
Il secondo tipo di HIV-2 è poco meno virulento
HIV-2 è strettamente imparentato con SIV (virus dell’immunodeficienza delle
scimmie)
Il contagio avviene per via :
•Sessuale
•Per inoculazione del sangue o dei suoi derivati
•Per via transplacentare
STADIO 1( durata variabile )
• Inizia generalmente dopo 2 o 3 mesi dal contagio. Si hanno eruzioni cutanee, febbre e linfonodopatia. Si
ha in questa fase una risposta anticorpale contro alcuni componenti del virus che è all’interno dei
linfonodi.
STADIO 2 ( lungo periodo )
• In questa fase si ha la distruzione dei linfociti T helper CD4+ ed un aumento della risposta anticorpale
contro gli antigeni virali
STADIO 3 ( variabile)
• Si ha uno sviluppo di linfoadenopatie dislocate in diversi settori
STADIO 4 ( variabile )
• I pazienti essendo affetti da immunodeficienza contraggono diversi tipi di infezioni dovute sia a germi
patogeni che opportunistici . Si possono avere complicanze come l’azione a livello del sistema nervoso
e il sarcoma di Kaposi.
ULTIMO STADIO ( la morte )
• I pazienti muoiono per deterioramento di tutto l’organismo.
Le principali patologie polmonari
-Polmonite da Pneumocystis jiroveci
-Tubercolosi
Le principali infezioni del tratto gastro-intestinale
-Esofagiti
-Diarrea cronica
Le principali patologie neurologiche
-Toxoplasmosi
- Leucoencefalite multifocale progressiva
-AIDS Dementia Complex
•I virus HIV infettano essenzialmente ma non esclusivamente i linfociti T helper
(CD4) ed i monociti/macrofagi .
•Per penetrare nelle cellule essi utilizzano principalmente una molecola di
superficie , la gp 120, che viene riconosciuta da un recettore , che è la
molecola CD4 , espressa dai linfociti T helper ed anche dai macrofagi.
•CD4 è sicuramente il più importante e diffuso recettore cellulare per il virus ma
non l’unico .
•Il virus può agganciarsi alle cellule e penetrare in esse attraverso recettori per le
chemochine.
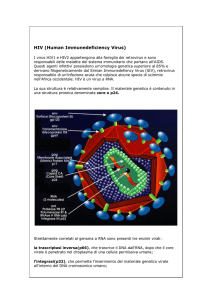
Appartiene al genus virale dei Lentivirus, della famiglia Retroviriadae
Ha una struttura sferica ed è formato da un capside circondato da un
envelope che deriva dall’insieme della membrana cellulare della cellula ospite e
della propria membrana.
Il capside è a forma di proiettile ed è formato dalla proteina virale più
abbondante la proteina p24 gag
•Sono presenti due molecole di RNA
uguali a costituire il genoma virale
•Associate alle molecole di RNA si
trovano 2 proteine p7 e la p9
•Sono presenti integrasi, proteasi,
trasriptasi inversa
•La superficie del virus è incastonata con
delle proteine dell’envelope (env) che
comprendono gp120 e la gp41
•Il complesso gp120-gp41 costituiscono
l’elemento chiave di riconoscimento per il
riconoscimento della cellula bersaglio.
•Sulla superficie di ogni virione esistono
72 trimeri di gp120-gp41 i quali
presentano un alto grado di
glicosilazione che determina
incapacitàdel sistema umorale anticorpomediato al riconoscimento del virus.
Simile a quello di tutti i retrovirus
1. I virioni si legano allo superficie
della cellula
2. Fusione membrana cellula-virus
3. Ingresso del capside virale
all’interno della cellula ospite
4. Retrotrascrizione del genoma virale
da RNA in DNA ed integrazione del
DNA virale di nuova sintesi nel
DNA della cellula ospite
5. Sintesi delle proteine del virus
attraverso l’utilizzo dei fattori
cellulari della cellula ospite
6. Assemblaggio di RNA e proteine
nei virioni di nuova sintesi
7. Fuoriuscita virioni dalla cellula
attraverso un processo di
gemmazione.
L’HIV contiene i 3 geni per le proteine strutturali presenti in tutti i retrovirus:
gag
Geni
strutturali
pol
env
Questi geni codificano le proteine virali e permettono il ciclo replicativo del
virus
Tat
Trans
attivatrice
REV
Regolatric
e virale
Sequenze
LTR
Proteine
costitutive
Vif
Fattore
infettività
virale
Vpu
Proteina
virale U
Nef
Fattore
negativo
di
regolazion
e
Vpr
Proteina
virioni R
Tat (proteina trans-attivarice)
• È fondamentale per la trascrizione di tutti i geni dell’HIV. Riconosce
una sequenza specifica all’interno delle frame delle LTR chiamata
TAR . Il genoma virale è compreso fra due LTR
Rev ( proteina regolatrice )
• È fondamentale per permettere il trasporto dei trascritti dell’HIV dal
nucleo al citoplasma della cellula infettata.
Nef ( negative factor )
• La sua trascrizione non è indispensabile per permettere la replicazione. Interviene nella
patogenesi e nella diminuita espressione delle molecole CD4. La gp120 si lega alle
molecole CD4 quindi interferirebbe con le funzioni del virus ecco perche si rende
necessario la diminuzione delle molecole di CD4
1. Legame di CD4 con gp 120 neosintetizzata
2. Degradazione CD4 da parte della proteina virale Vpu
3. Endocitosi del CD4 mediata da Nef
Vpr (proteina virionica R )
• È coninvolta in due processi fondamentali :
• 1 ) il trasporto nel nucleo del complesso virale reintegrato
• 2 ) l’arresto del ciclo cellulare
Vpu ( proteina virionica U )
•
•
•
•
È una proteina di membrana .
Sono riconosciute due funzioni inportanti :
1) Degradazione delle molecole CD4
2) Facilitazione del rilascio dei virioni dalla cellula infettata.
Vif (fattore di infettività virale )
• Sembra abbia un effetto nell’assemblaggio del virus HIV
• È incorporata nel core virale
La progressione dell’infezione ad AIDS è associata a una serie di complessi
difeftti della risposta immunitaria che coinvolge tutte le componenti del sistema
immune. Il preciso meccanismo di questi difetti è a tutt’oggi non chiaro.
•Vi è una drastica diminuzione della risposta cellulo-mediata con
suscettibilità ad infezioni di vario genere
•Si ha perdita della risposta anticorpale specifica
•Si ha immunità innata deficitaria
•I monociti/macrofagi possono essere infettati da HIV1
•La struttura dei linfonodi è alterata con sostituzione di tessuto fibroso
•Perdita dell’espressione delle cellule sia linfoidi che APC
Si osserva tanto l scomparsa delle cellule vergini CD45 RA+ quanto delle cellule
della memoria CD45 RO+ .
Esistono diverse teorie che cercano di spiegare la distruzione dei linfociti CD4+,
ma nessuna è ancora stata esaustiva.
•I linfociti T CD4+ possono morire per necrosi attraverso il diretto
contatto con nil virus
•Un altro fenomeno di morte è quello per apoptosi si pensa attraverso il
legame delle gp120 con le CD4
•Un altro fenomeno è la clearance delle cellule infettate da parte del
sistema immune tramite azione dei linfociti citotossici e i fenomeni di
ADCC( Citotossicità cellulare dipendente da anticorpi )
•La produzione ed il rilascio della gp120 in forma solubila dai virioni o
dalle cellule infettate potrebbe essere un eccanismo di deplezione dei
linfociti T
• Riduzione dei linfociti T al livello timico attraverso meccanismi di
selezione clonale dovute ad interferenze ad opera della gp120
Prof. Peter H. Duesberg
direttore del laboratorio di
Biologia Molecolare
dell'Università di Berkeley
in California
Robert C. Gallo 1984
“Science”
directore dell’istituto di
Virologia Umana,
all’università del Maryland
a Baltimora
“La cosa più importante nella scienza è non smettere mai
d'interrogarsi.”
Albert Einstein