LA RESPIRAZIONE
Il processo respiratorio consiste essenzialmente in una serie
di reazioni ossidative finalizzate a demolire le molecole
organiche (zuccheri, ma anche acidi grassi) per recuperare
parte dell’energia chimica in essa contenuta sotto forma di
energia libera (ATP)
Dal punto di vista biochimico il processo può considerarsi
suddiviso in tre fasi:
la GLICOLISI
il CICLO DEGLI ACIDI TRICARBOSSILICI TCA (detto anche
ciclo di Krebs o ciclo dell’acido citrico)
la FOSFORILAZIONE OSSIDATIVA ASSOCIATA ALLA CATENA
DI TRASPORTO ELETTRONICO
LA GLICOLISI
LA GLICOLISI
CONSISTE
IN
UNA VIA METABOLICA
CARATTERIZZATA DA 10 PASSAGGI CHE CONVERTONO UNA
MOLECOLA DI GLUCOSIO IN DUE MOLECOLE DI PIRUVATO CON LA
CONTEMPORANEA PRODUZIONE DI DUE MOLECOLE DI ATP
LA GLICOLISI AVVIENE NEL CITOSOL
LE 10 REAZIONI POSSONO ESSERE DISTINTE IN DUE DIVERSE FASI:
-FASE DI INVESTIMENTO ENERGETICO: gli zuccheri fosfati vengono
sintetizzati a spese dell’ATP ed il substrato a sei atomi di carbonio
viene scisso in 2 zuccheri a tre atomi di carbonio
-FASE DI PRODUZIONE ENERGETICA: i triosi fosfati sono convertiti
in composti ad alta energia che trasferiscono il fosfato all’ADP
sintetizzando ATP
LA RESA NETTA DEL PROCESSO GLICOLITICO PER
MOLE DI GLUCOSIO METABOLIZZATO E’ PARI A 2 MOLI
DI ATP E 2 MOLI DI PIRUVATO
VENGONO GENERATI ANCHE EQUIVALENTI RIDUTTIVI
SOTTO FORMA DI NADH (2 MOLI)
NEGLI ORGANISMI AEROBI, LA GLICOLISI E’ IL PRIMO
PASSAGGIO DELLA COMBUSTIONE COMPLETA DEL
GLUCOSIO A CO2 ED ACQUA
Fase di investimento energetico
GLUCOSIO
2 ADP
Fase di
produzione
energetica
4 ADP
2 NAD+
2 ATP
4 ATP
4 NADH
2 piruvato
Bilancio netto
Glucosio 2 Piruvato
2 ADP
2 ATP
2 NAD+ 2 NADH
FASE DI INVESTIMENTO ENERGETICO
LA FASE DI INVESTIMENTO E’ CARATTERIZZATA DA 5
REAZIONI
1)
FOSFORILAZIONE ATP-DIPENDENTE DEL GLUCOSIO
CATALIZZATA DALL’ENZIMA ESOCHINASI (G°’ = -16,7
kJ/mol). La fosforilazione del glucosio porta a due
obiettivi:
a. La reazione dell’esochinasi converte il glucosio nella
forma fosforilata nella quale non può essere
trasportato fuori dalla cellula
b. La forma “attivata” è più labile del glucosio e ne
permette la sua metabolizzazione
L’esochinasi è un enzima che ha bassa specificità per
gli zuccheri ed una bassa Km ed è inibita
retroattivamente dal suo prodotto il glucosio-6-P
E’ necessario lo ione Mg2+ poiché la forma reattiva
dell’ATP è il suo complesso chelato con Mg2+.
2) ISOMERIZZAZIONE DEL GLUCOSIO-6-P IN FRUTTOSIO-6-P
DA PARTE DELL’ENZIMA FOSFOGLUCOMUTASI (G°’ = +1,7
kJ/mol)
L’enzima è anche noto come FOSFOESOSOISOMERASI,
la reazione (isomerizzazione di un aldoso in un chetoso) è
reversibile alle normali concentrazioni cellulari dei due
esosi fosfati
3) FOSFORILAZIONE ATP-DIPENDENTE DEL FRUTTOSIO-6-P IN
FRUTTOSIO-1,6-bisP
DA
PARTE
DELL’ENZIMA
FOSFOFRUTTOCHINASI (PFK) (G°’ = -14,2 kJ/mol)
La reazione è praticamente irreversibile in vivo
Questo enzima rappresenta anche il sito primario della
regolazione della glicolisi; la PFK è un enzima allosterico
la cui attività è sensibile allo stato energetico della cellula,
così come ai livelli di citrato ed acidi grassi. Il suo
effettore allosterico è, come vedremo, uno degli ultimi
intermedi della intera via (FOSFOENOLPIRUVATO).
4) SCISSIONE DEL FRUTTOSIO-1,6-bis-P IN 2 INTERMEDI A 3
ATOMI DI CARBONIO CATALIZZATA DALL’ENZIMA ALDOLASI
(G°’ = + 23,9 kJ/mol)
I due intermedi sono la GLICERALDEIDE-3-FOSFATO
(GAP) ed il DIIDROSSIACETONFOSFATO (DHAP).
Questa reazione sottolinea un importante principio
metabolico. La reazione infatti è fortemente endoergonica
(G0’ = +23,9 kJ/mol). In realtà nella cellula le
concentrazioni di reagenti e prodotti sono tali che la
reazione procede verso destra. Si mette quindi in
evidenza la necessità di considerare le condizioni nella
cellula e non le condizioni standard per decidere quale sia
il senso della reazione.
L’aldolasi attiva il substrato rendendone possibile la
scissione mediante condensazione del carbonio
chetonico con il gruppo amminico del sito attivo e
formazione di una base di Schiff intermedia
(condensazione di un gruppo amminico con un gruppo
carbonilico).
5) ISOMERIZZAZIONE DEL DIIDROSSIACETONFOSFATO IN
GLICERALDEIDE-3-P DA PARTE DELLA TRIOSO FOSFATO
ISOMERASI (G°’ = +7,6 kJ/mol)
I due prodotti dell’aldolasi sono in equilibrio tra loro in
una reazione catalizzata dalla TRIOSO FOSFATO
ISOMERASI. Anche questa reazione è endoergonica (G0’
= +7,6 kJ/mol) in condizioni standard; la concentrazione
intercellualre di GAP è piuttosto bassa e questo sposta
l’equilibrio verso destra
FASE DI RESA ENERGETICA
LA FASE DI RESA E’ CARATTERIZZATA DA 5 REAZIONI
1) OSSIDAZIONE NAD-DIPENDENTE E FOSFORILAZIONE
DELLA
GLICERALDEIDE-3-P
IN
1,3-bis-P
GLICERATO
CATALIZZATA
DALL’ENZIMA GLICERALDEIDE-3-FOSFATO
DEIDROGENASI (G°’ = + 6.3 kJ/mol)
La seconda fase della glicolisi inizia con una reazione in
cui si ha la riduzione del NAD ossidato a NADH e la
contemporanea ossidazione del carbonio carbonilico con
scambio di due elettroni e produzione di un gruppo
carbossilico. La reazione è normalmente esoergonica, ma
diviene endoergonica perché l’enzima utilizza l’energia
rilasciata per sintetizzare un composto ad altissima
energia, l’acido 1,3-bis-FOSFOGLICERATO
2) FOSFORILAZIONE AL LIVELLO DEL SUBSTRATO CON
SINTESI DI ATP E FORMAZIONE DELL’1-3-bisP GLICERATO IN 3FOSFOGLICERATO OPERATA DALLA
FOSFOGLICERATO
CHINASI (G°’ = -18,8 kJ/mol)
Il composto precedentemente formato viene utilizzato da
questo enzima per la produzione di ATP e 3FOSFOGLICERATO (FOSFORILAZIONE AL LIVELLO DEL
SUBSTRATO)
L’1,3-bis-fosfoglicerato per il suo elevato potenziale di
trasferimento del gruppo fosfato possiede una grande
tendenza a cedere il suo gruppo fosfato all’ADP con
formazione di ATP
Essendo state investite 2 moli di ATP e con le due moli
che si formano in questa reazione, il bilancio netto in
produzione di ATP è uguale a 0
3) ISOMERIZZAZIONE DEL 3-FOSFOGLICERATO IN 2FOSFOGLICERATO
DA
PARTE
DELL’ENZIMA
FOSFOGLICERATO MUTASI (G°’ = +4,4 kJ/mol)
Il 3-fosfoglicerato viene quindi isomerizzato a 2fosfoglicerato. Nella reazione è richiesto anche lo ione
Mg2+
La reazione è di nuovo endoergonica in condizioni
standard, ma la concentrazione intracellulare di 3-PGA è
elevata rispetto a quella del 2-PGA, per cui la reazione
procede verso destra
4.
DISIDRATAZIONE
DEL
2-FOSFOGLICERATO
IN
FOSFOENOLPIRUVATO CATALIZZATA DALL’ENZIMA ENOLASI
(G°’ = + 1.7 kJ/mol)
Da questa reazione si libera il PEP, un altro composto ad
alta energia; la reazione prevede una disidratazione che
ha l’effetto di aumentare enormemente l’energia libera di
idrolisi del fosfato. Da –15.6 kJ/mol del 2-PGA a – 61.9 kJ/mol
del PEP
5. FOSFORILAZIONE AL LIVELLO DEL SUBSTRATO CON
SINTESI DI ATP E FORMAZIONE DEL PIRUVATO DA PARTE
DELLA PIRUVATO CHINASI (G°’ = - 31,4 kJ/mol)
Nell’ultima reazione della glicolisi il PEP trasferisce il suo
fosfato all’ADP nel corso di una FOSFORILAZIONE AL
LIVELLO DEL SUBSTRATO. La perdita del fosfato da parte
del PEP porta alla produzione della forma enolica del
PIRUVATO,
un
composto
molto
instabile
che
spontaneamente tautomerizza nella forma chetonica.
L’enzima richiede ioni Mg2+ e K+ . Questa reazione è un
altro punto di regolazione della glicolisi che determina la
produzione netta di 2 moli di ATP.
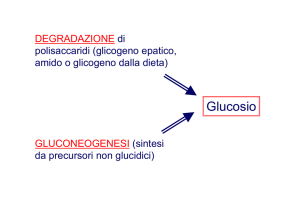
REGOLAZIONE DELLA GLICOLISI
La glicolisi è strettamente legata ad altre
importanti vie metaboliche per la produzione e
utilizzazione dell’energia; vedi utilizzazione
dell’amido, alla gluconeogenesi, alla via dei
pentosi fosfati ed al ciclo dell’acido citrico
Le reazioni catalizzate dalla ESOCHINASI,
FOSFOFRUTTOCHINASI e dalla PIRUVATO
CHINASI
procedono
con
una
riduzione
dell’energia libera E SONO TUTTE E TRE
REGOLATE ALLOSTERICAMENTE
1) La conoscenza dei meccanismi di controllo
della glicolisi è ancora imperfetta
La maggiore funzione regolatoria viene svolta
dalle
reazioni
catalizzate
dalla
FOSFOFRUTTOCHINASI e dalla PIRUVATO
CHINASI
Delle 10 reazioni coinvolte nella glicolisi, quelle
catalizzate
dalla
fosfofrutto-chinasi,
dalla
esochinasi e dalla piruvato chinasi sono
caratterizzate da un rapporto prodotto/substrato
molto più basso della loro costante di equilibrio
Questo significa che le reazioni catalizzate da
questi enzimi sono lontano dall’equilibrio e quindi
irreversibili in condizioni normali. Tutte le altre
reazioni della glicolisi sono invece molto vicine
all’equilibrio e quindi reversibili
Regolazione allosterica della
FOSFOFRUTTOCHINASI
Tra gli attivatori della PFK si annoverano :
- AMP
- ADP
- FRUTTOSIO-2,6-BISFOSFATO
Tra gli inibitori si annoverano :
- ATP
- CITRATO
- PEP
Regolazione allosterica della PIRUVATO
CHINASI
Tra gli inibitori
enzima l’ATP
si annovera anche per questo
Un secondo effetto allosterico è rappresentato
dall’attivazione a feedforward da parte del
FRUTTOSIO-1,6-bis-FOSFATO
- ACETIL-CoA
DESTINO METABOLICO DEL PIRUVATO
Il destino del piruvato è in funzione dello stato di
ossidazione della cellula
Nella reazione catalizzata dalla G3PDH una mole di
NAD+ viene ridotta a NADH. Per mantenere lo stato
redox della cellula questo NADH deve essere riossidato a NAD+
Quando la glicolisi avviene in condizioni
aerobiche questa funzione viene espletata dalla
catena di trasporto elettronico mitocondriale che,
tra l’altro, genera ATP
Quindi in condizioni di aerobiosi, l’ATP viene
generato direttamente dal processo glicolitico (2
moli) e successivamente dalla ri-ossidazione del
NADH
Ulteriori molecole di NADH vengono generate nel
ciclo successivo della respirazione (ciclo
dell’acido citrico o ciclo TCA). Il piruvato, infatti,
entra nel ciclo TCA nella forma di acetil-CoA che è
il prodotto della decarbossilazione ossidativa
operata dall’enzima PIRUVATO DEIDROGENASI
Diverso è il destino del piruvato in condizioni di
anaerobiosi, quando la catena di trasporto
elettronico mitocondriale non può funzionare così
come il ciclo TCA. L’ossidazione del NADH,
necessaria perché la glicolisi possa continuare a
funzionare, viene operata da due processi
alternativi: la FERMENTAZIONE LATTICA e la
FERMENTAZIONE ALCOLICA
La fermentazione è un processo che produce energia
attraverso molecole organiche che fungono da
donatore ed accettore di elettroni
I microrganismi sono capaci di effettuare diversi tipi di
fermentazione
La maggior parte dei composti naturali, ma anche i
prodotti
dell’uomo,
vengono
degradati
dai
microrganismi. In ambiente anaerobico questa
degradazione coinvolge il processo della fermentazione
Tutti i processi fermentativi si reggono su un principio
univoco:
Il NADH è sempre ossidato a NAD+
PERCHE’ ESISTE IL PROCESSO DELLA FERMENTAZIONE?
In assenza di ossigeno il ciclo TCA e la catena di trasporto
mitocondriale si bloccano proprio per il fatto che non c’è
l’accettore finale di elettroni
Quindi se il piruvato non può essere ulteriormente ossidato nel
ciclo TCA e la catena di trasporto elettronico mitocondriale non
funziona e quindi l’ATP non può essere sintetizzato, la glicolisi
rappresenta l’unica fonte di ATP per la cellula. Ma l’aumento
della concentrazione di piruvato determina una inibizione della
glicolisi e, se il NADH non viene ri-ossidato, si ha anche una
riduzione della concentrazione di NAD+ necessario per la
glicolisi
LA FERMENTAZIONE CONVERTE IL PIRUVATO IN COMPOSTI
ORGANICI
DIVERSI
E
QUINDI
RIDUCE
LA
SUA
CONCENTRAZIONE INTRACELLULARE E RIGENERA NAD+ DA
NADH
Esistono diversi tipi di fermentazione:
Fermentazione alcolica: è la fermentazione più importante a
carico dei glucidi, utilizzata da tempo immemorabile per la
produzione di vino, birra e pane. Il piruvato viene convertito in
alcol etilico e CO2
Fermentazione omolattica: trasforma il glucosio in acido
lattico, ad opera dei batteri Lactobacillus e Streptococcus.
Viene utilizzata per produrre yogurt, per la maturazione dei
formaggi, nella conservazione di alcuni vegetali (cetrioli, crauti,
olive in salamoia)
Fermentazione eterolattica: questa trasformazione produce,
oltre ad acido lattico, anche alcool etilico e anidride carbonica.
Viene utilizzata per la produzione di Kefir, un latte fermentato
acido-alcolico che si può produrre anche partendo da acqua
Fermentazioni ossidative: Queste trasformazioni non sono
vere e proprie fermentazioni, poiché avvengono in presenza di
ossigeno
FERMENTAZIONE ALCOLICA
IN QUESTO PROCESSO IL GLUCOSIO ED IL FRUTTOSIO
VENGONO CONVERTITI IN ALCOOL ETILICO CON LA
PRODUZIONE DI ANIDRIDE CARBONICA
MENTRE L’UVA CONTIENE COME TALI I DUE ESOSI, NEL
CASO DI ORZO E GRANO (per produrre birra e pane)
L'AMIDO DEVE ESSERE PRIMA IDROLIZZATO A
GLUCOSIO
VIENE
ATTUATA
DA
LIEVITI
DETTI
ANCHE
SACCAROMICETI, ORGANISMI UNICELLULARI EUCARIOTI
SI VERIFICA NEGLI ALIMENTI CONTENENTI CARBOIDRATI
CON pH SPICCATAMENTE ACIDO
LA REAZIONE DI FERMENTAZIONE ALCOLICA IN
AMBIENTE ANAEROBICO CONSENTE DI RI-OSSIDARE IL
NADH
QUOTIDIANAMENTE ABBIAMO A CHE FARE CON
FERMENTAZIONE ALCOLICA, AD ESEMPIO NEL VINO
LA
TROVIAMO PRESENTI SULLA BUCCIA DEGLI ACINI D'UVA
DEI LIEVITI CHE EFFETTUANO IL PROCESSO DELLA
FERMENTAZIONE ALCOLICA
QUESTO PROCESSO DEL VINO DURA GENERALMENTE DAI
6 AGLI 8 GIORNI
ALTRO ESEMPIO COMUNE E'
LA BIRRA,
OTTENUTA
AGGIUNGENDO AL MALTO D'ORZO O DI ALTRI CEREALI
SACCAROMICETI E LUPPOLO
PER QUANTO RIGUARDA IL PANE, I LIEVITI SI TROVANO
SULLA SUPERFICIE DEI CHICCHI DI GRANO. UNA VOLTA
OTTENUTA LA FARINA E MESCOLATA CON L'ACQUA SI
OTTIENE UN IMPASTO CHE VIENE FATTO CUOCERE
Nella prima reazione il piruvato viene decarbossilato dalla
piruvato decarbossilasi, un enzima che necessita per la sua
azione catalitica del coenzima tiamina pirofosfato (TPP).
La seconda reazione è reversibile e coinvolge la riduzione
dell’acetaldeide ad etanolo attraverso l’azione dell’enzima
alcool deidrogenasi. Il potere riducente per questa reazione
viene fornito dal NADH prodotto durante il processo
glicolitico. Il NAD+ generato durante il processo viene
riutilizzato per la glicolisi.
FERMENTAZIONE OMOLATTICA
L’acido lattico è l’unica molecola che si forma in questo
processo grazie alla riduzione del piruvato operata dalla
Lattato Deidrogenasi in condizioni di anaerobiosi. Questo
meccanismo alternativo comporta la riossidazione del
NADH attraverso la contemporanea riduzione del
PIRUVATO
E’ tipicamente condotta da specie del genere Lactobacillus
e da molti streptococchi
Questi batteri vengono utilizzati per la produzone di
yogurt, burro, formaggi etc.
Tipicamente avviene fermentazione omolattica in:
- CELLULE MUSCOLARI degli animali durante un intenso
esercizio fisico accumulano un debito di ossigeno che
induce la trasformazione dell'acido piruvico in acido lattico
che da' la sensazione di dolore e di fatica muscolare. Il
riposo ripristina una situazione di aerobiosi : l'acido lattico
è ritrasformato in acido piruvico e il dolore sparisce
- YOGURT è un latte fermentato. Il latte pastorizzato viene
fatto
fermentare
con
i
microrganismi
specifici
(Lactobacillus bulgaricus e Streptococcus termophilus),
raffreddato e conservato a 4°C fino al momento del
consumo, dove si presenta come prodotto vivo e vitale
- FORMAGGIO, è il prodotto della maturazione della
cagliata, ottenuta dalla coagulazione del latte intero o
scremato o della crema di latte, sufficientemente liberata
dal siero
FERMENTAZIONE ETEROLATTICA
Questa trasformazione produce, oltre ad acido lattico,
anche alcool etilico e anidride carbonica
Viene utilizzata per la produzione di Kefir, un latte
fermentato acido-alcolico che si può produrre anche
partendo da acqua
Questa via è caratterizzata dalla presenza dell’enzima
fosfochetolasi, che trasforma i pentosi in GAP ed acetilfosfato
E’
compiuta
soprattutto
da
batteri
eterolattici
(Lactobacillus e Leuconostoc) che vengono utilizzati
nell’industria fermentativa. Il kefir è un prodotto fermentato
del latte, analogo dello yogurt, ma è il prodotto della
fermentazione eterolattica
FERMENTAZIONI OSSIDATIVE
Queste trasformazioni non sono vere e proprie
fermentazioni, poiché avvengono in presenza di ossigeno
Quando l'ossidazione del glucosio è completa, si ottiene
anidride carbonica e ossigeno, se è incompleta si
ottengono sostanze diverse
È questo il caso della fermentazione acetica che ottiene
acido acetico da alcool etilico (utilizzata per produrre
aceto), e di quella citrica che ottiene acido citrico da
glucosio. Quest'ultima e altre fermentazioni sono utilizzate
industrialmente per produrre acido citrico e altre sostanze
di varia natura