Istituto Comprensivo “F. Jovine” - Scuola Secondaria di I grado
A.S. 2012-2013
Classi Prime
Disciplina: Scienze
Realizzato dal prof. Aurelio Nardelli
Gli stati della materia
La materia che compone il mondo
Materia: è tutto ciò
che occupa uno spazio,
cioè ha un volume, e ha
una massa e quindi un
peso
La materia che compone il mondo
Poiché esistono tanti tipi di materia, gli
scienziati li hanno classificati.
Ogni tipo di materia prende il nome di sostanza,
che può essere:
- organica, se compone i viventi, o inorganica, se
compone i non viventi;
- naturale, se esiste in natura, o artificiale, se
fabbricata dall'uomo.
La materia che compone il mondo
Una sostanza (o sostanza pura) è un tipo di
materia dotata di proprietà specifiche che la
distinguono da qualunque altra sostanza.
zucchero
acqua
filo di rame
alcol
La materia che compone il mondo
Ma che cosa rende le sostanze una diversa
dall'altra? Per rispondere a questa domanda
bisogna scendere all'interno della materia e
scoprirne la struttura.
La materia è composta da
particelle piccolissime
chiamate atomi.
Due o più atomi uguali o
diversi, uniti insieme,
formano una particella
piccolissima chiamata
molecola
La materia che compone il mondo
Le sostanze formate
da uno stesso tipo di
atomi
sono
dette
sostanze semplici o
elementi.
Es. mercurio
Le sostanze formate
da molecole costituite
da due o più atomi
diversi, sono dette
sostanze composte o
composti.
Es. Acqua
La materia che compone il mondo
Sostanze semplici
Sostanze pure
Sostanze composte
Materia
Omogenei *
Miscugli:
Miscela di due
o più sostanze
pure
Eterogenei
* i miscugli omogenei (es. acqua di mare) prendono anche il nome di soluzione
La materia che compone il mondo
Gli stati di aggregazione delle sostanze
Ogni sostanza, così come ogni miscuglio di sostanza,
può esistere in tre diversi stati di aggregazione che
sono caratteristici della materia: lo stato solido, lo
stato liquido e lo stato aeriforme o gassoso.
Proprietà dei solidi
Proprietà dei solidi
Le particelle che compongono un solido, sono
disposte le une vicino alle altre in posizioni
fisse, perchè tra esse agiscono potenti forze
di coesione che impediscono loro di spostarsi.
Pertanto, avremo
che i solidi hanno
una propria forma e
un proprio volume e
sono incomprimibili
Pirite
Forza di coesione
tra le molecole di
pirite
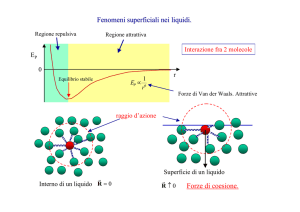
Proprietà dei liquidi
Proprietà dei liquidi
Possiamo immaginare un liquido come un insieme di
molecole vicine tra loro. Tra le molecole, agiscono forze
di coesione, più deboli rispetto ai solidi; perciò esse
hanno una certa libertà di movimento, che permette
loro di scorrere.
Proprietà dei liquidi
Le proprietà dei liquidi sono di seguito elencate:
- non hanno una propria forma
- hanno un proprio volume
- sono incomprimibili
- la superficie libera è sempre orizzontale
Proprietà dei liquidi
Tra le altre proprietà che caratterizzano il
comportamento dei liquidi abbiamo:
- La tensione superficiale
- Principio dei vasi comunicanti
- Capillarità
Proprietà dei liquidi
Tensione superficiale dell'acqua
Le molecole dell'acqua che si trovano sulla superficie
si comportano come una membrana elastica che
avvolge le molecole sottostanti, questo fenomeno è
detto tensione superficiale
Proprietà dei liquidi
Principio dei vasi comunicanti
un liquido contenuto in due o
più contenitori comunicanti
tra loro, in presenza di
gravità, raggiunge in tutti i
contenitori lo stesso livello
Proprietà dei liquidi
La Capillarità
è
un
fenomeno
che
permette
all'acqua
di
salire in tubicini molto
sottili. Questo fenomeno
è spiegato dall'esistenza
di forze di attrazione tra
le molecole dell'acqua e le
pareti del tubicino: tali
forze sono dette forze di
adesione.
Proprietà degli aeriformi
Proprietà degli aeriformi
Si chiamano aeriformi tutte le sostanze che
“hanno forma di aria", cioè godono delle
proprietà dell'aria.
Esempi:
- metano;
- elio;
- ossigeno;
- anidride carbonica;
- ecc.
Proprietà degli aeriformi
Gli aeriformi si distinguono in due categorie
Gas
Si definiscono gas le sostanze
che si trovano normalmente
allo stato aeriforme
Vapori
Sono vapori gli aeriformi
derivanti da sostanze che
sono normalmente allo
stato liquido o solido
Proprietà degli aeriformi
I gas non hanno una forma propria, ma tendono ad
occupare tutto lo spazio a loro disposizione.
Inoltre tra le molecole di gas non ci sono forze di
coesione, perciò sono libere e distanti tra loro: questo
è il motivo per cui i gas si lasciano comprimere
facilmente.
In conclusione possiamo dire che i gas non hanno una
propria forma ne un proprio volume
I cambiamenti di stato
I cambiamenti di stato
La solidificazione
La trasformazione di
una sostanza dallo
stato liquido allo stato
solido si chiama
solidificazione
I cambiamenti di stato
L'ebollizione e l'evaporazione
La trasformazione
rapida e tumultuosa
dallo stato liquido
allo stato di vapore
si chiama Ebollizione
Il passaggio lento
dallo stato liquido
allo stato di vapore è
chiamo Evaporazione
I cambiamenti di stato
La condensazione e la liquefazione
Il passaggio dallo
stato di vapore allo
stato liquido si
chiama
condensazione
La trasformazione
dei gas in liquidi
mediante
compressione e
raffreddamento si
chiama liquefazione
I cambiamenti di stato
La sublimazione
Il passaggio dallo stato
solido a quello di
vapore, senza passare
allo stato liquido, si
chiama sublimazione
I cambiamenti di stato
Il brinamento
La trasformazione
diretta da vapore
acqueo a ghiaccio viene
detto brinamento
Fine