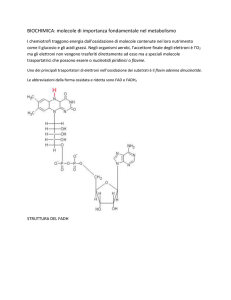
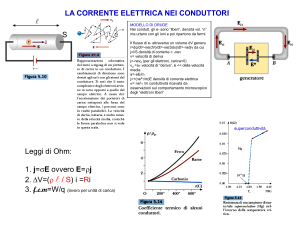
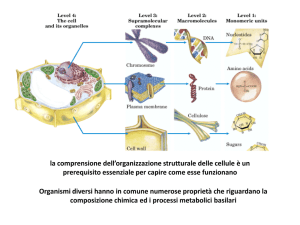
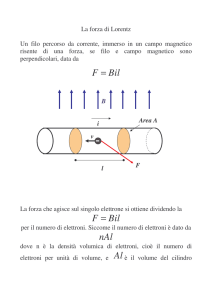
Corso di Laurea Specialistica in Ingegneria dei Materiali
Anno Accademico 2004-2005
Struttura della Materia
Prof. A. Barone
Studenti
Bonadies Irene
Farisco Loredana
Lanna Massimo
Romano Anna
INTRODUZIONE
2
1
4
SALI MOLECOLARI
1.1
Introduzione
4
1.2
Conduttori organici anisotropi
7
1.3
Superconduttività non convenzionale nei materiali organici
10
1.4
Sali di Bechgaard (TMTSF)2X e (TMTTF)2X
12
1.5
Conduttori organici bidimensionali: i sali (BEDT-TTF)2X
16
2
FULLERENI E NANOTUBI
21
2.1
Fullereni
21
2.2
Nanotubi
26
2.3
Struttura elettronica della molecola di C60
29
2.4
C60 e i suoi derivati
2.4.1
Superconduttività in M3 C60
2.4.2
Superconduttività nel C60 puro
3
ACENI
31
34
38
40
3.1
Introduzione
40
3.2
TTF-TCNQ
41
3.3
Gli aceni
3.3.1
La struttura e le proprietà
3.3.2
Struttura degli oligoaceni
3.3.3
Struttura dei poliaceni
3.3.4
Esempi di oligoareni ad anelli del tipo fenantrene
42
43
44
45
45
3.4
Da isolanti a superconduttori: il caso della superconduttività indotta mediante iniezione di carica in
cristalli molecolari
48
4
4.1
MATERIALI MOLECOLARI ORGANICI – APPLICAZIONI
Introduzione
52
52
4.2
Materiali conduttori a base organica
4.2.1
Trasporto di carica nei materiali organici
4.2.2
Applicazioni
52
54
56
4.3
Materiali organici elettroluminescenti
61
4.4
Materiali per la fotonica
64
BIBLIOGRAFIA
68
Introduzione
I progressi nel campo della superconduttività sono spesso legati alla scoperta di nuove
classi di materiali, gli ossidi cuprati ne sono un esempio lampante. I superconduttori
attualmente conosciuti coprono uno spettro di materiali molto ampio, spaziando in
complessità dagli elementi metallici alle leghe e ai composti binari, dai sistemi
multicomponente metallo-metalloide ai fullereni drogati e ai complessi a trasferimento di
carica.
Le sostanze organiche sono più attraenti delle loro controparti ceramiche poiché
possiedono una minore densità e si prestano potenzialmente meglio alla messa a punto
delle
proprietà
elettriche
ed
elettroniche
desiderate,
inoltre
il
loro
costo
è
considerevolmente minore.
La ricerca di superconduttori organici ebbe inizio nel 1965 a seguito della proposta di W.
A. Little secondo cui sarebbe stato possibile sintetizzare materiali organici che, come
alcuni metalli a bassa temperatura, avrebbero trasportato l’elettricità con resistenza nulla.
Da allora sono state identificate varie tipologie di superconduttori organici come ad
esempio i sali di Bechgaard ed i cristalli molecolari derivati dalla specie chimica
[bis(etilenditio)tetratiafulvalene].
In tempi più recenti è stata osservata la superconduttività nei fullereni, nei nanotubi, negli
aceni, nel tiofene, e negli oligomeri del polifenilenvinilene.
I materiali organici sono in genere considerati isolanti elettrici. McCoy e Moore nel 1911
suggerirono che sostanze come i radicali avrebbero potuto possedere le stesse proprietà
di conducibilità di un metallo senza presentare, tuttavia, atomi metallici nella loro struttura.
Il primo vero “metallo organico”, il TTF-TCNQ (tetratiafulvalene-7,7,8,8-tetraciano-pquinodimetano) fu sintetizzato solo nel 1973. Questo complesso a trasferimento di carica
mostrava una conducibilità di 1.7 × 104 ( cm)-1 a 66 K, questa persisteva fino alla
temperatura di 54 K in corrispondenza della quale il composto andava incontro ad una
transizione metallo-isolante.
In alcuni sali a trasferimento di carica sintetizzati da Bechgaard, la transizione metalloisolante poteva essere soppressa mediante l’applicazione di una pressione idrostatica, ciò
2
condusse alla scoperta del primo superconduttore organico, il (TMTSF)2PF6, composto a
base di tetrametil-tetraselenafulvalene.
Sebbene negli ultimi anni si sia riusciti a raggiungere nei fullereni drogati (in particolare nei
cristalli molecolari del tipo A3C60 dove A è un metallo alcalino) temperature critiche
prossime ai 40 K, le applicazioni dei superconduttori organici rimangono confinate in
ambito teorico.
D’altra parte, la scoperta di conduttori a base di carbonio, ha aperto la strada ai diodi ad
emissione di luce (OLED), ai sensori elettrici e addirittura alle batterie realizzati
integralmente in materiali polimerici, per non parlare dei Thin Film Transistor (TFT) per
schermi LCD e delle applicazioni nel campo della fotonica.
3
1 Sali molecolari
1.1 Introduzione
I sali molecolari, appartenenti alla famiglia dei conduttori organici, sono composti formati
da molecole organiche relativamente grandi, di circa 20 atomi, disposte secondo piani
sovrapposti.
I materiali composti da molecole organiche comunemente non sono conduttori a causa
dell’ibridazione che lascia piene le bande di valenza e di conduzione dando luogo alla
tipica struttura di un isolante. Un modo per rendere conduttori tali materiali è quello di
combinare le molecole organiche con anioni inorganici (ClO4, PF6 etc.) che fungono da
accettori o donori portando alla formazione di bande di conduzione e/o di valenza
parzialmente riempite. I materiali conduttori così ottenuti sono sali (detti a trasferimento di
carica) composti da un elettron-donore (solitamente la molecola organica) e un elettronaccettore (l’anione inorganico) alcuni dei quali mostrano proprietà superconduttive a
temperature molto basse.
La prima molecola organica con proprietà conduttive ottenuta è un sale a trasferimento di
carica: nel 1960 fu possibile osservare che il TCNQ (tetraciano-chinodimetano) formava
dei complessi cristallini per trasferimento di un elettrone da parte di un donore (che poteva
essere un metallo o un'
altra entità chimica ossidabile) verso lo stesso TCNQ, dando vita
ad un radicale-anione stabile TCNQ- che, complessato al controione positivo, risultava
essere un buon conduttore elettrico.
Nel 1974 fu possibile sintetizzare ed isolare il primo vero semiconduttore di origine
organica combinando un elettron-donore come il TTF (tetratiofulvalene) e un elettronaccettore come il TCNQ. Il TTF fu sintetizzato per la prima volta nel 1970 e può formare
un radicale-catione ossidandosi per trasferimento di un elettrone alla controparte elettronpovera, il TCNQ. Il composto organico così ottenuto, il TTF-TCNQ, presenta una
conducibilità massima di 104 S/cm alla temperatura di 59 K (figura 1).
4
Figura 1 Struttura chimica del conduttore organico TTF-TCNQ
Successivamente a questa scoperta la ricerca si è indirizzata verso la progettazione di
nuovi donori e nuovi accettori cercando di realizzare nuovi conduttori organici.
La possibilità di avere superconduttività in materiali organici fu suggerita da London nel
1937: egli avanzò l’ipotesi che i composti aromatici (antracene, naftalene…), sotto l’azione
di campi magnetici opportuni, potessero essere percorsi da una corrente superconduttiva
lungo gli anelli aromatici. L’esistenza dei superconduttori organici fu però teorizzata solo
nel 1964 da W. A. Little della Stanford University che suggerì che la temperatura di
transizione superconduttiva potesse essere aumentata fino a temperatura ambiente per
macromolecole opportunamente progettate: egli suggerì che i materiali a struttura
monodimensionale e bidimensionale (anisotropi) potessero essere superconduttori a
temperatura più alte rispetto a quelle a cui lo sono i materiali tridimensionali convenzionali
e applicò la sua teoria ai conduttori polimerici. Il meccanismo proposto da Little è
fortemente legato all’effetto isotopico, uno dei principali successi della teoria BCS per
l’interpretazione della superconduttività. L’interazione attrattiva tra elettroni (o buche), che
è il prerequisito per la condensazione delle coppie di elettroni (coppie di Cooper) nello
stato superconduttivo, per la teoria BCS dipende dalla massa degli ioni del reticolo
cristallino che subiscono uno spostamento finito quando gli elettroni passano attraverso di
essi (vale la relazione: Tc~M-1/2). Nel meccanismo proposto da Little c’è un’entità
elettronicamente polarizzabile usata al posto del reticolo ionico polarizzabile, di
conseguenza la piccola massa elettronica me porta ad un aumento di Tc dell’ordine di
(M/me)1/2 rispetto a quella osservata nei comuni superconduttori.
Il modello di Little si basava sull’uso di una lunga catena polimerica coniugata come quella
del poliacetilene con l’innesto di gruppi laterali polarizzabili.
Il primo superconduttore polimerico fu sintetizzato nel 1975 mentre solo nel 1980 fu
scoperto il primo conduttore organico con proprietà superconduttive a pressione
5
atmosferica: si tratta del sale (TMTSF)2ClO4 (tetrametiltetraselenafulvalene + accettore
inorganico) sintetizzato da Klaus Bechgaard e dal gruppo di ricerca francese di Jerome,
Mazaud e Ribault. Il TMTSF (figura 2) è ottenuto dalla famiglia dei tetratiofulvaleni
sostituendo gli atomi di zolfo con un elemento più pesante, il selenio, che stabilizza il
radicale-catione, mentre come anione non si utilizza il TCNQ ma uno ione inorganico
come il perclorato ClO4-. Il sale (TMTSF)2ClO4 risulta un ottimo conduttore a temperature
tra 0.5-1,5 K ma ha anche proprietà superconduttive. Nonostante questo composto
presenti una temperatura di transizione superconduttiva relativamente bassa (1,2 K), la
sua scoperta ha accresciuto l’interesse per la superconduttività nei materiali organici.
Figura 2 Struttura chimica del TMTSF
Dal 1980 sono stati sintetizzati più di 400 materiali organici con proprietà di conduzione,
dei quali più di 50 sono superconduttori alle basse temperature. Durante questo periodo la
temperatura di transizione superconduttiva in questi materiali è aumentata: nel 1987 è
stato sintetizzato il
-(BEDT-TTF)2I3 (bisetileneditiolotetra-tiofulvalene + accettore
inorganico) e successivamente preparato il (BEDT-TTF)2Cu(NCS)2 con una temperatura
di transizione vicina ai 10 K.
Anche il BEDT-TTF (figura 3) è ottenuto modificando il TTF per ottenere delle molecole
complicate con quattro atomi ad aumentare la stabilizzazione dei radicali-ioni.
Figura 3 Struttura chimica del BEDT-TTF
Attualmente la temperatura di transizione superconduttiva dei sali molecolari va da 1,2 K a
12,6 K (a pressione atmosferica). Nonostante la loro temperatura di transizione sia
relativamente bassa, le loro proprietà piuttosto inusuali li hanno resi attraenti per i
6
ricercatori: in questi materiali sono stati osservati un certo numero di stati interessanti
come quello di onde di densità di carica (CDW) e di onde di densità di spin (SDW) inoltre
presentano un’elevata magnetoresistenza. Quest’ultima proprietà è stata individuata nel
composto (TMTSF)2PF6: agli inizi del 1997 è stato infatti scoperto che esso è in grado di
resistere ad un campo magnetico di 6 tesla senza perdere le sue proprietà
superconduttive.
Rivolgeremo particolare attenzione ai sali monodimensionali di Bechgaard (TMTSF)2X e
(TMTTF)2X e ai superconduttori bidimensionali derivanti dal gruppo (BEDT-TTF).
Premettiamo alcune considerazioni teoriche che ci aiuteranno a comprenderne meglio le
proprietà.
1.2 Conduttori organici anisotropi
I metalli tridimensionali possono essere descritti mediante la nota teoria del liquido di
Fermi, che in genere si applica a sistemi tridimensionali di elettroni interagenti. Le
eccitazioni di una singola particella del liquido di Fermi sono le così dette quasi-particelle
che possono essere viste come particelle cariche singole (formalmente non interagenti)
circondate da una distribuzione di carica distorta. Le quasi-particelle hanno lo stesso
numero quantico delle particelle libere originarie e, come esse, obbediscono alla statistica
di Fermi-Dirac. Le interazioni elettrone-elettrone portano a una rinormalizzazione dei
parametri cinetici come la massa effettiva e ad una vita finita delle eccitazioni di singola
particella.
Il modello del liquido di Fermi che si applica ai sistemi tridimensionali non è valido in una
dimensione. Il modello adatto a descrivere un sistema di elettroni interagenti 1D è il
modello del liquido di Luttinger.
Una delle peculiarità dei liquidi di Luttinger è che le eccitazioni elettroniche elementari non
sono quasi-particelle di carica e- e spin ½ ma fluttuazioni collettive a carattere bosonico i
così detti spinoni e “holoni”. Queste eccitazioni di spin e di carica si propagano a differenti
velocità il che porta alla separazione di spin e carica. La figura 4 mostra un semplice
disegno di separazione spin-carica per un isolante antiferromagnetico, come si può vedere
in un esperimento di fotoemissione.
7
Figura 4 Separazione spin-carica per un isolante
antiferromagnetico
1D:
nel
processo
di
fotoemissione un elettrone viene eccitato e così una
buca (holone) viene prodotta nella catena. Il salto
della buca nei siti adiacenti o il salto dell’elettrone
vicino nel sito vuoto porta ad un disordine magnetico
(spinone). Ulteriori salti tuttavia, non causano
ulteriore disordine nella catena di spin. Così la buca
si separa in due difetti separati nella catena che
possono essere osservati come due particelle
separate.
Oltre alla separazione spin-carica, una caratteristica peculiare di un liquido di Luttinger è la
soppressione della larghezza spettrale in corrispondenza dell’energia di Fermi che fa
intuire la possibilità dell’apertura di uno pseudo-gap. Una soppressione della larghezza
spettrale è stata già osservata in molti composti 1D mediante esperimenti di fotoemissione
come nei composti organici TTF-TCNQ, (TMTSF)2X e (TMTTF)2X (X=PF4, ClO4, etc.).
Poiché questi composti tendono ad essere soggetti ad instabilità di Peierls o a transizioni
conduttore-isolante, le caratteristiche predette dei liquidi di Luttinger non possono essere
provate senza ambiguità.
L’instabilità di Peierls in sistemi di elettroni 1D è indotta dalla forte interazione elettronefonone dovuta alla topologia caratteristica della superficie di Fermi nei composti
monodimensionali. Per una singola catena monodimensionale di atomi la superficie di
Fermi consiste di due punti k=+kF e k=-kF; per una sequenza periodica tridimensionale di
catene non interagenti i punti di intersezione della banda di energia con l’energia di Fermi
giacciono su due piani paralleli perpendicolari alla direzione della catena e possono
essere shiftati l’uno sull’altro mediante una traslazione |k|=2kF. La sovrapposizione di parti
della superficie di Fermi come risultato di una traslazione è detto “annidamento” (nestling).
La superficie di Fermi e l’annidamento per sistemi di elettroni di diverse dimensioni sono
illustrate in figura 5: nel caso monodimensionale la sovrapposizione o “annidamento” è
perfetta mentre per un sistema bidimensionale la sovrapposizione si riduce a una linea
8
della superficie di Fermi cilindrica; per un sistema tridimensionale si riduce a un punto
singolo sulla sfera di Fermi.
Figura 5 Superficie di Fermi e annidamento di sistemi di elettroni di diverse dimensioni. Solo nel
caso monodimensionale l’annidamento, per una traslazione |k|=2 kF è perfetto.
Un conduttore monodimensionale è instabile nei confronti di distorsioni periodiche statiche
del reticolo cristallino al disotto di una temperature detta di Peierls a causa della proprietà
di annidamento della superficie di Fermi (instabilità di Peierls-figura 6).
Figura 6Instabilità di Peierls: un sistema di elettroni monodimensionale può abbassare la sua energia
totale mediante una distorsione del reticolo cristallino. Per una banda mezza-piena (a) un gap di
energia si apre in corrispondenza della nuova zona di contorno (c) a causa della distorsione del
reticolo.
Questa distorsione apre un gap di energia nella nuova zona di contorno e così l’energia
complessiva si riduce. La distorsione del reticolo provoca una modulazione della densità di
carica; il nuovo stato che si forma è chiamato stato di onda di densità di carica (CDW).
9
L’annidamento della superficie di Fermi nei metalli 1D favorisce pure lo sviluppo di onde di
densità di spin (SDW) ovvero una modulazione spaziale della densità di spin elettronico. In
contrasto con la transizione di Peierls non si verifica nessuna modulazione della densità
totale degli elettroni di conduzione o distorsione del reticolo cristallino. In relazione allo
sviluppo di densità di spin si apre un gap energetico in corrispondenza di EF, e quindi si ha
una transizione da conduttore a semiconduttore. Un tipico esempio di conduttore che
subisce questa transizione SDW è il sale (TMTSF)2PF6.
1.3 Superconduttività non convenzionale nei materiali organici
Il meccanismo della superconduttività nei superconduttori convenzionali è quello proposto
da Bardeen, Cooper, e Schrieffer (teoria BCS), per il quale gli elettroni superconduttori
sono accoppiati (coppie di Cooper) in uno stato di minima energia con vettore d’onda
totale nullo (cioè momento totale uguale a zero) e spin totale nullo (cioè stato di singoletto)
da una interazione debole degli elettroni di conduzione con i fononi cioè i modi normali di
vibrazione del reticolo cristallino (si parla di accoppiamento debole). Il momento angolare
orbitale relativo delle coppie può avere valore 0"("onda-s") ma anche 1"("onda-p"),
2"("onda-d"), e così via. Per massimizzare l’attrazione tra gli elettroni e i fononi, le coppie
di Cooper nelle teoria BCS si muovono nel più semplice canale di onda-s.
Pochi anni dopo che la teoria BCS fu formulata, Walter Kohn e Quin Luttinger
esaminarono la possibilità che si generasse un’attrazione debole residua tra gli elettroni
accoppiati in contrasto con l’insorgere della repulsione Colombiana. Trovarono che questa
attrazione si ha principalmente in un canale ad elevato momento angolare in cui agli
elettroni delle coppie di Cooper è impedito un avvicinamento eccessivo dalla presenza di
una barriera centrifuga. In alcuni materiali pesanti (ad esempio contenenti uranio) la
superconduttività può essere di onda-p (Heavy Fermion Systems). In generale tutti quegli
stati superconduttivi con deviazioni dal tipo convenzionale di accoppiamento degli elettroni
previsto dalla teoria BCS sono descritti dal termine “superconduttori non convenzionali”.
La natura del meccanismo di accoppiamento nei superconduttori organici rimane ancora
una questione aperta; evidenze sperimentali mostrano che la superconduttività organica è
molto sensibile alla presenza di impurità ed anche a difetti reticolari, che possono portare
alla formazione di un gap anisotropo nello stato superconduttivo. L’accoppiamento di
10
tripletto delle cariche attraverso lo scambio tra catene molecolari vicine è una possibile
causa dell’apertura di un gap anisotropo nella serie dei sali (TMTSF)2X.
Nel caso di un metallo tridimensionale dove la superficie di Fermi consiste di due punti a
kF e -kF sono possibili due stati per gli elettroni accoppiati con momento netto q=0:
superconduttivo con accoppiamento di singoletto con spin totale nullo e superconduttivo di
tripletto con spin totale pari a 1. L’accoppiamento di tripletto può essere possibile nei
metalli monodimensionali a causa della forte interazione di scambio ferromagnetico tra gli
elettroni. Al contrario della superconduttività di singoletto, le impurità influenzano
significativamente la superconduttività di tripletto e possono distruggerla completamente.
Analisi sul (TMTSF)2PF6 usando radiazione X per creare difetti nella struttura, mostrano
che la superconduttività svanisce quando la concentrazione dei difetti raggiunge un certo
valore limite.
Un aspetto della superconduttività nel (TMTSF)2X è il confine comune esistente tra la fase
superconduttiva e quella magnetica. Tipicamente i campi magnetici distruggono la
superconduttività perché l’energia che generano perturba la stretta interazione tra gli
elettroni delle coppie di Cooper, ma quando entrambi gli elettroni hanno spin di uguale
verso, quando mostrano il fenomeno dello spin di onda-p, il campo magnetico non può
distruggere la superconduttività. Questo avviene perché mentre il campo magnetico può
far variare l’energia totale degli elettroni, non può cambiare la differenza di energia tra di
loro. Il campo magnetico critico più alto nel (TMTSF)2PF6 supera il limite paramagnetico di
più del 200%. La forma anomala di Hc(T) è coerente con le più recenti previsioni del
comportamento non convenzionale dei superconduttori anisotropi, inclusa la possibilità di
accoppiamento di tripletto.
Esaminando le proprietà elettrodinamiche dei superconduttori possiamo imparare
qualcosa sull’eccitazione di elettroni dallo stato superconduttore a quello normale metallico
e sulla simmetria e dimensione del gap superconduttivo, per esempio attraverso la
dipendenza del gap dalla temperatura.
La scala di energie pertinente con la temperatura critica in accordo con la teoria BCS è E
=2 (0 K)=3,53 kBTC (con
gap energetico superconduttivo); ciò vuol dire che una
temperatura critica di 1 K porta a un gap energetico di circa 70 GHz. Quindi per lo studio
del gap superconduttivo si usano tecniche alle microonde e metodi ottici nel range
spettrale del lontano infrarosso.
11
1.4 Sali di Bechgaard (TMTSF)2X e (TMTTF)2X
I sali di Bechgaard (TMTSF)2X con X- anione monovalente (PF6-, AsF6-, SbF6- o ClO4-)
sono sistemi quasi-monodimensionali composti da molecole organiche disposte lungo
catene a zig-zag in direzione a, separate dagli anioni X- in direzione c (figure 7 e 8). Si
tratta di conduttori con una banda di conduzione riempita formalmente per ¾. Il
riempimento reale è pari a ½ a causa della debole dimerizzazione delle distanze
intermolecolari lungo le catene che divide la banda di conduzione in una banda piena a
energia minore separata da una banda mezza piena di energia più alta da un gap detto di
dimerizzazione.
Figura 7 Struttura del (TMTSF)2PF6. Le molecole organiche planari sono disposte lungo l’asse a
mentre in direzione c sono separate dagli anioni PF6-
Figura 8 Vista lungo i piani del (TMTSF)2PF6.
Le molecole del TMTSF sono orientate
lungo l’asse c; nella direzione b gli atomi di
selenio interagiscono a formare piani
bidimensionali.
12
Questi composti oltre a mostrare proprietà superconduttive alle basse temperature, sono
interessanti per diverse ragioni:
molti di questi sistemi sono buoni conduttori alle basse temperature prima di
diventare superconduttori;
nonostante siano fondamentalmente monodimensionali, le interazioni tra le catene
(la dimensionalità del sistema) possono essere modificate applicando una
pressione esterna o sostituendo gli anioni;
molti di questi sali presentano una transizione ad uno stato elettronico
fondamentale di onda di densità di spin o di onda di densità di carica;
la natura dell’anione può causare cambiamenti strutturali.
Mentre il (TMTSF)2ClO4 è il solo composto che a pressione atmosferica resta conduttivo al
di sotto della temperatura di 1 K, quando diventa superconduttivo, molti degli altri sali di
Bechgaard vanno incontro a transizione conduttore-isolante a temperature di circa 10 K; in
taluni casi la transizione può essere evitata con l’applicazione di una pressione esterna.
L’applicazione di una pressione esterna provoca una variazione della dimensione
prevalente delle molecole (dimensional crossover) e di conseguenza forti cambiamenti
delle proprietà elettroniche. Se un materiale è formato da catene conduttive singole e ben
distanziate (e dunque non interagenti) applicando una pressione esterna è possibile
diminuire la distanza tra le catene causando un accrescimento delle interazioni tra le
catene stesse. La dimensione da 1D diventa 2D passando attraverso la quasi-1D e infine
3D. Con il cambiamento dimensionale si verificano grossi cambiamenti nella fisica del
sistema: mentre i sistemi 1D possono essere descritti come liquidi di Luttinger per i sistemi
2D e 3D ci si aspetta un comportamento da liquido di Fermi. La trasformazione
dimensionale porta a variazioni delle correlazioni tra gli elettroni e delle eccitazioni
fononiche, in definitiva provoca transizioni di fase, e in alcuni materiali può indurre la
transizione superconduttiva.
Molti dei sali di Bechgaard (TMTSF)2X diventano superconduttivi sotto una pressione
esterna, con una temperatura massima di transizione superconduttiva di 1-2 K. La stessa
transizione dovuta agli effetti della pressione può essere indotta dalla pressione chimica
ovvero dalla eventuale sostituzione di atomi: la sostituzione dell’anione X- (-PF6-, AsF6-,
SbF6- o ClO4-) porta alla formazione di sistemi conduttori alcuni dei quali mostrano
proprietà superconduttive; anche dalla sostituzione degli atomi di selenio nelle molecole di
13
TMTSF è possibile ottenere altri sali a trasferimento di carica, in particolare la serie
isostrutturale dei sali (TMTTF)2X.
La grande varietà di stati fondamentali dei composti del (TMTSF)2X e del (TMTTF)2X con
diversi anioni X- può essere descritta da un diagramma di fase (T-P) (figura 9).
Figura 9 Diagramma di fase (T-P) dei sali quasi-1D (TMTSF)2X e (TMTTF)2X. A seconda della
pressione esterna o chimica (dimensioni dell’anione X-), c’è una grande varietà di stati fondamentali:
stato isolante con localizzazione di carica (LOC), stato d’ordine di carica (CO), stato di spin-Peierls
(SP), antiferromagnetico (AFM), stato di onde di densità di spin (SDW) e stato superconduttivo(SC).
Come mostra il diagramma di fase, i composti alla sinistra del diagramma sono isolanti al
disotto della temperatura ambiente mentre quelli alla destra del (TMTTF)2Br mostrano un
esteso intervallo di temperature nel quale hanno comportamento conduttivo. La causa del
comportamento isolante in molti di questi composti deve essere ricercata nel ruolo
comune che svolgono la repulsione elettronica e la bassa dimensionalità.
Un aspetto fondamentale del diagramma è l’esistenza di una grande varietà di stati
fondamentali esistenti al disotto dei 20 K. Per esempio, il composto (TMTSF)2PF6 mostra
un comportamento conduttivo sopra la temperatura TP=12 K, con un crossover da 1D a
2D al crescere della temperatura; sotto TP si assiste alla formazione di onde di densità di
spin. Applicando una pressione esterna P le proprietà del (TMTSF)2PF6 possono essere
variate sistematicamente: variando la pressione esterna questo composto può esplorare
tutta la serie di stati fondamentali. Per P>=7 kbar il composto è conduttivo fino a circa 1 K,
con un crossover dimensionale da 1D a 2D, e infine a 3D al decrescere della temperatura;
14
sotto circa 1 K il materiale diventa superconduttivo. Riportiamo in figura 10 l’andamento
della resistività elettrica del (TMTSF)2PF6 con la temperatura a diverse pressioni.
Figura 10 Resistività del (TMTSF)2PF6 a diverse pressioni (la corrente percorre il campione in
direzione parallela alle catene molecolari)
Effetti simili a quelli indotti dalla pressione esterna sono provocati dalla sostituzione
dell’anione X- con atomi di grandezze differenti cioè dalla pressione chimica. Ad esempio
(TMTSF)2ClO4 si comporta come (TMTSF)2PF6 sotto una pressione esterna: è conduttivo
fino a temperature basse mentre diventa superconduttivo a TC=1,2 K.
Comparati ai composti (TMTSF)2X, i sali (TMTTF)2X sono più monodimensionali poiché le
interazioni tra catene molecolari vicine sono più deboli. La dimensionalità ridotta porta ad
instabilità del sistema elettronico e influisce sulle proprietà di trasporto di carica e su quelle
magnetiche. Comunque, applicando una pressione esterna o una pressione chimica
avviene un crossover dimensionale verso dimensioni maggiori. I parametri cruciali che
determinano lo stato fondamentale restano quindi la pressione chimica da un lato e la
pressione esterna dall’altro.
Diversi studi hanno stabilito che questi materiali sono superconduttivi nel senso
convenzionale di esibire sia resistenza nulla al trasporto di carica che espulsione del
flusso magnetico (effetto Meissner). Comunque il meccanismo della superconduttività
risulta ancora incompreso.
Come mostrato dal diagramma di fase, il (TMTSF)2ClO4 se raffreddato rapidamente
diventa superconduttivo a 1,2 K; il (TMTSF)2PF6 d’altro canto necessita di una pressione
15
esterna di 6,5 kbar per diventare superconduttivo. Focalizzeremo la nostra attenzione sul
(TMTSF)2ClO4 perché è il solo composto sul quale sono stati condotti un gran numero di
esperimenti come le misure del calore specifico.
Figura 11 Andamento del calore specifico con la temperatura per il (TMTSF)2ClO4
La curva C(T) (figura 11) mostra infatti una evidente anomalia in corrispondenza di una
temperatura di circa 1,2 K. Sopra gli 1,22 K il calore specifico obbedisce alla relazione
classica valida per i metalli: C/T = + T2 dove
= 10,5 mJmol-1K-2. Il calore specifico
subisce un salto quando si ha: C/Tc = 1,67. L’andamento di C(T) nello stato
superconduttivo porta alla determinazione di un campo critico termodinamico Hc= 44 ± 2
Oe e ad un gap di singola particella 2 = 4 K che si deprime alla velocità di 1,1 mK/Oe-1
quando un campo magnetico viene applicato lungo l’asse c. Il carattere anisotropo della
struttura elettronica di questo composto, noto per l’anisotropia dei dati ottici, si riflette in
una severa anisotropia dei campi critici HC2 misurati lungo le tre direzioni principali della
struttura.
1.5 Conduttori organici bidimensionali: i sali (BEDT-TTF)2X
I conduttori organici bidimensionali sono cristalli molecolari conduttivi a temperatura
ambiente. Per raffreddamento alcuni di questi cristalli diventano superconduttivi sotto i 13
K, alcuni restano conduttivi, altri vanno incontro a transizione conduttore-isolante.
16
Figura 12 Struttura cristallina schematica di un conduttore organico basato sul BEDT-TTF. In rosso è
evidenziata una singola molecola di BEDT-TTF.
I cristalli sono composti di strati di molecole di BEDT-TTF (bisetileneditiotetratia-fulvalene)
(figura 12) disposti tra due strati di anioni. Gli orbitali elettronici
degli anelli aromatici del
BEDT-TTF si sovrappongono formando una banda di conduzione. Lo strato di anioni dona
elettroni alle molecole di BEDT-TTF, fornendo una carica negativa di circa 0,5 e- per
molecola di conseguenza la banda di conduzione risulta solo parzialmente piena e il
materiale diventa conduttivo. Le proprietà di conduzione si osservano solo all’interno degli
strati mentre in direzione perpendicolare lo strato isolante di anioni blocca il trasferimento
di carica; per questa ragione questi materiali sono chiamati conduttori bidimensionali.
La storia di questi materiali è un esempio eccitante di come una teoria fisica può aprire un
nuovo campo della fisica dello stato solido e portare alla scoperta di nuovi materiali. Nel
1964 fu pubblicato da Little lo studio che prediceva la superconduttività a temperatura
ambiente nelle molecole organiche (polimeri a quel tempo) ricche di elettroni; ironicamente
lo
scritto
era
fondamentalmente
sbagliato
in
quanto
riguardava
strutture
monodimensionali, che possono essere conduttive alle alte temperature ma che
presentano sempre uno stato fondamentale isolante. Comunque, gli scienziati dei materiali
cominciarono a lavorarci sopra, e nel 1979 fu scoperta la superconduttività nei cristalli
quasi monodimensionali (i sali di Bechgaard ) e nel 1984 apparve il primo conduttore
organico bidimensionale a pressione atmosferica: il
-(BEDT-TTF)2I3. Cambiando i
parametri chimici e fisici dei cristalli la temperatura della transizione superconduttiva è
cresciuta fino a 12 K per il -(BEDT-TTF)2Cu[N(CN)2]Br.
Questi materiali sono di grande interesse sia per i fisici teorici che sperimentali non solo
per le proprietà superconduttive, ma anche perché sono modelli ideali di superconduttori
bidimensionali. E’ stato proposto recentemente, che gli stati fondamentali osservati nei
17
conduttori basati sul BEDT-TTF cioè la superconduttività, uno stato isolante d’ordine di
carica, e le deviazioni dal comportamento di Drude nello stato conduttivo, sono tutti legati
allo stesso effetto: forti interazioni elettrone-elettrone. Come risultato, un piccolo
cambiamento della distanza di correlazione tra gli elettroni che formano le coppie, porta a
un cambiamento dello stato fondamentale del sistema.
Un esempio è il diagramma di fase in figura 13, dove è mostrata una dipendenza dello
stato fondamentale dal rapporto tra la repulsione elettronica e la larghezza di banda; le
frecce suggeriscono le posizioni dei materiali studiati più di recente.
Figura 13 Diagramma di fase proposto per un conduttore organico con una banda di conduzione
riempita per ¼. Le frecce indicano i composti: -(BEDT-TTF)2MHg(SCN)4 (M=Tl, K, NH4) e -(BEDTTTF)2I3.
Gli aspetti caratteristici di ciascuno stato fondamentale si osservano bene negli spettri di
conducibilità ottica (figura 14) ottenuti attraverso misure di riflettanza. Nello spettro dell’ (BEDT-TTF)2I3 è presente uno stato isolante a temperature inferiori a T=135 K. Un gap
superconduttivo di 25 cm-1 si osserva sotto Tc=8 K per l’ t-(BEDT-TTF)2I3. Nello spettro di
questo materiale e del superconduttore (Tc~1 K) -(BEDT-TTF)2NH4Hg(SCN)4 è presente
un evidente picco di Drude nello spettro dello stato normale a bassa frequenza. Di
maggior interesse sono i sistemi -(BEDT-TTF)2MHg(SCN)4 (M=K, Tl): la conducibilità in
corrente continua mostra che sono conduttivi sotto i 4 K, mentre nello spettro ottico appare
uno pseudo-gap in corrispondenza di 300 cm-1 sotto i 100 K. Questo viene interpretato
come una evidenza delle fluttuazioni dell’ordine di carica legate alla transizione di fase;
parte del sistema elettronico diventa ordinato, mentre uno stretto picco di Drude è
responsabile della conducibilità metallica. Quindi questi risultati supportano il diagramma
di fase ipotizzato.
18
Figura 14 Conducibilità ottica di alcuni composti organici con banda di conduzione riempita per ¼.
Anche più di 10 anni dopo la loro scoperta la questione se lo stato superconduttivo è del
tipo convenzionale BCS rimane controversa. Vari esperimenti volti a esaminare lo stato
superconduttivo dei sali del BEDT-TTF indicano deviazioni da quanto ci si aspetta
dall’accoppiamento debole tra gli elettroni. Il campo critico mostra un comportamento
inaspettato alle basse temperature mentre molte misure del calore specifico esibiscono
una strana dipendenza dalla temperatura (come T3), tuttavia altri esperimenti trovano il
calore specifico in accordo alla teoria BCS. Questi esperimenti sono stati interpretati in
termini di accoppiamento di tripletto, transizioni di onde di densità di spin sotto TC, e
transizioni vetrose di vortice come ci si aspetta da uno stato fondamentale con un
accoppiamento elettronico a più alto momento.
Misure di magnetizzazione a bassa frequenza con Hac parallela agli strati molecolari,
portano ad una inusuale profondità di penetrazione lungo il piano bc, e una dipendenza da
T2 suggerisce un maggiore accoppiamento dei momenti. Studi della magnetizzazione
reversibile, comunque, mostrano l’evidenza di un accoppiamento convenzionale alla
Cooper.
I modi più diretti per valutare il gap superconduttivo sono esperimenti di tunneling e ottici.
Mentre le prime misure degli spettri da tunneling nello stato superconduttivo mostrano
chiaramente una struttura a gap, nonostante questo sia più largo di quanto ci si aspetta,
19
misure di assorbimento ottico del (BEDT-TTF)2Cu(NCS)2 a temperature di circa 6 K non
mostrarono alcuna indicazione di una transizione superconduttiva per frequenze basse
(approssimativamente di 10 cm-1). Questa discrepanza non è stata risolta fino ad adesso e
ulteriori indagini sono necessarie. Sarebbe molto interessante studiare la dipendenza dalla
temperatura del gap e la sua dipendenza dal campo magnetico esterno. Recentemente
sono state condotte misure di riflettanza nel vicino infrarosso del superconduttore organico
at-(BEDT-TTF)2I3 fino a frequenze di 10 cm-1 (figure 15 e 16). Nello stato superconduttivo
si apre un gap energetico a 25 cm-1 che corrisponde a 2 /kBTc=4,4 in accordo con un
accoppiamento moderato.
Figura 15 Conducibilità relativa dell’at-(BEDT-TTF)2I3
Figura 16 Riflettanza e conducibilità
dell’ at-(BEDT-TTF)2I3
20
2 Fullereni e nanotubi
2.1 Fullereni
Si è ritenuto a lungo che diamante e grafite fossero le uniche forme allotropiche del
carbonio, tuttavia era noto da tempo che alcune particolarità degli spettri di assorbimento
delle regioni interstellari erano da attribuire alla presenza di grosse molecole di carbonio.
Allo scopo di generare tali molecole in laboratorio, Kroto et al. (1985) hanno studiato gli
spettri di massa di vapori di carbonio ottenuti da cristalli di grafite con laser ad alta energia.
Con sorpresa furono osservati picchi di massa da attribuirsi a varie specie di carbonio in
fase vapore: la più abbondante tra queste specie era un cluster costituito da 60 atomi di
carbonio in una struttura regolare ed elegante. Questo cluster C60 ha la forma di una
gabbia sferica cava, di diametro 7.1 Å, formata da atomi di carbonio triconnesso
(approssimativamente ibridizzato sp2) uniti a formare una rete chiusa di 12 pentagoni e 20
esagoni (figura 1), esattamente come un pallone da football.
Figura 1 Disposizione degli atomi di carbonio nella molecola di C60.
Per la somiglianza di tali molecole con le cupole geodetiche disegnate in precedenza dal
famoso architetto americano Buckminster Fuller la nuova forma allotropica del carbonio fu
denominata fullerene (il nome completo è in realtà buckminsterfullerene) o più
semplicemente “buckyball”. Oggi sappiamo che essa è solo uno dei costituenti di una più
grande famiglia di molecole a gabbie di atomi di carbonio del tipo Cn chiamate
genericamente “fullereni”. Questi, in generale, si presentano come "poliedri sferici " che
21
contengono sulla superficie cicli a sei membri e cicli a cinque membri (questi ultimi sempre
isolati, cioè completamente circondati da anelli a sei membri).
Assieme alla molecola di C60, la seconda specie a gabbia predominante nei vapori di
grafite è C70, con 70 atomi di carbonio a forma di palla da rugby (figura 2).
Figura 2 Due modalità di rappresentazione della molecola di C70.
Altre specie interessanti della famiglia (e.g. C76, C78, C84) sono state identificate di recente.
Si possono poi ipotizzare fullereni sempre più grandi come, ad esempio, le tre gigantesche
molecole (C240, C540 e C960) illustrate in figura 3.
Figura 3 Fullereni giganti C240, C540 e C960.
Pur essendo C60 una specie stabile, inizialmente non fu possibile studiarla in laboratorio
fino al 1990, poiché non c’era ancora modo di ottenere quantità sufficienti di materiale. Un
completo cambiamento della situazione si verificò nel 1990, quando W. Krätschmer e D.
22
Huffmann trovarono un semplice metodo di laboratorio per preparare in poche ore
milligrammi di C60 e C70.
Data la disponibilità del materiale, le ricerche nell’area si sono sviluppate in modo
esplosivo, con un entusiasmo nel mondo scientifico paragonabile solo a quello per la
scoperta dei superconduttori ad alta Tc nel 1987.
Gli studi sono stati focalizzati in particolare sulle molecole di C60 e C70 che sono state
caratterizzate dal punto di vista della struttura cristallina, delle spettroscopie UV-visibile,
NMR, IR e Raman, nonché della microscopia elettronica ad alta risoluzione.
A temperatura ambiente, lo spettro
13
C NMR di C60 mostra un solo segnale, indicando
l’equivalenza di tutti gli atomi di carbonio.
Le distanze di legame nel fullerene cadono in due gruppi, 1.40 Å per i legami C-C che
uniscono (che sono in comune tra) due esagoni, e 1.45 Å per i legami che uniscono (che
sono in comune tra) un esagono e un pentagono; tutti i pentagoni in C60 sono isolati (in
quanto completamente circondati da esagoni). Confrontando questi valori con normali
legami singoli e doppi in composti organici, 1.54 Å e 1.33 Å, rispettivamente, osserviamo
che i legami C-C in C60 sono di ordine di legame intermedio. Queste distanze di legame,
sono anche intermedie tra quelle del diamante e quelle della grafite (C-C 1.39 Å). Il
diamante è un perfetto isolante mentre la grafite è un conduttore; C60 è un isolante con
gap di banda di 2.2 eV.
Non è sorprendente che nel C60 cristallino le molecole si dispongano secondo i principi
degli impacchettamenti compatti. A temperatura ambiente, C60 ha una struttura fcc, con a
= 14.17 Å, in cui le molecole C60 mostrano un certo disordine orientazionale, legato alla
forma sferica delle molecole che possono orientarsi casualmente. La simmetria
icosaedrica, Ih, di C60 rappresenta la massima simmetria puntuale possibile per la
molecola. La separazione tra molecole di C60 adiacenti si può calcolare come metà della
diagonale di faccia della cella cubica, cioè a 2/2 = 10.0 Å. Il “diametro da sfera rigida”
della molecola C60 è calcolato pari a 7.1 Å, il che lascia un gap di 2.9 Å tra molecole
adiacenti per le interazioni di van der Waals.
23
Figura 4 Struttura cristallina cubica a facce centrate del C60.
Poiché le molecole C60 non sono esattamente sferiche, esse si dispongono in modo più
ordinato ad una temperatura al di sotto dei 249 K, dando luogo ad una fase più cristallina.
La forza spingente che porta alla situazione ordinata è l’ottimizzazione del legame tra
molecole di C60 adiacenti. In particolare, considerando la struttura in una data direzione
[110] dell’impacchettamento compatto, un legame corto C-C (elettron-ricco) che unisce
due esagoni in una molecola C60 punta direttamente al centro di un pentagono (elettrondeficiente) su una seconda molecola C60 (figura 5).
Questa disposizione delle molecole da un lato minimizza le sovrapposizioni dirette C-C,
ma dall’altro rende massime le interazioni donatore-accettore tra molecole adiacenti.
Figura 5 Lunghezze di legame nella molecola di C60.
Anche altri fullereni, come C70, formano strutture compatte, anche se le molecole non hanno forma
sferica. La molecola C70 è ellissoidale (con un asse lungo di 8.34 Å e un asse corto di 7.66 Å), ma
nei cristalli, a temperatura ambiente, gli ellissoidi sono in grado di ruotare liberamente generando
entità mediamente quasi-sferiche, che formano una struttura fcc con a = 15.01 Å.
24
I fullereni dal punto di vista tecnico rientrano in una categoria più ampia di superconduttori
detti appunto superconduttori organici, che fanno parte della famiglia dei conduttori
organici comprendente:
•
•
•
sali molecolari;
polimeri;
nanotubi al carbonio e composti a base di C60.
Figura 6 I risultati raggiunti nello studio della superconduttività nel secolo scorso
Il grande fascino dei fullereni e derivati nasce dalla vasta gamma di possibilità che essi
offrono. Oltre alla superconduttività ad alta Tc, sono di interesse per l’impiego come
ferromagneti molecolari e come trappole molecolari. C60 offre immense possibilità nella
sintesi organica. Sono inoltre di interesse l’impiego in catalisi e in chimica organometallica
e come parti di strutture polimeriche.
25
2.2 Nanotubi
Oltre ai fullereni esistono molte altre strutture di carbonio, formate da anelli a 5, 6 e 7
membri (principalmente 6). Di fatto in seguito al C60, furono presto scoperte nuove forme.
Speciale menzione si deve fare dei nanotubi di carbonio scoperti in maniera fortuita nel
1991 dal ricercatore giapponese S. Iijima, che ne ha osservato la presenza tra i prodotti
secondari di fullereni. E'estremamente difficile dare una definizione precisa dei nanotubi
di carbonio, soprattutto a causa dell'
enorme varietà di taglie e conformazioni che essi
possono avere. In generale è possibile dividere i nanotubi in due grandi famiglie: i
nanotubi a parete singola (single-walled nanotubes, o SWNT) e i nanotubi a parete
multipla (multi-walled nanotubes, o MWNT). I SWNT possono essere considerati, per
conformazione e struttura, come degli appartenenti alla famiglia dei fullereni, mentre i
MWNT sono più prossimi alla famiglia dei nanofilamenti, di cui rappresentano un caso
particolare.
I primi nanotubi scoperti erano essenzialmente costituiti da strati arrotolati di grafite (anelli
a 6 membri) multipli concentrici, con un numero variabile di strati grafitici. Di recente sono
stati anche trovati nanotubi a parete singola. I tubi sono chiusi a entrambe le estremità da
anelli a cinque membri (figura 7).
Figura 7 Schematizzazione di nanotubi a parete singola
I tubi possono essere aperti alle estremità per ossidazione, se scaldati con piombo o
bismuto all’aria, e i metalli vengono risucchiati all’interno. In assenza di ossigeno tutto ciò
26
non si verifica (l’ossigeno sembra attaccare selettivamente le estremità). L’ossidazione
con acido nitrico a 900 °C apre i tubi molto selettivamente. I tubi aperti possono facilmente
inglobare molte specie, come AgNO3 e AuCl3 da soluzioni acquose concentrate. Anche
composti organometallici come Co(C5H5)2 sono stati introdotti all’interno di tali
nanostrutture.
I primi SWNT sono stati prodotti nel 1993 per mezzo di un sistema ad arco elettrico con
elettrodi composti da una miscela carbone-cobalto. Un SWNT ideale può essere descritto
come un tubo in carbonio formato da uno strato di grafite arrotolato su se stesso a formare
un cilindro, chiuso alle due estremità da due calotte emisferiche; in base alle direzioni di
arrotolamento degli strati di grafite i SWNT prendono i nomi di "armchair" e "zig-zag"
(figure 8 e 9).
Il corpo del nanotubo è formato da soli esagoni, mentre le strutture di chiusura (le due
semisfere) sono formate da esagoni e pentagoni, come i normali fullereni. Per questa
ragione i SWNT possono essere considerati come una sorta di "fullereni giganti", e sono
per questo motivo chiamati anche "buckytubes".
Nella realtà i nanotubi presentano spesso dei difetti strutturali o delle imperfezioni nella
struttura geometrica (ad esempio la presenza di strutture pentagonali o ettagonali nel
corpo del tubo) che deformano il cilindro.
Figura 8 Nanotubo "armchair"
Figura 9 Nanotubo "zig-zag"
27
I MWNT sono nanotubi formati da più SWNT concentrici, e vengono perciò chiamati
nanotubi "a parete multipla". Possono essere presenti dei legami tra le varie pareti (lip-lip
interactions) che sembra stabilizzino la crescita di questi nanotubi (figura 10). Il diametro
dei MWNT è di norma maggiore di quello dei SWNT, e cresce con il numero di pareti,
potendo arrivare fino a qualche decina di nanometri.
Il confine tra i nanotubi a pareti multiple e i nanofilamenti non è molto ben definito, e un
MWNT di grandi dimensioni può essere considerato come un caso particolare di fibra
tubolare. L'
eventuale presenza di un grande numero di difetti strutturali o di interazioni tra
pareti all'
interno del tubo rende ancora più labile questa separazione.
I MWNT hanno spesso un grande numero di imperfezioni nella loro struttura, e mostrano
un'
estrema varietà di forme nella loro zona terminale.
Figura 10 Immagini di DWNT (double wall nanotube) con e senza interazioni tra pareti.
La struttura elettronica dei nanotubi è molto simile a quella della grafite, dotata di buone
capacità di conduzione in direzione planare, e sarebbe quindi lecito aspettarsi un
comportamento simile da parte dei nanotubi. I nanotubi hanno invece mostrato delle
sorprendenti proprietà di conduttività che cambiano secondo la loro geometria: i SWNT
"armchair" mostrano un comportamento metallico, gli altri un comportamento
da metallo o da semiconduttore a seconda dei casi.
E' stato anche notato che, in determinate condizioni, gli elettroni possono passare
all'
interno di un nanotubo senza scaldarlo (fenomeno chiamato "conduzione balistica").
Queste proprietà rendono i nanotubi molto interessanti per lo sviluppo di "nanocavi" o "cavi
28
quantici", che potrebbero sostituire il silicio nel campo dei materiali per l'
elettronica, e
consentire il passaggio dalla microelettronica alla nanoelettronica.
Per fare ciò occorrerebbe però sviluppare una tecnica di produzione di nanotubi di forme e
dimensioni diverse e strettamente controllabile, cosa che al momento è ancora
impossibile.
Le proprietà di conduzione dei nanotubi può essere variata "drogandoli", ovverosia
inserendo nella loro struttura degli atomi di azoto e di boro (figura 11).
Figura 11 Immagine di un nanotubo formato di atomi di azoto e boro.
Tra i risultati più interessanti in questo campo c'
è un nanodiodo formato da due nanotubi
(di cui un conduttore e un semiconduttore) fusi tra loro, che agisce come un normale
diodo, facendo passare la corrente in un senso e non nell'
altro.
Un'
altra possibile applicazione della proprietà di conduzione dei nanotubi è il loro uso
come cannoni elettronici per la produzione di schermi al plasma ad altissima definizione.
2.3 Struttura elettronica della molecola di C60
Prima di approfondire le proprietà elettroniche del solido è importante dare uno sguardo
alla struttura elettronica di una singola molecola di C60 .
Una molecola di fullerene ha 240 elettroni di valenza, ma ciascun atomo di carbonio ha tre
legami
con gli atomi vicini, utilizzando 180 elettroni per questo scopo. L’energia di questi
elettroni è ben al di sotto del livello di Fermi: essi stabilizzano la struttura ma non
contribuiscono alla conduzione. I restanti 60 elettroni sono sistemati sulla molecola negli
orbitali elettronici che scaturiscono dagli orbitali molecolari
nei legami C-C. Ci troviamo
in una situazione molto simile al caso della grafite con due importanti differenze.
29
Prima di tutto i tre legami attorno all’atomo di carbonio nel C60 (così come in ogni altra
molecola di fullerene) non formano un piano. Quindi se nella grafite gli elettroni hanno la
stessa probabilità di trovarsi sopra o sotto il piano, nei fullereni gli elettroni
tendono a
passare più tempo fuori che dentro la gabbia.
Inoltre nel C60 le lunghezze di legame C-C non sono uguali; gli elettroni
non sono
esattamente delocalizzati intorno ai sei membri dell’anello di carbonio (come nel benzene
o nella grafite), ma sono distribuiti su 30 orbitali elettronici che sporgono dalla molecola di
C60. Le altre 60 orbite a minor densità elettronica collegano coppie carbonio –carbonio con
lunghezze di legame più ampie. La sovrapposizione tra questi orbitali su molecole
adiacenti determina le proprietà della banda elettronica di conduzione tipiche dei solidi
drogati.
Dieci elettroni dei 60 non interagenti vengono sistemati negli orbitali hu, f1u e f1g (in ordine di
energia crescente). Le degenerazioni di questi livelli energetici sono rispettivamente 10, 6
e 6. Ciò significa che lo stato hu è completamente occupato dagli ultimi 10 elettroni che è
dunque il più alto orbitale molecolare occupato HOMO (Highest Occupied Molecular
Orbit), e il livello f1u diventa il più basso orbitale molecolare non occupato LUMO (Lowest
Unoccupied Molecular Orbit). Il gap tra i due livelli energetici è di circa 2eV.
Nello stato solido le bande che si originano dalla sovrapposizione degli orbitali molecolari
HOMO e LUMO sono le più importanti, per ciò che riguarda il fenomeno della conduzione,
poiché sono i più prossimi alla superficie di Fermi.
Nel solido di C60 la banda LUMO ha un ampiezza di circa 0.5 eV, inferiore di molto
all’ampiezza del gap HOMO-LUMO. Il materiale puro è dunque un isolante con una banda
derivante dal livello HOMO completamente piena. Nei composti di metalli alcalini MnC60 o
in altri materiali drogati gli elettroni donati vanno a collocarsi nella banda LUMO
consentendo il fenomeno della conduzione.
Secondo il modello delle bande tali composti dovrebbero avere un comportamento
metallico per ogni 0<n<6 (corrispondenti ad una banda parzialmente piena). Diversi
esperimenti contraddicono tale assunzione teorica. L’interazione tra elettroni e fononi e
quella elettrone-elettrone possono modificare o cambiare drasticamente i risultati della
teoria delle bande.
E’ possibile studiare l’evoluzione delle proprietà elettroniche dei fulleruri a base di elementi
alcalini a partire dagli andamenti della resistività di un cristallo di C60 drogato con atomi di
potassio in funzione della temperatura ricavati sperimentalmente.
30
Kn C60 con n=1 ed n=3 ha un comportamento metallico in un ampio intervallo di
temperature. Per n=4 e n=6 il materiale è un semiconduttore. La semplice teoria delle
bande prevedeva invece un comportamento metallico per 0<n<6.
2.4 C60 e i suoi derivati
In un solido a impacchettamento compatto costituito da grandi molecole organiche, come
le molecole di C60 le cui dimensioni lineari sono all’incirca dieci volte più grandi di un
qualsiasi atomo, c’è di solito molto spazio vuoto a disposizione: altri atomi, ioni o molecole
più piccole possono dunque posizionarsi facilmente in questi vuoti. Le strutture compatte
hanno infatti cavità ottaedriche e tetraedriche, e nei cristalli molecolari di fullerite questi siti
sono abbastanza grandi da poter essere occupati dai cationi alcalini di grandi dimensioni.
La molecola C60 reagisce con i metalli alcalini a dare fulleruri (cristalli di fullerite drogati con
elementi alcalini e alcalino-terrosi tipo Na, K, Rb, Cs, Ca, Sr e Ba) di formula generale
M3C60 in cui tutti i siti interstiziali T+, T- e O sono occupati (figura 12).
Figura 12 Schematizzazione dei fulleruri.
La molecola di fullerene può essere quindi considerata un’unità costruttiva per i conduttori
organici in quanto consente di preparare, a partire da uno stesso composto organico, una
grande varietà di materiali (veri e propri metalli molecolari) con una struttura di base simile
ma con differenti proprietà elettroniche.
Il fullerene C60 risulta stabile, ha una struttura vibrazionale ed elettronica piuttosto ricca e
gli orbitali molecolari
parzialmente vuoti possono formare bande elettroniche nello stato
solido, il che è alla base dei fenomeni di conduzione. Poiché i legami C-C nel fullerene
31
sono insaturi, ci sono numerosi stati elettronici pronti ad accettare elettroni provenienti da
opportuni donori: i metalli alcalini e alcalino-terrosi appunto. Questi materiali sono metallici
poiché gli elettroni dei metalli sono trasferiti alla banda di conduzione della rete di atomi in
C60, che per esempio nel caso di M3C60 risulta semi-occupata. A basse temperature molti
di questi materiali diventano superconduttori.
La scoperta della superconduttività nei fulleruri a base di metalli alcalini risale al 1991
anno in cui Robert Haddon e Bell Labs riscontrarono la transizione a superconduttore
K3C60 alla temperatura di 18 K. Uno dei valori più alti di temperatura critica Tc (a cui si ha la
transizione da metallo a superconduttore) nei fulleruri è stato osservato di recente (1999)
nel composto Tl2RbC60 ed è pari a circa 45 K.
Questi cristalli così ottenuti, sono superconduttori a una temperatura molto maggiore degli
analoghi intercalati di grafite: fra 30 e 40 K (fra –230° e –240° C), meno dei
superconduttori ad alta Tc, ma molto più della grafite intercalata (che diventa
superconduttrice a meno di 1 K) e anche del miglior superconduttore tradizionale (23 K).
Esistono altri fulleruri con diversi patterns di occupazione dei siti intersiziali, che portano a
strutture tipo NaCl o sfalerite in MC60 e tipo fluorite in M2C60. E’ anche possibile aumentare
il numero di ioni M per C60 oltre 3; in M4C60 (M = Na), si hanno clusters Na4 in siti ottaedrici.
Si arriva anche a M6C60, in cui l’impacchettamento delle molecole C60 cambia da fcc a bcc
(infatti la struttura bcc ha un gran numero di siti interstiziali disponibili).
E’ molto interessante il fatto che nella famiglia MnC60 le proprietà elettroniche variano da
isolanti a metalliche, fino alla superconduzione, in funzione del valore n.
La struttura a gabbia della molecola di C60 offre due altre possibilità di drogaggio (figura
13):
•
mediante inserimento di un atomo M estraneo all’interno della gabbia (endohedral
doping);
•
mediante sostituzione di uno o più atomi di carbonio nella gabbia di C60 con atomi
aventi una diversa struttura elettronica (exohedral doping).
32
Figura 13 Esempi di endohedral ed exohedral doping nella molecola di fullerene
Nel primo caso si ottiene una supermolecola MC60, nel secondo caso il composto C59M.
Uno degli aspetti che ha suscitato subito interesse è il tentativo di incorporare un atomo
estraneo nella cavità sferoidale. In via di principio, si può pensare di intrappolare un’ampia
varietà di atomi metallici in queste cavità.
Per la preparazione della supermolecola MC60 (dove M sta per N, P, Li, Ca, Na, K, Rb)
bisogna ricorrere a metodi che implicano forze notevoli in cui gli ioni o atomi vengono
accelerati e impiantati nella gabbia. Gli ioni devono avere energia sufficiente ad aprire la
gabbia ed entrarvi. La prima collisione dovrebbe assorbire e ridistribuire gran parte
dell’iniziale energia cinetica così che l’atomo una volta entrato nella gabbia non ne può più
uscire. Con tecniche di questo tipo si possono preparare solo piccole quantità di prodotto,
quantità maggiori possono essere preparate mediante co-evaporazione (tipica tecnica
utilizzata per la produzione del fullerene). Ricerche e studi hanno dimostrato che l’atomo
introdotto all’interno della molecola di fullerene non sempre trasferisce la sua carica alla
gabbia (se tale atomo resta neutro allora resta al centro della gabbia come nel caso di
NC60). Composti come LaC60 sono molto interessanti in quanto il completo trasferimento di
carica da La alla gabbia di C60 porta alla formazione di una molecola carica trivalente
(secondo alcuni studiosi il cristallo di LaC60 dovrebbe essere un superconduttore stabile in
aria).
Un esempio di fulleruro ottenuto per “exohedral doping” è il C59N (azafullerenes) in cui un
atomo di carbonio viene sostituito da un atomo di azoto con conseguente addizione di un
elettrone sulla gabbia. Ciò comporta localmente un cambiamento della struttura, riduce la
simmetria della molecola e separa gli orbitali elettronici degeneri; inoltre questa
sostituzione chimica rende la molecola molto reattiva grazie alla sua alta affinità
elettronica.
33
2.4.1 Superconduttività in M 3 C60
L’importanza della struttura sulle proprietà di superconduzione è ben dimostrata nel caso
dei metalli molecolari, che includono i solidi C60 drogati da metalli alcalini, di stechiometria
M3C60. Il solido M3C60 presenta un impacchettamento cubico compatto, con gli atomi M in
tutte le cavità ottaedriche e tetraedriche. Memori della stabilità di C5H5-, ci si può attendere
che C60, che contiene anelli a cinque, abbia notevole tendenza ad attirare elettroni. Di
fatto, il sistema di livelli secondo il metodo di Hückel (figura 14, i numeri a destra indicano
le degenerazioni) permette di accomodare facilmente sei elettroni aggiuntivi, a dare un
semiconduttore (banda piena f1u). Con tre elettroni si ottiene una banda semi-piena per
M3C60 che rende il materiale non solo metallico ma anche superconduttore, con un’alta Tc
di 35 K nel caso M3 = Rb2Cs.
Figura 14 Il sistema dei livelli energetici secondo il metodo di Hückel.
Sin dalla scoperta della superconduttività nei fulleruri gli studi sono stati focalizzati in
particolare su M3 C60. Un notevole impegno è stato posto per la determinazione della
resistività intrinseca e della sua dipendenza dalla temperatura attraverso misure sia su di
un film sottile che su di un singolo cristallo. I più bassi valori di resistività per il sistema K3
C60 è di circa 1m ·cm, da cui si ricava un valore del cammino libero medio del
trasportatore di carica di circa 3.5
, valore inferiore alla distanza C-C tra due molecole
adiacenti di C60. Procedendo verso le alte temperature (T>500K) la resistività intrinseca
non mostra una tendenza alla saturazione e inoltre il cammino libero medio raggiunge
valori prossimi alla distanza di legame C-C. Un comportamento apparentemente metallico
con un libero cammino medio più piccolo della distanza reticolare è uno dei problemi
34
irrisolti della fisica dello stato solido (anche altri sistemi come i cuprati e i manganati
presentano questo comportamento anomalo).
A partire dal 1991 sono stati effettuati numerosi progressi nel comprendere il fenomeno
della superconduzione nei composti M3 C60. Con successo è stata condotta una linea di
studi sulla relazione esistente tra la temperatura di transizione superconduttiva e la
distanza reticolare. In accordo con i risultati sperimentali le variazioni sostanziali del
parametro reticolare per azione di modeste pressioni (10-20 kbar) sono accompagnate da
una variazione significativa della temperatura di transizione. Inoltre anche mediante
inserimento di differenti elementi metallici si ottiene una variazione del parametro di cella.
Combinando l’azione della pressione con quella dell’inserimento di metalli alcalini è
possibile ottenere variazioni continue del parametro di cella da 13.9 a 14.5 . In figura15
è illustrata la dipendenza di Tc dal parametro di cella (lato della cella cubica) che varia al
variare dei droganti alcalini.
Figura 15 Andamento della temperatura critica con il parametro di cella.
Questo comportamento può essere ricondotto ad una semplice dipendenza della struttura
a bande dalla struttura cristallina. Al crescere delle dimensioni medie del metallo M, le
unità C60 vengono allontanate tra di loro. Ciò comporta, oltre all’aumento delle dimensioni
di cella, una diminuzione dell’integrale di sovrapposizione tra molecole adiacenti (figura
16) che determina l’ampiezza delle bande.
35
Figura 16 Variazione dell’integrale di sovrapposizione con la distanza intermolecolare
Rimanendo costante la densità integrata totale degli stati nella banda (l’area della banda),
se l’ampiezza diminuisce aumenta la densità degli stati al livello di Fermi. Effetti analoghi
possono essere ottenuti variando la pressione sul campione solido, per una data
composizione.
La riduzione della temperatura di transizione per valori sempre più piccoli del parametro di
cella è in generale attribuita all’aumento dell’ampiezza della banda che comporta una
diminuzione della densità degli stati al livello di Fermi. Il comportamento può essere
compreso almeno qualitativamente prendendo in considerazione l’equazione che esprime
la Tc nella teoria BCS:
k BTC ≈
ωD
1.45
exp −
1
λ
=
ωD
1.45
exp −
1
ρ ( EF )V
In questa equazione = (EF)V è la costante di accoppiamento elettrone-fonone, (EF) è la
densità degli stati al livello di Fermi e V è il potenziale attrattivo elettrone-elettrone al livello
di Fermi,
Dè
la frequenza di Debye. Considerando che V e
D
sono indipendenti dalla
distanza intermolecolare e che la densità degli stati elettronici è inversamente
proporzionale all’ampiezza di banda ( (EF)
1/W) e aumenta quando il parametro
reticolare decresce possiamo concludere dicendo che la temperatura Tc diminuisce se il
reticolo subisce una compressione. In figura 17 è riportato il grafico di lnTc contro 1000/
(EF).
36
Figura 17 Andamento di lnTc in funzione di 1000/ (EF).
In termini dei parametri della teoria BCS, la superconduttività nei composti del tipo A3 C60 è
caratterizzata da una costante di accoppiamento intermedia * = 1, un discreto valore del
parametro di repulsione elettrone-elettrone
* = 0.2 ed una frequenza fononica
caratteristica individuabile nella parte più bassa dello spettro molecolare vibrazionale
200-1000 cm
ln
=
-1
L’alta temperatura critica è quindi dovuta al fatto che, al contrario di un semplice metallo,
in questo solido molecolare gli elettroni possono accoppiarsi in misura notevole ai modi
vibrazionali ad alta frequenza dei fononi.
Diminuendo l’ampiezza di banda al crescere della distanza tra le unità C60, vi sarà una
separazione limite alla quale il modello delocalizzato diviene inappropriato e gli elettroni
tenderanno a localizzarsi. Una tale instabilità elettronica tenderà non solo a distruggere la
superconduttività ma anche lo stato metallico. In termini più generali, si può dire che la
superconduttività, normalmente associata con una alta densità degli stati elettronici al
livello di Fermi (EF), si trova spesso nei solidi in competizione con altri processi guidati
dalla struttura elettronica.
La cosa più interessante è che se si fanno entrare cationi
alcalini di diametro maggiore nella struttura fcc del fullerene, conseguentemente si fa
aumentare il parametro di cella (che risulta essere inversamente proporzionale al fattore
d’impacchettamento), aumenta anche la temperatura critica, Tc, a cui avviene la
trasformazione in superconduttore. Ciò è dovuto all’aumento della densità dei livelli di
Fermi all’aumento della costante reticolare.
37
Figura 18 Temperatura di passaggio a superconduttore T (°K) in funzione del parametro reticolare a0
( ) per varie composizioni del M C .
La correlazione tra Tc e la costante reticolare a0 (figura 18)fa pensare che si possano
ottenere materiali a più alta Tc immettendo nella struttura cristallina cationi sempre più
grossi. Ci sono due potenziali problemi nell’applicare questa strategia:
•
Se lo ione di C60 si sposta, il flusso di elettroni si interrompe;
•
Se il catione diviene troppo largo per entrare negli interstizi ottaedrici e
tetraedrici della cella fcc allora struttura si riorganizza, ciò porta alla perdita della
superconduttività.
2.4.2 Superconduttività nel C60 puro
E’ possibile osservare la superconduttività nel C60 anche senza drogaggio chimico, così
come è stato dimostrato recentemente da Batlogg e collaboratori. Un elevato campo
elettrico applicato perpendicolarmente alla superficie del cristallo è in grado di portare sulla
superficie del cristallo un numero sufficiente di elettroni per produrre la superconduttività.
L’esperimento è stato effettuato mediante un transistor ad effetto di campo FET (Field
Effect Transistor). Gli elettroni all’interfaccia tra il cristallo di C60 e lo strato isolante di
allumina Al2O3 diventano conducenti se il cristallo e l’interfaccia sono di elevata purezza. Il
valore di Tc dipende dalla polarità e intensità del campo elettrico applicato. I risultati
ottenuti per l’applicazione di voltaggi negativi hanno portato ad una temperatura critica
38
piuttosto alta di circa 52K. Poiché l’applicazione di un voltaggio negativo comporta un
“hole doping” della superficie del cristallo diciamo che si è ottenuto un esempio di
superconduttività nel C60 per drogaggio con buche elettroniche. La più alta temperatura
critica è stata ottenuta con un drogaggio mediante tre buche elettroniche per banda
HOMO nel C60. Per voltaggi positivi si ha un “electron doping” che porta a risultati del tutto
in accordo con la superconduttività nel C60 drogato con metalli alcalini: la più alta
temperatura critica in questo caso viene raggiunta per una banda LUMO semipiena (tre
elettroni
per
C60),
e
il
valore
della
temperatura
critica
è
di
circa
11K.
39
3 Aceni
3.1 Introduzione
London fu il primo a sostenere nel 1937 che i composti aromatici, in presenza di campi
magnetici, potessero esibire una corrente superconduttiva circolante lungo gli anelli
aromatici, anche se il concetto di un metallo sintetico era stato precedentemente lanciato
da McCoy e Moore quando proposero “di preparare sostanze composte metalliche a
partire da costituenti non metallici”.
Come si evince dal loro nome, l’applicazione di materiali elettronici è basata sullo speciale
comportamento degli elettroni in tali mezzi. Per i materiali elettronici organici (molecolari),
il comportamento di un singolo elettrone, incluso il trasporto/trasferimento di un elettrone, i
processi di doping n/p, e così via, dipende principalmente dall’energia dei livelli
dell’orbitale molecolare più alto occupato (HOMO) e dell’orbitale molecolare più basso non
occupato (LUMO), e dalle interazioni tra orbitali. Progettando molecole con livelli HOMO e
LUMO adattabili, si può aver il controllo sulle proprietà dei materiali e quindi sul
comportamento dei dispositivi elettronici basati su di essi. Le molecole con bassi gap
HOMO/LUMO sono di particolare importanza per la loro abilità di essere facili donatori (da
HOMO) o accettori (da LUMO) di un elettrone, che è il processo basilare in tutti i dispositivi
elettronici.
Ci sono due strategie fondamentali per ottenere un basso gap HOMO/LUMO nelle
sostanze organiche: 1) estendere la congiunzione
covalenti D-A (D è un donatore di elettroni
nelle molecole, 2) costruire composti
, e A è un accettore di elettroni
) in cui gli
orbitali HOMO/LUMO possono essere regolati in maniera relativamente indipendente.
Entrambi i principi sono stati realizzati con successo nella progettazione di polimeri
-
coniugati. Per piccole molecole ad orbitali completi (closed-shell) un gap HOMO/LUMO
stretto è una caratteristica rara, sebbene sia stato ottenuto con la prima strategia in
oligo(aceni) e fullereni. Ci sono molti esempi di HOMO/LUMO gap adattabili secondo il
secondo principio, come i vari derivati del tetrathiafulvalene (TTF).
40
3.2 TTF-TCNQ
Il TTF-TCNQ è il prototipo dei composti a trasferimento di carica (charge-transfer) dove le
bande HOMO e LUMO, rispettivamente dei donatori e accettori con orbitali non completi
(open-shell), contribuiscono alla conduzione. Questo è stato anche il primo conduttore
organico a presentare una larga conduttività in un ampio dominio di temperature al di sotto
dei 59 K, dove si osserva una brusca transizione da metallo a isolante.
Il TTF-TCNQ è un materiale comprendente pile (stacks) uniformi, parallele e isolate con
orbitali
che contribuiscono alle due bande di conduzione (figura 1). La sovrapposizione
degli orbitali molecolari, che è più larga lungo la direzione delle pile e più debole tra di loro,
rende la dispersione degli elettroni mono-dimensionale. In una prima approssimazione,
l’energia dipende solo dal vettore d’onda dell’elettrone lungo la direzione b* nello spazio
invertito.
Figura 1 Vista laterale lungo l’asse a dell’impacchettamento molecolare lungo l’asse b.
L’energia più bassa si ha nel TCNQ quando tutti gli orbitali molecolari sono in fase (a k=0
nello spazio invertito); invece la struttura a bande delle pile di TTF è al massimo
dell’energia nella zona centrale (figura 2). Tale andamento a croce fa si che le bande si
intersechino in un singolo vettore d’onda di Fermi, ± kf, in modo da preservare la completa
neutralità. Conseguentemente tutti gli stati tra – /b e +
/b sono occupati con la
restrizione che tra kf e + kf gli stati occupati appartengono alla banda del TCNQ, mentre
al di fuori di questo dominio appartengono alla banda del TTF.
41
Figura 2 Struttura a bande invertite del TTF-TCNQ.
L’annuncio fatto nel 1973 da Heeger e il gruppo Pennsylvania della scoperta di un
gigantesco picco di conduttività dell’ordine di 5x104 o 105 (
cm)-1 a 60 K, proprio sopra la
brusca transizione verso lo stato isolante a temperature più basse, innescò un grande
interesse in questi composti e nella conducibilità organica. Gli autori di questa scoperta
suggerirono addirittura che questo enorme valore della conducibilità (superiore a quella
del rame a temperatura ambiente con un numero di portatori di carica più piccolo di
centinaia di volte) potesse essere ascritto tra i segni precursori di un incipiente
comportamento da superconduttore.
Questo primo lavoro suggerì che la transizione metallo-isolante dovesse essere la
manifestazione dell’instabilità dovuta alla distorsione spontanea del reticolo con vettore
d’onda 2kf, come era stato predetto da Peierls nel 1955 per un conduttore monodimensionale. Mentre l’enorme picco di conducibilità annunciato nel 1973 non sopravvisse
alle indagini sperimentali effettuate da altri gruppi, si promossero i lavori nella ricerca nel
campo di conduttori mono-dimensionali e conduttori organici che portarono alla scoperta
della superconducibilità organica nel 1979.
3.3 Gli aceni
Gli idrocarburi policiclici aromatici (PAHs) sono tra i materiali organici
-funzionali più
ampiamente studiati. La conducibilità intrinseca della grafite così come la scoperta negli
42
anni settanta della conducibilità in trans-poliacetilene dopato, ha stimolato l’indagine sulle
proprietà elettroniche dei poliaceni (PAs); per i poliaceni più larghi, ad esempio, è stato
predetto un piccolo HOMO/LUMO gap cioè un comportamento simile a quello dei
conduttori organici mono-dimensionali (zero band gap semiconductor). Particolare
attenzione è stata posta ai PAHs lineari composti di anelli benzenici lateralmente fusi e
chiamati aceni lineari o semplicemente aceni, per la loro importanza come materiali
semiconduttori organici.
Nel periodo 2000-2002 l’attenzione rivolta agli aceni fu dovuta soprattutto alle diverse
asserzioni sulla superconduttività degli antraceni, tetraceni, e pentaceni (Tc= 4, 2.7, e 2 K
rispettivamente), alla estremamente alta mobilità nel pentacene sia delle buche (fino a
1200 cm2 V-1 s-1) che degli elettroni (fino a 320 cm2 V-1 s-1), all’iniezione laser allo stato
solido basata su tetraceni e all’osservazione di un “fractional quantum hall effect” per il
tetracene e il pentacene con mobilità di buche ed elettroni che supera i 104 cm2 /V*s a 2 K.
3.3.1 La struttura e le proprietà
Il benzene, il più piccolo membro della famiglia degli aceni e il più stabile composto
aromatico conosciuto, è stato scoperto nel 1825 ed ha dato origine a ad una famiglia di
composti aromatici che rappresenta uno dei maggiori campi della chimica. Gli oligoaceni
sono molecole aromatiche, ma il loro grado di aromaticità è stato oggetto di recenti
dibattiti, che sembrano essere così reattive da poter esser indagate solo in teoria. Il più
basso omologo, dal benzene all’antracene, può essere estratto dal carbone, mentre il più
alto omologo, come il pentacene o l’esacene, può essere ottenuto solo mediante sintesi a
più stadi. L’accessibilità sintetica degli oligoaceni è limitata all’esacene (figura 3-136.6), e
una completa conoscenza delle proprietà elettroniche arriva al pentacene (figura 3-136.5).
Alcuni risultati inerenti la sintesi di più altri omologhi, specialmente eptacene, sono stati
pubblicati ma la loro sintesi rimane comunque controversa.
43
Figura 3 Aceni e oligoceni conosciuti.
3.3.2 Struttura degli oligoaceni
Per descrivere la struttura elettronica dei poliaceni sulla base della determinazione degli
orbitali molecolari e delle energie del monomero corrispondente – naftaline - fu usata la
teoria quantitativa degli orbitali molecolari, MO.
Le alte temperature per la superconducibilità e il ferromagnetismo dei poliaceni furono
proposte teoricamente da Kivelson e Chapman nel 1983. Le prime indagini si incentrarono
sulla predizione di quale delle tre strutture dei poliacheni - non distorta, cis-distorta o transdistorta - fosse energeticamente favorita (figura 4); ovviamente le proprietà elettroniche, la
struttura della banda e le proprietà di conducibilità dei poliaceni dipendono dalla struttura
preferita.
Figura 4 Le tre strutture dei poliaceni.
44
3.3.3 Struttura dei poliaceni
I poliaceni (così come i cicloaceni) furono descritti da Houk e coll. come costituiti da due
nastri non alternati completamente delocalizzati e uniti da legami relativamente lunghi. Per
i poliaceni sono stati predetti gap di banda più piccoli dei corrispondenti polieni e un livello
zero (ground state) triplo per nove o più anelli benzenici. Le strutture, le energie e le altre
proprietà di una serie di oligoaceni furono paragonate con quelle delle corrispondenti serie
di oligoareni ad anelli del tipo fenantrene e si trovò che i composti di quest’ultima serie
avevano un’energia totale più bassa di quella dei loro isomeri della prima serie.
Figura 5 Esempi di oligoaceni tipo fenantrene.
3.3.4 Esempi di oligoareni ad anelli del tipo fenantrene
L’aumento del numero di anelli nelle strutture PAs risulta nella successiva riduzione del
gap della banda (riflessa nello spettro UV), nella riduzione del potenziale di ionizzazione e
nell’aumento delle affinità nei protoni ed elettroni, che si riflette anche nella diminuita
stabilità. Queste progressioni nelle proprietà dei PAs furono spiegate con la perdita
sequenziale del carattere benzoidico (aromaticità). Poiché solo un anello in ogni acene
può essere assegnato a tre doppi legami senza duplicazione, il numero di anelli non
esagonali aumenta lungo le serie di aceni. Un altro punto di vista è stato presentato
recentemente da Schleyer e coll.. Malgrado l’aumento nella reattività come risultato della
benzoinanellazione (dal benzene all’eptacene), fu predetto che l’energia di risonanza degli
aceni per -elettroni fosse all’incirca costante.
J. Aihara analizzò la stabilità cinetica degli oligoaceni usando alcuni indici convenzionali
definiti dalla teoria degli orbitali molecolari di Huckel (HMO); egli concluse che i membri più
alti della serie di oligoaceni sono aromatici e spiegò la loro alta reattività usando indici
convenzionali della stabilità cinetica, come l’energia di localizzazione e l’energia di
separazione HOMO-LUMO.
È ben noto che, eccezionalmente, tutti gli aceni, dal benzene al pentacene, così come
diversi olgotiofeni e oligofenileni, cristallizzano nelle strutture a spina di pesce (figura 6).
45
Figura 6 Struttura a spina di pesce del pentacene (in alto) e del benzene (in basso).
Gavezzotti e coll. analizzarono la struttura di numerosi PAHs e trovarono che tutti i
composti esaminati cristallizzano in strutture a strati e che le strutture tra gli strati
dipendono dalla relativa abbondanza delle interazioni C-H e C-C. Se predominano le
interazioni C-H (o se il PAs contiene un numero relativamente grande di H), si trova una
struttura a spina di pesce mentre con un aumento relativo di C-C, la struttura diviene più
simile a quella della grafite.
Generalmente gli idrocarburi aromatici mostrano una grande propensione al polimorfismo,
infatti sono state scoperte diverse forme polimorfe del pentacene e per tre strutture sono
disponibili i valori completi ottenuti ai raggi X.
Venuti e coll. dimostrarono, in base ai calcoli sulla dinamica del reticolo, che la fase
PENTACENE02 coincide con quella PENTACENE01 e confermarono che la fase
PENTACENE è significativamente differente; inoltre essi suggerirono che il fattore
determinante per ottenere l’una o l’altra struttura non è il metodo di crescita dei cristalli (da
fase vapore o soluzione), più critiche sono la purezza del campione o la temperatura di
crescita.
Della Valle e coll. predissero diverse centinaia punti di minimo nella superficie di energia
potenziale del pentacene cristallino che potrebbero corrispondere alle diverse strutture
polimorfe, con due minimi di profondità corrispondenti alle strutture dei due tipi di polimorfi
conosciuti. Calcoli effettuati da Tiago e coll. mostrarono che i gap di energia per le diverse
strutture polimorfe sono leggermente differenti. Le interazioni intermolecolari sono
maggiormente favorite nella crescita della struttura in fase vapore.
46
Dai risultati ottenuti con calcoli della teoria di Huckel delle strutture elettronica delle bande
dei progenitori e dei derivati dei pentaceni sostituiti, si è trovato che i progenitori delle
forme polimorfe del pentacene sono bidimensionali nella loro struttura elettronica della
banda con dispersioni moderate. Le ampiezze di banda nell’intervallo polimorfo 14.1 Å d
(la crescita in fase vapore) sono notevolmente più larghe (0.09-0.28 eV) di quelli per
l’intervallo polimorfo 14.5 Å d (0.07-0.18 eV, crescita in soluzione), in accordo con le
proprietà fisiche superiori trovate per l’intervallo polimorfo 14.1 Å d. Si è calcolato che la
dispersione situata nella più alta banda di valenza dell’intervallo polimorfo 14.1Å d è circa
0.2 eV lungo la direzione X.
La conoscenza del mezzo di trasporto dei portatori di carica nei materiali semiconduttori
organici come il pentacene, è un aspetto importante e non solo d’interesse accademico,
ma anche di grande rilevanza tecnica in campi promettenti come quello degli organic field
effect transitors, dei diodi organici emettenti luce (OLED) o delle celle fotovoltaiche. A
livello microscopico, il meccanismo di trasporto di carica può essere descritto come un
processo implicante il trasferimento di un elettrone da una molecola carica ad una
adiacente neutra. La mobilità dei portatori di carica, , determina il mezzo di trasporto dei
portatori di carica per un dato solido semiconduttore. Le proprietà del trasporto di carica
dipendono dal grado di ordine delle molecole, dalle energie e dalla sovrapposizione
intermolecolare degli orbitali molecolari e dai difetti chimici o strutturali.
Secondo calcoli semiempirici, in assenza di impurità o difetti, gli elettroni possono essere
mobili come le buche nei cristalli di pentacene perché le funzioni d’onda sono molto simili
sia per gli elettroni che per le buche (~47 meV). Si è anche concluso che il trasporto di
carica nel pentacene ha un carattere dominante bidimensionale e avviene all’interno degli
strati nelle direzioni che sono quasi perpendicolari ai lunghi assi molecolari. Si è stimato
che le ampiezze delle bande di conduzione e di valenza nei cristalli di pentacene sono
circa 588 e 608 meV, rispettivamente. Recentemente sono state calcolate le ampiezze di
banda del naftalene, antracene, tetracene e pentacene e si è trovato che sono dell’ordine
di 0.1-0.5eV.
47
3.4 Da isolanti a superconduttori: il caso della superconduttività
indotta mediante iniezione di carica in cristalli molecolari
In condizioni normali, l’antracene, il tetracene e il pentacene sono isolanti ma secondo
Battlogg e coll. possono essere convertiti in superconduttori mediante un’iniezione di
carica e l’abbassamento della temperatura.
I cristalli organici studiati da Battlogg e coll. sono composti da 3 (antracene) a 5
(pentacene) anelli legati tra loro di atomi di carbonio. Come parti di un transistor questi
materiali possono condurre elettricità, e alle basse temperature di 2-4 K la loro resistenza
elettrica cade a zero. Questo comportamento superconduttivo è distrutto con
l’applicazione di un campo magnetico. La resistenza nulla e l’espulsione dei campi
magnetici sono le caratteristiche intrinseche di un vero stato superconduttivo.
Da un articolo dello stesso Battlogg e coll. si legge: ” qui presentiamo una nuova classe di
superconduttori: cristalli molecolari organici isolanti che sono resi metallici mediante
iniezione di carica. I primi esempi sono il pentacene, il tetracene e l’antracene,
quest’ultimo avente la più alta temperatura di transizione a 4 K”.
L’approccio sperimentale seguito è quello di iniettare un’alta concentrazione di portatori di
carica nei cristalli molecolari organici di alta qualità, usando una geometria tipo transistor a
effetto campo (figura 7).
Figura 7 Struttura schematica di un transistor field effect a singolo cristallo organico.
Battlogg continua: “I nostri studi sui semiconduttori organici molecolari, come il pentacene,
hanno rivelato che basse densità di difetti possono essere raggiunte in dispositivi FET e
che, in aggiunta, l’energia di Fermi può essere spostata attraverso il gap di banda
portando a un trasporto ambipolare. Da ciò si deduce che il segno e la concentrazione dei
portatori di carica può essere variata in un ampio range. La struttura elettronica dei cristalli
di poliacene è caratterizzata da un gap di energia di diversi elettron volt tra gli stati
48
derivanti da HOMO e da LUMO: antracene, 4.1 eV; tetracene, 3.1 eV; pentacene, 2.5 eV.
Inoltre, si è proposto su basi teoriche, che la superconducibilità in diversi semiconduttori
molecolari grazie all’accoppiamento elettrone-fonone. Qui è riportata l’osservazione di uno
stato superconduttivo in un FET basato su aceni lineari, pentacene, tetracene e antracene.
L’aumento della temperatura di transizione da 2 a 4 K passando dal pentacene
all’antracene è in linea con l’accoppiamento elettrone-fonone che aumenta al diminuire
della lunghezza della congiunzione e, perciò, sostiene l’idea della superconduttività
mediante le interazioni elettrone-fonone.
I superconduttori organici conosciuti possono essere classificati come composti
trasportatori di carica (charge transfer compounds) e consistono di entità elettronegative
ed elettropositive. In contrasto, i cristalli indagati qui sono costituiti da molecole organiche
neutre, e sono isolanti quando vengono preparati altamente puri. Abbiamo trovato che il
trasporto di carica nei cristalli di acene, come il naftalene, l’antracene, il tetracene o il
pentacene, è dominato dall’interazione elettrone-fonone. Inoltre è stato suggerito che
l’acene infinito lineare, poliacene, può mostrare superconduttività. Nel nostro approccio,
abbiamo ottenuto il trasporto di carica mediante l’applicazione di una tensione di sblocco
in una geometria FET piuttosto che mediante interazioni chimiche. Questo permette un
preciso controllo della carica per molecola senza cambiare l’arrangiamento molecolare
con i dopanti. Grazie alle loro buone prestazioni come FETs, l’antracene, il tetracene, e il
pentacene sono i materiali che abbiamo scelto.
Facciamo notare tra parentesi che lo strato metallico prodotto nel canale del mezzo è nel
più stretto contatto con un materiale isolante (la parte isolante dello stesso materiale);
questo offre l’opportunità di studiare come il dielettrico può influenzare l’accoppiamento
superconduttivo”.
La scoperta significante di questo studio è mostrata in figura 8: per un più alto voltaggio di
sblocco, la resistenza sotto i 2 K cade a zero entro i limiti sperimentali, suggerendo una
transizione a uno stato superconduttivo.
49
Figura 8 Resistenza di sblocco di uno strumento field-effect con voltaggi ai due gate in funzione della
temperatura. Per alti voltaggi ai gate (Vg), quasi un elettrone per molecola il materiale diventa
metallico. La resistenza decade con il diminuire della T portando ad un aumento della mobilità degli
elettroni. Per una concentrazione di portatori di carica più alta (più alti voltaggi ai gate) la resistenza
scende a zero sotto i 2 K, indicando così la superconduttività.
Una simile transizione è osservata nel tetracene e nell’antracene alla temperatura critica
di Tc=2.7 K e 4 K, rispettivamente (figura 9).
Figura 9 Resistenza di sblocco di strumenti field-effect di pentacene, tetracene e antracene in
funzione della temperatura. La densità di elettroni per ogni canale è all’incirca di un elettrone per
molecola.
50
La figura 10 mostra un diagramma dettagliato della resistenza in funzione della
temperatura e della polarizzazione del gate -gate bias- (o densità degli elettroni per
molecola). Alla concentrazione di circa un elettrone per molecola, il canale FET diventa
superconduttivo al di sotto dei 2 K. Dopo un brusco onset, la temperatura di transizione
diventa significativamente indipendente dalla concentrazione. Comunque non è possibile
raggiungere attendibilmente concentrazioni più alte a causa della rottura del dielettrico.
Figura 10 Resistenza di sblocco di uno strumento field-effect di pentacene in funzione della
temperature e del voltaggio del gate. Si osserva chiaramente la transizione allo stato
superconduttivo al di sotto dei 2 K e per voltaggi ai gate di circa 12V. la densità elettronica per
molecola è calcolabile assumendo un densità omogenea solo nel primo strato molecolare.
Sul meccanismo di accoppiamento microscopico si possono solo far congetture, ma
sembra che la polarizzabilità del cristallo molecolare sia un primo candidato. Assumendo
un meccanismo convenzionale Bardeen-Cooper-Schrieffer con interazioni elettronefonone, e la stessa densità di stati al livello di Fermi, l’aumento di Tc dal penatcene
all’antracene può essere attribuito all’aumento dell’accoppiamento elettrone-fonone con la
diminuizione della lunghezza di coniugazione (o con il numero di elettroni
delocalizzati),
in accordo con i calcoli teorici.”
Tale articolo, insieme ad altri sottoscritti sempre dal gruppo di Batlogg è stato recentemente soggetto di una
indagine condotta per ordine dei Bell Laboratories, Lucent Technologies. Una commissione ha esaminato la
validità dei dati associati ai dispositivi di misura descritti e in seguito ai risultati gli articoli di Batlogg sono stati
ritirati. Il primo autore di tali articoli (J.H. Schon), che è il responsabile per la maggior parte degli esperimenti,
desidera essere dissociato da questa ritrazione perché egli crede nella scienza presentata nei suoi
manoscritti.
51
4 Materiali molecolari organici – Applicazioni
4.1 Introduzione
Sali di Bechgaard, aceni e fullereni appartengono ad una classe di materiali ben più ampia
la cui caratteristica fondamentale è quella di essere costituiti da molecole organiche isolate
che, allo stato solido, possono ordinarsi in cristalli; questi nella generalità dei casi non
sono di grandi dimensioni, inoltre, il loro insieme si presenta spesso come polvere
incoerente (si pensi ad esempio al saccarosio, sostanza cristallina incapace di auto
supportare una forma).
E’ chiaro dunque che un uso di tali composti in ambito strutturale è totalmente da
escludere; d’altra parte, i materiali funzionali emergenti a base organica sono innumerevoli
essi comprendono, per citarne solo alcuni:
a) I materiali conduttori, sia a base di complessi a trasferimento di carica, sia a base di
polimeri conduttori ottenuti da vari monomeri eterociclici (pirrolo, tiofene, etc.)
variamente funzionalizzati;
b) I materiali elettroluminescenti per LED (Light Emitting Diodes), impiegati per la
realizzazione di display e schermi televisivi ultrapiatti;
c) I materiali emettitori nell’infrarosso, per l’industria delle telecomunicazioni;
d) I materiali per la fotonica.
4.2 Materiali conduttori a base organica
Le plastiche, una classe di materiali polimerici, vengono comunemente utilizzate per le
loro eccellenti proprietà meccaniche, quali resistenza e flessibilità, e per il loro
comportamento da isolanti elettrici. Tutti i giorni si ha modo di sfruttare queste
caratteristiche: dai sacchetti per la spesa e le sedie da giardino ai rivestimenti dei fili
elettrici.
Il largo utilizzo dei materiali plastici è essenzialmente dovuto al loro elevato rapporto
qualità-prezzo.
Le unità chimiche (i monomeri) costituenti questa tipologia di materiali sono molecole
organiche più o meno semplici.
52
Alla luce di quanto detto, può sorprendere che alcuni composti organici conducano la
corrente elettrica, sia completamente (conduttori) sia parzialmente (semiconduttori).
Figura 1 Intervallo di conduttività dei polimeri conduttori confrontato con quello dei materiali
organici. Si noti che lo stesso materiale polimerico può fungere sia da semiconduttore che da
conduttore a seconda del livello di drogaggio (ossidazione).
La classe più ampia di questi sistemi non isolanti è quella dei polimeri coniugati conduttori
(fra cui il politiofene) che, opportunamente trattati (processo di ossidazione o riduzione del
polimero o -impropriamente- drogaggio), possono presentare conduttività comparabili a
quelle di noti sistemi inorganici (figura 1).
Figura 2 Politiofene.
Figura 3 Esempi di polimeri coniugati conduttori a) Poliacetilene, b) Poli-p-fenilenvinilene, c) Derivato
del politiofene.
I polimeri conduttori di nuova generazione sono tecnologicamente molto interessanti
perché dotati sia di elevata conduttività sia di buona processabilità (simile a quella del
polipropilene).
53
Accanto ai polimeri conduttori, esistono anche altre classi di composti organici, non
polimerici, capaci di condurre corrente e alcuni in particolare lavorabili come fossero
materie plastiche.
Tra i sistemi più importanti vi sono i complessi a trasferimento di carica, gli oligomeri del
tiofene, alcuni tipi di ftalocianine e gli idrocarburi benzenoidi polinucleati (figura 4).
Figura 4 Esempi di composti organici conduttori non polimerici (a sinistra: oligomero del tiofene, a
destra: ftaloantocianina).
Prima di procedere è opportuno capire come la peculiare struttura elettronica di questi
materiali, pur così diversi dai metalli, consenta il trasporto di corrente.
4.2.1 Trasporto di carica nei materiali organici
Secondo la teoria delle bande, due sono i requisiti affinché un materiale sia conduttore
I. Deve presentare un sistema continuo di orbitali p interagenti tali da portare alla
formazione di una struttura elettronica a bande;
II. Deve possedere un numero di elettroni insufficiente per riempire tali bande
completamente.
La banda ad energia più bassa, completamente occupata, è detta di valenza (VB), mentre
quella a più alta energia è detta di conduzione (CB).
Dal punto di vista elettronico metalli, semiconduttori e isolanti possono essere classificati
in base a quanto queste due bande sono separate in termini energetici ovvero in funzione
di quanto facilmente alcuni elettroni della banda di valenza possono raggiungere quella di
conduzione.
Nei metalli le due bande sono sovrapposte a formarne una sola semipiena, quindi gli
elettroni di valenza che non sono “ancorati” ai nuclei possono facilmente muoversi
permettendo il trasporto di carica. Per gli isolanti, il gap è così elevato che in condizioni
normali gli elettroni risultano “imprigionati” nella VB. I semiconduttori hanno proprietà
intermedie.
54
Nel caso di sistemi polimerici è possibile immaginare una struttura a bande tipica di un
isolante, il drogaggio ha dunque la funzione di creare nuove bande di conduzione nella
zona tra la VB e la CB, con conseguente riduzione del gap energetico (figura 5).
Figura 5 Il meccanismo della conduzione secondo la teoria delle bande. La differenza tra metallo,
semiconduttore e isolante è evidenziata dal gap tra banda di valenza (VB) e banda di conduzione
(CB)
Nei metalli e nei semiconduttori convenzionali, il trasporto di carica ha luogo in stati
delocalizzati, ed è limitato dallo scattering dei portatori, principalmente a causa dei fononi,
deformazioni del reticolo cristallino indotte termicamente. Questo modello non è più valido
in materiali a bassa conducibilità come i semiconduttori amorfi e quelli organici, in cui si
stima che il libero cammino medio dei portatori sia più piccolo della distanza interatomica
media.
In questi materiali, il trasporto ha luogo grazie all’hopping ovvero al salto delle cariche
attraverso stati localizzati. Una differenza fondamentale fra il trasporto delocalizzato e
quello localizzato, è che il primo è ostacolato dall’interazione con i fononi mentre l’altro ne
è favorito.
In accordo con ciò, nei semiconduttori convenzionali la mobilità delle cariche diminuisce
all’aumentare della temperatura mentre nella maggior parte dei materiali organici è vero il
contrario.
Sono stati proposti diversi modelli per interpretare il meccanismo dell’hopping, nella
maggior parte dei casi, la dipendenza della mobilità dalla temperatura segue una legge del
tipo
µ = µ0 exp[−(T0 / T )1/ α ]
Dove
è un intero compreso fra 1 e 4.
Il confine fra il meccanismo delocalizzato e quello localizzato viene usualmente fissato per
valori di mobilità compresi fra 0.1 e 1 cm2V-1s-1.
Nei cristalli molecolari altamente ordinati la mobilità è vicina a questo limite cosicché vi
sono ancora controversie sul meccanismo di conduzione in tali materiali.
55
La localizzazione nelle molecole organiche coniugate ha luogo attraverso la formazione di
un polarone. Un polarone deriva dalla deformazione della catena coniugata sotto l’azione
della carica.
In altre parole, in una molecola coniugata, una carica viene intrappolata dalla
deformazione che essa stessa induce nella catena.
Questo meccanismo è spesso descritto assumendo la comparsa di stati localizzati con
energie comprese nel gap che separa la banda di valenza e quella di conduzione (figura
6).
Figura 6 Un polarone nel tiofene. In alto: distribuzione della carica nella struttura chimica. In basso:
diagramma dell’energia corrispondente.
L’esistenza di tali livelli in polimeri coniugati drogati ed oligomeri è stata realmente
osservata mediante spettroscopia UV-visibile.
4.2.2 Applicazioni
Tra le possibili applicazioni di questa classe di materiali organici una delle più attraenti
riguarda la fabbricazione di transistor. L’effetto transistor ha rappresentato una delle
maggiori scoperte del Novecento: non c’è apparecchio elettronico, TV, computer che non
sia provvisto di questo dispositivo.
Il principio di funzionamento del transistor a effetto campo (FET) fu per la prima volta
proposto da Lilienfeld nel 1930.
Fondamentalmente, un FET opera come un condensatore in cui un piatto funge da canale
di conduzione fra due contatti ohmici, gli elettrodi source (sorgente) e drain (pozzo). La
densità dei portatori di carica viene modulata dal voltaggio applicato al secondo piatto,
l’elettrodo gate.
Fu solo nel 1960 che Kahng ed Atala fabbricarono il primo MOSFET (Metal-OxydeSemiconductor
FET).
Questi
dispositivi
vengono
oggigiorno
realizzati
in
silicio
monocristallino grazie alla eccellente qualità dell’interfaccia silicio-ossido di silicio.
56
Esiste tuttavia un mercato in espansione che richiede di poter utilizzare transistor con
particolari caratteristiche meccaniche (flessibilità, leggerezza) e di lavorabilità. Esempi
sono i flexible display (schermi flessibili),
le smart card, le electronic label (etichette
elettroniche), i circuiti integrati polimerici.
Figura 7 Dispositivo TFT a base di pentacene sul suo supporto in policarbonato.
Sebbene le prime descrizioni dell’effetto campo nei semiconduttori organici risale al 1970,
gli OFET (Organic FET) sono stati identificati come potenziali costituenti di dispositivi
elettronici solo nel 1987 a seguito delle esperienze condotte da Koezuka et al. su di una
struttura a base di politiofene polimerizzato per via elettrochimica. Da allora le prestazioni
degli OFET sono state incrementate continuamente tanto che alcuni di essi competono
con i transistor a base di silicio amorfo, preferiti a quelli in silicio monocristallino per
applicazioni su larga scala perché meno costosi.
Il “transistor di plastica” è già una realtà. La Philips Research ne ha realizzato uno in cui i
tre elettrodi sono in polianilina (PANI), il semiconduttore è in politienilvinilene (PVT), ed il
materiale isolante è il polivinilfenolo (PVP), il tutto su di un supporto poliimmidico. Inoltre è
stata dimostrata la fattibilità di circuiti integrati, cioè strati impilati e sovrapposti di
transistor, costituiti completamente di materiali polimerici.
Figura 8 Scema di un transistor realizzato esclusivamente con materiali organici.
57
4.2.2.1 TFT (Thin Film Transistor) LCD Display
Il primo display a cristalli liquidi fu sviluppato dalla RCA Laboratories nel 1968, da allora gli
LCD sono stati istallati su quasi tutti i tipi di dispositivi elettronici, dagli orologi ai computer
agli schermi per TV.
Un tale schermo opera come una “valvola” bloccando la luce o permettendone il
passaggio. L’immagine viene formata
applicando un campo elettrico che altera le
proprietà chimiche di ciascuna LCC (Liquid Crystal Cell) del display in modo da cambiare
le proprietà di assorbimento del pixel.
La LCC trasforma l’immagine prodotta dalla sorgente nell’output richiesto dal dispositivo di
controllo dello schermo. Le celle sono in genere monocromatiche, la luce acquista il colore
desiderato mediante appositi processi di filtraggio.
Per capire come funziona un LCD, è più agevole descrivere il percorso di un raggio
luminoso dalla retro illuminazione all’utente.
La sorgente è disposta immediatamente dietro il display e può essere costituita da LED o
da dispositivi convenzionali a fluorescenza. Il raggio attraversa inizialmente un
polarizzatore in modo da poter interagire con la matrice liquido cristallina, questa stabilisce
se il pixel sarà acceso o spento. Se il pixel è acceso la matrice viene attivata
elettricamente così da allineare le molecole presenti nella fase liquido cristallina lasciando
passare la luce indisturbata.
Se il pixel è spento il campo è rimosso cosicché le molecole non allineate danno luogo a
fenomeni di diffusione, ciò riduce drasticamente l’intensità luminosa che attraversa lo
schermo.
In un display a colori il raggio attraversa, oltre che la matrice, anche un filtro (vetro di
solito); questo blocca tutte le lunghezze d’onda eccetto quelle di interesse.
In un tipico display RGB, il filtro cromatico è integrato nel vetro superiore, questo risulta
colorato a livello microscopico per rendere ciascun pixel rosso, verde o blu. Le zone
comprese fra i vari pixel sono rese nere in modo da aumentare il contrasto.
All’uscita dal filtro cromatico il raggio passa attraverso un altro polarizzatore in modo da
conferire all’immagine maggiore nitidezza e così da eliminare il riverbero.
58
Figura 9 Percorso di un raggio luminoso all’interno di un display LCD.
In uno schermo a cristalli liquidi a matrice attiva (AMLCD) ciascuna LCC è stimolata
individualmente da un transistor, a tal proposito la tecnologia predominante, anche se
costosa, prevede l’impiego di TFT.
4.2.2.2 Il Thin Film Transistor
Il concetto di transistor a film sottile fu introdotto per la prima volta da Weimer nel 1962. La
struttura è particolarmente indicata per materiali a bassa conducibilità ed è attualmente
utilizzata nei transistor a base di silicio amorfo. Gli elettrodi source e drain costituiscono
contatti ohmici direttamente innestati sul canale di conduzione. A differenza dei MOSFET
e dei MESFET non vi è zona di svuotamento (depletion region) che separa il dispositivo
dal substrato (figura 11). La bassa conduttività del semiconduttore, da sola, garantisce
correnti poco intense. Un’altra differenza cruciale rispetto al MISFET è che, sebbene il
TFT sia un dispositivo con gate isolato, esso opera in regime di accumulazione e non di
inversione.
L’assenza della zona di svuotamento porta ad una caratteristica del tipo:
Id =
V
Z
µ Ci Vg − Vt − d Vd
L
2
Dove:
ID: corrente all’elettrodo drain;
Z: larghezza del canale di conduzione;
L: lunghezza del canale di conduzione;
µ: mobilità dei portatori;
Ci: capacità dell’isolante;
Vg: differenza di potenziale fra source e gate;
59
Vt: voltaggio di soglia;
Vd: differenza di potenziale fra source e drain.
Qui il voltaggio di soglia è il potenziale a cui deve trovarsi l’elettrodo gate affinché la
conduttanza del canale sia uguale a quella dell’intero strato semiconduttore. Vale la
seguente relazione:
Vt =
qNd
Ci
Dove N è la densità dei centri di drogaggio (donori o accettori a seconda che il
semiconduttore sia di tipo n o p), q la carica dell’elettrone e d lo spessore del canale di
conduzione.
L’equazione appena scritta è valida nell’ipotesi per cui tutti i centri di drogaggio siano
ionizzati, tuttavia, questa evenienza è lontana dall’essere soddisfatta nei semiconduttori
organici.
Nel regime di saturazione la corrente è data dalla relazione:
I d , sat =
Z
µC i (V g − Vt ) 2
2L
Ancora una volta questa espressione è valida in ipotesi non sempre verificate nel caso dei
semiconduttori organici, in particolare quella di mobilità costante.
Figura 10 Caratteristica per un dispositivo TFT a base di pentacene.
60
Fin dalla scoperta nel 1987 le prestazioni dei TFT e più in generale degli OFET sono state
incrementate in modo continuo tanto che oggigiorno possono competere con i dispositivi a
base di silicio amorfo.
I passi in avanti sono stati compiuti principalmente grazie alla possibilità di ottenere film
altamente ordinati e sono certamente più significativi per le piccole molecole che per
polimeri.
Figura 11 Configurazione di un dispositivo OTFT: a) Top contact, b) Bottom contact.
4.3 Materiali organici elettroluminescenti
L’elettroluminescenza è il fenomeno di emissione della luce da parte di un materiale
sottoposto ad una differenza di potenziale.
L’emissione di luce da parte di materiali organici non è molto comune. E’ ben noto,
tuttavia, che alcune creature viventi come le lucciole, sono in grado di emettere luce per
mezzo di un pigmento naturale organico con straordinaria efficienza. A confronto,
apparecchi di uso comune come le lampade fluorescenti e a filamento e gli schermi
televisivi sono molto meno efficienti.
L’emissione da cristalli organici è stata studiata sin dagli anni sessanta ma l’elevato
potenziale richiesto per generare la luce (1000 Volt o più) ne ha ostacolato le applicazioni
fino all’avvento di dispositivi a film sottile.
61
Figura 12 Dimostrazione pratica del funzionamento di un OLED.
Un dispositivo organico elettrofluorescente viene detto OLED (Organic Light Emitting
Diode) ed è costituito da un film sottile di materiale organico disposto a sandwich tra due
elettrodi. I trasportatori di carica, gli elettroni (e-) di molecole cariche negativamente e le
lacune (hole, h+) di molecole cariche positivamente, vengono iniettate dal campo elettrico,
migrano dagli elettrodi e si ricombinano nella porzione centrale del dispositivo per formare
molecole energeticamente eccitate, il cui decadimento allo stato fondamentale genera la
luce emessa. Di solito il catodo è costituito da un metallo elettropositivo come il calcio, il
magnesio o l’alluminio, mentre l’anodo è un vetro conduttore come l’ITO (Indium – Tin
Oxide) per permettere l’uscita della luce dal sistema.
Il materiale organico può essere un singolo composto o, più comunemente, due o tre
composti disposti a strato in modo da incrementare l’efficienza globale del dispositivo
(figura 13).
Figura 13 Rappresentazione schematica di un OLED.
Nel caso in cui venga utilizzato un singolo materiale organico è necessario che questo sia
in grado di trasportare elettroni e lacune, e che sia un buon emettitore.
In generale, possono essere utilizzati nei dispositivi materiali organici sia molecolari che
polimerici. I primi sono costituiti essenzialmente da piccole molecole (peso molecolare
circa 500-2000) che si possono depositare sul supporto per formare il film tramite
deposizione sotto vuoto. Film polimerici si formano per immersione del supporto in una
soluzione del polimero (dipping) o per spin-coating, dove qualche goccia della soluzione
62
viene depositata sul supporto in rapida rotazione. Il film si forma per evaporazione del
solvente.
Figura 14 Principali materiali molecolari organici utilizzati per la realizzazione di LED.
Il primo importante successo nella produzione di OLED si è avuto nel 1987 da parte di un
gruppo della Eastman – Kodak. Il materiale impiegato fu il tri(8-idrossichinolinato) di
alluminio (AlQ3) il quale, con potenziale applicato di 10 V, emette luminescenza nel verde
con intensità paragonabile a quella dei tubi catodici e delle lampade a fluorescenza.
Risultati decisamente migliori furono ottenuti nel 1990 da Richard Friend dell’Università di
Cambridge, che riportò emissione di luce dal poli(p-fenilenvinilene) (PPV). Di recente lo
stesso gruppo ha ottenuto per questi sistemi efficienze apprezzabili, tempi di vita di
migliaia di ore e valori estremamente elevati di luminosità.
Figura 15 Spettro di emissione di un materiale elettroluminescente.
I
display
sono
una
delle
più
importanti
applicazione
dei
materiali
organici
elettroluminescenti. Lo scopo è ottenere schermi con elevate prestazioni e particolari
proprietà di leggerezza e flessibilità. Il primo display a OLED ad alta risoluzione è stato
63
introdotto dalla Pioneer nel 1997. Questo display monocromatico presenta un’elevata
efficienza e una vita media di 10 000 ore.
Figura 16 Display flessibile realizzato integralmente con materiali polimerici.
Stanno per essere immessi sul mercato display policromatici ottenuti combinando micro
OLED che emettono ciascuno nel rosso, verde e blu in modo da ottenere tutti i colori dello
spettro (figura 17).
Figura 17 Struttura di un OLED RGB.
4.4 Materiali per la fotonica
Da alcuni anni è diventato obiettivo comune della ricerca di carattere sia fondamentale sia
applicativo la sostituzione del maggior numero possibile di applicazioni che coinvolgono la
conduzione elettronica con analoghe basate sul trasporto e la modulazione di segnali
luminosi.
Infatti, i fotoni, veri e propri “carriers” della luce, sono i vettori di informazione più veloci
che esistano, assai più veloci degli elettroni che sono limitati nel loro cammino anzitutto
dalla reciproca repulsione, oltre che da vari ostacoli o “trappole”.
I composti organici offrono pressoché infinite possibilità di risposte ottiche in quanto le
proprietà di emissione e di assorbimento dipendono dalla natura più o meno coniugata
64
della molecola, cioè dalla presenza di doppi legami carbonio-carbonio messi in serie. Si
tenga conto che con il termine “luce”, non ci si riferisce solo a quella naturale ma anche a
quella dei laser, treni di fotoni estremamente intensi, coerenti, unidirezionali e
monocromatici e che possono viaggiare con intervalli anche brevissimi. Accanto alla
fotonica lineare ci sono interessanti sviluppi per quella non lineare sia del 2° sia del 3°
ordine1.
La sintesi organica permette oggi di modulare opportunamente la risposta fotonica.
Un materiale con proprietà ottiche non lineari del 2° ordine ha la capacità di raddoppiare la
frequenza della radiazione incidente. In questi sistemi le molecole devono essere
altamente polarizzabili e si devono disporre in modo da costituire un sistema non
centrosimmetrico2.
Per essere fortemente polarizzabili le molecole NLO-fore, cioè portatrici di proprietà Non
Linear Optical (di ottica non lineare), devono contenere legami delocalizzabili ossia
caratterizzati da elettroni “mobili” lungo l’intera struttura.
Figura 18 Nel caso di transizioni ottiche lineari, un elettrone assorbe un fotone dalla luce incidente e
subisce una transizione verso il più vicino stato permesso non occupato a più alta energia. Quando
l’elettrone “rilassa” emette un fotone con frequenza minore o uguale a quella della luce incidente (a
sinistra). La generazione di seconda armonica, d’altra parte, è un processo a due fotoni in cui
l’elettrone eccitato assorbe un ulteriore fotone transendo così verso uno stato ad energia ancora
superiore. La particella, tornando allo stato fondamentale, emette un fotone con frequenza doppia
rispetto a quella della luce incidente (a destra).
Legami delocalizzabili sono presenti in molecole costituite da un insieme di doppi legami
carbonio-carbonio fra loro adiacenti (sistemi coniugati) e aventi in testa e in coda alla
catena gruppi elettron-donatori D (donors) cioè capaci di donare una certa quantità di
densità elettronica ed elettron-attrattori EW (electron withdrawing): la donazione
elettronica del donatore D verso l’accettore EW fa sì che ai doppi legami competa parziale
carattere di legame semplice e, viceversa, ai legami semplici competa parziale carattere di
legame doppio conferendo una certa polarità alla molecola. La donazione elettronica dal
1
La polarizzazione P indotta da un campo elettrico applicato E può essere espansa in serie di potenze del vettore campo
elettrico: P = χ E + χ EE + χ EEE + etc. dove le (i) sono le suscettibilità ai vari ordini.
Si può dimostrare che in un sistema centrosimmetrico i termini del tipo (2n) dell’espansione in serie di P sono nulli.
(1)
(2)
(3)
2
65
donatore all’accettore conferisce inoltre alla molecola la necessaria polarizzabilità: la
molecola così concepita si dice essere un sistema push-pull (il donatore “spinge”,
l’accettore “tira”).
A che cosa serve l’incontro di una radiazione luminosa con un sistema molecolare push –
pull?
Ad esempio a trasformare un laser poco costoso, che emette luce rossa, in uno che
emette luce blu, quindi con raddoppio della frequenza.
Meno facile è costruire l’architettura molecolare non centrosimmetrica necessaria per
avere un sistema di ottica non lineare del 2° ordine. Se la molecola dotata di attività ottica
è incorporata in una opportuna matrice è possibile iso-orientare tutte le molecole sotto
l’influsso di un campo elettrico esterno (poling) sfruttando il momento dipolare non nullo
posseduto dalle molecole push-pull. Alternativamente, nel caso sia necessario depositare
uno o più strati di molecole su una superficie, è possibile sfruttare forze cooperative fisiche
intermolecolari come nel caso dei film di Langmuir-Blodgett, o funzionalizzare le molecole
in modo che si leghino con forti legami chimici agli atomi esposti della superficie di un
opportuno supporto.
L’attività ottica non-lineare delle molecole organiche non si limita al 2° ordine ma può
essere anche del 3° ordine.
In analogia con quanto fanno le molecole dei materiali del 2° ordine, quelle dei materiali
del 3° ordine possono triplicare la frequenza della radiazione incidente.
All’ottica lineare del terzo ordine sono associati, tuttavia, molti altri fenomeni, talvolta
anche complessi.
Fra questi va citata la capacità della molecola di raggiungere lo stesso stato
elettronicamente eccitato non solo assorbendo un fotone di una certa energia, ad esempio
a 400 nanometri, ma anche assorbendo due fotoni di energia dimezzata, quindi a 800
nanometri. Si hanno quindi sistemi molecolari che assorbono a due fotoni (Two Phonons
Absorption Molecules, Molecole TPA). Lo stato eccitato può successivamente evolvere
riportandosi allo stato fondamentale o in modo radiante, per esempio emettendo
fluorescenza, o in modo non radiante con svolgimento di calore.
Perché è importante questo fenomeno? Per almeno due ragioni.
66
La prima ragione è legata al fatto che la maggior parte dei materiali organici, compresi
quelli biologici, nell’assorbire un fotone sono opachi per esempio a 400 nm, ma sono
trasparenti a 800 nm. E’ quindi possibile eccitare con due fotoni “deboli” una molecola
dotata di proprietà ottiche non lineari del 3° ordine, anche se “schermata” da “normali”
molecole organiche che assorbono fotoni ad alta energia: è quindi possibile eccitare una
molecola dispersa in una matrice che sia trasparente a 800 nm ma opaca a 400 nm,
penetrando con un laser a 800 nm. La seconda ragione è legata al fatto che la radiazione
a 800 nm è assai meno energetica (e quindi praticamente non distruttiva) di una
radiazione a 400 nm: è quindi possibile osservare molecole attive al 3° ordine ospitate in
una matrice biologica senza che questa venga distrutta. E’ facile immaginare una potente
applicazione di questo fenomeno: ottenere delle immagini di reperti biologici senza che
questi vengano danneggiati. Questo fenomeno viene sfruttato ad esempio per
l’osservazione di sistemi cellulari con una tecnica avanzata nota come microscopia
confocale a due fotoni. Il risultato è simile a quello di una radiografia a raggi X ma di
qualità fotografica.
Un’altra importante applicazione delle molecole otticamente attive al 3° ordine è
l’ottenimento di limitatori ottici. Questi materiali hanno la prerogativa di essere molto meno
trasparenti di quanto atteso se colpiti da una radiazione di grande potenza. A differenza
dei normali filtri, essi permettono di limitare la trasmissione di radiazioni con lunghezza
d’onda compresa in un certo intervallo, svolgendo quindi un’azione selettiva. Si osserva
che l’intensità della radiazione trasmessa è considerevolmente minore rispetto a quella
incidente e precisamente, a saturazione, il rapporto è di 1 a 16. La struttura delle molecole
che danno assorbimento bifotonico e che in particolare rispondono ai requisiti di limitatori
ottici è coniugata: presenta una serie di doppi legami intervallati da legami semplici e può
essere di tipo push-pull o push-push o ancora pull-pull.
Un possibile impiego di tali materiali riguarda il campo militare, i sistemi di protezione della
retina dalle radiazioni molto intense e interruttori ottici.
67
Bibliografia
1) G. Horowitz, Organic Field-Effect Transistors, Adv. Materials 1998, 10, No. 5.
2) A. Facchetti, G. Pagani, Nuovi materiali da molecule organiche, Le Scienze quaderni
2000, 09, No. 115.
3) Chen, Sheau and I. C. Hsieh. "Polysilicon TFT Technology will solve problems of
mobility, pixel size, cost, and yield." Solid State Technology. January 1996 (pp 113120).
4) Chinnock, Chris. "Color to go." Byte. June 1995 (pp115-121).
5) Takahashi, Seiki et al. "Optimum design of Color Pixel Arrangement for 5-in Diagonal
TFT-LCD Suitable for Character and TV Images" IEEE Transactions on Electron
Devices Vol. 39 No. 5. May 5, 1992 (pp 1115-1121).
6) van Duijnhoven, F.; Bastiaansen, C. Adv. Mater.1999, 11, 567.
7) H. E. Katz, Organic molecular solids as thin film transistor semiconductors, J. Mater.
Chem., 7(3), 369-376.
8) W. Ubachs, Non linear optics, Lecture notes, 2001.
9) P. Batail, Molecular conductors, Chem. Rev., 9, Vol. 104, No. 11.
10) www.projectorpeople.com
11) www.kodak.com
12) www.powerlight.com
13) www.hwsands.com
14) M. Bendikov et al., “Tetrathiafulvalenes, Oligoacenes, and their Buckminsterfullerene
Derivatives: the Brick and Mortar of Organic Electronics”, Chemical Reviews, 2004,
Vol.104, No.11, 4891-4945.
15) D. Jérome, “Organic Conductors: From Chrage Density Wave TTF-TCNQ to
Superconducting (TMTSF)2PF6”, Chemical Reviews, 2004, Vol.104, No.11, 5565-5591.
16) J.H. Schön, C. Kloc, B. Batlogg, “Superconductivity in molecular crystals induced by
charge injection”, Nature, 2000, Vol.406, 702-704. For a retraction, see: Nature,
2003,Vol.422, 93.
17) P. Philips, “From insulator to superconductor”, Nature, 2000, Vol.406, 687-688.
18) D. Jérome and K. Bechgaard, “Superconducting plastic”, Nature, 2001, Vol.410, 162163.
19) Kresin, Little; Organic Superconductivity, Plenum press, 1990
20) M. Dumm et al., Phys. Rev. B 62, 6512 (2000).
21) R. E. Peierls, Quantum theory of solids, Clarendon, Oxford (1955).
22) M. Dressel, Optical Response of Sliding Charge Density Waves, Transparencies
(2002)
23) D. Jerome, A. Mazaud, M. Ribauld, K. Bechgaard, J. Physique Lett. 41, L95-98 (1980).
24) K. Bechgaard, C. S. Jacobsen, K. Mortensen, J. H. Pederson, N. Thorup, Solid State
Commun. 33, 119 (1980).
25) T. Ishiguro, K. Yamaji, G. Saito, Organic superconductors, Springer, Berlin (1998).
26) J. Wosnitza, Physikal. Blätter 56, 4/41 (2000); J. Moser, M. Gabay, P. Auban-Senzier,
D. Jerome, K. Bechgaard, J. M. Fabre, Eur. Phys. J. B 1, 39 (1998).
27) M. Dressel, J. Supercond. 13, 823 (2000).
28) W. A. Little. Possibility of synthesizing an organic superconductor. Phys.Rev. 134,
A1416- A1424
29) M. Dressel et al., Phys. Rev. B 50, 13603 (1994)
30) N. Drichko, P. Haas, B. Gorshunov, D. Schweitzer,and M. Dressel, LANL Preprint
Server: Cond. Mat., 0204425 (2002).
68
31) Làzslò Forrò, Làslzò Mihàly , “Electronic Properties of doped fullerenes”, Reports on
progress in physics (2001) 649-699.
32) Cooper, Korin-Hamzic, “Organic Conductors: Fundamentals and applications” JP,
Farges (1992).
33) P. Philips, “From insulator to superconductor”, Nature, 2000, Vol.406, 687-688.
34) D. Jérome and K. Bechgaard, “Superconducting plastic”, Nature, 2001, Vol.410, 162163.
35) Fleming R M, et al. 1991 Nature 352 701-703.
69