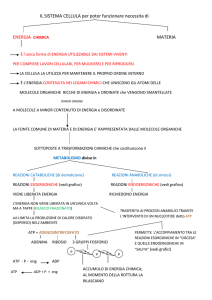
BIOENERGETICA
Studio delle variazioni di energia che
accompagnano le reazioni biochimiche
(Termodinamica)
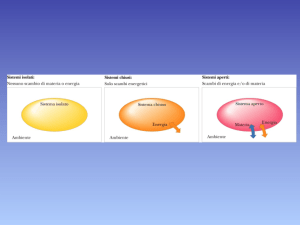
Sistemi viventi = isotermici
utilizzano energia chimica per attivare i processi
vitali
Reazioni spontanee e non
Per la reazione A + B ÅÆ C + D
∆ G = ∆Go' + RT ln
[C] [D]
[A ] [B]
∆G > 0 processo ENDOERGONICO
∆G < 0 processo ESOERGONICO
Reazioni spontanee e non
Per la reazioneA + B ÅÆ C + D
[C] [D]
∆G = ∆Gº' + RT ln
[ A ] [ B]
∆Go' di una reazione può essere positivo anche
quando ∆G è negative (dipendenza dalle concentrazioni
cellulari di reagenti e prodotti).
Molte reazioni il cui ∆Go‘>0 possono, all’interno delle nostre
cellule, essere momentaneamente spontanee (∆G<0) perchè
altre reazioni causano una deplezione dei prodotti oppure
mantengono elevate le concentrazioni dei reagenti.
Reazioni endoergoniche
• Reazioni chimiche che richiedono una
immissione netta di energia.
energia
• Esempio:
1. Fotosintesi
Sole
fotoni
6CO2 + 6H2O
→
Luce
Energia
C6H12O6 + 6O2
(glucosio)
Reazioni Esoergoniche
• Reazioni chimiche che rilasciano
energia.
energia
• Esempio:
1. Respirazione Cellulare
Energia
C6H12O6 + 6O2 → 6CO2 + 6H2O + ATP
(glucosio)
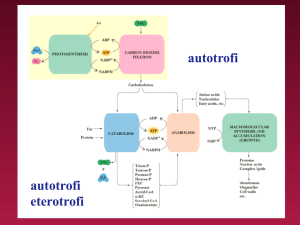
Metabolismo Cellulare
• La somma totale delle attività chimiche di tutte
le cellule.
cellule
• Reazioni Endoergoniche e Esoergoniche
• 2 Esempi:
1. Processi Anabolici
2. Processi Catabolici
Processi Anabolici
• Reazioni metaboliche che consumano energia
(endoergoniche) per costruire molecole
complesse a partire da molecole più semplici.
• Esempio:
1. Fotosintesi
6CO2 +
6H2O
Sole
→
C6H12O6 +
(glucosio)
luce
6O2
Processi Catabolici
• Reazioni metaboliche che rilasciano energia
(esoergoniche) attraverso la demolizione di
molecole complesse in composti più semplici.
• Esempio:
1. Respirazione Cellulare
C6H12O6 + 6O2 → 6CO2 + 6H2O +
(glucosio)
energia
ATP
Accoppiamento
I processi vitali (sintesi, contrazione muscolare,
trasmissione impulsi nervosi, etc) ottengono l'energia
necessaria attraverso l'unione, o accoppiamento, con
reazioni di ossidazione
Meccanismi di accoppiamento
:
.
A) INTERMEDIO COMUNE
B) Sintesi di un composto ad alto POTENZIALE
ENERGETICO
A) INTERMEDIO COMUNE
A+C
I
B +D
consente controllo della velocità dei processi ossidativi
A. Intermedio comune: un esempio
A + ATP ↔ B + AMP + PPi
∆Go' = + 15 kJ/mol
PPi + H2O ↔ 2 Pi
∆Go' = – 33 kJ/mol
A + ATP + H2O ↔ B + AMP + 2 Pi
∆Go' = – 18 kJ/mol
Pirofosfato (PPi) il prodotto di una reazione che
necessita di una “spinta” esterna
La sua idolisi, catalizzata dall’enzima Pirofosfatasi,
spinge la reazione da cui deriva PPi stesso.
Meccanismi di accoppiamento:
B) Sintesi di un composto ad alto POTENZIALE
ENERGETICO
Composto ad
ALTO POTENZIALE ENERGETICO
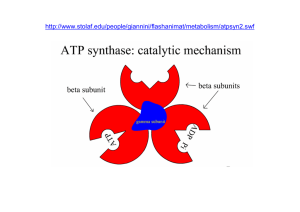
ATP = ADENOSINA TRIFOSFATO
E’ il principale intermedio ad alto contenuto
energetico nelle cellule viventi
Componenti:
1.
adenina: base azotata
2.
ribosio: pentoso
3.
gruppo fosfato : catena di tre
adenina
gruppo fosfato
P
ribosio
P
P
Composti ad
ALTO POTENZIALE ENERGETICO
Il valore intermedio di energia libera dell'idrolisi
dell'ATP, rispetto a quello di altri fosfati organici, ha un
significato importante.
L’ATP permette
l'accoppiamento di
reazioni
termodinamicamente
sfavorevoli con altre
termodinamicamente
possibili.
L’ATP è un DONATORE IMMEDIATO DI
ENERGIA LIBERA
MOVIMENTO
TRASPORTO ATTIVO
BIOSINTESI
ATP
ADP
FOTOSINTESI
o
FOSFORILAZIONE OSSIDATIVA
ESEMPIO
Pi + glucosio ↔ glucosio-6-P + H2O
∆Go' = +14 kJ/mol
ATP + H2O ↔ ADP + Pi
∆Go' = −31 kJ/mol
Reazione accoppiata:
ATP + glucosio ↔ ADP + glucosio-6-P
∆Go' = -17 kJ/mol !!
L’ATP è un DONATORE IMMEDIATO DI
ENERGIA LIBERA
In condizioni normali, una molecola di ATP è
consumata circa 1 minuto dopo la sua sintesi
Æ TURNOVER dell’ATP è molto rapido
A riposo, consumati 40 Kg in 24 ore
Sotto sforzo, anche 0,5 kg/minuto
Produzione di ATP
Produzione di ATP
•
•
•
•
•
•
Fase I : scissione macromolecole in piccole unità
Fase II: ulterire trasformazione in poche unità semplici (acetil
CoA)
Fase IIIa Ciclo dell’acido citrico
Fase IIIb Fosforilazione ossidativa
Fase I-II-IIIa: OSSIDAZIONE progressiva di macromolecole e
contemporanea riduzione di molecole che fungono da
“trasportatori” di elettroni (e idrogeno).
Fosforilazione di substrato.
NAD e FAD
Fase IIIb: trasferimento degli elettroni (riduzione) sull’ossigeno
e produzione di ATP. (Fosforilazione ossidativa)
Regolazione della produzione di
ATP: la CARICA ENERGETICA
[ATP] + ½ [ADP]
0<
<1
[ATP] + [ADP] + [AMP]
Velocità
Produzione
Di ATP
Consumo
di ATP
0
0.25
0.5
0.75
Carica energetica
1