Glicolisi
Glucosio
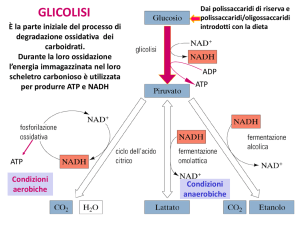
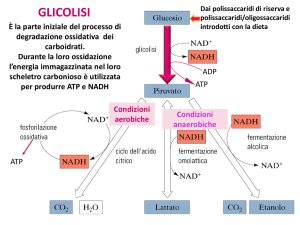
Principali vie di utilizzo del glucosio
La via della glicolisi
Nella glicolisi una molecola di glucosio (a sei atomi di carbonio) viene
degradata mediante una serie di reazioni enzimatiche, che producono
due molecole di piruvato, un composto a tre atomi di carbonio
In tutto sono necessarie dieci reazioni catalizzate da enzimi citosolici,
le prime cinque delle quali costituiscono la fase preparatoria (con
dispendio di energia), mentre nelle successive cinque si ha la fase di
recupero energetico (con produzione di energia)
La reazione complessiva è:
Glucosio + 2NAD+ + 2ADP + 2Pi → 2Piruvato + 2NADH + 2H+ + 2ATP + 2H2O
La via della glicolisi
Il destino del piruvato
Termodinamica della glicolisi
Concentrazioni allo stato stazionario dei
metaboliti della glicolisi negli epatociti
Tutti gli intermedi glicolitici sono fosforilati, poiché il gruppo
fosforico può avere tre funzioni utili:
1. Conferisce impermeabilità alla membrana plasmatica
2. Permette di conservare l’energia metabolica (legami ad alta
energia)
3. Riduce l’energia di attivazione ed aumenta la specificità della
reazione enzimatica
Tappa 1: Prima reazione d’innesco
Fosforilazione del glucosio sul C-6 con formazione di glucosio 6fosfato, catalizzata dall’esochinasi
L’esochinasi è una trasferasi, che ha bisogno di ioni Mg2+ per la sua
attività catalitica e va incontro ad un adattamento indotto
nel legame con il glucosio
Nell’uomo esistono 4 diversi isozimi (I – IV), di cui l’esochinasi
IV (o glucochinasi) degli epatociti ha proprietà cinetiche e di
regolazione peculiari, con importanti implicazioni fisiologiche
Glucosio-6-P
Il Glucosio-6-P è un punto di ramificazione
Tappa 2: la fosfoglucoisomerasi catalizza
l’isomerizzazione del glucosio-6-P
Conversione reversibile del glucosio 6-fosfato a fruttosio 6-fosfato,
catalizzata dalla fosfoesosio isomerasi (detto anche fosfoglucosio
isomerasi o glucosio fosfato isomerasi)
La reazione d’isomerizzazione è fondamentale, per consentire le
tappe successive della glicolisi a carico di un esosio più simmetrico
e divisibile in due unità a tre atomi di carbonio
Meccanismo d’azione della fosfoglucoisomerasi
Tappa 3: Seconda reazione d’innesco
Fosforilazione del fruttosio 6-fosfato a fruttosio 1,6-bisfosfato,
catalizzata dalla fosfofruttochinasi-1 (PFK-1)
Questa è la prima reazione “di comando” della via glicolitica,
poiché il fruttosio 1,6-bisfosfato è un intermedio esclusivo della
glicolisi, a differenza degli intermedi precedenti che possono avere
destini metabolici alternativi
Fosfofruttochinasi
La PFK-1 è soggetta ad una complessa regolazione allosterica:
•viene attivata dalla diminuzione di ATP o dall’accumulo di prodotti
d’idrolisi di ATP ed ADP e (soprattutto) dall’AMP e dal fruttosio 2,6bisfosfato (quest’ultimo è un potente mediatore della regolazione
ormonale di glicolisi e gluconeogenesi) ;
•viene inibita dall’aumento di ATP e di citrato
Regolazione della fosfofruttochinasi
Tappa 4: creazione di 2 intermedi a 3 atomi di C
Scissione del fruttosio 1,6-bisfosfato in diidrossiacetone fosfato
(DHAP, un chetosio) e gliceraldeide 3-fosfato (un aldosio),
catalizzata dalla fruttosio 1,6-bisfosfato aldolasi (o semplicemente
aldolasi)
La reazione è l’inverso di una condensazione aldolica reversibile,
che ritroveremo anche nella gluconeogenesi
Le aldolasi di classe I (animali e piante) formano una base di Schiff
come intermedio, mentre quelle di classe II (funghi e batteri)
utilizzano lo ione Zn2+ per stabilizzare un intermedio enolato
Meccanismo d’azione dell’aldolasi
Tappa 5: la trioso fosfato isomerasi completa
la prima fase della glicolisi
Interconversione rapida e reversibile del diidrossiacetone fosfato
in gliceraldeide 3-fosfato, catalizzata dalla trioso fosfato isomerasi
Meccanismo d’azione della trioso fosfato isomerasi
Tappa 6: generazione di un intermedio
ad alta energia
Ossidazione della gliceraldeide 3-fosfato a 1,3-bisfosfoglicerato,
catalizzata dalla gliceraldeide 3-fosfato deidrogenasi
Il prodotto è un’anidride tra un gruppo carbossilico e l’acido fosforico,
cioè un acil fosfato con un’alta energia libera standard d’idrolisi
(-49,3 kJ/mole)
La gliceraldeide 3-fosfato si lega covalentemente all’enzima, con
formazione di un intermedio tioemiacetalico con una cisteina
del sito attivo
Inizia la fase di recupero energetico della glicolisi!
Meccanismo d’azione della gliceraldeide-3fosfato deidrogenasi
Tappa 7:la fosfoglicerato chinasi catalizza
la reazione che porta al pareggio
Trasferimento del gruppo fosforico dall’1,3-bisfosfoglicerato all’ADP,
catalizzato dalla fosfoglicerato chinasi
Le tappe 6 e 7 della glicolisi nel loro insieme costituiscono un processo
di accoppiamento energetico, in cui la seconda reazione (fortemente
esoergonica) trascina la prima (endoergonica)
La somma delle due reazioni è esoergonica (ΔG’° = -12,2 kJ/mole) ed è
una fosforilazione a livello del substrato:
Gliceraldeide 3-fosfato + ADP + Pi + NAD+ → 3-Fosfoglicerato + ATP + NADH + H+
Formazione e decomposizione del 2,3-BPG
Tappa 8: la fosfoglicerato mutasi catalizza
il trasferimento di un gruppo fosforico
Conversione del 3-fosfoglicerato in 2-fosfoglicerato,
catalizzata dalla fosfoglicerato mutasi
La reazione è reversibile e richiede Mg2+
Meccanismo di reazione della fosfoglicerato mutasi
Tappa 9: la disidratazione catalizzata
dall’enolasi genera il PEP
Deidratazione del 2-fosfoglicerato a fosfoenolpiruvato (PEP),
catalizzata dall’enolasi
La reazione comporta un intermedio enolico stabilizzato dall’Mg2+
In condizioni cellulari il ΔG è molto vicino a zero
Tappa 10: la reazione della piruvato chinasi
fornisce altro ATP
Trasferimento del gruppo fosforico dal fosfoenolpiruvato all’ADP,
catalizzato dalla piruvato chinasi
La reazione è una fosforilazione a livello del substrato e richiede
K+ e Mg2+ (oppure Mn2+)
La piruvato chinasi possiede siti allosterici per diversi effettori:
•È attivata dall’AMP e dal fruttosio-1,6-bisfosfato
•E’ inibita (soprattutto nella sua forma fosforilata) dall’ATP,
dall’acetil-CoA e dall’alanina
Tappa 10: la reazione della piruvato chinasi
fornisce altro ATP
Circa la metà dell’energia rilasciata dall’idrolisi del PEP (ΔG’° = -61,9
kJ/mole) viene conservata nella formazione del legame
fosfoanidridico dell’ATP (ΔG’° = -30,5 kJ/mole), mentre la parte
restante trascina la reazione di biosintesi
L’equazione complessiva della glicolisi è:
Glucosio + 2NAD+ + 2ADP + 2Pi → 2Piruvato + 2NADH + 2H+
+ 2ATP + 2H2O
In condizioni aerobiche le due molecole di NADH + H+ che si
formano nel citosol vengono riossidate a NAD+, con simultaneo
trasferimento dei loro elettroni alla catena di trasporto mitocondriale,
che li trasferisce all’ossigeno:
2NADH + 2H+ + O2 → 2NAD+ + 2H2O
Effetto Pasteur: La velocità della glicolisi e la quantità totale di glucosio consumato
sono più elevate in condizioni anaerobiche rispetto a quelle aerobiche
Infatti, la resa in ATP della glicolisi è 15 volte inferiore rispetto a quella che si ottiene
dall’ossidazione completa del glusio a CO2 (2 ATP rispetto a 30 o 32 ATP), quindi in
condizioni anaerobiche bisogna consumare 15 volte più glucosio per ottenere la
stessa quantità di ATP
Effetto Warburg: In quasi tutti i tipi di tumori la velocità della glicolisi è più elevata
(anche di 10 volte) di quella dei tessuti normali, anche quando è disponibile
l’ossigeno
Infatti, la maggioranza delle cellule tumorali cresce in condizioni ipossiche e dipende
dalla sola glicolisi per la sintesi di ATP, “mimando” così le condizioni dell’effetto
Pasteur
Il fattore di trascrizione indotto dall’ipossia (HIF-1) stimola la sintesi di almeno 8
enzimi glicolitici e dei trasportatori di glucosio
Fermentazione alcolica e lattica
Come viene regolata la glicolisi nelle cellule?
Mannosio, galattosio, fruttosio ed altri semplici
substrati possono entrare nella glicolisi
Il metabolismo del galattosio: la via di Leloir
L’ingresso del glicerolo nella via glicolitica
Il glicerolo è un metabolita che viene generato in quantità
significative dalla decomposizione dei triacilgliceroli.
Può essere convertito in glicerolo-3-fosfato dall’azione della
glicerolo chinasi
e poi ossidato a diidrossiacetone
dall’azione della glicerolo fosfato deidrogenasi, con NAD+
richiesto come coenzima
Mg2+
sn-Glicerolo-3-P + ADP
sn-Glicerolo-3-P + NAD+
DHAP + NADH + H+
Glicerolo + ATP
Intolleranza al lattosio
Intolleranza al lattosio
La lattasi si trova sull’apice dei villi intestinali
Intolleranza al lattosio
•
•
•
•
•
Due to lactase deficiency
Lactase splits lactose into monosaccharides:
Glucose
Galactose
Monosaccharides absorbed by active transport
Undigested lactose moves into colon:
– Change in osmotic pressure
– Provides substrate for microbial
fermentation
Results in
– Excess fluid
– Organic acids
– Gases including hydrogen
Cosa causa l’ipolactasia?
Three types of lactose intolerance:
Congenital alactasia
Present from birth
Idiopathic lactase deficiency
Natural attrition after infancy
Affects about 80% of the world’s adult population
Secondary lactase deficiency
Results from damage to the lactase-producing brush border cells,
often as a result of intestinal infection
Usually temporary condition that resolves once the infection of
intestinal damage resolves
Cosa causa l’ipolactasia?
The persistence or not persistence of the expression of lactase is associated
with the so-called point polymorphism C/T 13910.
This consists in the substitution of a single nucleotide base in a sequence of
DNA, that carries regulatory on the lactase gene:
C/T-13910 and T/T-13910 genotypes associated with normolactasia
C/C -13910 genotype is strongly associated with hypolactasia