dal particolare al generale
La spirale del male:
dissezione iatrogena coronarica ed aortica
Paolo Canova, Giuseppe Musumeci, Roberta Rossini, Mauro Gori, Michele Senni, Orazio Valsecchi
Dipartimento Cardiovascolare, ASST Papa Giovanni XXIII, Bergamo
Iatrogenic coronary and aortic dissection is one of the worst complication during a percutaneous coronary
intervention. Nevertheless, it can be approached and effectively resolved by a percutaneous way, sealing
the false lumen “entry door” with a covered stent, even if this device is more thrombogenic than other
bare-metal or drug-eluting stents. We report the case of a 60-year-old man with acute ST-elevation myocardial infarction complicated by both iatrogenic dissection and multiple stent thrombosis.
Key words. Iatrogenic dissection; Myocardial revascularization; Stent thrombosis.
G Ital Cardiol 2016;
CASO CLINICO
Un uomo di 60 anni ad elevato profilo di rischio cardiovascolare (iperteso in terapia con calcioantagonista, fumatore di 26
pacchetti/anno, dislipidemico non trattato) giunge in Pronto
Soccorso per l’insorgenza di angor da circa 2h. In anamnesi
si rileva solo una pregressa ulcera gastrica trattata mediante
terapia medica. L’ECG di presentazione mostra uno sfumato
sopraslivellamento del tratto ST in D1 e aVL (Figura 1) in paziente ancora sintomatico (troponina I 5.15 ng/ml), per cui si
decide di eseguire una coronarografia d’urgenza.
Il quadro coronarografico, visualizzato mediante accesso
arterioso radiale destro, mostra malattia diffusa dei tre vasi
(Figura 2A-B) con una stenosi subocclusiva della circonflessa al tratto medio (culprit lesion) che viene trattata mediante
impianto di stent medicato a rilascio di zotarolimus (2.75x30
mm). Considerato il pregresso problema gastrico, viene scelta
l’associazione clopidogrel e acido acetilsalicilico come duplice
terapia antiaggregante.
Dopo l’angioplastica primaria il paziente prosegue la propria
degenza in Unità Coronarica, rimanendo asintomatico e in buon
compenso di circolo. L’ecocardiogramma non evidenzia deficit
della cinesi segmentaria e agli esami ematochimici il picco degli
enzimi di miocardionecrosi è modesto (troponina I 15.21 ng/ml).
In quarta giornata tuttavia recidiva il dolore toracico con corrispondente sopraslivellamento del tratto ST infero-posteriore
all’ECG. La coronarografia non evidenzia occlusioni coronariche,
ma si decide di trattare la lesione al tratto distale della coronaria
destra, responsabile verosimilmente dell’evento acuto.
All’inizio della procedura il catetere guida (Judkins destro
4.0, 6 Fr) danneggia l’ostio della coronaria destra causando
un’inquietante dissezione spirale anterograda e retrograda
coinvolgente la parete aortica (Figura 2C-E). Posizionata rapidamente una guida nel vero lume coronarico, vengono rilasciati in
© 2016 Il Pensiero Scientifico Editore
Ricevuto 01.02.2016; accettato 23.02.2016.
Gli autori dichiarano nessun conflitto di interessi.
Per la corrispondenza:
Dr. Paolo Canova Dipartimento Cardiovascolare,
ASST Papa Giovanni XXIII, Piazzale OMS 1, 24127 Bergamo
e-mail: [email protected]
serie due stent metallici (3.0x33 mm e 3.5x28 mm), dal tratto
medio fino all’ostio, post-dilatati ad elevate atmosfere, senza
più evidenza di doppio lume e con ottimo flusso coronarico
finale (TIMI 3) (Figura 2D). L’aortografia mostra invece la rima di
dissezione spiraliforme estesa dalla radice aortica fino all’arco,
con risparmio dell’ostio del tronco comune perfuso dal vero
lume (Figura 2F). Il paziente dopo un’iniziale ipotensione risolta
con riempimento volemico e supporto inotropo (dopamina 4
μg/kg/min) rimane emodinamicamente stabile: viene attivato
l’Heart Team e si decide di eseguire un’angio-tomografia computerizzata (TC), la quale localizza una dissezione spirale estesa
dal seno coronarico destro fino al tratto soprarenale dell’aorta
addominale, senza interessamento dei vasi epiaortici e con il
falso lume quasi completamente trombizzato.
Considerata la stabilità emodinamica, l’assenza di dolore
e la duplice terapia antiaggregante in corso, si decide collegialmente di monitorare il paziente in Terapia Intensiva, ripetendo una TC a 48-72h, salvo instabilità clinica. Il paziente
rimane sempre asintomatico, mantiene un buon compenso di
circolo senza alcun supporto inotropo con conservata funzione sistolica all’ecocardiogramma.
L’angio-TC ripetuta a distanza di 3 giorni non rivela ulteriori evoluzioni con opacizzazione del falso lume limitata al
tratto prossimale dell’aorta ascendente. In quarta giornata il
paziente viene pertanto sottoposto a nuovo controllo coronarografico che conferma un buon risultato delle precedenti
procedure interventistiche, mentre un’iniezione selettiva mette in evidenza la porta d’ingresso della dissezione (Figura 3A)
localizzata all’ostio della coronaria destra, che viene fissata
mediante l’impianto di uno stent (4x23 mm) ricoperto di pericardio equino (Figura 3B), senza più opacizzazione del falso
lume aortico alla successiva iniezione (Figura 3C).
Il paziente rimane stabile durante la successiva degenza;
la TC conferma l’esclusione completa del falso lume (Figura
3D), per cui dopo 7 giorni viene dimesso in una struttura riabilitativa. Tuttavia, dopo circa 4 mesi dall’ultima angioplastica
il paziente ritorna in Pronto Soccorso per infarto miocardico
sopraslivellamento del tratto ST inferiore: condotto direttamente in Emodinamica il quadro è quello di una restenosi con
trombosi degli stent al tratto ostio-prossimale della coronaria
destra (Figura 3E), trattata mediante tromboaspirazione e dig ital cardiol |
1
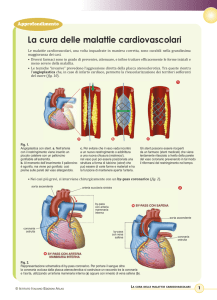
Figura 1
P Canova et al
Figura 1. ECG di presentazione in Pronto Soccorso.
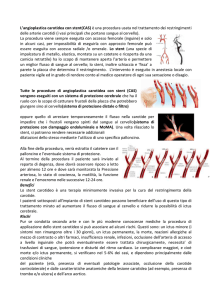
Figura 2
Figura 2. Quadro coronarografico di presentazione: (A) coronaria sinistra; (B) coronaria destra;
(C) dissezione coronarica ed aortica; (D) “sealing” della dissezione coronarica; (E-F) aortografia
(le frecce indicano l’opacizzazione del falso lume).
latazioni ad elevate atmosfere (Figura 3F-G). Viene comunque
ripetuta un’aortografia che non mostra alcuna opacizzazione
del falso lume (Figura 3H). Per l’alto carico trombotico viene
eseguito un carico più infusione di eptifibatide per 12h, quindi sostituito clopidogrel con ticagrelor.
Trasferito in Terapia Intensiva, dopo circa 40 min dalla
sospensione dell’antagonista della glicoproteina IIb/IIIa, si ha
nuovamente un marcato sopraslivellamento del tratto ST inferiore per trombosi acuta dello stent, trattato efficacemente
mediante tromboaspirazione, con normalizzazione dell’ECG.
Il paziente successivamente rimane asintomatico, tuttavia
agli esami ematochimici la troponina I raggiunge un picco di
300 ng/ml e l’ecocardiogramma mostra un’acinesia inferiore e un’ipocinesia medio-basale laterale, condizionante una
lieve disfunzione ventricolare sinistra (frazione di eiezione 4550%).
La successiva degenza procede fortunatamente senza ulteriori complicanze per cui viene dimesso in decima giornata
e ad 1 anno di follow-up rimane clinicamente stabile, senza
alcuna limitazione funzionale nelle proprie attività.
2
g ital cardiol |
DISCUSSIONE
La dissezione coronarica iatrogena rappresenta una rara, temuta e potenzialmente letale complicanza di una qualsiasi angioplastica coronarica. In letteratura vi sono diversi casi clinici
di dissezioni coronariche ostiali da catetere trattate sia conservativamente che efficacemente per via percutanea1 o con
un approccio combinato, percutaneo e chirurgico2; tuttavia,
come per le dissezioni coronariche spontanee, non vi è alcuna
linea guida che definisca quale sia il trattamento migliore.
Il registro italiano di Lettieri et al.3 comprende 134 pazienti con una documentata dissezione coronarica spontanea, di
cui il 58% trattato conservativamente, mentre il 42% è stato
rivascolarizzato per via percutanea o mediante bypass. La sopravvivenza a 6 anni di follow-up era globalmente del 94%
senza alcuna differenza in termini prognostici tra i due gruppi.
In linea generale ciò che spinge l’emodinamista al trattamento percutaneo piuttosto che ad un approccio conservativo sono sostanzialmente i sintomi riferiti associati all’instabilità emodinamica, il ridotto flusso coronarico a valle4, nonché
l’estensione della rima di dissezione, talora meglio definita da
Figura 3
Dissezione iatrogena coronarica ed aortica
Figura 3. Esclusione del falso lume aortico: (A) risultato angiografico dello stent della coronaria
destra con opacizzazione retrograda del falso lume; (B) “sealing” della porta d’ingresso del falso
lume aortico; (C) coronarografia destra; (D) angio-tomografia dell’aorta ascendente; (E) trombosi
tardiva di stent; (F) angioplastica della coronaria destra ostio-prossimale; (G) risultato angiografico; (H) aortografia.
metodiche di imaging intravascolare (ecografia intravascolare
o tomografia a coerenza ottica)5.
Tuttavia, ancor più drammatica è la dissezione coronarica
iatrogena coinvolgente, per via retrograda, la radice aortica.
Tale evento è generalmente più frequente in seguito a manovre di cannulazione della coronaria destra rispetto alla sinistra,
ma in entrambi i casi molto spesso si associa ad una grave instabilità emodinamica che può portare all’exitus del paziente
o richiedere un intervento chirurgico urgente6.
Nel primo registro internazionale di dissezioni aortiche7
pubblicato nel 2002, il 27% dei casi era secondario a procedure interventistiche e la prognosi di questi pazienti era spesso infausta.
Anche per questo tipo di terribile complicanza, non vi è
mai stato un “gold standard” di trattamento e si è sempre
pensato che l’approccio chirurgico fosse in un certo senso più
garante di successo sia nel breve che nel lungo termine. Tale
complicanza può però essere efficacemente gestita anche nel
laboratorio di Emodinamica mediante la chiusura della porta
BIBLIOGRAFIA
1. Zilio F, Napodano M, Fedrigo M,
Angelini A, Tarantini G. La peggiore complicanza durante rivascolarizzazione coronarica percutanea: la dissezione iatrogena del tronco comune. G Ital Cardiol
2015;16:385-8.
2. La Franca E, Piraino D, Cortese B, et
al. Immediate decision making in a case of
iatrogenic dissection of left main coronary
artery: a successful synergetic treatment.
Int J Cardiol 2016;202:77-9.
3. Lettieri C, Zavalloni D, Rossini R, et
al. Management and long-term prognosis
d’ingresso del falso lume con stent metallici, medicati o ricoperti. Un approccio “conservativo”, come quello scelto da noi
nel caso in questione, sembrerebbe infatti avere un outcome
favorevole sia nel breve che nel lungo termine, come recentemente pubblicato nel registro RAID8.
RIASSUNTO
La dissezione iatrogena aortica e coronarica è una delle peggiori
complicanze di un intervento di rivascolarizzazione miocardica percutanea. Tuttavia, può essere approcciata ed efficacemente trattata per via percutanea, chiudendo la “porta d’ingresso” del falso
lume con uno stent ricoperto, anche se questo dispositivo ha una
maggior trombogenicità rispetto ad altri stent metallici o medicati.
Descriviamo un caso di infarto miocardico con sopraslivelllamento
del tratto ST all’ECG, complicato sia da dissezione iatrogena da
catetere sia da multiple trombosi dello stent ricoperto impiantato.
Parole chiave. Dissezione iatrogena; Infarto miocardico; Trombosi
dello stent.
of spontaneous coronary artery dissection.
Am J Cardiol 2015;116:66-73.
4. Tweet MS, Eleid MF, Best PJ, et al.
Spontaneous coronary artery dissection:
revascularization versus conservative therapy. Circ Cardiovasc Interv 2014;7:777-86.
5. Paulo M, Sandoval J, Lennie V, et al.
Combined use of OCT and IVUS in spontaneous coronary artery dissection. JACC
Cardiovasc Imaging 2013;6:830-2.
6. Noguchi K, Hori D, Nomura Y, Tanaka H. Iatrogenic acute aortic dissection
during percutaneous coronary interven-
tion for acute myocardial infarction. Ann
Vasc Dis 2012;5:78-81.
7. Januzzi JL, Sabatine MS, Eagle KA, et
al.; International Registry of Aortic Dissection Investigators. Iatrogenic aortic dissection. Am J Cardiol 2002;89:623-6.
8. Nunez-Gil IJ, Bautista D, Cerrato E,
et al.; Registry on Aortic Iatrogenic Dissection (RAID) Investigators. Incidence,
management, and immediate- and longterm outcomes after iatrogenic aortic
dissection during diagnostic or interventional coronary procedures. Circulation
2015;131:2114-9.
g ital cardiol |
3