LA BIOENERGETICA
A CURA DI MICHELE MONCELLI
La bioenergetica è la branca della biochimica che studia tutti i processi
attraverso cui le cellule utilizzano, immagazzinano e scambiano energia.
È un'area di ricerca biologica che prevede lo studio di processi cellulari
quali ad esempio la respirazione cellulare, e di molti altri
processi metabolici che possono portare alla produzione e utilizzazione
di energia sotto forma di molecole ATP.
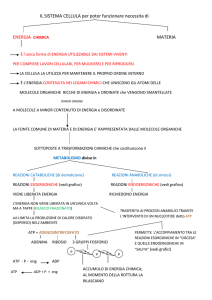
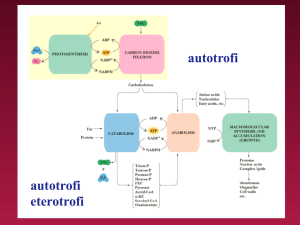
METABOLISMO CELLULARE: Insieme delle reazioni di trasformazione della
materia e dell’energia all’interno della cellula.
CATABOLISMO: Insieme delle reazioni di degradazione delle molecole complesse in
sostanze più semplici. Si tratta di reazioni esoergoergoniche.
ANABOLISMO: Insieme delle reazioni di sintesi dei costituenti a partire da composti
semplici. Si tratta di reazioni endoergoniche.
ATP
•
È la « MONETA» di scambio energetico cellulare che permette il collegamento tra
le reazioni cataboliche e quelle anaboliche.
•
L’ ATP (adenosin trifosfato) è un nucleotide costituito da un nucleoside
(adenosina) e tre gruppi fosfato. Ogni giorno consumiamo ca 1 quintale di ATP che
rappresenta un evidente segnale del benessere energetico cellulare.
COME SI PRODUCE ATP?
•
L a reazione di sintesi dell’ATP è 1 reazione endoergonica (7,3
kcal/mole) e si realizza mediante un processo di CONDENSAZIONE:
•
•
ADP + Pi
ATP + H2O
Quando l’ATP viene idrolizzato ad ADP + Pi viene liberata la stessa
quantità di energia necessaria per la sua sintesi. L’ IDROLISI dell’ ATP è
una reazione esoergonica la cui energia è sfruttata per realizzare tutte
le attività cellulari.
•
•
•
•
COME VIENE UTILIZZATO L’ATP?
Scissione fosforica : ATP+ X
X-Pi + ADP
Scissione pirofosforica : ATP + X
X-P-Pi + AMP
Scissione pirofosforica : ATP + X
X-AMP + P-Pi
COFATTORI
NAD
FAD
COFATTORI: composti di natura in/organica fondamentali per l’attività
catalitica.
NAD (NICOTINAMMIDE ADENIN DINUCLEOTIDE ).
Interviene nelle reazioni redox trasportando equivalenti di riduzione * da un
substrato DONATORE ad 1 altro ACCETTORE. Deriva dalla vit PP.
*Possono essere: - elettroni liberi
- atomi di H
- ioni idruro H-
COSA SI INTENDE PER IONE IDRURO?
È 1 atomo di H che porta 2 elettroni e che deriva da una scissione ASIMMETRICA di una molecola
biatomica di idrogeno (H2).
NORMALMENTE una molecola H2 si dissocia in 2H ciascuno con un protone e 1 elettrone.
In questo caso invece avremo una scissione ASIMMETRICA con liberazione di un H+ e uno ione idruro
(H-) quindi 1 atomo di idrogeno con 2 elettroni.
Nel ciclo di questa reazione si passa dalla forma ossidata ( NAD+) alla forma ridotta (NADH) attraverso
l’addizione di uno ione idruro:
Uno dei 2 elettroni viene captato dall’atomo di N con ridistribuzione dei suoi elettroni;
Il secondo elettrone viene utilizzato per contrarre un legame C-H utilizzando il protone derivato dalla
scissione asimmetrica di H2. si passa quindi alla forma ridotta.
NAD+
NADH + H+ ( fosforilazione ossidativa )
Esiste inoltre la forma fosforilata del coenzima ( NADP) che si differenzia solo per la presenza di
un radicale fosforico esterificato in posizione 3 primo della struttura del NAD .
La fx resta la stessa solo che la forma non fosforilata prende parte soprattutto a reazioni di
ossidazione mentre la forma fosforilata interviene nelle reazioni di riduzione.
NADP+ + 2 ELETTRONI + 2 H+
NADPH + H+ ( fotosintesi )
FAD (FLANIN ADENININ DINUCLEOTIDE)
È 1 altro cofattore coinvolto nelle reazioni redox (deriva dalla vit B2) che trasporta
equivalenti di riduzione sottoforma di atomi di H in quanto lega sequenzialmente un
elettrone e un protone.
Contrariamente al NAD ( trasportatore obbligato di 2 equiv di riduzione per volta) un
coenzima flavinico può trasportare elettroni uno per volta oppure a coppie in quanto dallla
forma ossidata ( FAD) attraverso l’ingresso di 1 elettrone si passa ad un intermedio radicalico
(cioè con 1 elettrone spaiato) detto SEMICHINONE . Successivamente si avrà una
protonazione dell’intermedio accettando anche un secondo elettrone.
Dunque un coenzima flavinico può trasportare 2 oppure un solo equivalente.
FAD + 2 e- + 2 H+
FADH2 ( Glicolisi e Ciclo di KREBS)
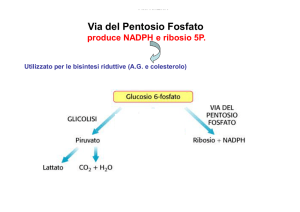
LA GLICOLISI
La principale fonte di energia per le cellule è la demolizione del glucosio ( C6H12O6) che
coinvolge diverse fasi e può procedere fino all’ossidazione completa con produzione di CO2
oppure arrestarsi a livello di composti intermedi.
La GLICOLISI è la prima fase dell’ossidazione e rappresenta una serie di reazioni attraverso
cui il glucosio è demolito ad acido piruvico. È praticamente presente in tutte le cellule .
Avviene in condizioni di ANAEROBIOSI nel CITOPLASMA di tutte le cellule.
Comprende 9 reazioni biochimiche ciascuna catalizzata da uno specifico enzima.
Nel corso di questa via metabolica 1 molecola di glucosio a 6C viene gradualmente
trasformata in 2 molecole di Acido Piruvico (C3H403) liberando energia.
L’energia liberata durante la glicolisi viene sfruttata per produrre 2 molecole di ATP e 2
molecole di NADH.
L’EQUAZIONE GLOBALE DELLA GLICOLISI E’:
C6H12O6 + 2 Pi + 2 ADP + 2 NAD+
2C3H4O3 + 2 ATP + 2 NADH + 2 H+
Glicolisi è sinonimo di fermentazione cioè un fenomeno di utilizzo anaerobio di glucosio mediante il
quale il glucosio può fornire energia a prescindere dalle ossidazioni della catena respiratoria.
Essa infatti può realizzarsi anche laddove non ci sono mitocondri ( per es negli eritrociti privi di MT)
oppure a livello del tessuto muscolare laddove l’O2 diventa limitante.
GLICOLISI NELLE FIBRE MUSCOLARI BIANCHE ( VELOCI)
Durante l’attività muscolare si ha 1 adeguato metabolismo:
1.Aumenta la ventilazione polmonare
2.Aumenta la frequenza cardiaca
3.Si ha vasodilatazione.
Tutti questi processi favoriscono un maggiore afflusso di sangue e quindi di ossigeno al tessuto
muscolare nel frattempo si riduce la pO2 a livello tissutale per effetto del consumo e l’O2 diventa
limitante. Questo è particolarmente vero a livello delle fibre veloci o bianche.
Esse sono definite veloci perché sono destinate a sostenere attività fisiche rapide e intense ( corsa
veloce, sollevamento pesi…). In queste fibre il n° di enzimi glicolitici è elevatissimo ed esse hanno
questo tipo di metabolismo perché sono limitate dalla riossidazione del NADH
RIOSSIDAZIONE DEL NADH
Per quanto riguarda la disponibilità di NAD+ , la riossidazione del NADH nelle fibre veloci bianche non può
avvenire a livello MT perché i MT sono presenti ( se lo sono) in bassissimo n°.
Per questo motivo sono definite fibre bianche: i MT hanno pigmenti colorati ( citocromi) che qui
scarseggiano inoltre il loro contenuto in Mioglobina è basso.
In queste condizioni la riossidazione del NADH avviene sempre nel citosol per opera dell’enzima lattico
deidrogenasi (LDH) che è NAD-dipendente.
La forma OX del coenzima viene riciclata perché rientra nella reazione globale della glicolisi.
L’acido lattico formato invece non viene più riciclato e si accumula determinando una condiz di
ACIDOSI LATTICA.
La fermentazione in questo caso sarà definita appunto FERMENTAZIONE LATTICA.
FERMENTAZIONE ALCOLICA
L’altra reazione a cui può andare incontro l’acido piruvico è la seguente:
I lieviti ( appartenenti al regno dei funghi) convertono il glucosio in alcol etilico.
Saccaromyces cerevisiae è il lievito utilizzato per la panificazione.
Saccaromyces elipsoideus e apiculatus sono usati invece per la produzione del vino.
RESPIRAZIONE CELLULARE
Nel caso in cui si ha a che fare con un tessuto AEROBIO che NON tollera alcuna forma di
acidosi ( cuore e cervello) alla glicolisi p.d. fa seguito il metabolismo ossidativo terminale.
Per ossidativo si intende un metabolismo che determina consumo di O2 a livello MT
attraverso una serie di enzimi che viene detto CATENA RESPIRATORIA a cui è associato un
processo di sintesi di ATP MT detto fosforilazione ossidativa.
FOSFORILAZIONE perché avviene per addizione di un radicale fosforico ad una molecola di
ADP.
OSSIDATIVA perché la sintesi di ATP è associata a reazioni di ossidazione soprattutto
dell’NADH ad opera dell’O2 molecolare.
Dunque in presenza di O2 il piruvato viene ossidato e demolito totalmente con produzione
di H2O e CO2 nel processo definito RESPIRAZIONE CELLULARE.
Tale processo ha luogo nei MT e viene diviso in 3 fasi principali:
1.DECARBOSSILAZIONE OSSIDATIVA DELL’AC.PIRUVICO
2.CICLO DI KREBS ( O DELL’ AC. CITRICO)
3.CATENA RESPIRATORIA
DECARBOSSILAZIONE OSSIDATIVA
L’ acido piruvico ( C3H4O3) appena formato nel citosol passa attraverso la MMI per il
tramite di un carrier specifico ( che può fx come simport con n H+ o come 1 antiport con
un OH-).
Sfruttando la differenza transmembrana esso fa il suo ingresso e va incontro alla reazione
di DECARBOSSILAZIONE OSSIDATIVA catalizzata dalla PDH.
Si perde CO2 , si forma acetato legato al CoA e si libera coenzima sottoforma di NADH.
La PDH è 1 COMPLESSO MULTIENZIMATICO costituito da 3 enzimi:
E1: Decarbossilasi
E2: Transacetilasi
E3: Deidrogenasi
CICLO DI KREBS ( O dell’ Ac. Citrico)
È un crocevia metabolico , un ciclo di natura “ anfibolica” cioè ha sia carattere catabolico che
anabolico ( in condizioni di biosintesi).
Tale ciclo è costituito da reazioni cicliche che coinvolgono enzimi indipendenti tra loro.
Nella prima reazione il gruppo acetile
( a 2C) si lega all’acido ossalacetico
( a 4c), formando l’ac.Citrico ( a 6C).
Successivamente l’ac. Citrico subisce
una serie di ossidazioni che portano alla
formazione di :
- 2 molecole di CO2
- 3 molecole di NADH
- 1 molecola di GTP a livello della sesta
reazione che non potendo esser
utilizzato trasferisce un Pi sull’ADP per
formare ATP.
- 1 molecola di FADH2.
L’ultima reazione del ciclo rigenera l’acido ossalacetico che può così iniziare un nuovo ciclo.
L’equazione di un ciclo completo del ciclo di krebs è la seguente:
Ac.Ossalacetico+ Acetil-CoA+ ADP+ Pi +3 NAD+ + FAD
Ac.ossalacetico + 2CO2+ CoA+ ATP +3NADH+ 3H+ +FADH2.
Le reazioni di ossidazione della glicolisi e del ciclo di krebs NON richiedono O2.
RENDIMENTO ENERGETICO DELL’OSSIDAZIONE DEL GLUCOSIO
La glicolisi ( fermentativa e citosolica) ci dà:
2ATP glicolitici
6 ATP dovuti al NADH citosolico perché per ogni mole di NADH si producono 3 moli di ATP.
6 ATP dovuti al NADH prodotto dalla decarbossilazione ox dell’ac. Piruvico ( ovviam x2)
L’ aCoA prosegue il suo cammino nel ciclo dell’acido citrico e per ogni mole di aCoA che viene
ossidata si formano 12 moli di ATP
3NADH danno 9 ATP
1 FADH2 danno 2 ATP
1 GTP viene convertito in ATP
-----------------------------------------------------12 moli di ATP x 2= 24 moli di ATP
CATENA RESPIRATORIA E FOSFORILAZIONE OSSIDATIVA
Attraverso il ciclo di krebs si producono ampie quantità di coenzimi ridotti ( sottoforma di
NADH) che alimentano la catena respiratoria essendo DONATORI DI ELETTRONI ALL’ O2,
attraverso reazioni complesse.
La catena respiratoria è costituita da una serie di proteine enzimaticooligomeriche integrali
di membrana localizzate nella MMI. A tale livello sono localizzati anche i trasportatori di
membrana.
La MMI è ASSOLUTAMENTE IMPERMEABILE a qualsiasi molecola tranne che all’O2, H2O e
alcune molecole liposolubili.
La C.R. è costituita da una serie di enzimi oligomerici detti COMPLESSI ( ce ne sono 5)
disposti in serie e che si passano gli elettroni che i substrati cedono, quando si ossidano , ai
coenzimi che poi li cedono ai trasportatori intermedi di elettroni dai coenzimi all’O2.
Perché non è costituita da un singolo enzima?
Perché se cosi fosse NON si potrebbe generare l’intero gradiente di protoni richiesto per la
sintesi dell’ATP.
I complessi sono collegati tra loro da enzimi:
Il complesso 1 è collegato al complesso 3 tramite l’ UBICHINONE.
Il complesso 3 è collegato al complesso 4 tramite il CITOCROMO C *
Il complesso 4 trasferisce elettroni sull’O2.
OGNI VOLTA CHE GLI ELETRONI PASSANO ATTRAVERSO I COMPLESSI (1-3-4) VENGONO
POMPATI ALL’ESTERNO H+. Si crea un gradiente elettrochimico di H+ .
Il complesso 5 o ATP SINTETASI sfrutta tale gradiente per produrre ATP facendo rientrare
H+.
•CITOCROMI: sono delle emoproteine con diverso gruppo eme. A differenza delle
emoproteine respiratorie che fx fin quando il Fe è ridotto, i citocromi invece basano il loro fx
sulla Transizione dello ione Fe da ossidato a ridotto. FX DA TRASPORTATORI DI e-.
•L’ultimo trasportatore della catena cede e- all’O2 ( accettore finale) trasformandolo in H20.
COMPLESSO I
Lega la forma ridotta del NAD.
È un complesso transmembrana costitito da
circa 43 subunità: di queste solo 8 sono
coinvolte nel trasferimento di e1 flavoproteina
7 Fe-S proteine.
Il NADH si lega, viene ossidato e si ha poi il
trasferimento di e- attraverso i singoli centri
redox fino all’ACCETTORE che è l’UBICHINONE.
QUINDI IL C.1 è detto NADH UBICHINONE *
OSSIDOREDUTTASI.
Quando gli e- passano attraverso il complesso
vengono traslocati 4H+.
*SI TRATTA DI 1 ENZIMA UBIQUITARIO DISPOSTO NEL CORE LIPIDICO DELLE
MEMBRANE. La forma ox può accettare 2 elettroni ma sempre uno per volta per cui
si forma prima un intermedio radicalico detto SEMICHINONE. POI ACCETTA 1 ALTRO
e- e 2 H+ E PASSA NELLA FORMA RIDOTTA.
•È anche 1 accettore di altre DH come la SUCCINATO DH ( COMPLESSO II)
COMPLESSO III
L’Ubichinone che viene ridotto e passa
a UQH2 viene poi ossidato dal
complesso III detto anche
UQH2- cyt C- REDUTTASI.
Il passaggio di e- attraverso il
complesso genera la traslocazione di
2H+.
Tale complesso è costituito da una serie
di componenti che fx da trasportatori di
e- dal DONATORE ( UQH2) all’
ACCETTORE ( Cyt-C)
COMPLESSO IV
Si chiama Cyt-C OSSIDASI perché il
citocromo C fornisce gli e- , gli H+ vengono
prelevati dall’esterno e si forma H2O
utilizzando l’O2.
ANCHE IN QUESTO CASO SI AVRA’
PROTRUSIONE ALL’ESTERNO DI 4H+.
IN TOTALE DUNQUE IL n°DI PROTONI
ESTRUSI è PARI A 10.
TALE FENOMENO è DETTO DI
ACCOPPIAMENTO CHEMIO-OSMOTICO.
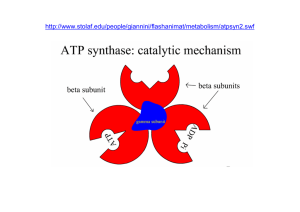
COMPLESSO V
È detto anche ATP SINTETASI ed è costituito da:
-1 porzione idrofobica ( F0)
-1 collo
- 1 porzione idrofilica (F1) che sporge nella
matrice mitocondriale.
il settore F0 costituisce il canale per il passaggio
degli H+ ( CANALE PROTONICO)
Il settore F1 fx da elemento catalitico cioè
abbiamo qui la sintesi di ATP. Esso è costituito da
3 dimeri αβ che si trovano in 3 stati
conformazionali diversi:
-STATO O ( OPEN) non lega nulla
- STATO L ( LOOSE) lega debolmente ADP
- STATO T ( TIGHT) lega saldamente ATP.
l’immissione di energia altera la conformazione
determinando una ROTAZIONE.
IL FLUSSO DI e- CHE RIENTRANO NELLA MATRICE
SECONDO GRADIENTE FORNISCE L’ENERGIA
NECESSARIA PER SINTETIZZARE ATP a partire da
ADP+ Pi.
CONCLUSIONI
Dall’ossidazione completa di 1 molecola di glucosio si ottengono 38 molecole di ATP.
Di queste solo 2 dalla glicolisi mentre le altre 36 dalla respirazione cellulare che è
dunque la via metabolica più efficace per liberare l’energia presente nel glucosio.
Il bilancio totale della demolizione AEROBICA del glucosio è:
C6H12O6 + 6 O2
6CO2 + 6 H2O + 686 Kcal/mole
Delle 686 Kcal/mole 266 sono usate per sintetizzare ATP mentre le restanti sono
disperse nell’ambiente sottoforma dia CALORE.
IL RENDIMENTO ENERGETICO DELL’INTERO PROCESSO E’ PERCIO’ DI CA IL 40%.
Una gran parte di quello che i medici
sanno, è insegnata loro dai malati.
Marcel Proust, I Guermantes, 1920